氧化铜催化零价铁还原水中亚硝基二甲胺
2017-06-28王济禾李微微蒋贝贝浙江工业大学建筑工程学院浙江杭州3004浙江工业大学环境学院浙江杭州3004
韩 莹,王济禾,李 军,李微微,蒋贝贝,姚 杰(.浙江工业大学建筑工程学院,浙江 杭州 3004;2.浙江工业大学环境学院,浙江 杭州 3004)
氧化铜催化零价铁还原水中亚硝基二甲胺
韩 莹1,王济禾1,李 军2*,李微微1,蒋贝贝1,姚 杰1(1.浙江工业大学建筑工程学院,浙江 杭州 310014;2.浙江工业大学环境学院,浙江 杭州 310014)
为去除水中亚硝基二甲胺(NDMA)对环境的污染,研究采用氧化铜(CuO)催化零价铁还原NDMA.考察了反应效能以及CuO的投量、pH值、溶解氧、反应器转速等因素的影响,进行了产物分析并对动力学规律和反应机理进行探讨.实验结果表明:CuO可以有效地催化零价铁还原NDMA,反应18h后去除率可达99%以上.CuO投量越大,pH值越低,反应进行越快.富氧状态抑制NDMA的还原.反应器转速过快或过慢都会影响反应的进行.随着NDMA的降解,偏二甲肼(UDMH)和二甲胺(DMA)随之生成.催化加氢被提出是该反应的机理.
氧化铜;亚硝基二甲胺;零价铁;催化;还原
亚硝基二甲胺(NDMA)具有高致癌风险,其在加拿大的饮用水厂出水和美国的火箭引擎测试场附近的饮用水井中被检出后,饮用水界的研究者提高了对它的关注度[1-3].之后的调查及研究表明其在氯、氯胺消毒以及臭氧氧化后的水中均有生成[3].欧洲和亚洲的一些国家在水源水、饮用水厂出水和污水处理厂的出水中也陆续检出了 NDMA[4-5].鉴于 NDMA在水体中的广泛存在[6-10],十分必要找寻有效的技术对其进行控制.
零价铁还原技术由于其原料来源广泛且操作简便引起了广泛关注,其被用于去除环境中的污染物质,包括各种氯代有机物、偶氮染料、硝基芳香族化合物等[11].零价铁能还原降解NDMA,但反应时间较长[2,12],需要找寻提高反应速率的方法.氧化铜(CuO)在家用供水铜管的腐蚀产物中存在并且曾被用于催化丙烯和水中酚的氧化[13],三卤甲烷的脱氯等[13-14],因此将其运用在催化零价铁还原NDMA中具有很大的潜力.
本文考察了CuO催化零价铁还原NDMA的效能及CuO投量、pH值、溶解氧、转速等因素对于处理效果的影响并进行产物分析及机理探讨,从而为提出一种新的可运用于实际水处理中对于NDMA的控制方法提供数据基础.
1 材料与方法
1.1 试剂及仪器

图1 (a)铁粉和(b)CuO粉末的扫描电镜图Fig.1 Scanning electron microscopy images of (a) iron powders and (b) CuO powders
NDMA标准品(1000mg/L,1mL)购自上海安谱实验科技股份有限公司,实验所用 NDMA(纯度>99%)为实验室合成产品,4-羟乙基哌嗪乙磺酸(HEPES)缓冲试剂购自上海安谱实验科技股份有限公司,盐酸二甲胺(DMA·HCl,99%)购自上海麦克林生化科技有限公司,盐酸偏二甲肼(UDMH·HCl,98%)购自东京化成工业株式会社,甲醇(色谱纯)购自德国CNW公司,三羟甲基甲胺基丙磺酸(TAPS)缓冲试剂购自百灵威科学公司,1, 4-哌嗪二丙磺酸(PIPPS)缓冲试剂购自英国Fluorochem 化学有限公司.实验用水为超纯水(Milli-Q制备).铁粉(分析纯)购自天津博迪化工股份有限公司,粉状CuO购自上海国药集团化学试剂有限公司,图1是所用铁粉和CuO粉末的扫描电镜图,铁粉和 CuO均呈现无规则的形状,铁粉粒径大都在100µm以下,CuO粉末粒径大都在10µm以下.
1.2 试验方法
配置一定浓度的缓冲溶液(pH=4,PIPPS缓冲剂;pH=6、7,HEPES缓冲剂; pH=8、9,TAPS缓冲剂)并用NaOH调节到所需pH值(pH=7,考察pH值时除外).缓冲溶液初始溶解氧浓度为 8mg/L,考察溶解氧浓度时向缓冲溶液中通入氮气或氧气以降低或提高溶解氧浓度到所需浓度.在40mL棕色萃取瓶中加入缓冲溶液,之后分别加入一定量的铁粉、CuO和NDMA,其中铁粉的投量为10g/L, CuO的投量为5mmol/L(考察CuO投量时除外),效能及影响因素考察时 NDMA的起始浓度为100µg/L,产物分析时为0.05mmol/L.盖紧瓶盖,放置在 QB-328旋转培养器上以一定转速(45r/min,考察转速时除外)旋转,定时取样,样品采用真空泵经0.22µm的膜进行抽滤分离未反应的铁粉和CuO,从而终止反应,所得水样以备分析.试验进行时的温度为20℃.
1.3 NDMA的分析方法
采用HPLC法[15]测定NDMA的质量浓度变化,流动相为甲醇/水溶液,二者体积比为1:4,流速为1.0mL/min,紫外检测器波长为230nm.
1.4 DMA的分析方法
采用HPLC法[12]测定DMA的质量浓度变化,流动相为0.2%乙酸/甲醇,二者体积比为2:3,流速为1.0mL/min,紫外检测器波长为380nm.
1.5 UDMH的分析方法
采用柱前衍生HPLC法[16]测定UDMH的质量浓度变化.流动相为乙腈/水,二者体积比为4:1,流速为1.0mL/min,紫外检测器波长为390nm.
1.6 数据分析
拟一级动力学方程由式(1)表示,其中 C0为NDMA的起始浓度,C为某一反应时间点NDMA的浓度,t为反应时间,k为拟一级反应速率常数:

两边取对数后可得式(2):

2 结果与讨论
2.1 CuO催化零价铁还原水中NDMA的效能
图2为CuO催化零价铁还原NDMA的效果.如图所示,单独投加铁粉或 CuO粉末,反应进行18h后NDMA的去除率分别为12.91%和5.13%,说明单独零价铁对NDMA的还原效果较差,而单独 CuO对 NDMA的微量去除可能是由于NDMA在CuO表面的吸附.采用CuO催化零价铁的反应体系中,反应18h后,NDMA的去除率为98.84%,相较单独零价铁还原 NDMA的去除率有了大幅提高.同时较单独零价铁和单独CuO对NDMA的去除率的加和高出80个百分点,这说明 CuO具有很高的催化活性,而不只起到吸附NDMA、增加反应表面的作用.
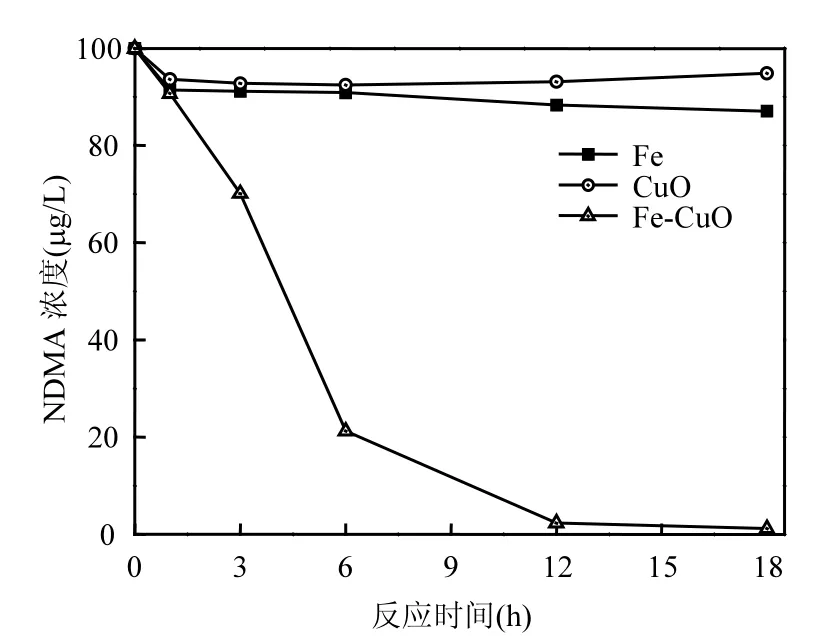
图2 CuO催化零价铁还原水中NDMA的效能Fig.2 Efficiency of copper oxide-catalyzed reduction of NDMA with zero-valent iron in water
2.2 CuO投量的影响
图3为CuO投量对CuO催化零价铁还原NDMA的影响.如图所示,CuO的投量分别为1、2、5、10、15mmol/L,反应18h后NDMA去除率分别为 20.88%、91.99%、98.84%、98.47%和99.50%.当CuO投量从1mmol/L增加到2mmol/L时,NDMA去除率明显提高.这可能是因为 CuO投量太少催化生成的反应活性位点或者活性物质少,当 CuO投量增加时,催化生成的反应活性位或活性物质增多,使得反应加快.当 CuO投量超过2mmol/L时,NDMA去除率没有大幅度提高,这可能是因为NDMA的初始浓度不变,所需要的反应活性位点或活性物质也是一定的.
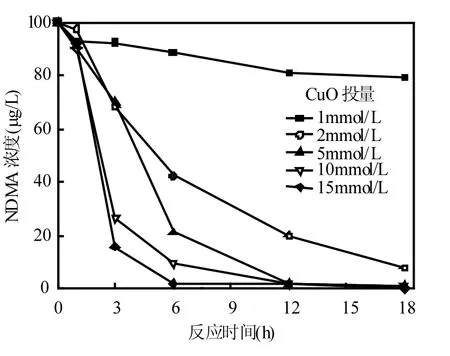
图3 CuO投量对CuO催化零价铁还原NDMA的影响Fig.3 Effect of copper oxide dosage on the copper oxidecatalyzed reduction of NDMA with zero-valent iron
在不同CuO投量的条件下,对NDMA还原反应进行拟一级动力学分析,结果见表1.CuO投量为 1mmol/L时,反应不符合一级反应动力学,进一步说明CuO投量少时催化生成的活性点位或者活性物质少.CuO投量为2、5、10、15mmol/L时,反应符合一级反应动力学.随着 CuO投量的增加,反应速率常数(k值)随之增加,说明CuO投量为2~15mmol/L时,CuO投量越多,零价铁活性越高,反应速率越快.CuO的投量和 k值之间呈一定的线性关系,用公式表达即为 k=0.0414× [CuO投量],R2=0.8823.这和之前研究中的现象一致[17-19],说明在此投量范围内,相较零价铁, CuO对反应所需活性物质的生成起到更决定性的作用.
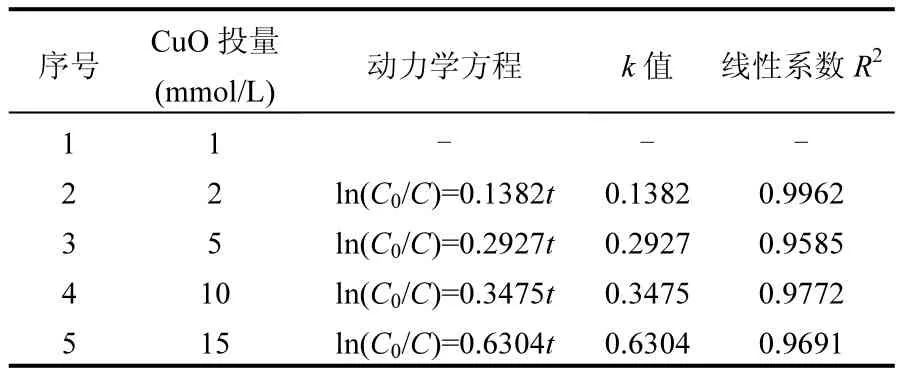
表1 不同CuO投量条件下还原NDMA的动力学Table 1 Kinetics of NDMA reduction with different dosages of copper oxide
2.3 溶液pH值的影响
图4为溶液pH值对CuO催化零价铁还原NDMA的影响.如图所示,溶液 pH=4、6、7时,反应进行18h后NDMA去除率分别为99.90%、99.90%和98.84%.这主要是因为酸性或中性条件下,溶液中的氢离子越多, 铁的表面不易形成钝化膜,另外酸性条件下可能生成了更多活性物质,有利于还原反应进行.溶液pH=8、9时,反应18h后反应体系对NDMA没有明显去除.这是因为溶液中的氢离子很少,溶液中的氢氧根离子与铁离子生成氢氧化铁,包裹在铁的表面形成钝化膜,阻碍了反应的进行.pH=9的溶液比pH=8的溶液中可用的氢离子少,更易生成钝化膜,去除率更低.在不同pH值的条件下,对NDMA还原反应进行拟一级动力学分析,结果见表 2.在酸性和中性条件下,pH值越低,反应速率越快,说明氢离子确实促进了反应进行.在碱性条件下,反应不符合一级反应动力学,反应进行缓慢,与上述推断一致.
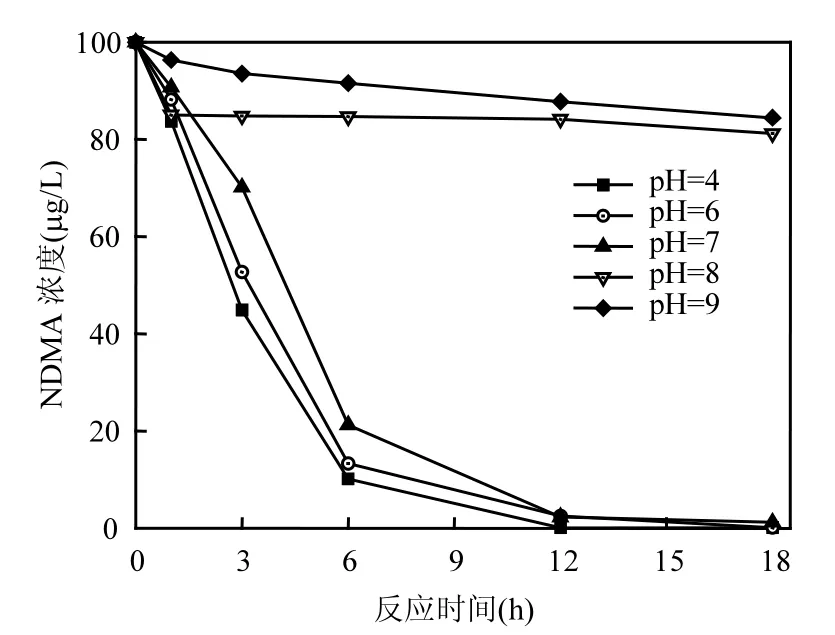
图4 溶液pH值对CuO催化零价铁还原NDMA的影响Fig.4 Effect of solution pH on the copper oxide-catalyzed reduction of NDMA with zero-valent iron

表2 不同pH值条件下还原NDMA的动力学Table 2 Kinetics of NDMA reduction under different pH values
2.4 溶液溶解氧的影响
图 5为溶解氧对 CuO催化零价铁还原NDMA的影响.如图所示, 溶解氧分别为0、4、6、8mg/L,反应 18h后 NDMA去除率分别为99.84%、98.89%、94.82%、98.84%.在此溶解氧浓度范围内,溶解氧变化对NDMA的最终去除率影响不大.溶解氧浓度为10mg/L时,反应18h后NDMA去除率仅为 16.67%,溶液处于富氧条件时抑制反应体系对NDMA的去除.这是由于零价铁的标准电势值是-0.44V,氧的标准氧化还原电位是 1.224V[20],溶液中溶解氧浓度高时,零价铁优先与氧气反应从而减少活性氢的生成,同时形成氢氧化铁附着在铁的表面,阻碍反应进行.
在不同溶解氧浓度下,对NDMA还原反应进行拟一级动力学分析,结果见表 3.当溶液溶解氧为8mg/L以下时,还原反应符合一级反应动力学,不同溶解氧浓度下反应速率常数(k值)与溶解氧的浓度未呈现线性相关关系.这可能是因为在溶液溶解氧浓度小于8mg/L时,溶解氧对活性氢生成的影响比较随机,同时可能在铁表面随机生成不完整的钝化膜,这些钝化膜会不同程度地影响反应速率.当溶液达到富氧状态,反应不符合一级反应动力学,反应速率缓慢,这是由于溶解氧充足时在铁表面形成了致密完整的钝化膜阻碍了CuO催化零价铁还原NDMA的进行.
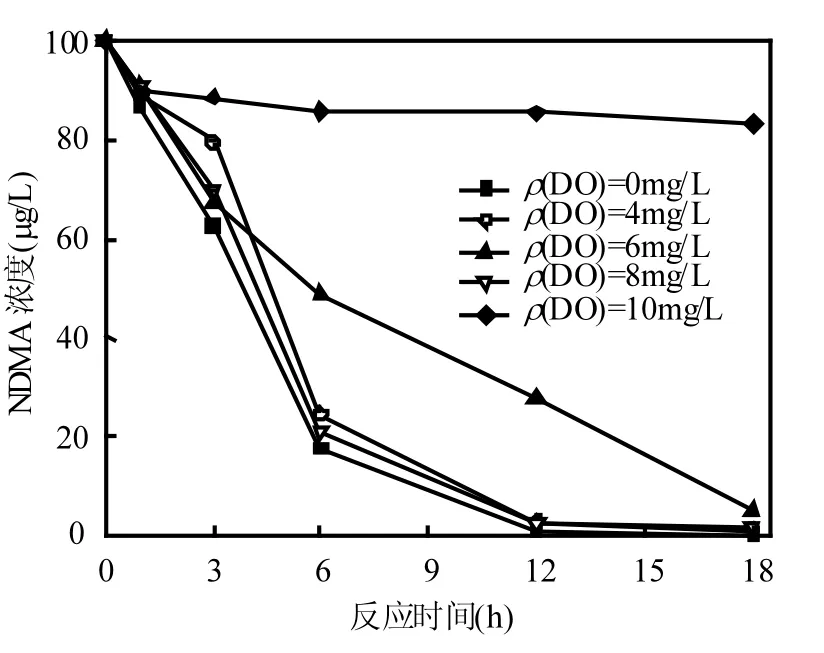
图5 溶解氧浓度对CuO催化零价铁还原NDMA的影响Fig.5 Effect of dissolved oxygen concentration on the copper oxide-catalyzed reduction of NDMA with zero-valent iron
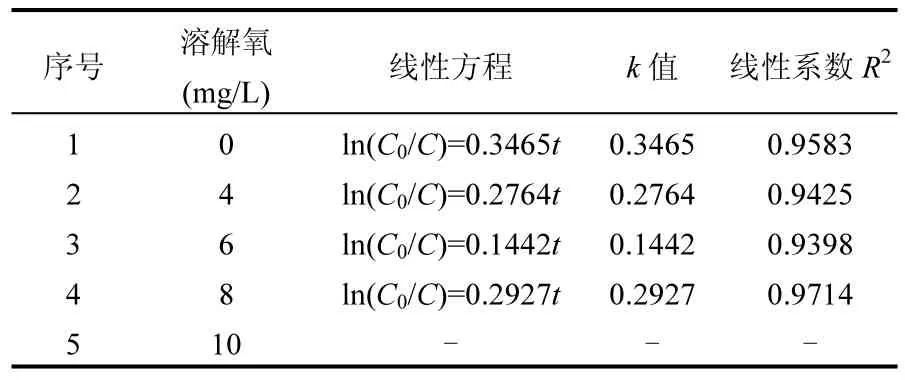
表3 不同溶解氧浓度下还原NDMA的动力学Table 3 Kinetics of NDMA reduction with different concentrations of dissolved oxygen
2.5 转速的影响
图6为转速对CuO催化零价铁还原NDMA的影响.如图所示,转速分别为 15、30、45、60和75r/min时,反应18h后NDMA去除率分别为19.40%、16.47%、98.84%、98.30%、75.47%.这说明传质对反应的影响很大,反应需要CuO、零价铁和NDMA充分接触,转速过快或过慢,物质传递都不够充分.在不同转速的条件下,对NDMA还原反应进行拟一级动力学分析,结果见表4.当转速为15r/min和30r/min时,反应不符合一级反应动力学,说明转速过慢导致传质不充分.当转速为45、60、75r/min时,反应符合一级反应动力学,但转速为75r/min时的k值远小于前两者时的k值.这说明反应速率未随着转速的加快而增大.当转速太大时离心力太大,铁粉与 CuO 始终保持在瓶底或者瓶口无法与NDMA充分接触.
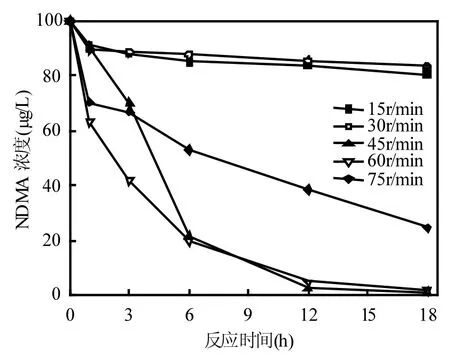
图6 转速对CuO催化零价铁还原NDMA的影响Fig.6 Effect of rotation speed on the copper oxidecatalyzed reduction of NDMA with zero-valent iron
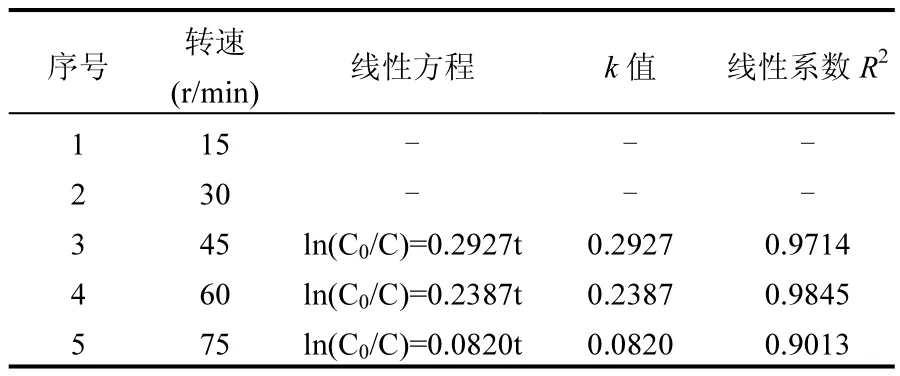
表4 不同转速条件下还原NDMA的动力学Table 4 Kinetics of NDMA reduction with different rotation speeds
2.6 产物分析及机理探讨
图7为CuO催化零价铁还原NDMA的产物情况.如图所示,随着 NDMA的降解,DMA和UDMH的浓度不断增加.在NDMA还原体系的报道中 UDMH是 NDMA还原的关键中间产物,NDMA首先被还原生成UDMH,之后UDMH再进一步被还原为 DMA[17,21-23].在本反应体系中UDMH和DMA两种关键的中间产物均被检出.
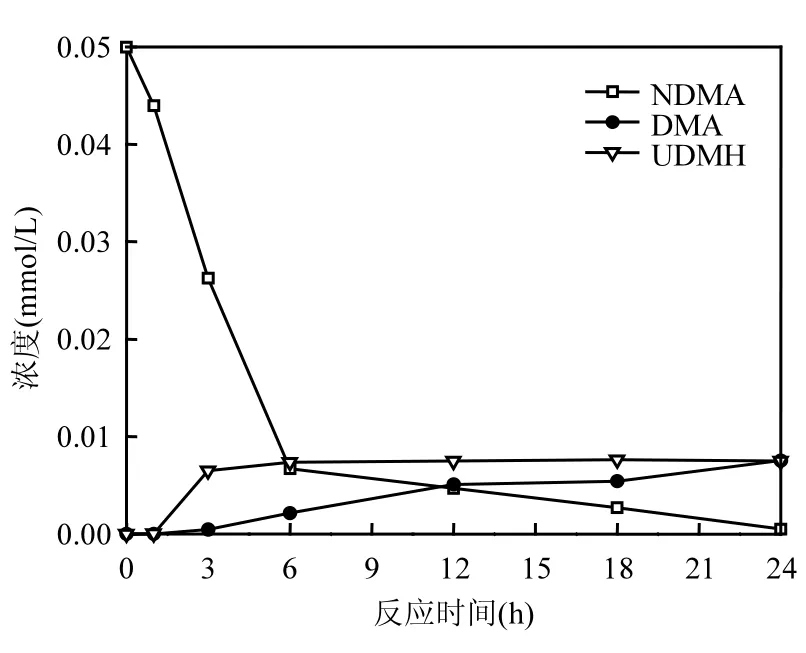
图7 CuO催化零价铁还原NDMA的产物Fig.7 Products of the copper oxide-catalyzed reduction of NDMA with zero-valent iron
现在认为零价金属还原水中NDMA的机理是催化加氢[17,21-22],主要的反应过程包括:(1)金属提供电子和水中的氢离子反应生成氢原子;(2)氢原子结合生成氢分子;(3)氢分子在金属表面被活化成活性氢原子,步骤(1)和步骤(3)中的氢原子均具有活性,被称为活性氢原子;(4)活性氢原子在还原 NDMA的过程中起到还原剂的作用.因此本体系中主要的反应过程如下:零价铁通过上述前三个步骤生成活性氢原子,之后活性氢原子首先还原NDMA的N=O键生成UDMH, UDMH随后被活性氢原子还原生成DMA,而氧化铜在上述的某些步骤中起到了催化作用.
3 结论
3.1 CuO可以有效催化零价铁还原 NDMA,反应18h后NDMA的去除率可达99%以上.
3.2 CuO投量越大,pH值越低,反应进行越快.
3.3 富氧状态抑制NDMA还原反应的进行.
3.4 转速过快或过慢都会影响反应的进行.
3.5 随着NDMA的降解,UDMH和DMA随之生成,催化加氢被认为是该反应的机理.
[1]吕 娟,沈 静,曹先仲,等.药物对A/A/O系统中NDMA及其总前体物去除的影响 [J]. 中国环境科学, 2015,35(5):1335-1342.
[2]杨 娟,李咏梅.纳米零价铁去除水中微量 N-亚硝基二甲胺的研究 [J]. 中国环境科学, 2014,34(7):1696-1702.
[3]Mitch W A, Sharp J O, Trussell R R, et al. NNitrosodimethylamine (NDMA) as a drinking water contaminant:a review [J]. Environmental Engineering Science, 2003,20(5):389-404.
[4]Planas C, Palacios O, Ventura F, et al. Analysis of nitrosamines in water by automated SPE and isotope dilution GC/HRMSOccurrence in the different steps of a drinking water treatment plant, and in chlorinated samples from a reservoir and a sewage treatment plant effluent [J]. Talanta, 2008,76(4):906-913.
[5]Bei E, Shu Y, Li S, et al. Occurrence of nitrosamines and their precursors in drinking water systems around mainland China [J]. Water Research, 2016,98:168-175.
[6]Asami M, Oya M, Kosaka K. A nationwide survey of NDMA in raw and drinking water in Japan [J]. Science of the Total Environment, 2009,407(11):3540-3545.
[7]Krauss M, Longrée P, Dorusch F, et al. Occurrence and removal of N-nitrosamines in wastewater treatment plants [J]. Water Research, 2009,43(17):4381-4391.
[8]Ma F, Wan Y, Yuan G, et al. Occurrence and source of nitrosamines and secondary amines in groundwater and its adjacent Jialu river basin, China [J]. Environmental Science & Technology, 2012,46(6):3236-3243.
[9]Wang W, Hu J,Yu J, et al. Determination of NDMA in drinking water by UPLC-MS/MS [J]. Journal of Environmental Sciences, 2010,22(10):1508-1512.
[10]Luo Q, Wang D, Wang Z. Occurrences of nitrosamines in chlorinated and chloraminated drinking water in three representative cities, China [J]. Science of the Total Environment, 2012,437(20):219-225.
[11]王文成,吴德礼,马鲁铭,等.零价金属还原降解水中污染物的应用研究综述 [J]. 四川环境, 2007,26(3):99-103.
[12]Gui L, Gillham R W, Odziemkowski M S. Reduction of N-Nitrosodimethylamine with granular iron and nickel-enhanced iron. 1. pathways and kinetics [J]. Environmental Science & Technology, 2000,34(16):3489-3494.
[13]Li B, Qu J, Liu H, et al. Effects of copper(II) and copper oxides on THMs formation in copper pipe [J]. Chemosphere, 2007, 68(11):2153-2160.
[14]Zhang H, Andrews S A. Factors affecting catalysis of copper corrosion products in NDMA formation from DMA in simulated premise plumbing [J]. Chemosphere, 2013,93(11):2683-2689.
[15]陈忠林,徐冰冰,齐 虹,等.高效液相色谱测定水中痕量亚硝基二甲胺 [J]. 中国给水排水, 2007,23(8):84-87.
[16]韩 莹,陈忠林,沈吉敏,等.高效液相色谱法测定水中痕量偏二甲肼 [J]. 哈尔滨工业大学学报, 2013,45(8):34-38.
[17]Han Y, Chen Z, Shen J, et al. The role of Cu(II) in the reduction of N-nitrosodimethylamine with iron and zinc [J]. Chemosphere, 2017,167:171-177.
[18]Bransfield S J, Cwiertny D M, Roberts A L. Influence of copper loading and surface coverage on the reactivity of granular iron toward 1,1,1-trichloroethane [J]. Environmental Science & Technology, 2006,40(5):1485—1490.
[19]Davie M G, Reinhard M, Shapley J R. Metal-catalyzed reduction of N-Nitrosodimethylamine with hydrogen in water [J]. Environmental Science & Technology, 2006,40(23):7329-7335.
[20]唐 顺,杨宏伟,王小亻毛,等.铸铁还原氯乙酸的影响因素与机制研究 [J]. 环境科学, 2014,35(3):972-978.
[21]Odziemkowski M S, Gui L, Gillham R W. Reduction of N-Nitrosodimethylamine with granular iron and nickel-enhanced iron. 2. mechanistic studies [J]. Environmental Science & Technology, 2000,34(16):3495-3500.
[22]Han Y, Chen Z, Tong L, et al. Reduction of NNitrosodimethylamine with zero-valent zinc [J]. Water Research, 2013,47(1):216-224.
[23]Lund H, Krabisch L, Zimmer E C. Electroorganic Preparations. III. Polarography and Reduction of N-Nitrosamines [J]. Acta Chemica Scandinavica, 1957,11:990-996.
Copper oxide-catalyzed reduction of N-nitrosodimethylamine with zero-valent iron in water.
HAN Ying1, WANGJi-he1, LI Jun2*, LI Wei-wei1, JIANG Bei-bei1, YAO Jie1(1.College of Civil Engineering and Architecture, Zhejiang University of Technology, Hangzhou 310014, China;2.College of Environment, Zhejiang University of Technology, Hangzhou 310014, China). China Environmental Science, 2017,37(6):2100~2105
To remove the environmental pollution of N-nitrosodimethylamine (NDMA), copper oxide (CuO) was utilized to catalyze the NDMA reduction with zero-valent iron. The reaction efficiency, the influences of the CuO dosage, pH value, dissolved oxygen concentration and rotation speed were investigated. The products were analyzed and the kinetic laws and reaction mechanism were also discussed. The results indicated that CuO could effectively catalyze the reduction of NDMA with zero-valent iron. The removal efficiency could be greater than 99% after 18h. The reaction proceeded faster with higher dosage of CuO and lower pH value. Oxygen-enriched state inhibited the reduction of NDMA. The reaction will be affected when the reactor speed was too fast or too slow.1,1-dimethylhydrazine (UDMH) and dimethylamine (DMA) formed with the degradation of NDMA. Catalytic hydrogenation was proposed as the mechanism.
copper oxide (CuO);N-nitrosodimethylamine (NDMA);zero-valent iron;catalysis;reduction
X52,X131.2
A
1000-6923(2017)06-2100-06
韩 莹(1986-),女,河南周口人,讲师,博士,主要研究方向为金属还原技术.发表论文10余篇.
2017-01-03
浙江省自然科学基金项目(LQ15E080009);国家自然科学基金项目(51508510);国家级大学生创新创业训练计划(201610337016);浙江省环境科学与工程重中之重学科开放基金(20150307)
* 责任作者, 教授, tanweilijun@zjut.edu.cn
