蒽与叔丁醇Friedel-Crafts烷基化反应
2017-03-07叶金鑫周明东
叶金鑫, 孙 京, 王 欣, 周明东
(辽宁石油化工大学 化学与材料科学学院,辽宁 抚顺 113001)
蒽与叔丁醇Friedel-Crafts烷基化反应
叶金鑫, 孙 京, 王 欣, 周明东
(辽宁石油化工大学 化学与材料科学学院,辽宁 抚顺 113001)
分子筛催化剂是一种高效、环保、绿色的具有特定空间结构的固体酸催化剂,被广泛应用于石油化工和有机合成等领域。利用离子交换方法合成了一种酸性微孔β分子筛催化剂,并且研究了该分子筛催化剂催化蒽与叔丁醇的Friedel-Crafts烷基化反应,通过GC-MS、FT-IR、1H-NMR、元素分析等手段对反应产物进行了细致的表征。在此基础上,对蒽与叔丁醇的Friedel-Crafts烷基化反应机理进行了初步的探讨。结果表明,所合成的酸性分子筛催化剂具有较高的催化活性,异辛烷不仅仅作为反应溶剂,还能与分子筛形成叔丁基碳正离子促进反应进行,反应主要生成2-叔丁基蒽和2,6-二叔丁基蒽两种产物,具有很好的工业应用前景。
蒽; 酸性分子筛; Friedel-Crafts烷基化
Friedel-Crafts反应是一类芳香族亲电取代反应,是非常重要的有机合成反应之一[1-4]。自被发现以来,在医药、农药、燃料、香料、石油化工、日化品合成等领域中有着非常广泛的应用,因此科研工作者们对Friedel-Crafts反应的研究有着浓厚的兴趣[5-10]。Friedel-Crafts反应以Lewis酸和Brönsted酸等作为最常用的催化剂,它们催化反应活性高、反应条件温和,但是这些传统的酸催化剂用量大且不可再生,同时对设备有着严重的腐蚀性。为解决这些问题,人们一直在寻求探索环境友好的固体酸催化剂来代替强腐蚀性的液体酸催化剂。本文通过离子交换方法合成了一种酸性微孔β分子筛催化剂(Hβ),并将其成功地应用于催化蒽的烷基化反应,通过GC-MS、1H-NMR、FT-IR、元素分析等方法对烷基化产物进行分析和表征。
1 实验部分
1.1 试剂与仪器
试剂:蒽,质量分数98%,山东西亚化学工业有限公司;叔丁醇,分析纯,纯度大于99%,上海阿拉丁生化科技股份有限公司;异辛烷,分析纯,国药集团化学试剂有限公司;β分子筛,南开大学催化剂厂。
仪器:马福炉(KSL-1200X,合肥科晶材料技术有限公司);气质联用色谱仪(GC-MS,Agilent 5975C,美国安捷伦科技公司);傅里叶变换红外光谱仪(FT-IR,Spectrum GX型,美国Perkin Elmer公司);核磁共振波谱仪(1H-NMR,Varian Mercury-plus 300BB,美国Varian公司)
1.2 催化剂的制备
将β分子筛原粉在550 ℃马福炉中焙烧6 h,除去模板剂,配置过量的1 mol/L的硝酸铵溶液,再称取一定量焙烧好的β分子筛加入到硝酸铵溶液中,在80 ℃条件下回流搅拌4 h,使用大量的去离子水洗涤,然后在120 ℃烘箱内干燥,干燥后的分子筛在550 ℃马福炉中焙烧5 h,得到Hβ分子筛。
1.3 2-叔丁基蒽的合成
2-叔丁基蒽的合成反应式如图1所示。
图1 2-叔丁基蒽的合成
实验步骤:在1 000 mL装有冷凝管的三口烧瓶中加入8.0 g蒽,然后加入一定量溶剂,在一定温度下恒温搅拌,待蒽全部溶解后加入20.0 g分子筛催化剂(反应液中催化剂的颜色变成暗绿色),使用恒压滴液漏斗加入适量的叔丁醇。回流温度下反应,每隔1 h取样分析测试。反应结束后趁热过滤,用溶剂(苯)洗涤催化剂滤饼,滤液旋蒸除去溶剂后得到白色混合固体产品,催化剂滤饼经洗涤、干燥、焙烧再生后循环使用。
2 结果与讨论
由于该反应有其他副产物的生成,在蒽的烷基化反应中,对反应后的反应产物通过GC-MS分析,进一步确认生成物的种类以及类型。
2.1 2-叔丁基蒽的GC-MS分析
2-叔丁基蒽的分析条件:柱温50 ℃,进样器温度250 ℃,检测器温度250 ℃,程序升温,50 ℃开始升温,20 ℃/min升温至250 ℃,保温15.00 min。反应结束后生成物的GC谱图见图2,不同保留时间的MS谱图见图3—5。

图2 生成物的GC谱图
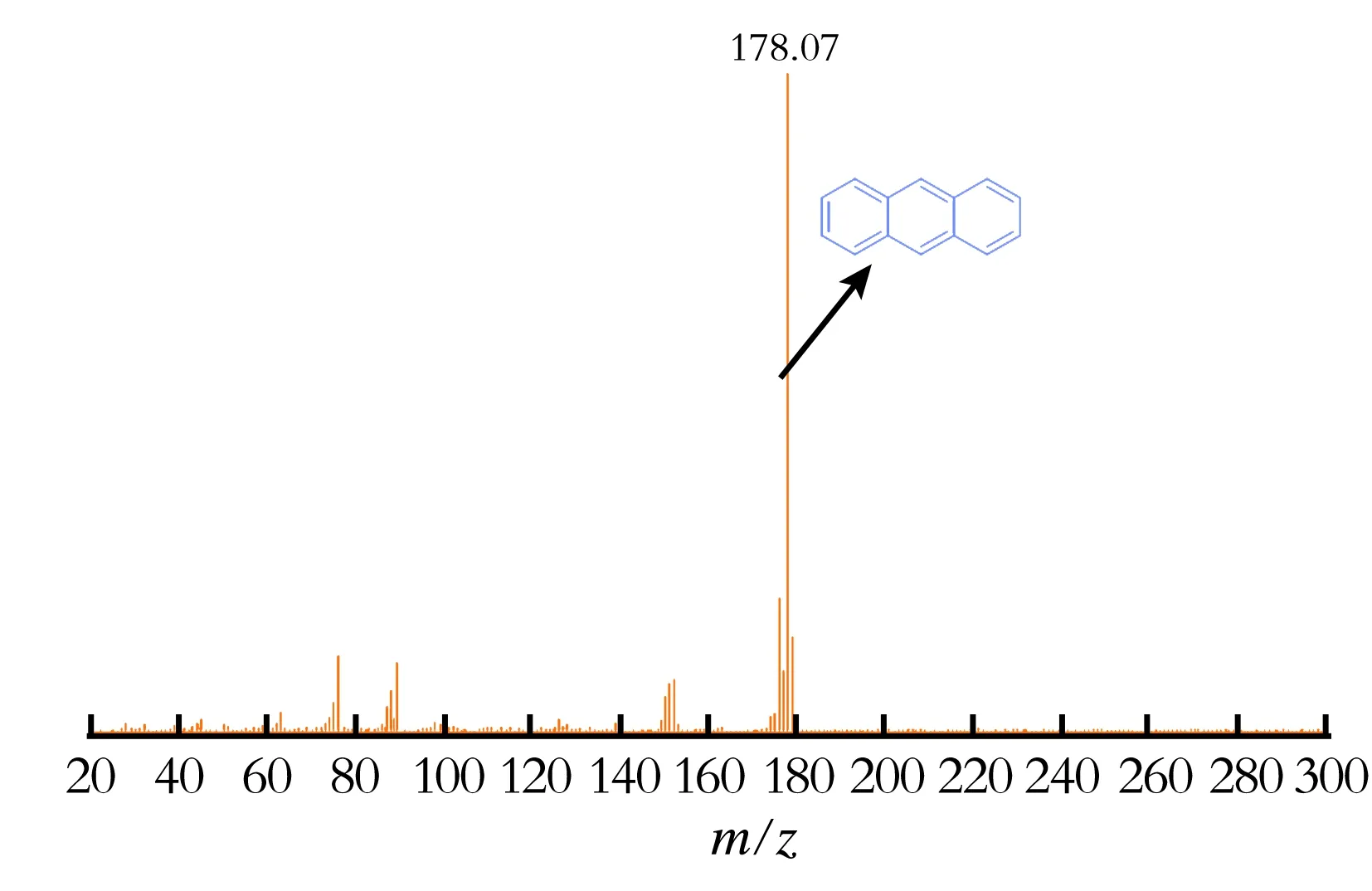
图3 保留时间在12.12 min的蒽MS谱图
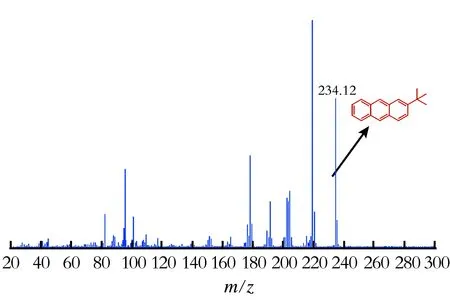
图4 保留时间在15.00 min的2-叔丁基蒽MS谱图
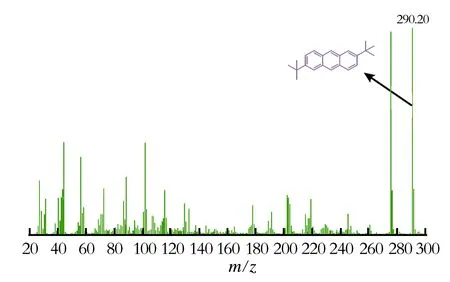
图5 保留时间在20.02 min的2,6-二叔丁基蒽MS谱图
由图2—5可以看出,保留时间在12.12 min出现的分子离子峰(m/z=178.07),恰好与原料蒽的相对分子质量吻合,保留时间在15.00 min出现的分子离子峰(m/z=234.12),恰好与生成物2-叔丁基蒽的相对分子质量吻合,保留时间在20.02 min出现的分子离子峰(m/z=290.20)恰好与2,6-二叔丁基蒽的相对分子质量吻合,由此可以推测该烷基化反应生成了主产物2-叔丁基蒽,以及二取代的2,6-二叔丁基蒽副产物。
在蒽与叔丁醇的烷基化反应中,除了生成单取代的烷基蒽主产物外,还有二取代的副产物,因此,反应结束后需要对产物进行分离提纯,得到每个生成物的产品,进行相应的分析表征。
生成物的分离与纯化:取反应结束后的白色固体适量,然后通过薄层层析柱,以石油醚为淋洗剂进行柱分离,得到纯净的单取代叔丁基蒽。
2.2 2-叔丁基蒽的红外光谱分析
图6为叔丁基蒽的红外谱图。从图6中可以看出,3 056 cm-1处的峰为蒽环上的C—H伸缩振动,1 746、1 628 cm-1处的峰为蒽环骨架的特征吸收峰,802、897 cm-1为C—H的面外弯曲振动,2 960 cm-1处为叔丁基的C—H伸缩振动。1 460、1 376 cm-1处分别为甲基摇摆振动和剪式振动。由于上述的基团均存在于2-叔丁基蒽中,从而推测该物质为2-叔丁基蒽。
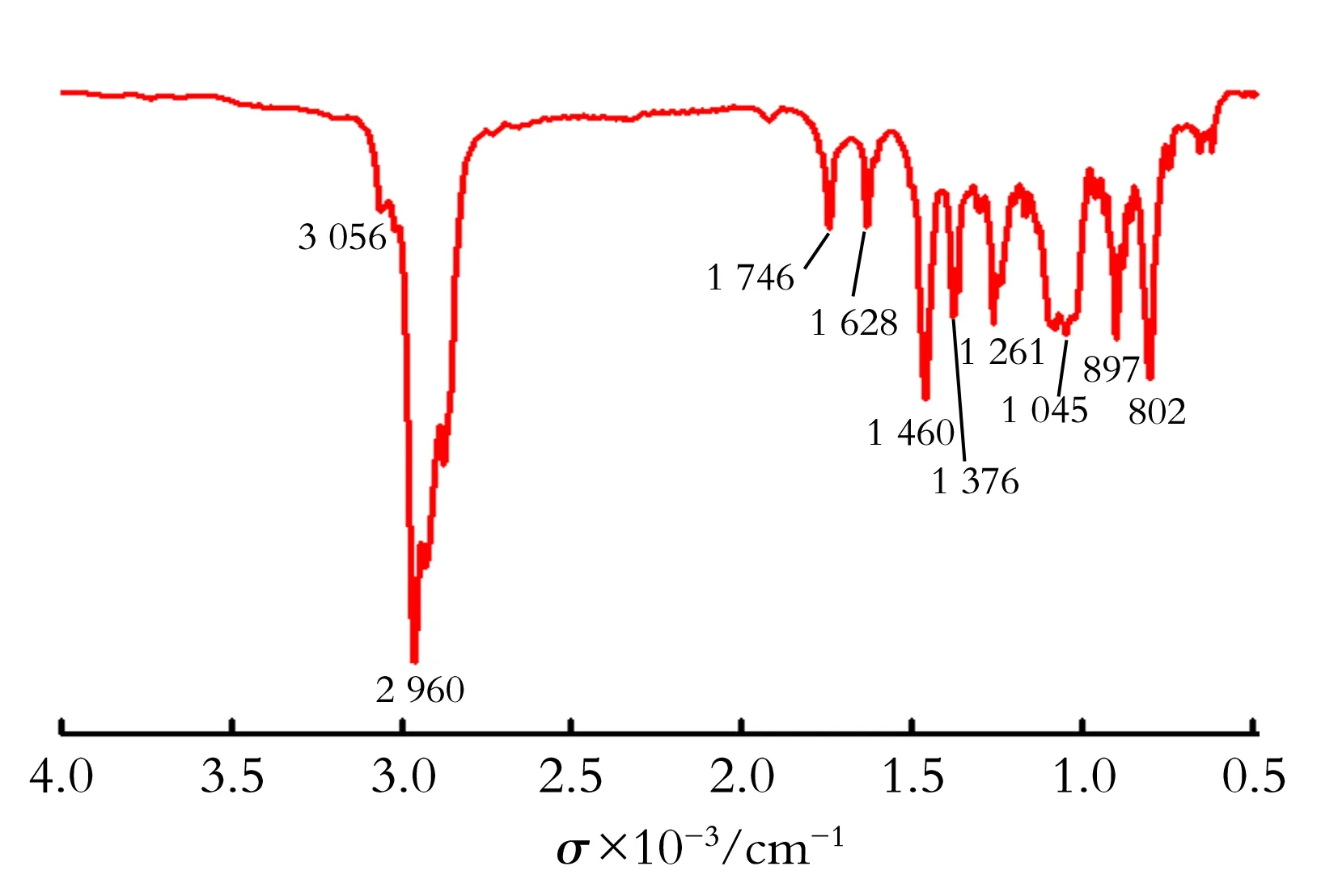
图6 叔丁基蒽的红外谱图
2.3 2-叔丁基蒽的核磁共振氢谱分析
核磁共振氢谱1H-NMR (500 MHz, DMSO-d6, rt):δ7.461~8.560 (m, 9 H), 1.406 (s, 9 H)。
图7为2-叔丁基蒽的核磁共振氢谱,对相应的蒽环区域进行了局部的放大处理。从图7中可以看出,化学位移在7.461~8.560出现的多重峰归属于蒽环上没有发生取代的位置,总共9个H,化学位移在1.406出现的单峰为叔丁基的3个—CH3上的H,由上述H的化学位移和H的个数可以推测出该物质为2-叔丁基蒽。

图7 2-叔丁基蒽的核磁共振氢谱
2.4 2,6-二叔丁基蒽的核磁共振氢谱分析
核磁共振氢谱1H-NMR (500 MHz, CDCl3, rt):δ7.533~8.320 (m, 8 H), 1.444 (s, 18 H)。
图8为2,6-二叔丁基蒽的核磁共振氢谱,对相应的蒽环区域进行了局部的放大处理。从图8中可以看出,化学位移在7.533~8.320出现的多重峰归属于蒽环上没有发生取代的位置,总共8个H,化学位移在1.444出现的单峰为2个叔丁基的6个—CH3上的H,由上述H的化学位移和H的个数可以推测出该物质为2,6-二叔丁基蒽。
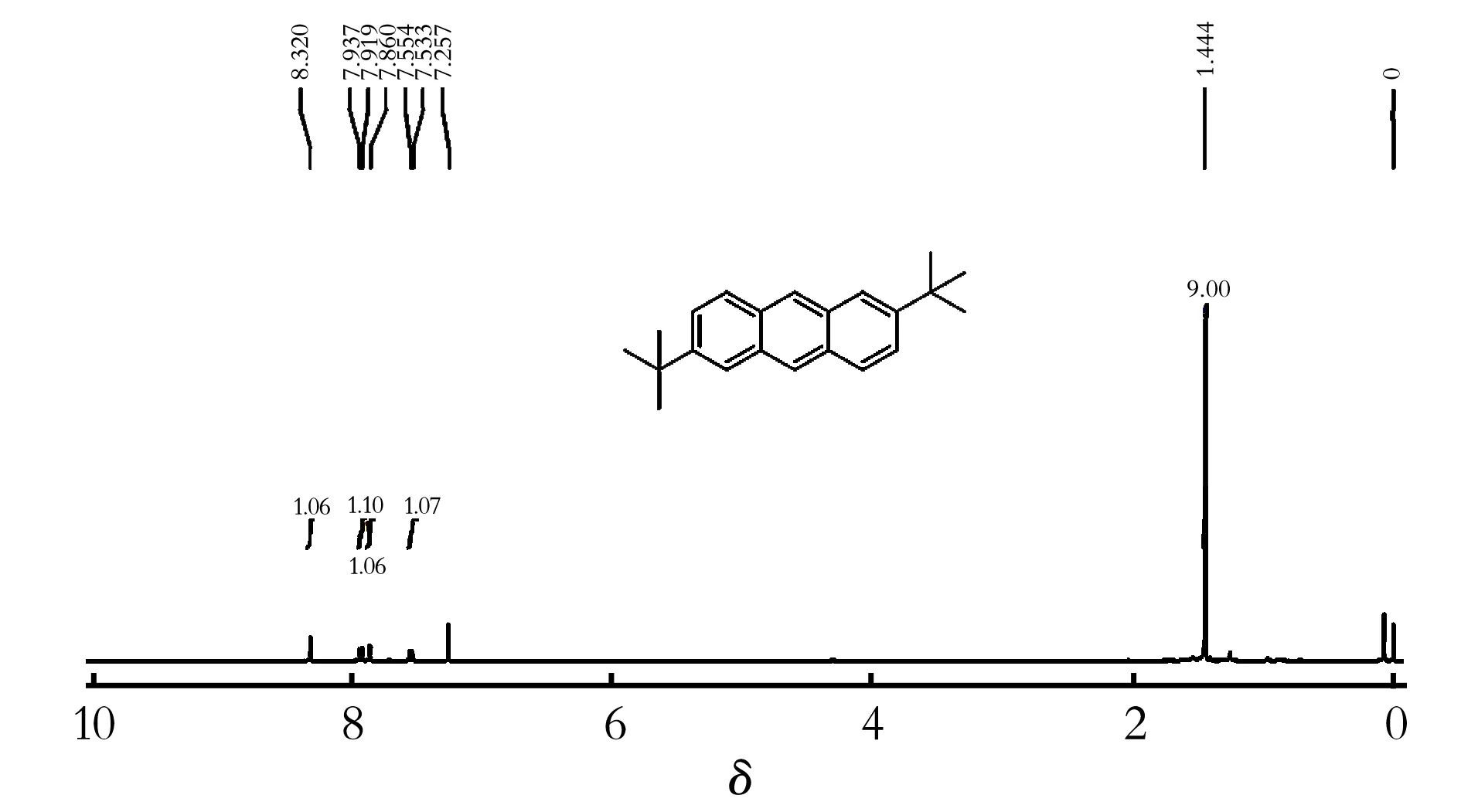
图8 2,6-二叔丁基蒽的核磁共振氢谱分析
2.5 2-叔丁基蒽的元素分析
化学式:C18H18M(234.335 5);元素分析(%)理论值:C(92.26)、H(7.74);元素分析(%)实测值:C(92.27)、H(7.73)。元素分析实测值与理论值基本一致,可初步认定其为同一物质。
2.6 蒽与叔丁醇烷基化反应机理
图9为蒽与叔丁醇的烷基化反应机理[11]。由图9可知,在沸石分子筛催化蒽与叔丁醇制备烷基蒽的反应中,2-叔丁基蒽(2-TBA)是主要产物,还有一定量的二取代的烷基蒽副产物,以及痕量的2-(1,1,3,3-四甲基丁基)蒽(2-TMBA)的生成,通过对该烷基化反应机理的研究可以看出,异辛烷在蒽与叔戊醇的烷基化反应中,不仅是该烷基化反应的溶剂还对该反应的发生起到一定的促进作用,异辛烷在一定的温度下能够与沸石分子筛形成叔丁基碳正离子促进反应的进行。
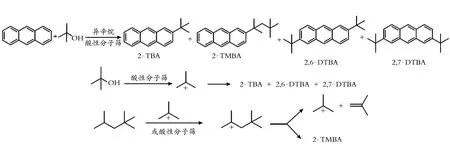
图9 蒽与叔丁醇的烷基化反应机理
3 结 论
在蒽与叔丁醇烷基化反应中,分子筛Hβ具有较高的催化活性,通过GC-MS分析,得到2-叔丁基蒽和2,6-二叔丁基蒽两种产物,柱层析方法分别得到纯净的2-叔丁基蒽和2,6-二叔丁基蒽,并通过1H-NMR和FT-IR检测分析为该物质。
[1] 李健,李永祥. 分子筛在异丁烷/丁烯烷基化中的应用进展[J].化工进展,2013, 32(Z1):122-126.
[2] 雷志刚,陈标华,李成岳. 苯与烯烃烷基化反应的研究进展[J].化学反应工程与工艺,2002, 18(1):1-5.
[3] 盛益飞,张安将,郑晓建,等. 有机催化的不对称傅克烷基化反应[J].有机化学,2008, 28(4):605-616.
[4] Sartori G, Maggi R. Use of solid catalysts in Friedel-Crafts acylation reactions[J].Chemical Reviews, 2006, 106(3):1077-1104.
[5] Kaur J, Kozhevnikova E F, Grifin K, et al. Friedel-Crafts acylation and related reactions catalyzed by heteropoly acids[J].Applied Catalysis A:General, 2003, 256(1-2):3-18.
[6] Jadhav A H, Chinnappan A, Hiremath V, et al. Synthesis and characterization of AlCl3impregnated molybdenum oxide as heterogeneous nano-catalyst for the friedel-crafts acylation reaction in ambient condition[J].Journal of Nanoscience and Nanotechnology, 2015, 15(10):8243-8250.
[7] Liang D Q, Li J J, Li Y N, et al. Novel and potent Lewis acid catalyst:Br2-catalyzed Friedel-Crafts reactions of naphthols with aldehydes[J].Synthetic Communications, 2016, 46(4):379-385.
[8] Nia A H, Amini A, Taghavi S, et al. A facile Friedel-Crafts acylation for the synthesis of polyethylenimine-grafted multi-walled carbon nanotubes as efficient gene delivery vectors[J].International Journal of Pharmaceutics, 2016, 502(1-2):125-137.
[9] Suzuki N, Tsuchihashi S, Nakata K. SnBr4-promoted Friedel-Crafts type dehydrative alkylation reaction of diarylmethanols with 2-naphthol derivatives[J].Tetrahedron Letters, 2016, 57(13):1456-1459.
[11] Elvira A, Avelino C, Hermenegildo G, et al. Acid zeolites as catalysts in organic reaction.tert-Butylation of anthracene, naphthalene and thianthrene[J].Applied Catalysis A:General, 1997, 149(2):411-423.
(编辑 宋官龙)
Friedel-Crafts Reaction of Anthracene withtert-Butanol
Ye Jinxin, Sun Jing, Wang Xin, Zhou Mingdong
(CollegeofChemistryandMaterialScience,LiaoningShihuaUniversity,FushunLiaoning113001,China)
Zeolite is an efficient, environment friendly, green and specific space structure solid acid catalyst, which is widely used in petrochemical and organic synthesis. The acidic property of the Hβ zeolite was prepared by using ion-exchange. The Friedel-Crafts reaction of anthracene withtert-butanol catalyzed by the zeolite catalyst was investigated. The products were fully characterized and analyzed by GC-MS, FT-IR, H-NMR and element analysis. The mechanism of this reaction was also proposed. The results showed that the isotcane not only acted as a solvent, but also formed thetert-butyl cation to accelerate the transformation; the zeolite catalyst exhibited high catalytic activity to afford the 2-(tert-butyl)anthracene and 2,6-di-tert-butytylanthracene which had a good industrial application prospects.
Anthracene; Zeolite; Friedel-Crafts alkylation
1672-6952(2017)01-0014-04
投稿网址:http://journal.lnpu.edu.cn
2016-04-13
2016-05-21
国家自然科学基金项目(21101085)。
叶金鑫(1989-),男,硕士研究生,从事催化化学及有机合成化学的研究;E-mail:598559591@qq.com。
周明东(1980-),女,博士,教授,从事金属催化和有机合成化学的研究;E-mail:mingdong.zhou@hotmail.com。
TE624.4; TQ031.2
A
10.3969/j.issn.1672-6952.2017.01.003
