塞来昔布联合化疗治疗晚期胃癌的疗效分析
2017-02-06郜娜娜马馨贺新爱
郜娜娜 马馨 贺新爱
胃癌是常见的消化道恶性肿瘤,多数患者就诊时已属中晚期,手术难以达到根治性治疗,且术后短期内易复发转移,临床上对于术后复发及晚期胃癌患者多采用多学科参与的综合治疗,联合化疗是其中重要的治疗手段,但预后不佳,5年生存率往往低于20%[1-2]。多西他赛和替吉奥联合方案作为晚期胃癌标准治疗方案之一,已广泛应用于临床。近年来,联合化疗在晚期胃癌治疗中的疗效并不理想。多数研究表明胃癌组织中环氧合酶 2(cylooxygenase-2,COX-2)高表达可影响患者预后[3],选择性COX-2抑制剂在体外可抑制胃癌细胞增殖和迁移,杀伤肿瘤细胞,增强常规化疗药物的疗效[3-5]。Mcgettigan 等[6]分析认为常规应用塞来昔布不增加心血管疾病的发生率,但由于潜在的胃肠道出血风险,很大程度上阻碍COX-2抑制剂在抗肿瘤领域进一步应用和研究。本研究采用选择性COX-2抑制剂塞来昔布联合多西他赛和替吉奥方案治疗晚期胃癌,现将结果报道如下。
1 资料和方法
1.1 一般资料
选取2013年6月至2015年6月于我院肿瘤内科住院的晚期胃癌患者为研究对象,纳入标准:⑴经组织病理学或细胞学检查确诊;⑵预计生存期>3个月;⑶KPS评分≥80分;⑷影像学检查资料齐全,根据RECIST评价标准至少有1个可测量病灶;⑸既往未接受过放疗、化疗或接受化疗患者的末次治疗时间至今间隔大于3个月;⑹治疗前心电图、肝肾功能、血常规检查均正常。共50例患者符合标准纳入研究,随机分为试验组和对照组,每组25例,试验组男性15例,女性10例,年龄34~72岁,平均年龄53岁;肿瘤TNM分期:Ⅲb期17例,Ⅳ期8例;肿瘤原发部位:胃窦12例,胃体13例;病理类型:腺癌21例,其他4例。对照组男性13例,女性12例,年龄33~71岁,平均年龄51岁;肿瘤TNM分期:Ⅲb期15例,Ⅳ期10例;肿瘤原发部位:胃窦11例,胃体14例;病理类型:腺癌22例,其他3例。两组患者性别、年龄、肿瘤临床分期、发病部位、病理类型等一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经我院医学伦理委员会批准,所有患者均知情同意,并签署化疗知情同意书。
1.2 治疗方案
两组均采用多西他赛联合替吉奥方案化疗,具体用药方法如下:多西他赛75 mg/m2,静脉输注2 h,第1天;替吉奥胶囊剂量根据体表面积个体化治疗:⑴体表面积(S)<1.25 m2,40 mg po,bid;⑵1.25 m2≤S<1.5 m2,50 mg,po,bid;⑶S≥1.5 m2,60mg,po,bid;口服14 d,休息7 d,21 d为1个周期,2个周期为1个疗程;试验组于治疗当日应用塞来昔布(西乐葆)400 mg,2次/d,饭后口服,直至病情进展或出现严重不良反应不能耐受,否则期间不减少塞来昔布口服剂量。所有患者完成2个周期化疗后评估临床疗效、不良反应和生活质量。对于疾病有效且稳定的患者继续原方案治疗6个周期,停药后门诊或住院随访,随访时间从化疗开始至死亡、失访或随访结束,随访截至2015年6月,统计无疾病进展生存期(progressive-free survival,PFS)和总生存期(overall survival,OS)。PFS定义为随机分组治疗开始至疾病进展或死亡的时间。OS定义为随机治疗开始至死亡或末次随访的时间。化疗治疗前常规应用5-HT受体拮抗剂预防性止吐治疗,同时复查血常规,Ⅲ度及其以上骨髓抑制者给予粒细胞刺激因子治疗。
1.3 疗效评价
按照WHO实体瘤评判标准评价疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD),有效率(RR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。不良反应评判按照WHO急性亚急性毒性表现分度标准,分0~Ⅳ度。生活质量评分参照Kamosky法评估,改善:与治疗前相比,治疗后提高>10分;下降:降低>10分;稳定:提高或降低≤10分。
1.4 统计学方法
采用SPSS 21.0软件进行数据分析,计数资料比较采用χ2检验,计量资料采用独立样本t检验进行比较,生存分析采用Kaplan-Meier法,组间差异比较行log-rank检验,以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效比较
2个周期化疗治疗后,试验组获CR 0例,PR 15例,SD 9例,PD 1例,RR为60%,DCR为96%;对照组获CR 0例,PR 13例,SD 10例,PD 2例,RR为52%,DCR为92%,两组RR和DCR比较差异均无统计学意义(P>0.05)。
2.2 不良反应
两组主要不良反应主要有血液学毒性、消化道反应、肝功能损害、口腔黏膜炎、末梢神经炎等,未发现消化道出血者。以0~Ⅰ度为主,不良反应发生率比较差异无统计学意义(P>0.05),见表 1。
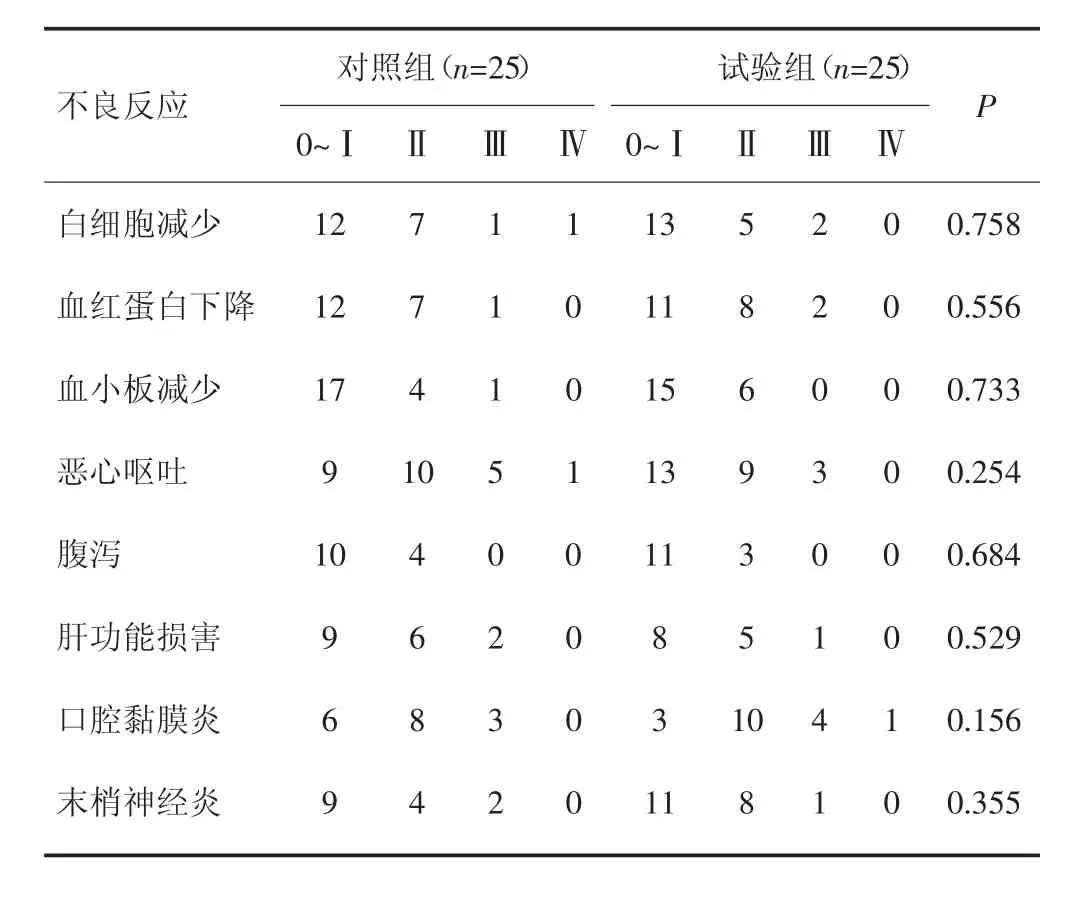
表1 两组患者主要不良反应的比较(n)
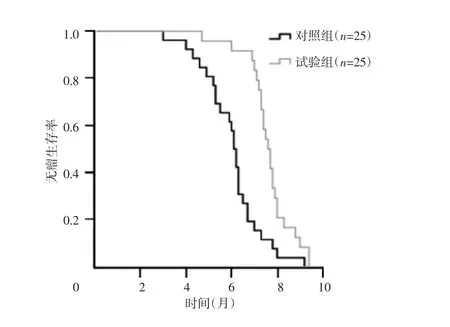
图1 试验组与对照组无疾病进展生存曲线
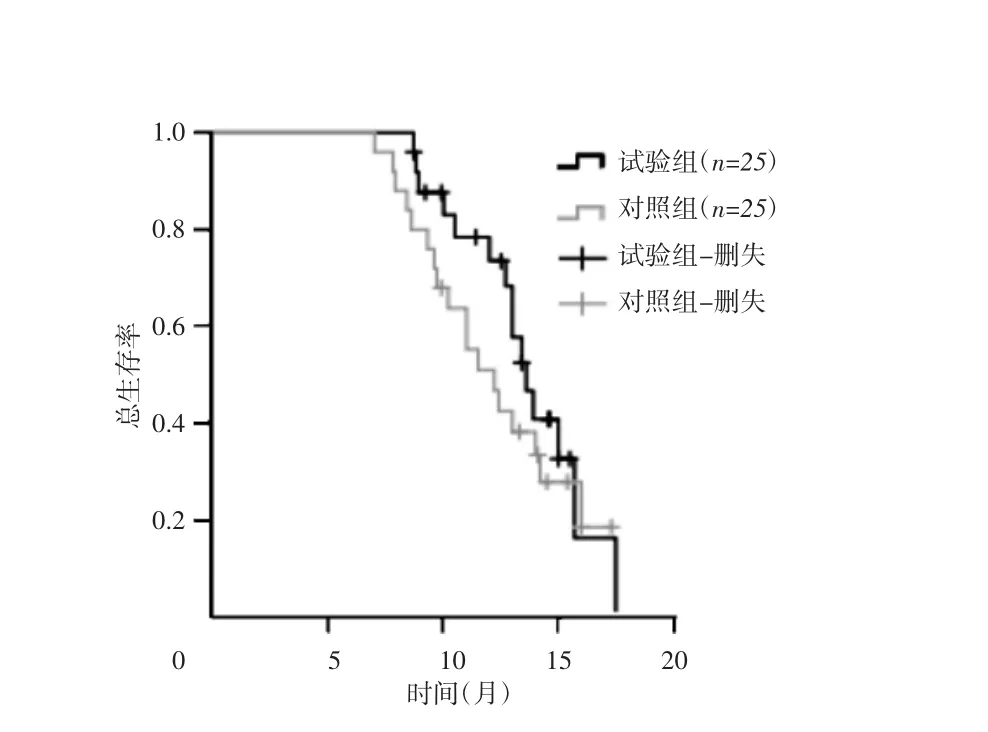
图2 试验组与对照组总生存曲线
2.3 生活质量比较
治疗后,试验组患者生活质量改善15例,稳定8例,下降2例,改善率为60%;对照组患者生活质量改善8例,稳定13例,下降4例,改善率为32%,两组改善率比较差异有统计学意义(P<0.05)。
2.4 生存情况
两组患者均出现疾病进展,试验组中位PFS为7.6个月(95%CI:7.2~7.9个月),对照组为6.3个月(95%CI:5.8~6.3个月),两组比较差异有统计学意义(P<0.05),见图1。
截至随访日期,全组50例患者失访2例,随访率为96%;48例患者中存活17例,死亡31例。试验组中位OS为13.6个月(95%CI:12.4~14.7个月);对照组中位 OS为 12.2个月(95%CI:10.0~14.3个月),两组比较差异无统计学意义(χ2=1.003,P=0.317),见图 2。
3 讨论
胃癌是消化系统常见的恶性肿瘤之一,发病率及死亡率呈上升趋势,晚期胃癌以化疗为主要治疗手段,但无统一的“金标准”方案,常采用联合化疗,如多西他赛联合替吉奥方案[7]。塞来昔布作为选择性COX-2抑制剂,具有解热、抗炎、镇痛等作用。在近年研究[8-10]中显示了多种抗肿瘤效果,可能与通过抑制COX-2诱导前癌物质活化、诱导肿瘤血管生成、抑制肿瘤细胞凋亡、增强肿瘤细胞侵袭能力及免疫抑制等作用有关,具体机制尚需进一步研究证实。黄茂涛等[11]研究发现应用塞来昔布联合奥曲肽,有助于抑制胃癌细胞在人体内转移。冉俊涛等[12]采用塞来昔布对胃癌患者进行术前短期干预,发现可显著下调E-cadherin表达,推测其可能改善患者预后。多项研究[4,13]亦发现替吉奥联合塞来昔布治疗晚期胃癌安全、有效,且可改善患者机体免疫功能,耐受性良好。
本研究纳入50例晚期胃癌患者,对照组采用多西他赛联合替吉奥方案化疗,试验组在对照组的基础上加用口服C0X-2抑制剂塞来昔布,结果显示,1个疗程治疗后,试验组有效率和疾病控制率均略高于对照组,但差异无统计学意义。不良反应方面,两组均出现血液学毒性、消化道反应、肝功能损害、口腔黏膜炎、末梢神经炎等不良反应,但均以0~Ⅰ度为主,差异无统计学意义,且均未出现COX-2抑制剂潜在的消化道出血不良反应和化疗相关性死亡,说明多西他赛+替吉奥联合塞来昔布治疗晚期胃癌可获得较好的近期疗效,且不增加不良反应,具有一定安全性。进一步通过随访发现,试验组中位PFS高于对照组;中位OS(13.6个月)略高于对照组(12.2个月),但差异无统计学意义。对于试验组PFS优势未能转换为OS获益,考虑可能与本研究观察例数较少及中位PFS评价的主观偏移有关。
综上所述,塞来昔布联合多西他赛和替吉奥方案可改善晚期胃癌患者生活质量,获得良好的近期疗效,具有一定安全性,同时可延长PFS,但OS未明显获益。由于本研究观察例数较少,数据有一定局限性,有关结论尚需进一步研究证实。
[1] 左婷婷,郑荣寿,曾红梅,等.中国胃癌流行病学现状[J].中国肿瘤临床,2017,44(1):52-58.
[2] 邹文斌,李兆申.中国胃癌发病率及死亡率研究进展[J].中国实用内科杂志,2014,34(4):408-415.
[3] 张彬,周业江.胃癌中COX-2的表达及其与胃癌淋巴结转移的关系[J].实用医学杂志,2011,27(18):3320-3323.
[4] 寇卫政,杨留中,褚秀峰,等.替吉奥联合塞来昔布治疗晚期胃癌疗效观察[J].新乡医学院学报,2015,32(4):336-339.
[5] Wang Z,Chen JQ,Liu JL.COX-2 inhibitors and gastric cancer[J].Gastroenterol Res Pract,2014,2014:132320.
[6] Mcgettigan P,Henry D.Cardiovascular risk with non-steroidal antiinflammatory drugs:systematic review of population-based controlled observational studies[J].PLoS Med,2011,8(9):e1001098.
[7] 郑盈盈,李同荟,王少雄.塞来昔布抗消化道肿瘤作用机制的研究进展[J].临床合理用药杂志,2017,10(23):176-178.
[8] Ugras N,Özgün G,Ocakolu G,et al.Relationship between HER-2,COX-2,p53 and clinicopathologic features in gastric adenocarcinoma.Do these biomarkers have any prognostic significance?[J].Turk J Gastroenterol,2014,25(Suppl 1):176-181.
[9] Su HJ,Zhang Y,Zhang L,et al.Methylation status of COX-2 in blood leukocyte DNA and risk of gastric cancer in a high-risk Chinese population[J].BMC Cancer,2015,15:979.
[10] Meng C,Lu Z,Fang M,et al.Effect of celecoxib combined with chemotherapy drug on malignant biological behaviors of gastric cancer[J].Int J Clin Exp Pathol,2014,7(11):7622-7632.
[11]黄茂涛,陈志新,魏兵,等.塞来昔布联合奥曲肽抑制人胃癌生长的临床研究[J].中华消化杂志,2005,25(9):534-538.
[12]冉俊涛,周永宁,唐承薇,等.塞来昔布术前干预对人胃癌组织E钙粘蛋白表达的影响[J].癌症,2009,28(4):361-365.
[13]田丹,汪森明,李华珍,等.塞来昔布联合XELOX方案治疗晚期胃癌的临床研究[J].广州医科大学学报,2017,45(1):63-65.
