基于咔唑的双光子荧光次氯酸根探针光学性质及响应机理
2016-12-29张玉瑾王传奎
王 昕 张玉瑾 王传奎
(山东师范大学物理与电子科学学院,济南250014)
基于咔唑的双光子荧光次氯酸根探针光学性质及响应机理
王 昕 张玉瑾 王传奎*
(山东师范大学物理与电子科学学院,济南250014)
采用含时密度泛函理论与响应函数理论相结合的方法,研究了两种实验室新合成的水溶性双光子荧光次氯酸根(ClO-)探针分子HCH和HCM的单光子吸收、双光子吸收和荧光发射性质。计算结果表明,HCH和HCM分子与ClO-反应后,生成物的光吸收和光发射性质均发生明显变化,相应的吸收和发射峰位都发生了明显蓝移,荧光强度展现出明显的增强。另外,两探针分子都具有较大的双光子吸收截面,且与ClO-反应后,生成物的双光子吸收截面值显著增加,因此两分子均可作为性能优良的双光子荧光探针分子。此外,通过分析HCH和HCM分子与ClO-反应前后的Mulliken电荷布居情况,从理论上证实了该系列荧光探针分子的识别机理是C=N异构化。
荧光探针;双光子吸收;次氯酸根;C=N异构化
1 引言
作为人体内重要的活性氧之一,次氯酸根(ClO-)直接参与生命体众多的生理过程,在生命活动中发挥着至关重要的作用1-4。一方面,次氯酸根能够维持细胞内的氧化还原平衡状态,同时在免疫系统中展现出强大的抗菌能力5,6。另一方面,过量的次氯酸根又会导致组织损伤,并且引发一系列疾病,例如动脉硬化症、关节炎等7-9。因此,对次氯酸根的探测成为一个重要的研究课题。在诸多的探测方法中,荧光显微法由于具有高效、灵敏等一系列优势而被广泛采用。
近年来,开发新型次氯酸根荧光探针越来越受到人们的关注。Cheng等10设计合成了基于氟硼吡咯的HClO探针,该探针分子的三苯基磷基团能够靶向活细胞的线粒体,实验结果显示,该探针分子能够对次氯酸实现特异性识别,随着次氯酸的滴定,溶液展现出肉眼可区分的颜色转变。Xiao等11以吩噻嗪基团作为荧光团,以季铵化吡啶部分作为线粒体的靶向基团,设计合成了ClO-荧光探针PZ-Py。并利用该探针实现了对巨噬细胞和活体细胞中内源性ClO-的荧光成像检测。然而,之前所报道的多数次氯酸根探针分子,包括以上提到的两探针,都是基于单光子激发的荧光探针分子。单光子荧光显微技术由于短波激发限制了其在深层成像中的应用,并伴有光损伤、光漂白等危害。近几年来,双光子荧光显微因其高选择性和灵敏度,能够实时检测,数据采集简单快捷,时空分辨率高等优点而被广泛应用12-18。
近日,Li等19在实验上合成了基于咔唑的水溶性双光子荧光探针分子HCH和HCM,两探针分子均以肟基团作为ClO-的识别基团,利用该系列探针分子能够实现长波激发下,对ClO-的快速响应、高选择性识别以及活细胞中ClO-的检测和生物成像。尽管实验测量结果显示HCH和HCM探针分子展现出良好的应用前景,但目前两探针分子的响应机理尚未得到充分的理论研究。另外,虽然末端烷基基团对探针分子探测性能的影响在实验工作中得到了讨论,但是仍然缺乏相关的理论研究。本文中,采用含时密度泛函理论(TDDFT)和响应理论相结合的方法,系统地研究了实验室合成的双光子荧光探针分子HCH和HCM与ClO-反应前后的单、双光子吸收和荧光发射性质,并在此基础上通过分析分子体系电荷布居探究了其响应机理。
2 计算方法
本文所使用的理论方法参见文献20,这里仅给出计算细节。在B3LYP水平上优化了分子的基态几何结构,基于优化得到的分子基态几何结构,在密度泛函理论(DFT)/CAM-B3LYP水平上采用响应理论方法计算了分子的单光子吸收性质,包括激发能、激发波长、振子强度和跃迁特性。基于相同的分子基态几何结构,在DFT/B3LYP水平上计算了分子最低八个激发态的双光子吸收性质,包括激发能、对应的双光子吸收波长和双光子吸收截面。在含时密度泛函理论/B3LYP水平上优化了分子第一激发态的几何结构并得到了分子的荧光发射性质。其中,分子结构优化是在Gaussian 09程序包21上进行的,同时为了确保优化后结构的稳定性,我们在相同的计算水平上进行了频率计算;分子单光子吸收、荧光发射性质的计算是在Gaussian 09程序包上进行的,双光子吸收性质的计算是在Dalton 2013.3程序包22上进行的。以上计算均选用了6-31g**基组,并采用极化连续模型(PCM)来描述周围的溶剂环境水(H2O)和二甲亚砜(DMSO)对分子光学性质的影响。为了直观地展现分子电荷分布,我们利用GaussView 5.0做出了分子的静电势(MEPs)图。
3 结果与讨论
3.1 分子结构
荧光探针分子HCH和HCM的几何结构如图1所示,两分子都以肟基团作为ClO-的识别基团,而其吡啶所连的末端基团分别为己基和甲基。探针分子HCH和HCM与ClO-反应后,肟基团发生氧化脱氢作用生成氧化腈,碳氮双键被氧化成碳氮三键,对应的生成物分别为HCH-CNO分子和HCM-CNO分子。
表1给出了水溶液中,分子优化后的部分键长和二面角情况。HCH分子的C1―N2键长为0.149 nm,将HCH分子吡啶所连的末端基团己基替换成甲基,即在HCM分子中,C1―N2键长缩短为0.148 nm。当两探针分子分别与ClO-反应后,
C10―C11、 C11=/≡N12、 N12―O13的 键 长 分 别 由0.147、0.128、0.139 nm缩短为 0.143、0.117、0.123 nm,这是由于ClO-使末端肟基团发生氧化脱氢作用引起结构上的变化而造成的。探针分子HCH和HCM的吡啶平面与咔唑平面间的二面角分别为179.564°和179.428°,与ClO-反应后,对应二面角分别为179.821°和179.652°。可见两探针分子均具有较好的平面性,并且与被探测底物作用以后,分子体系的平面性得到了增强,另外与HCM分子和HCM-CNO分子相比,HCH分子和HCHCNO分子对应的平面性更好一些,这有利于分子内电荷转移的发生,因此推测HCH分子具有更强的光吸收性质。
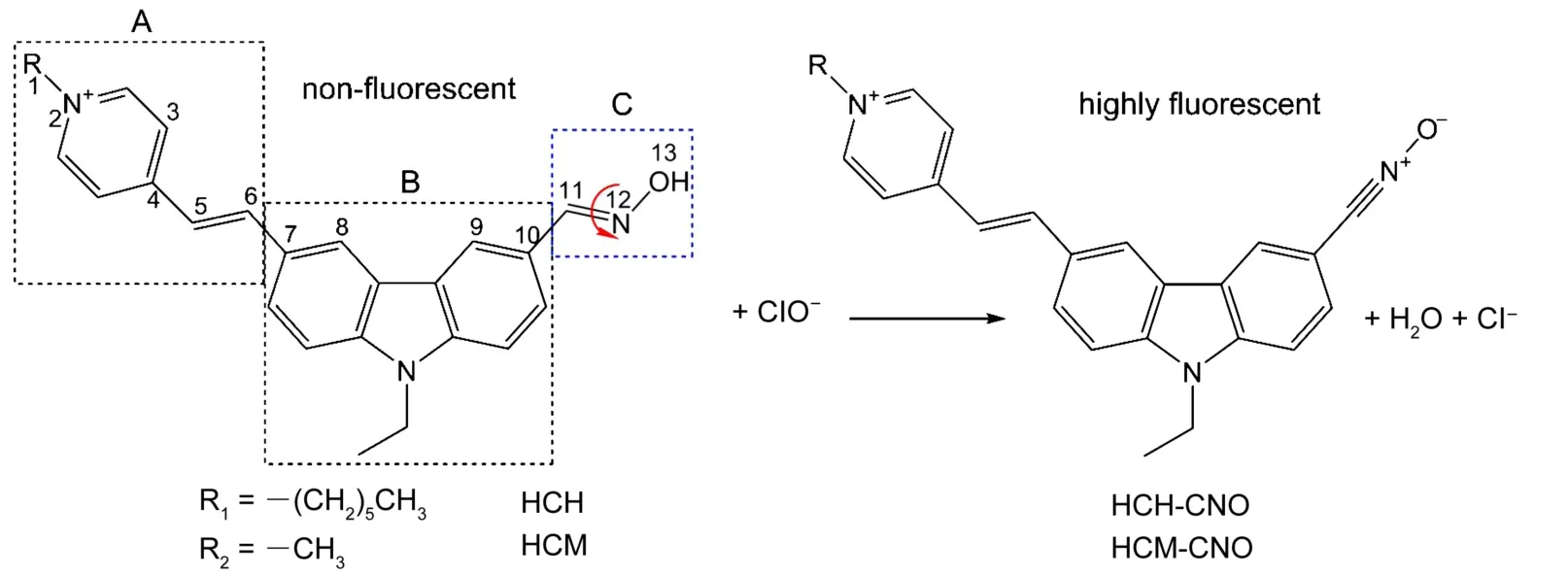
图1 探针分子HCH,HCM的几何结构示意图及与ClO-反应过程Fig.1 Geometric structures of probe molecules HCH,HCM and reaction process for sensing ClO-
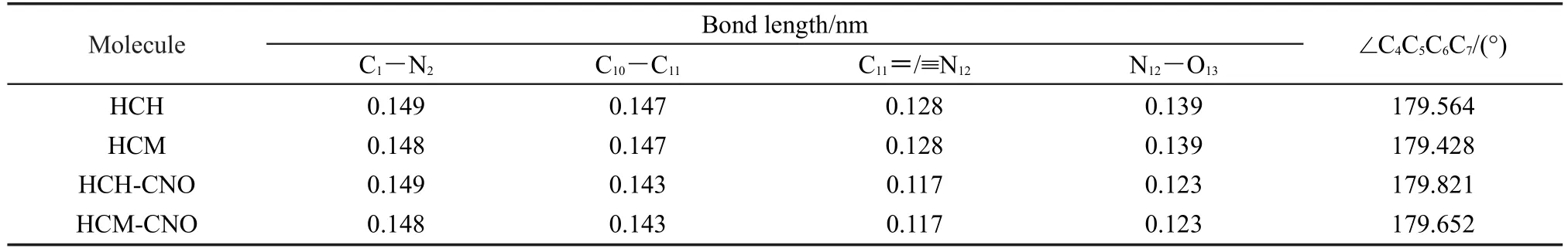
表1 水中分子优化后的部分键长和二面角Table 1 Selective bond lengths and dihedral angles of the optimized compounds in H2O
3.2 单光子吸收性质
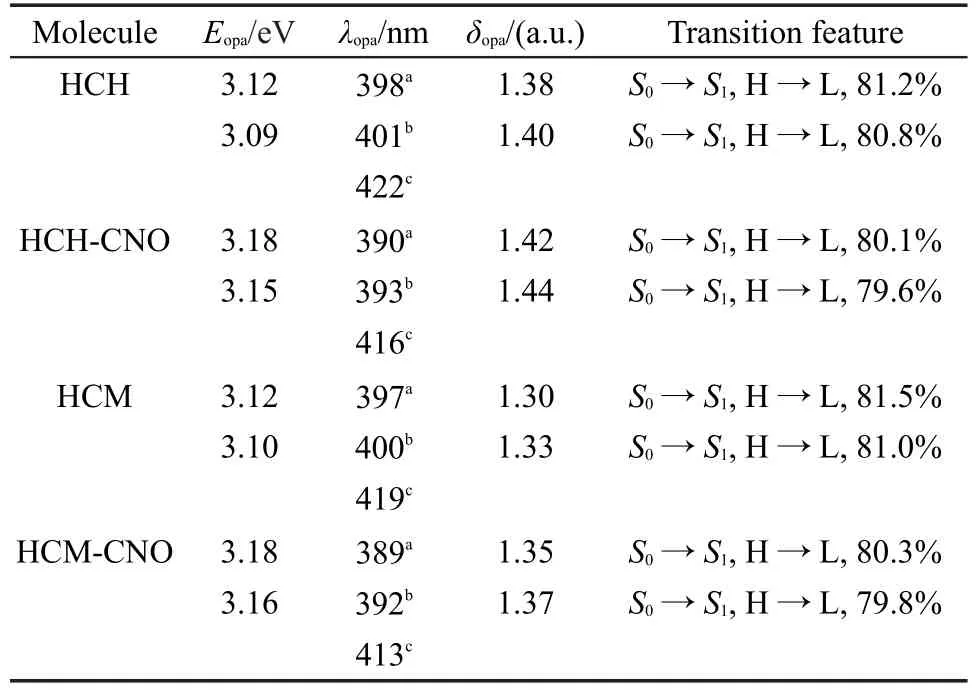
表2 分子在低能量范围内的单光子吸收性质,包括激发能(Eopa)、对应的吸收波长(λopa)、振子强度(δopa)和跃迁特性Table 2 One-photon absorption properties of the compounds in lower energy region,including the excitation energy(Eopa),the corresponding absorption wavelength (λopa),the oscillator strength(δopa),and the transition feature
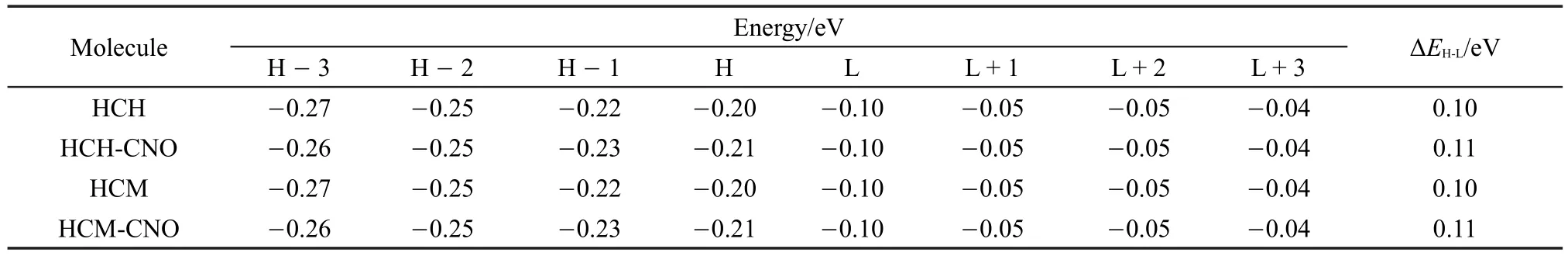
表3 水中分子的前线轨道能量Table 3 Frontier orbital energies of the compounds in H2O
3.3 双光子吸收性质
表4给出了在DMSO溶液中分子最低八个激发态对应的激发能、双光子吸收波长和双光子吸收截面。在低能量范围内,两探针分子HCH、HCM的最大双光子吸收均发生在第六激发态,其最大双光子吸收截面分别为1421、1207 GM,对应的双光子吸收峰位于618、621 nm处。与ClO-反应后,生成物HCH-CNO、HCM-CNO分子的最大双光子吸收均发生在第八激发态,其最大双光子吸收截面分别为2824、2427 GM,对应的双光子吸收峰位于600、603 nm处。两探针分子HCH、HCM在与ClO-反应后,最大双光子吸收波长均蓝移了18 nm,最大双光子吸收截面值显著增加,分别增加了1403、1220 GM。值得注意的是,与HCM-CNO分子相比,HCH-CNO分子的最大双光子吸收截面较大,这与实验测量结果定性一致19。
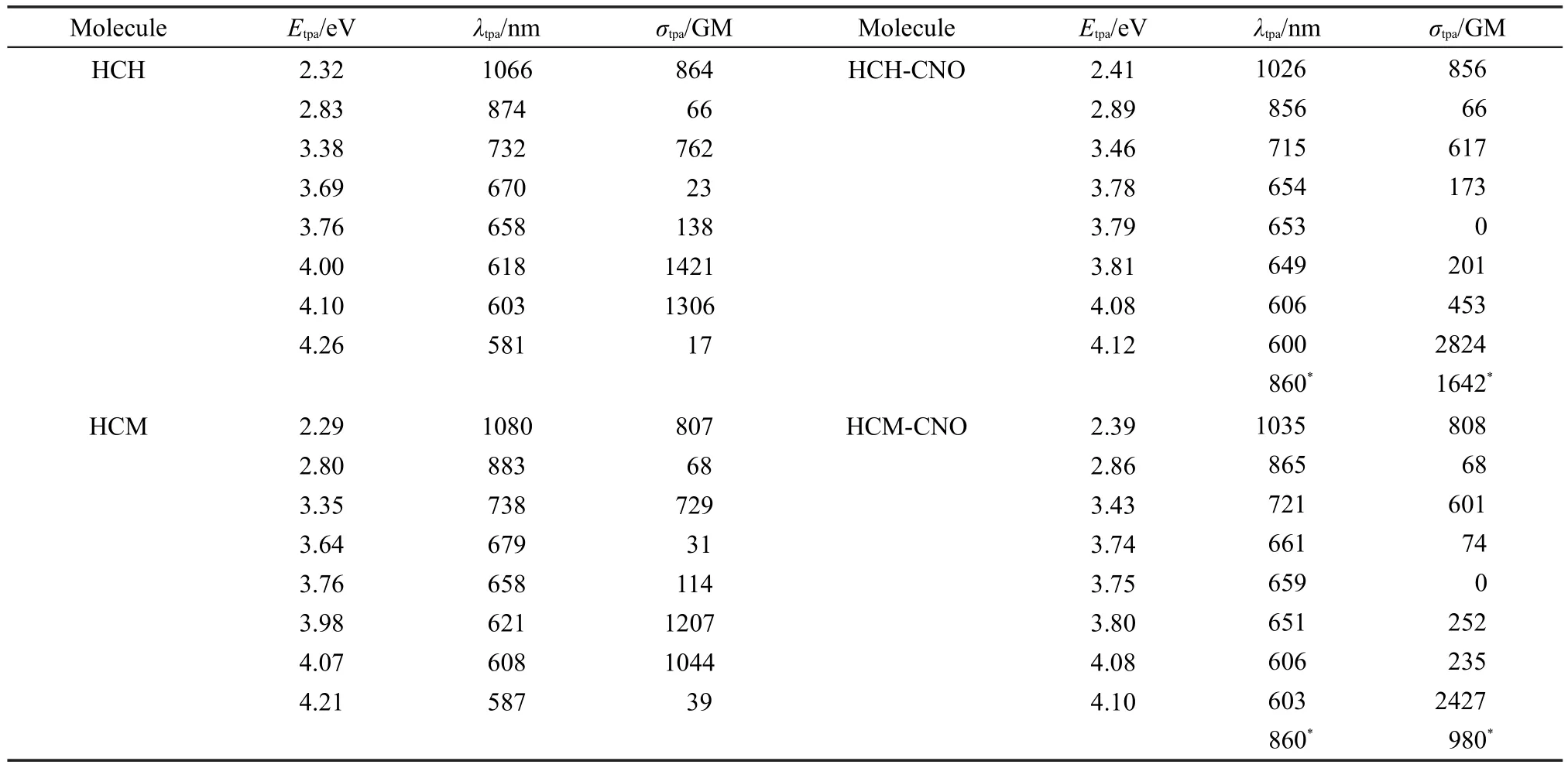
表4 分子在DMSO溶液中最低八个激发态的激发能(Etpa)、对应的双光子吸收波长(λtpa)以及双光子吸收截面(σtpa)Table 4 Excitation energy(Etpa),the corresponding two-photon absorption(TPA)wavelength(λtpa),and the TPAcross section(σtpa)of the lowest eight excited states for the compounds in DMSO solvent
表5给出了所研究的分子体系在水溶液中的双光子吸收性质,从表中可以看到,在水溶液中HCH和HCM分子的最大双光子吸收截面分别为1479、1265 GM,对应的双光子吸收波长分别位于623、621 nm处,而加入ClO-以后,分子体系的最大双光子吸收截面增加到2825和2501 GM,对应的吸收波长分别蓝移到599、602 nm处。其中,HCH和HCM分子在水溶液中的最大双光子吸收截面比在DMSO溶液中的最大双光子吸收截面均增大了58 GM,这是由于溶剂效应导致的。在同种溶剂中,HCH分子的最大双光子吸收截面大于HCM分子的最大截面,可见末端烷基长度的增加可以提高分子的双光子吸收截面,这与实验测量结果在趋势上是吻合的。而与实验测量得到的HCH-CNO和HCM-CNO分子的最大双光子吸收截面1642、980 GM相比较,理论计算的数值偏大,这主要是由于目前的理论研究忽略了光场和分子间相互作用及分子的振动对双光子吸收截面的影响。
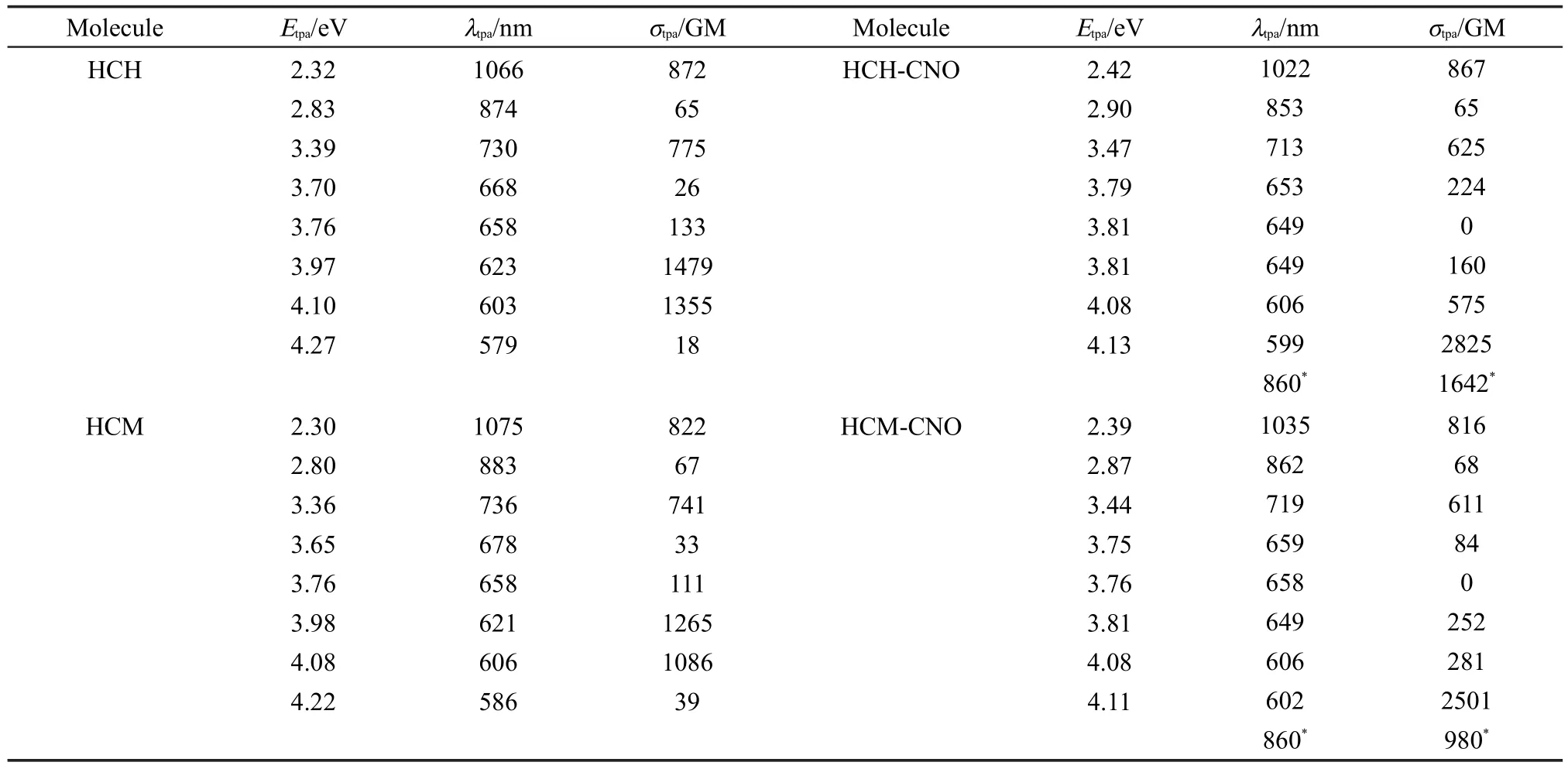
表5 分子在水中最低八个激发态的激发能、对应的双光子吸收波长以及双光子吸收截面Table 5 Excitation energy,the corresponding two-photon absorption wavelength,and the TPAcross section of the lowest eight excited states for the compounds in H2O
以上计算结果表明,两探针分子HCH和HCM均具有较大的双光子吸收截面,并且与ClO-反应后,分子的最大双光子吸收截面有不同程度的增大,这意味着两分子均可作为较好的双光子荧光探针,此外以己基作为吡啶所连的末端基团的HCH分子具有更大的双光子吸收截面,并且与反应后分子的双光子吸收能力增强更为明显,因此可以预测该分子可作为性能更优的双光子荧光探针。
3.4 荧光性质
Li等19在实验上给出了探针分子探测前后的发射波长变化情况,结果表明随着的不断滴定,含有HCH分子和HCM分子的溶液分别在546、544 nm处展现出增强的荧光发射峰。理论计算得到的分子发射能量、对应的荧光波长、振子强度、跃迁特性以及由Einstein跃迁几率公式23得到的荧光寿命在表6中列出。可以看到,HCH、HCM分子在水溶液和在DMSO溶液中的荧光发射峰位分别位于589、592 nm处和593、596 nm处,对应的荧光发射强度分别为0.59、0.56 a.u.和0.57、0.54 a.u.,与ClO-反应后,HCH-CNO、HCM-CNO分子在水溶液和在DMSO溶液中的荧光发射峰位分别蓝移到了550、553 nm处和553、557 nm处,对应的荧光发射强度增强到了0.77、0.72 a.u.和0.73、0.68 a.u.。ClO-的加入使得体系荧光强度增强,这与实验结果定性一致,说明这两分子均可作为性能优良的荧光探针。
荧光寿命是衡量探针性能的重要参数,与反应前的分子体系HCH和HCM分子相比,HCHCNO和HCM-CNO分子在水溶液和在DMSO溶液中的荧光寿命均发生了不同程度的缩短,因此与探测底物反应以后,分子发出的荧光信号更容易被探测到,这同样证明了两分子均可作为性能优异的荧光探针。另外,HCH和HCH-CNO分子具有比HCM和HCM-CNO分子更短的荧光寿命,因此HCH分子可作为性能更优的荧光探针分子。
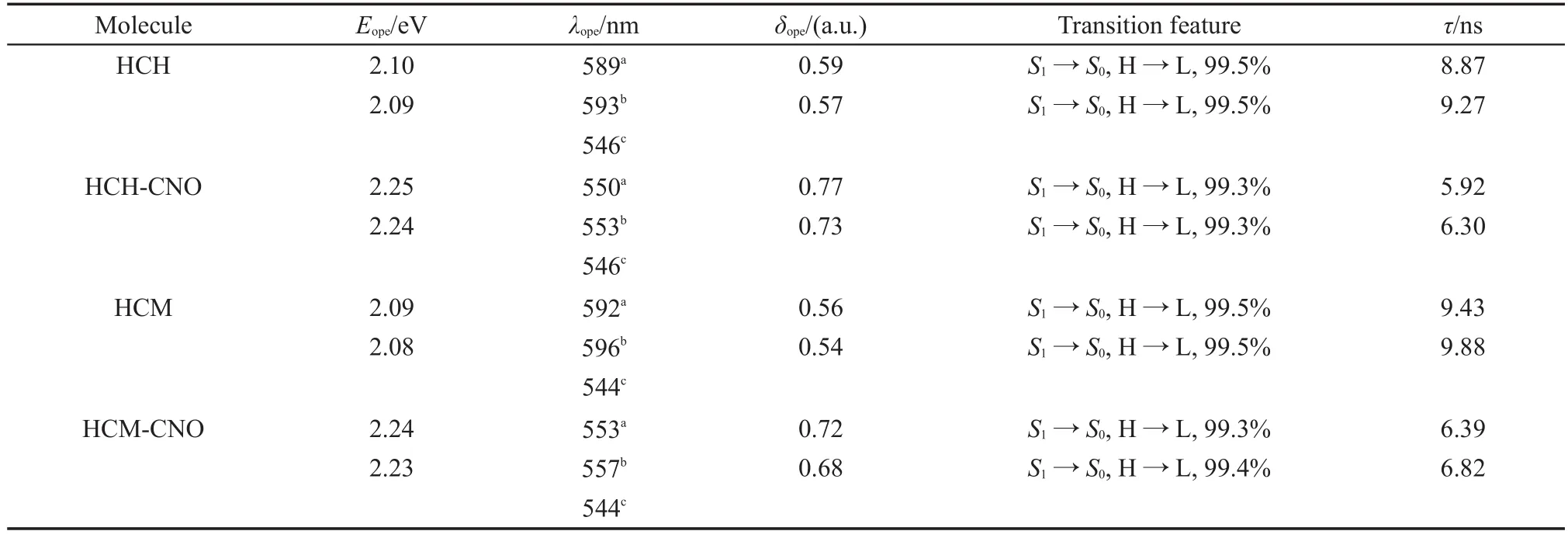
表6 分子在低能量范围内的发射性质,包括发射能(Eope)、对应的发射波长(λope)、振子强度(δope)、跃迁特性和荧光辐射寿命(τ)Table 6 Emission properties of the compounds in lower energy region,including the emission energy(Eope),the corresponding emission wavelength(λope),the oscillator strength(δope),the transition feature and the emission lifetime(τ)
3.5 响应机理
分子体系的光学性质强烈依赖于电荷分布情况,因此为了探究探针分子的响应机理,我们进一步理论计算了分子在基态和电荷转移态的Mulliken电荷分布以及在两态之间的电荷转移情况,为了更清晰地展示结果,我们将所研究的分子体系分为三个部分(见图1)。A部分和C部分为分子的末端基团,B部分为分子共轭桥部分。表7列出了各部分基态和电荷转移态的Mulliken电荷分布以及在两态之间的电荷转移情况。由表中数据可以看到,在基态时,HCH分子和HCM分子的A、B、C部分的电荷量均为0.917e、0.112e、-0.029e,与ClO-反应后,生成物HCH-CNO分子和HCM-CNO分子A、B、C部分的电荷量分别为0.927e、0.318e、-0.245e和0.926e、0.318e、-0.244e,可见ClO-的加入使得识别基团肟中的碳氮双键被氧化为碳氮三键,末端基团由―OH变为―O-,进一步影响了分子体系的电荷分布和光学性质。为了直观地看到结合对两探针分子电荷分布的影响,我们做出了分子的MEPs。如图2所示,与反应后,HCH分子和HCM分子C部分的负电荷密度稍有增大,且两探针分子在反应前后的正电荷密度都主要分布在A部分。对于两探针分子HCH和HCM,电荷分布的变化是由分子末端基团中C=N键的结构变化引起的。之前的一些报道发现,当化合物分子中含有C=N键时,C=N异构化会加剧分子的激发态的非辐射跃迁,成为激发态能量主要的衰减途径,从而使得分子荧光淬灭;当通过桥键将C=N键固定以后,C=N异构化会受到抑制,从而使得分子的荧光恢复24-27。因此该系列探针分子的响应机理可归于ClO-的加入使得C=N异构化被抑制,进而导致了荧光信号的增强。
第一激发态构型下,探针分子HCH和HCM中A、C部分的电荷量较基态构型下的电荷量增加到0.784e、-0.103e和0.783e、-0.103e,而B部分的电荷量分别减小到0.319e、0.320e,因而A、C部分均表现出得电子的能力,而B部分表现出失电子能力。与ClO-反应后,生成物HCH-CNO和HCMCNO在第一激发态构型下A、B、C基团电荷量分别为0.789e、0.480e、-0.269e和0.788e、0.481e、-0.269e。需要注意的是,探针分子与ClO-反应前后从基态到第一激发态的电荷转移量发生了较大变化。与探针分子HCH相比,HCH-CNO分子B基团的供电荷量由0.207e减小到0.162e,C基团的得电荷量由0.074e减小到0.024e。与探针分子HCM相比,HCM-CNO分子B基团的供电荷量由0.208e减小到0.163e,C基团的得电荷量由0.074e减小到0.025e。以上结果表明,ClO-的加入使得肟基团中的碳氮双键被氧化为碳氮三键,同时―OH变为―O-,因而改变了体系激发过程中的电荷转移情况。
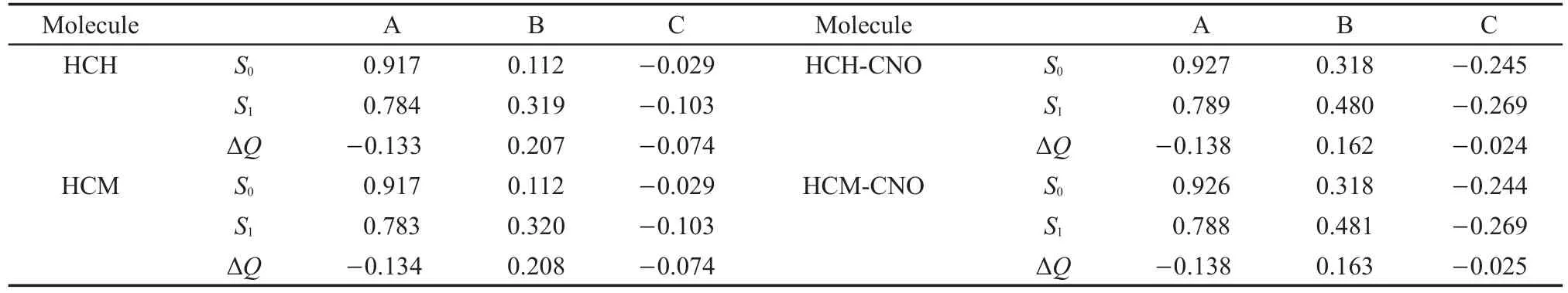
表7 分子在基态和电荷转移态下A、B、C三部分的Mulliken电荷量以及两态之间的电荷转移量Table 7 Mulliken charges of groupsA,B and C of compounds for the charge-transfer state and ground state and their charge difference
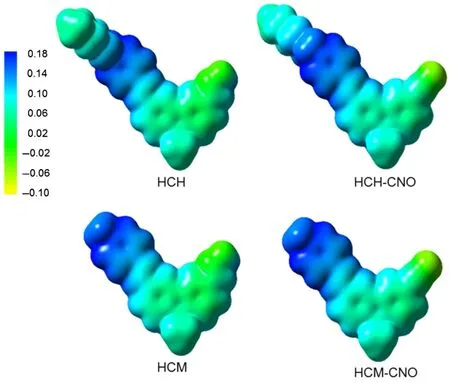
图2 分子的静电势图Fig.2 Diagram of molecular electrostatic potential
4 结论
(1) Gomes,A.;Fernandes,E.;Lima,J.L.F.C.J.Biochem. Biophys.Methods 2005,65(2),45.doi:10.1016/j. jbbm.2005.10.003
(2) Fink,M.P.Curr.Opin.Crit.Care.2002,8(1),6.doi:10.1097/ 00075198-200202000-00002
(3) Li,X.H.;Zhang,G.X.;Ma,H.M.;Zhang,D.Q.;Li,J.;Zhu, D.B.J.Am.Chem.Soc.2004,126(37),11543.doi:10.1021/ ja0481530
(4) Cui,L.L.;Zhou,D.H.;Li,M.M.Acta Phys.-Chim.Sin.2013, 29(4),745.[崔俐丽,周丹红,李苗苗.物理化学学报,2013,29 (4),745.]doi:10.3866/PKU.WHXB201302064
(5) Yuan,L.;Wang,L.;Agrawalla,B.K.;Park.S.J.;Zhu,H.; Sivaraman,B.;Peng,J.J.;Xu,Q.H.;Chang,Y.T.J.Am.Chem. Soc.2015,137,5930.doi:10.1021/jacs.5b00042
(6) Xu,Q.;Heo,C.H.;Kim,G.;Lee,H.W.;Kim,H.M.;Yoon,J. Angew.Chem.Int.Ed.2015,54,4890.doi:10.1002/ anie.201500537
(7) Pattison,D.I.;Davies,M.J.Chem.Res.Toxicol.2001,14(10), 1453.doi:10.1021/tx0155451
(8) O′Brien,P.J.Chem.Biol.Inter.2000,129(2),113. doi:10.1016/S0009-2797(00)00201-5
(9) Podrez,E.A.;Abu-Soud,H.M.;Hazen,S.L.Free Radical Biol. Med.2000,28(12),1717.doi:10.1016/S0891-5849(00)00229-X
(10) Cheng,G.H.;Fan,J.L.;Sun,W.;Sui,K.;Jin,X.;Wang,J.Y.; Peng,X.J.Analyst 2013,138,6091.doi:10.1039/c3an01152f
(11) Xiao,H.D.;Xin,K.;Dou,H.F.;Yin,G.;Quan,Y.W.;Wang,R. Y.Chem.Commun.2015,51,1442.doi:10.1039/c4cc07411d
(12) Setsukinai,K.;Urano,Y.;Kakinuma,K.;Majima,H.J.; Nagano,T.J.Biol.Chem.2003,278(5),3170.doi:10.1074/jbc. M209264200
(13) Takats,Z.;Koch,K.J.;Cooks,R.G.Analyt.Chem.2001,73 (18),4522.doi:10.1021/ac010338r
(14) Yang,W.J.;Zhang,Y.J.;Wang,C.K.Acta Phys.-Chim.Sin. 2015,31(12),2303.[杨文静,张玉瑾,王传奎.物理化学学报, 2015,31(12),2303.]doi:10.3866/PKU.WHXB201510233
(15) Zhou,D.H.;Li,M.M.;Cui,L.L.Acta Phys.-Chim.Sin.2013, 29(7),1453.[周丹红,李苗苗,崔俐丽.物理化学学报,2013,29(7),1453.]doi:10.3866/PKU.WHXB201304244
(16) Meng,X.M.;Wang,S.X.;Li,Y.M.;Zhu,M.Z.;Guo,Q.X. Chem.Commun.2012,48,4196.doi:10.1039/c2cc30471f
(17) Yin,H.J.;Zhang,B.C.;Yu,H.Z.;Zhu,L.;Feng,Y.;Zhu,M. Z.;Guo,Q.X.;Meng,X.M.J.Org.Chem.2015,80,4306. doi:10.1021/jo502775t
(18) Ning,P.;Jiang,J.C.;Li,L.C.;Wang,S.X.;Yu,H.Z.;Feng,Y.; Zhu,M.Z.;Zhang,B.C.;Yin,H.;Guo,Q.X.;Meng,X.M. Biosens.Bioelectron.2016,77,921.doi:10.1016/j. bios.2015.10.061
(19) Li,D.X.;Feng,Y.;Lin,J.Z.;Chen,M.;Wang,S.X.;Wang,X.; Sheng,H.T.;Shao,Z.L.;Zhu,M.Z.;Meng,X.M.Sens. Actuators B 2016,222,483.doi:10.1016/j.snb.2015.08.098
(20) Ding,H.J.;Sun,J.;Zhang,Y.J.;Wang,C.K.Chem.Phys.Lett. 2014,591,142.doi:10.1016/j.cplett.2013.11.015
(21) Frisch,M.J.;Trucks,G.W.;Schlegel,H.B.;et al.Gaussian 09, RevisionA.01;Gaussian Inc.:Wallingford,CT,2009.
(22) Aidas,K.;Angeli,C.;Bak,K.L.;et al.WIREs Comput.Mol. Sci.2014,4,269.doi:10.1002/wcms.2014.4.issue-3
(23) Zhang,Y.J.;Zhang,Q.Y.;Ding,H.J.;Song,X.N.;Wang,C. K.Chin.Phys.B 2015,24(2),023301.doi:10.1088/1674-1056/ 24/2/023301
(24) Wang,X.M.;Wang,X.H.;Feng,Y.;Zhu,M.Z.;Yin,H.;Guo, Q.X.;Meng,X.M.Dalton Trans.2015,44(14),6613. doi:10.1039/c5dt00012b
(25) Wu,J.S.;Liu,W.M.;Zhuang,X.Q.;Wang,F.;Wang,P.F.; Tao,S.L.;Zhang,X.H.;Wu,S.K.;Lee,S.T.Org.Lett.2007,9 (1),33.doi:10.1021/ol062518z
(26) Liu,Z.D.;Xu,H.J.;Chen,S.S.;Sheng,L.Q.;Zhang,H.;Hao, F.Y.;Su,P.F.;Wang,W.L.Spectrochim.Acta A 2015,149,8. doi:10.1016/j.saa.2015.04.030
(27) Torawane,P.;Tayade,K.;Bothra,S.;Sahoo,S.K.;Singh,N.; Borse,A.;Kuwar,A.Sens.Actuators B 2016,222,562. doi:10.1016/j.snb.2015.08.104
Optical Properties and Responsive Mechanism of Carbazole-Based Two-Photon Fluorescent Probes for the Detection of Hypochlorite
WANG Xin ZHANG Yu-Jin WANG Chuan-Kui*
(School of Physics and Electronics,Shandong Normal University,Jinan 250014,P.R.China)
The one-and two-photon absorption and emission properties of the two newly synthesized watersoluble two-photon fluorescent probes(HCH and HCM)for the detection of ClO-were investigated using timedependent density functional theory in combination with response theory.Dramatic changes in the photophysical properties of the molecules following reaction with ClO-were predicted.The photoabsorption and photoemission peaks for both compounds were clearly blue shifted,while the emission intensities were enhanced.Both probes were also found to have large two-photon cross sections.Importantly,in the presence of ClO-the two-photon cross section of the molecules increased significantly,which indicated that both HCH and HCM should be good two-photon fluorescent probes for sensing ClO-.The responsive mechanism of the probes was explored by analyzing the molecular Mulliken charge population,which was attributed to C=N isomerization.
Fluorescent probe;Two-photon absorption;ClO-;C=N isomerization
O644;O641
10.3866/PKU.WHXB201609301
Received:June 6,2016;Revised:September 30,2016;Published online:September 30,2016.
*Corresponding author.Email:ckwang@sdnu.edu.cn;Tel:+86-531-86180892.
The project was supported by the National Natural Science Foundation of China(11404193),Natural Science Foundation of Shandong Province, China(ZR2014AM026),and Taishan Scholar Project of Shandong Province,China.
国家自然科学基金(11404193),山东省自然科学基金(ZR2014AM026)和山东省泰山学者资助项目
