分级氢氧化铟材料的合成及其尿酸电化学敏感特性研究*
2016-11-12黄清优许楚峰王炳荣王小红涂进春
黄清优,黄 玮,许楚峰,王炳荣,王小红,涂进春,曹 阳
(海南大学 材料与化工学院,海南省特种玻璃重点实验室, 海口 570228)
分级氢氧化铟材料的合成及其尿酸电化学敏感特性研究*
黄清优,黄 玮,许楚峰,王炳荣,王小红,涂进春,曹 阳
(海南大学 材料与化工学院,海南省特种玻璃重点实验室, 海口 570228)
在不添加高分子表面活性剂的条件下,采用一种简单的水热合成方法制备出In(OH)3纳米材料,并应用于尿酸的非酶电化学检测。X射线衍射(XRD)和扫描电子显微镜(SEM)显示,样品具有较好结晶性和均匀的分级三维花状结构。实验发现,该材料在氢氧化钠溶液体系中对尿酸表现出良好的电催化活性,且相比于In2O3具有更好的电极稳定性。基于该材料修饰的电极对尿酸的检测极限为75 nmol/L(S/N=3),线性检测范围上限为4.969×10-4mol/L,灵敏度高达301.3 μA·mmol/L·cm2,具有良好的选择性。
氢氧化铟;尿酸;电化学
0 引 言
尿酸(2,6,8-三羟基嘌呤),是嘌呤、核酸和蛋白质的代谢产物,存在于血液、血清、尿液或生物体液中[1-2]。尿酸水平异常能反映嘌呤代谢失调和一些疾病,例如:痛风,心肌梗死和生理失调[3-4]。因此,准确检测尿酸水平对人类健康至关重要。基于尿酸酶的电化学生物传感器,具有小型化、高选择性等特点,而被广泛关注。但是,酶价格昂贵且使用条件苛刻,大大的限制了电化学生物传感器的发展[5]。因此,大家逐渐将目光转向了尿酸非酶电化学生物传感器。而在非酶电化学传感器中,敏感材料的选择与设计对于传感器的性能具有决定性的作用。
在已有的研究中,过渡金属[6]、合金[7-8]、碳纳米管[9-10]和金属氧化物[11-12]等材料常被作为尿酸非酶电极敏感材料,在这些敏感材料的催化作用下尿酸可以被直接氧化成碳水化合物而不会造成表面的污染,其工作过程主要依赖电极材料的固有电子结构和表面扩散反应。氧化铟是一种重要的n-型半导体氧化物,由于具有较宽的禁带宽度(Eg= 3.6 eV)和较高的电导率而被广泛应用于电化学等领域[13-14],其中氧化铟分级材料的设计与构筑是关键。目前的合成方法中,氧化铟大多通过高温煅烧铟的氢氧化物前驱物得到,其分级结构在高温晶化和除模板过程中不稳定,往往伴随结构的部分坍塌,增加了氧化铟结构设计与构筑的难度。In(OH)3是一种宽带隙半导体(Eg=5.15 eV),一般情况下为水热合成氧化铟材料的中间体,在过去的材料研究中往往被忽略。近期研究表明,金属氢氧化物由于设计与构筑过程相对简单,且不需要后期热处理,表面具有丰富的羟基等官能团[15],在电化学应用时具有器件稳定性高,分级结构保存完好而有利于扩散等优势。
本文在不添加任何高分子表面活性剂的情况下,通过一种简单的水热合成方法得到分散均匀的In(OH)3,避免了后期热处理除模板过程可能伴随的结构坍塌,有效保持了材料的原始分级结构。进一步的测试结果表明样品具有较好结晶性和均匀的分级三维花状结构。通过在玻碳电极表面简单滴涂的办法,制备了非酶电化学传感器电极,考察了该材料对尿酸的敏感特性。
1 实 验
1.1 In(OH)3的制备
将0.1 g InCl3·4H2O溶解到20 mL的去离子水中配成溶液,然后将0.2 g 的尿素(浓度对照实验为0.04,0.16 g)加入上述溶液中并搅拌至澄清透明。最后将溶液转移到30 mL聚四氟乙烯内衬的不锈钢反应釜中,140 ℃下密封保温12 h(时间对照实验为18,24 h)。自然冷却至室温后,离心收集白色沉淀,并用蒸馏水和无水乙醇离心洗涤数次,60 ℃下干燥12 h得到白色粉末样品。
1.2 工作电极的制备和电化学测试方法
所有电化学测量在CHI660E电化学工作站(上海辰华,中国)上进行,采用三电极体系:玻碳电极(GCE)(直径3 mm)为工作电极,Ag/AgCl电极为参比电极,Pt电极为对电极。玻碳电极用1.0,0.3和0.05 μm氧化铝粉依次抛光打磨,每次抛光后用乙醇和去离子水彻底清洗,在空气中干燥。将一定量的In(OH)3溶液(5 mg/mL)滴涂在处理好的玻碳电极表面。5 mL一定浓度的氢氧化钠作为电解质溶液备用。
1.3 材料的性能及表征
X射线衍射(XRD)图谱采用德国Bruker AXS D8衍射仪(Cu Kα,λ=0.154178 nm)测定,在管电压40 kV,管电流30 mA 下扫描。场发射扫描电子显微镜(FE-SEM)照片在JEOL JSM-6700F型场发射扫描电镜上完成。
2 结果与讨论
2.1 材料的表征及其机理分析
图1为尿素加入量为 0.2 g,140 ℃下保温12 h 所得白色粉末样品的 XRD 谱图。
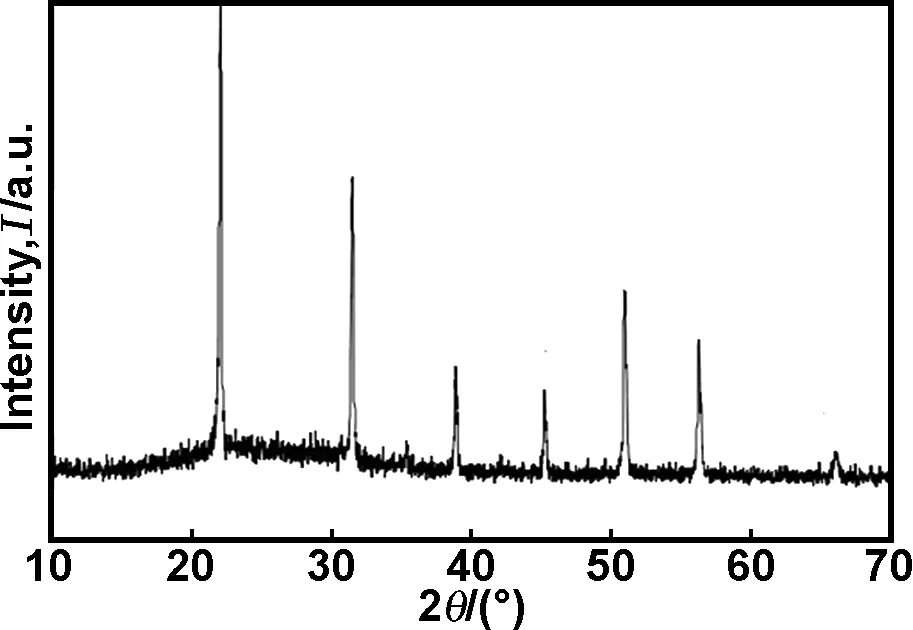
图1 所得白色粉末样品的XRD谱图
从图中可以看出,所得样品具有尖锐的衍射峰且所有的衍射峰均与In(OH)3(JCPDS 76-1463)相匹配,证明样品为体心立方相结构(空间群:Im3(204))。此外,在谱图中并没有发现其它明显的杂质峰,表明所得的样品主要为立方相In(OH)3。
图2为反应温度为140 ℃时,不同尿素浓度和水热反应时间下所得In(OH)3的FE-SEM图像。从图2(a)到(c)中,反应时间为 12 h,尿素加入量依次为0.04,0.16和0.2 g。当尿素浓度较低时(0.04 g),所得的In(OH)3产物主要为立方形貌的小颗粒且颗粒的均匀性和分散性较差(图2(a));随着尿素用量的增加(0.16 g),视野范围内出现了立方、纳米棒和纳米花几种形貌的混合物且以纳米棒和纳米花为主(图2(b));进一步将尿素的用量增加到0.2 g时,产物虽然仍存在少数方形颗粒,但基本以尺寸均匀(约3 μm)的纳米花为主,且每个纳米花由直径为100~300 nm变为800~1 000 nm的纳米棒组装而成(图2(c))。为了进一步研究纳米花的生长趋势,我们在尿素浓度为0.2 g 的基础上设置了一个时间对照实验,即:将反应时间从12 h 延长到24 h,得到图2(d)所示形貌。对比图2(d)与2(c)可以发现,随着反应时间的延长,样品的纳米花状形貌并没有明显的改变,只是组成纳米花的纳米棒略有长粗长长,纳米花颗粒的整体尺寸也由12 h的4 μm 左右变化为24 h的4.8 μm左右。

图2 140 ℃下不同尿素浓度和水热时间下所得样品的FE-SEM照片
从前面的描述中可以发现,随着体系尿素浓度的增加,所得In(OH)3颗粒的形貌有从方形逐渐转变为纳米棒,并最终由纳米棒组装成纳米花的演变规律;延长体系的水热反应时间并不会对颗粒的花状形貌造成明显改变,只是使颗粒整体长大。因此,我们就氢氧化铟可能的形成机理进行了研究。众所周知,晶体的生长分为形核和生长两个阶段,晶体生长的最终形貌与本征晶体结构和外部因素有关。氢氧化铟纳米晶生长过程的反应可如下表示[16]
(1)
(2)
(3)
(4)
当尿素浓度较低时(加入0.04 g),水解程度大,主要作用是提供OH-与In3+结合形成In(OH)3颗粒单元,溶液中以反应(1)-(3)为主。水热条件下,由于大量In(OH)3颗粒单元的存在,溶液体系能量高,In(OH)3颗粒单元开始聚集形核并进一步长大,以降低系统能量。上述过程遵从典型的热力学控制,颗粒倾向于生长成为本征立方晶体结构。因此,图1中In(OH)3的微观立方相(空间群Im3(204))晶体结构在图2(a)中的宏观立方形貌中得到了较好体现。
当尿素浓度较高时(加入 0.2 g),一方面水解提供OH-与In3+结合形成In(OH)3颗粒单元,另一方面以单分子或多分子(统一写为murea)形式起表面活性剂的作用,即溶液中除发生反应 (1)-(3) 外,还发生反应(4),这一点也尤为重要。水热反应的初期,由于溶液体系能量过高, 热力学控制在反应过程中占主导,In(OH)3颗粒单元发生典型的成核生长过程,长大为数十纳米的颗粒。此时,体系能量被降低,溶液中存在的大量尿素表面活性剂吸附在颗粒表面(反应(4)),颗粒的热力学生长过程被大大的阻碍,转而发生对系统能量要求相对较低的动力学生长过程,即:当两个临近的颗粒发生碰撞时,在表面活性剂的协同作用下,如果具有共同的晶格取向,就会沿着该方向结合生长。由于颗粒中各晶面表面能之间的差异,必定导致某些晶格方向上的择优生长,从而产生了图2(b)中的纳米棒形貌;在形成纳米棒的基础上,为了进一步降低系统能量,纳米棒倾向于进一步自组装成表面能更低的如图2(c)所示的纳米花,且随着水热反应时间的延长,纳米棒自身长粗长长。当尿素浓度适中(加入 0.16 g)时,热力学控制与动力学控制在整个水热反应过程中同时起主导作用,从而导致所得样品中同时存在立方结构和纳米花形貌的In(OH)3纳米颗粒。

图3 尿素浓度(1)较低和(2)较高情况下In(OH)3结构生长的可能形成机理
总之,尿素的用量和水热时间对In(OH)3纳米颗粒的形貌有重要的影响。尿素在整个反应过程中起着碱性介质、表面活性剂等多重作用。尿素的用量直接对反应体系中的热力学过程和动力学过程造成影响,而水热时间则对颗粒的尺寸有着直接的调控。
2.2 材料的电化学性能研究
从图4可以看出在最优配比下所得三维花状In(OH)3修饰的电极,表现出良好的导电性、低背景电流和更好的电催化活性。
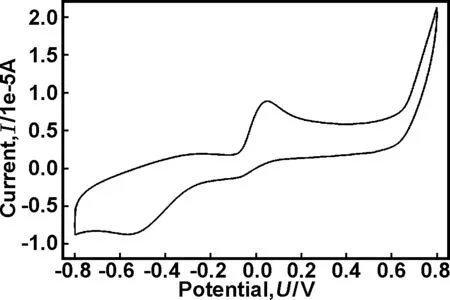
图4 In(OH)3/GCE的循环伏安图
在1 mmmol/L尿酸的0.1 mol/L氢氧化钠溶液中,电压范围从-0.8~+0.8 V,在不同的扫描率下In(OH)3修饰的玻碳电极得到的CV曲线如图4所示。其中氧化峰位于+0.07 V,还原峰位于-0.07 V,峰值差ΔEp=140 mV,表明电极表面发生了极化。
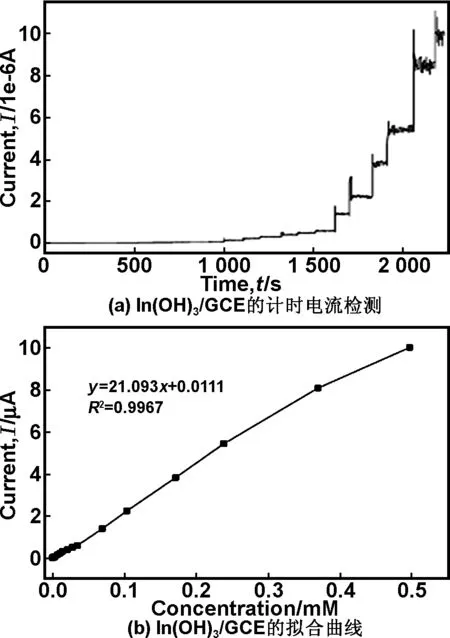
图5 In(OH)3/GCE的计时电流检测与拟合曲线
图5(a)为三维花状In(OH)3修饰的电极对尿酸的安培计法检测曲线,图5(b)是5(a)对应的拟合曲线。从图中可以看出,在0.1 mol/L NaOH 溶液和+0.1 V的工作电位条件下,成功实现了对尿酸的快速响应,在尿酸浓度改变后10 s左右就达到稳定水平。从图5(b)的拟合结果显示所制备的电极对尿酸表现出优异的电催化性能,检测限为75 nmol/L(S/N = 3),线性相关系数为0.9967,线性检测范围上限为4.969×10-4mol/L,灵敏度高达301.3 μA·mmol/L·cm2。此结果与目前其它相关研究(表1)相比,可以看出该三维花状In(OH)3修饰电极的检测限和检测范围优于大多数其它材料修饰的电极。这主要是因为In(OH)3对尿酸的优异的电催化性能和其三维花状的特殊结构有利于尿酸扩散到电极的表面。
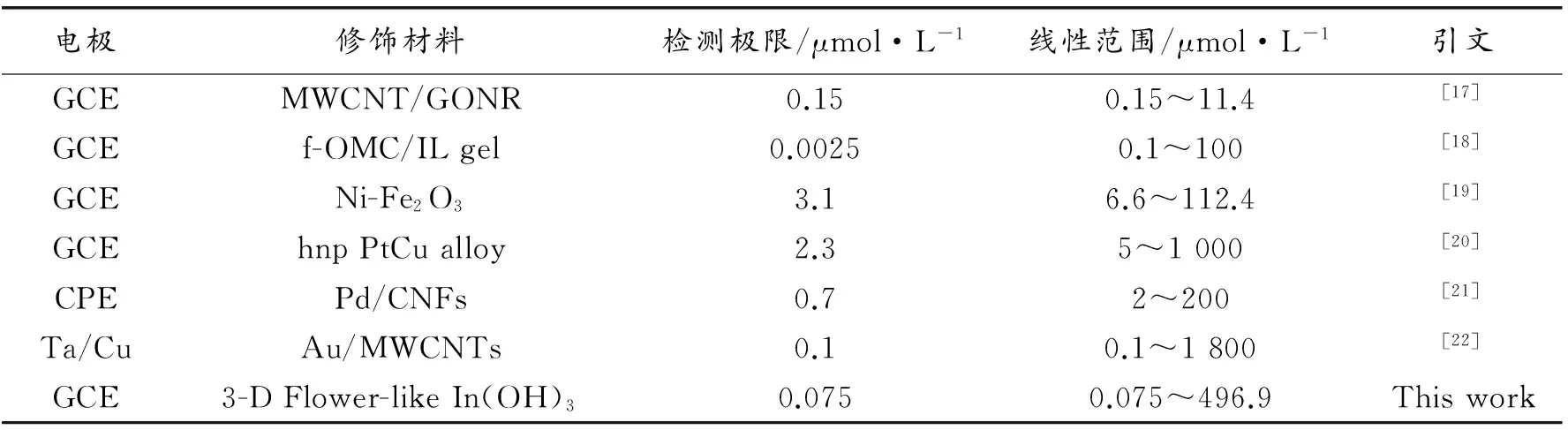
表1 不同修饰电极对尿酸的检测限和检测线性范围的对比
缩写: GCE: 玻碳电极; CPE: 碳糊电极; Ta/Cu:钽薄片/铜电极;MWCNT/GONR: 核壳MWCNT/GONR(氧化石墨烯纳米带) 异质结构;f-OMC/IL:功能化的有序介孔碳离子液体;hnp PtCu alloy:分层纳米多孔PtCu合金。
在尿酸非酶传感器的实际检测中经常会受其它化合物的影响,因为肌酐 (Cre)、尿素(Urea)等化合物通常与尿酸共存于人体体液中,为了研究三维花状In(OH)3修饰的玻碳电极的抗干扰能力,我们在+0.1 V的测量电压下向0.1 mol/L氢氧化钠溶液中连续加入10 mmol/L尿酸、10 mmol/L肌酐、10 mmol/L尿素,如图6所示。从图中可以看出,与尿酸的电流响应相比,电极对其它干扰物的响应微乎其微。所以,我们所制备的电极具有较好的抗干扰能力,展现出良好的应用前景。
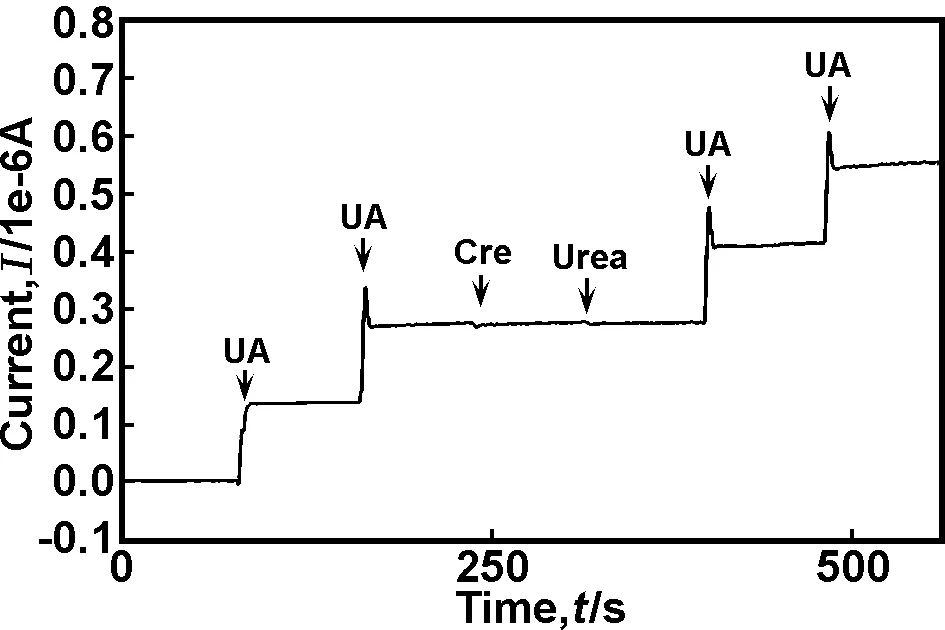
图6 In(OH)3/GCE对尿酸、肌酐、尿素的电流响应
3 结 论
通过一个简单的没有任何表面活性剂的水热方法合成三维花状In(OH)3,从XRD和SEM的结果显示,样品具有良好的晶体结构,尺寸为纳米级。通过研究三维花状In(OH)3修饰的电极对尿酸的检测,结果表明,所制备的电极表现出优异的生物传感器性能,其检测极限为75 nmol/L(S/N=3),线性检测范围上限为4.969×10-4mol/L,灵敏度高达301.3 μA·mmol/L·cm2,对尿酸具有良好的选择性。对此,一种可能的解释是三维花状In(OH)3的分级结构进一步提高了活性面积和电催化活性。
[1] Lesch M, Nyhan W L. A familial disorder of uric acid metabolism and central nervous system function [J]. The American Journal of Medicine, 1964, 36(4): 561-570.
[2] Jindal K, Tomar M, Gupta V. Inducing electrocatalytic functionality in ZnO thin film by N doping to realize a third generation uric acid biosensor [J]. Biosensors and Bioelectronics, 2014, 55:57-65.
[3] Zhang F, Wang X, Ai S, et al. Immobilization of uricase on ZnO nanorods for a reagentless uric acid biosensor [J]. Analytica Chimica Acta, 2004, 519(2): 155-160.
[4] Suresh R, Giribabu K, Manigandan R, et al. Fabrication of Ni-Fe2O3magnetic nanorods and application to the detection of uric acid [J]. RSC Advances, 2014, 4(33): 17146-17155.
[5] Wang J. Electrochemical glucose biosensors [J]. Chemical Reviews, 2008, 108(2): 814-825.
[6] Yogeswaran U, Thiagarajan S, Chen S M. Nanocomposite of functionalized multiwall carbon nanotubes with nafion, nano platinum, and nano gold biosensing film for simultaneous determination of ascorbic acid, epinephrine, and uric acid [J]. Analytical Biochemistry, 2007, 365(1): 122-131.
[7] Yan J, Liu S, Zhang Z, et al. Simultaneous electrochemical detection of ascorbic acid, dopamine and uric acid based on graphene anchored with Pd-Pt nanoparticles [J]. Colloids and Surfaces B: Biointerfaces, 2013, 111:392-397.
[8] Wang S, Lu L, Lin X. A selective voltammetric method for uric acid detection at a glassy carbon electrode modified with electrodeposited film containing DNA and Pt-Fe(Ⅲ) nanocomposites [J]. Electroanalysis, 2004, 16(20): 1734-1738.
[9] Chauhan N, Pundir C S. An amperometric uric acid biosensor based on multiwalled carbon nanotube-gold nanoparticle composite [J]. Analytical Biochemistry, 2011, 413(2): 97-103.
[10] Zhang F F, Wang X L, Li C X, et al. Assay for uric acid level in rat striatum by a reagentless biosensor based on functionalized multi-wall carbon nanotubes with tin oxide [J]. Anal Bioanal Chem, 2005, 382(6): 1368-1373.
[11] Jindal K, Tomar M, Gupta V. CuO thin film based uric acid biosensor with enhanced response characteristics [J]. Biosensors and Bioelectronics, 2012, 38(1): 11-18.
[12] Solanki P R, Kaushik A, Agrawal V V, et al. Nanostructured metal oxide-based biosensors [J]. NPG Asia Mater, 2011, 3:17-24.
[13] Li C, Zhang D, Liu X, et al. In2O3nanowires as chemical sensors [J]. Applied Physics Letters, 2003, 82(10): 1613-1615.
[14] Qurashi A, Irfan M F, Alam M W. In2O3nanostructures and their chemical and biosensor applications [J]. Arabian Journal for Science and Engineering, 2010, 35(1C): 126-130.
[15] Oliva P, Leonardi J, Laurent J F, et al. Review of the structure and the electrochemistry of nickel hydroxides and oxy-hydroxides [J]. Journal of Power Sources, 1982, 8(2): 229-235.
[16] He Z, Chen Z, Li Y, et al. Molar ratio of In to urea directed formation of In2O3hierarchical structures: cubes and nanorod-flowers [J]. Cryst Eng Comm, 2011, 13(7): 2557-2565.
[17] Sun C L, Chang C T, Lee H H, et al. Microwave-assisted synthesis of a core-shell MWCNT/GONR heterostructure for the electrochemical detection of ascorbic acid, dopamine, and uric acid [J]. Acs Nano, 2011, 5(10): 7788-7795.
[18] Dong J, Hu Y, Zhu S, et al. A highly selective and sensitive dopamine and uric acid biosensor fabricated with functionalized ordered mesoporous carbon and hydrophobic ionic liquid [J]. Anal Bioanal Chem, 2010, 396(5): 1755-1762.
[19] Suresh R, Giribabu K, Manigandan R, et al. Fabrication of Ni-Fe2O3magnetic nanorods and application to the detection of uric acid [J]. RSC Advances, 2014, 4(33): 17146-17155.
[20] Zhao D, Fan D, Wang J, et al. Hierarchical nanoporous platinum-copper alloy for simultaneous electrochemical determination of ascorbic acid, dopamine, and uric acid [J]. Microchimica Acta, 2015, 182(7-8): 1345-1352.
[21] Huang J, Liu Y, Hou H, et al. Simultaneous electrochemical determination of dopamine, uric acid and ascorbic acid using palladium nanoparticle-loaded carbon nanofibers modified electrode [J]. Biosensors and Bioelectronics, 2008, 24(4): 632-637.
[22] Wang J, Zhang W D. Sputtering deposition of gold nanoparticles onto vertically aligned carbon nanotubes for electroanalysis of uric acid [J]. Journal of Electroanalytical Chemistry, 2011, 654(1-2): 79-84.
Synthesis of hierarchical In(OH)3and application in electrochemical sensing properties of uric acid
HUANG Qingyou, HUANG Wei, XU Chufeng, WANG Bingrong, WANG Xiaohong,TU Jinchun, CAO Yang
(College of Materials and Chemical Engineering, Hainan University, Haikou 570228,China)
Nanostructured Indium hydroxide (In(OH)3) was synthesized through a facile hydrothermal route without any polymer surfactants, which was applied to the non-enzymatic electrochemical detection of uric acid (UA). The results characterized from X-ray diffraction (XRD) and scanning electron microscopy (SEM) indicated that the powders owned good crystallinity and uniform hierarchical 3-D flower-like structure. The experiment results revealed that the obtained material exhibited good electrocatalytic activity for the detection of UA in sodium hydroxide solution. In addition, compared with In2O3, In(OH)3showed higher electrode stability. The non-enzymatic electrochemical sensor was used in the detection of UA with a detection limit of 75 nmol/L(S/N = 3), a wide linear detection ranged up to 4.696×10-4mol/L, a high sensitivity of 301.3 μA·mmol/L·cm2and good selectivity toward UA.
In(OH)3; uric acid; electrochemical
1001-9731(2016)10-10113-05
国家自然科学基金资助项目(51361009)
2015-10-19
2016-01-21 通讯作者:曹 阳,E-mail: caowang507@163.com
黄清优 (1991-),男,江西吉安人,硕士,师承曹阳教授,从事生物传感器材料研究。
O649
A
10.3969/j.issn.1001-9731.2016.10.020
