Fe3+-H2O2-刚果红体系阻抑动力学光度法检测鱼肉中氟含量
2016-10-21熊海涛
熊海涛
1(陕西理工大学,陕西省催化基础与应用重点实验室,陕西 汉中,723000) 2(陕西理工大学 化学与环境科学学院,陕西 汉中,723000)
Fe3+-H2O2-刚果红体系阻抑动力学光度法检测鱼肉中氟含量
熊海涛1,2*
1(陕西理工大学,陕西省催化基础与应用重点实验室,陕西 汉中,723000)2(陕西理工大学 化学与环境科学学院,陕西 汉中,723000)
在酸性介质中,痕量F-对Fe3+催化H2O2化刚果红褪色反应有显著的抑制作用,且阻抑褪色的程度与氟离子含量呈良好的线性关系,由此建立了一种新阻抑动力学光度法测定微量氟离子含量的新方法。在最优化的反应条件下,氟含量在8.0×10-7~2.0×10-5mol/L内符合比尔定律,检出限为2.8×10-7mol/L。该法用于鱼肉中氟离子含量的测定,回收率在95.50%~98.00%。
Fe3+;H2O2;刚果红;阻抑动力学;氟;鱼肉
氟是人类生命活动所必需的微量元素之一[1],其以氟离子的形式广泛分布于水、土壤和动植物中, 人体摄入适量的氟元素,能够促进骨骼的发育、牙齿的钙化,增强骨骼强度。另一方面,如果长期食用高含量氟离子的食品又会引起累积性氟中毒,如导致人体关节疼痛、韧带钙化、骨质增生、行动不便等症状,严重的甚至还会造成脊椎弯曲、瘫痪等[2]。因此,有关氟离子在食品中的含量检测及安全性分析研究对人类的饮食健康有着重要的指导意义。
目前,检测氟离子含量的分析方法较多,主要有氟离子选择电极法[3-5]、离子色谱法[6-8]、高效液相色谱法[9-10]、气相色谱法[11-12]、极谱法[13-14]、荧光光度法[1, 15-16]及光度分析法[17-19]等,尤其是催化动力学光度法应用较广[20-21]。其中氟离子选择电极法尽管操作简便,但容易受电极质量以及测试液条件等因素影响。而离子色谱法是一种利用色谱柱进行分离测定的分析方法,是目前同时测定多种阴离子的首选方法,但定性能力较差。另外,高效液相色谱法与气相色谱法虽然分析准确,但设备昂贵且检出限低,单扫描极谱法则容易带来二次污染。而荧光光度法尽管能满足氟离子的高选择性及灵敏检测,但是经常需要合成新型的荧光探针,以致使整个过程繁琐且成本较高。而作为催化动力学光度法的分支之一的阻抑动力学光度法因其具有设备简单、分析成本低及较高的灵敏度等优点,因此在实际应用中较为广泛。如刘红梅[20]等人基于氨基乙酸-HCl缓冲体系中,Fe3+对H2O2氧化2,4-二氨基苯酚(DAP)褪色具有催化作用,F-则会拟制该催化褪色体系,据此建立了一种催化抑制光度法测量微量F-的新方法。然而到目前为止,未见文献报道利用Fe3+-H2O2-刚果红催化褪色体系来检测微量F-。
本研究工作利用在硫酸介质中,Fe3+能催化H2O2氧化刚果红(Congored,CR)褪色,而当加入少量氟离子后,该催化褪色褪色程度明显减弱,基于此建立了一种抑制动力学光度法检测氟离子含量的新方法。该方法操作简便,具有较高的灵敏度,可用于鱼肉中氟含量准确分析。
1 材料与方法
1.1仪器与试剂
722G型紫外可见分光光度计,上海精密科学仪器有限公司;HH型数显恒温水浴锅,华普达教学仪器有限公司;EL104电子天平,梅特勒-托利多仪器有限公司;WX-4000微波快速消解系统,上海屹尧仪器科技发展有限公司。
2.5×10-4mol/L铁(III)标准储备溶液;7.0×10-4mol/L刚果红(CR)溶液;1.0mol/LH2O2溶液;0.05mol/LH2SO4溶液;1.0×10-2mol/LF-标准储备溶液:取一定量的NaF放入干燥箱中,烘干后准确称取0.420 5g于烧杯中溶解,将溶液定容至1 000mL的容量瓶中,储存于聚乙烯瓶中,使用时再稀释成所需浓度。
鲤鱼:购自汉中市汉台区水产市场。
所用试剂均为分析纯,试剂用水均为高纯水。
1.2实验方法
取2支规格相同的10mL具塞比色管,分别加入一定量的CR、稀H2SO4、H2O2及适量的Fe3+标准储备溶液,再向其中一支比色管中加入一定量氟标准溶液,作为抑制反应体系,另一支不加氟标准溶液作为非抑制反应体系,均用高纯水定容至刻度,摇匀。接着,将2支比色管同时置于数显恒温水浴锅中,于90 ℃沸水浴中加热10min后取出,放入冰水浴中冷却至室温以终止反应。最后,使用1cm的比色皿,在吸收波长为500nm处,以蒸馏水作参比,分别测定抑制体系的吸光度(A1)和非抑制体系的吸光度(A2),计算ΔΑ=A1-A2。
2 结果与讨论
2.1不同反应体系吸收光谱
按照1.2实验方法配制不同体系溶液,在波长400~600nm范围内分别对4个不同体系进行波长扫描,并绘制吸收曲线。图1结果表明:4个体系均在500nm处有最大吸收峰,但是在稀H2SO4介质中,曲线2要比曲线1的吸收峰值低,这说明H2O2会氧化CR,而适量Fe3+的加入则能显著催化H2O2氧化CR褪色(曲线4)。但是当少量F-存在时,H2O2-CR体系的褪色有明显的抑制,这可能是基于加入的F-能与反应体系中Fe3+优先结合生成[FeF6]3-,从而致使H2O2-CR体系的褪色程度有所减弱。因此,本研究选择测定波长为500nm。

1-H2SO4(2.0×10-3 mol/L)+CR(1.0×10-5 mol/L);2-H2SO4(2.0×10-3 mol/L)+H2O2(2.0×10-2 mol/L)+ CR(1.0×10-5 mol/L);3-H2SO4(2.0×10-3 mol/L)+ H2O2(2.0×10-2 mol/L)+ CR(1.0×10-5 mol/L)+ Fe3+(2.0×10-5 mol/L)+F-(2.0×10-6mol/L); 4-H2SO4(2.0×10-3 mol/L)+H2O2 (2.0×10-2 mol/L)+ CR(1.0×10-5 mol/L)+Fe3+(2.0×10-5 mol/L)图1 吸收光谱图Fig.1 Absorption spectra
2.2硫酸浓度对阻拟褪色体系的影响
初步研究表明,在稀H2SO4介质中,少量F-对褪色反应体系(Fe3++H2O2+CR)的阻拟作用最为明显。进一步考查了硫酸浓度对褪色反应体系的影响。从图2上可以看到,H2SO4浓度为310-3mol/L时,吸光度差值ΔΑ最大。因此,本文选择硫酸浓度为310-3mol/L。
2.3反应温度的影响
反应温度是影响少量F-对褪色反应体系阻拟作用的重要因素之一。实验考察了水浴在40~100 ℃范围内,反应温度对阻拟催化褪色反应程度的影响(见图3)。结果表明,在较低的反应温度下,随着温度的升高,体系的吸光度差值ΔΑ逐渐增大,但是当反应温度达到80 ℃时,ΔΑ较大且在更高的反应温度下基本保持不变。故本研究选择反应温度为80 ℃。

C[H2SO4]=3.0×10-3 mol/L; C[H2O2]=2.0×10-2 mol/L;C[CR]=2.0×10-5 mol/L;C[Fe3+]=2.0×10-5 mol/L;C[F-]=1.0×10-5 mol/L;反应时间:8 min图3 反应温度影响Fig.3 Effect of reaction temperature on the relative absorbance
2.4反应时间的影响
在选定的硫酸浓度及反应温度下,实验探讨了反应时间对阻拟褪色程度的影响。图4表明,在4~10min内,ΔΑ随反应时间的增加而增大,超过10min后ΔΑ值基本不再变化。因此,选择10min作为随后研究的反应时间。

C[H2SO4]=3.0×10-3 mol/L; C[H2O2]=2.0×10-2 mol/L;C[CR]=2.0×10-5 mol/L;C[Fe3+]=2.0×10-5 mol/L;C[F-]=1.0×10-5 mol/L;反应温度:80 ℃图4 反应时间影响Fig.4 Effect of reaction time on the relative absorbance
2.5刚果红浓度的影响
CR作为反应体系的唯一显色剂,其浓度对阻拟褪色程度有较大影响。从图5可以明显看出:CR浓度在1.010-5~1.010-4mol/L范围内,吸光度差值ΔΑ随浓度呈现出先增大后减小的趋势,仅当其浓度为6.0×10-5mol/L时ΔΑ有最大值。因此,实验选择6.0×10-5mol/L为CR的最佳浓度。

C[H2SO4]=3.0×10-3 mol/L; C[H2O2]=2.0×10-2 mol/L;C[Fe3+]=2.0×10-5 mol/L;C[F-]=1.0×10-5 mol/L;反应温度:80 ℃;反应时间:10 min图5 刚果红浓度影响Fig.5 Effect of CR concentration on the relative absorbance
2.6Fe3+浓度的影响
研究考查了Fe3+浓度在1.0×10-5~4.0×10-5mol/L范围内其对阻拟褪色程度的影响(如图6所示)。我们发现:当反应体系中加入的Fe3+浓度为2.5×10-5mol/L时,拟制体系与非拟制体系的吸光度差值ΔΑ最大。因此,本文选择2.5×10-5mol/L的Fe3+为接下来研究工作的反应浓度。
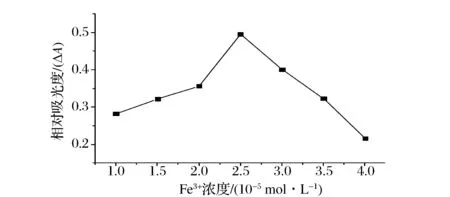
C[H2SO4]=3.0×10-3 mol/L; C[H2O2]=2.0×10-2 mol/L;C[CR]=6.0×10-5 mol/L;C[F-]=1.0×10-5 mol/L;反应温度:80 ℃;反应时间:10 min图6 Fe3+浓度影响Fig.6 Effect of Fe3+ concentration on the relative absorbance
2.7H2O2浓度的影响
在固定上述各选定的实验条件下,考察了H2O2浓度对反应体系阻拟褪色程度的影响。图7显示:2个反应体系的吸光度差值ΔΑ随着H2O2浓度先增大后减小,仅在浓度为0.06mol/L时ΔΑ获得最大值。因此,选择H2O2的最佳浓度为0.06mol/L。
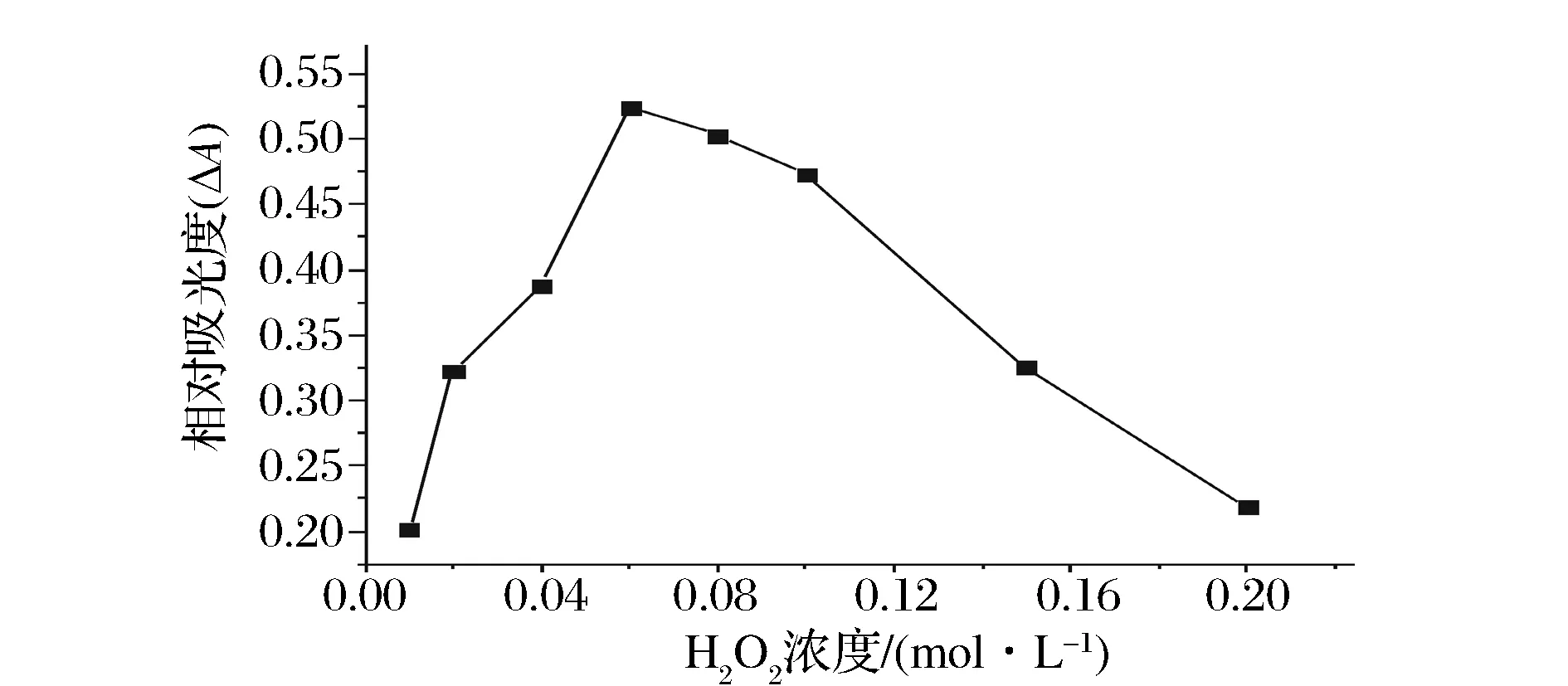
C[H2SO4]=3.0×10-3 mol/L; C[Fe3+]=2.5×10-5 mol/L;C[CR]=6.0×10-5 mol/L;C[F-]=1.0×10-5 mol/L;反应温度:80 ℃;反应时间:10 min图7 H2O2浓度影响Fig.7 Effect of H2O2 concentration on the relative absorbance
2.8方法线性范围、标准曲线及检出限
在以上优化的实验条件下,测定不同F-浓度下的阻抑体系与非阻抑体系的吸光值,以ΔΑ为纵坐标、F-浓度为横坐标绘制工作曲线(见图8)。在8.010-72.010-5mol/L浓度范围内,体系吸光度ΔΑ与F-浓度呈良好的线性关系,其线性回归方程为ΔΑ=0.003 6C(mol/L)+0.104 8,相关系数r=0.992 3。按照IUPAC建议,计算出方法的检出限为2.810-7mol/L。对2.010-6mol/L的F-标准溶液平行测定8次,相对标准偏差为4.9%。
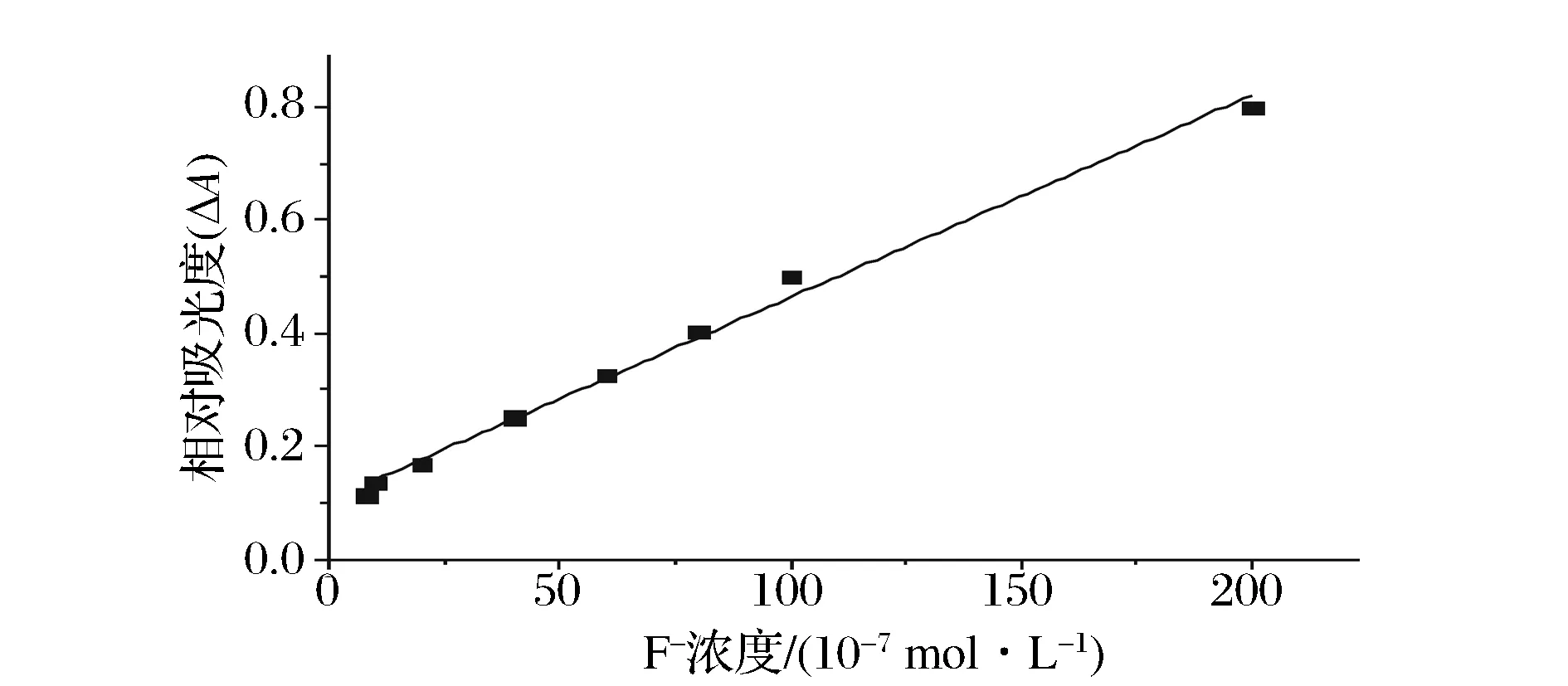
图8 标准工作曲线Fig.8 Standard curve
2.9共存离子的影响
可在酸性溶液中通过阳离子交换树脂分离除去。
2.10样品分析
2.10.1样品制备
取适量鱼肉样品于粉碎机中粉碎成泥状并混匀,准确称取0.200 8g于聚四氟乙烯消解罐中,同时加入5mL浓HNO3和1mL双氧水,放置12h。然后,分3步进行密闭微波消解约20min(从100 ℃升至180 ℃),消解结束后冷却至室温并放置在控温板上加热赶尽残酸,之后将其转移到10mL的容量瓶中,以高纯水定容至刻度线,摇匀待用。
2.10.2样品测定结果及加标回收率
按照实验方法1.2对鱼肉中氟离子含量进行测定,并以标准加入法检验方法的准确性。由表1可知,加标回收率为95.50%~98.00%,故此法能准确的测定鱼肉中氟含量。

表1 样品回收率的测定结果(n=3)
3 结论
本文基于酸性介质中,少量F-能阻拟Fe3+-H2O2-刚果红褪色体系而建立了一种测定微量F-的新光度分析法。该法试剂廉价、操作简单且具有较高的灵敏度。使用本文建议的光度法测得鲤鱼中F-的平均含量为20.32g/g,略低于国标中氟含量(21μg/g)且回收率结果较理想。因此,本研究所建立起的新阻拟褪色光度法不仅能检测鱼类F-含量,还有望用于其他生物样品中F-含量的灵敏检测,更能为食品监督部门提供一定的数据参考。
[1]LILong,JIYu-zhuo,TANGXin-jing.Quaternaryammoniumpromotedultraselectiveandsensitivefluorescencedetectionoffluorideioninwaterandlivingcells[J].AnalyticalChemistry, 2014, 86(20):10 006-10 009.
[2]中国营养学会编著. 中国居民膳食营养素参考摄入量. 北京:中国轻工业出版社,2006:210.
[3]石生勋,石一均,成永强,等. 硝酸消化直接测定蔬菜中微量氟的离子选择性电极法[J]. 河北大学学报:自然科学版,2011, 31(1):48-51.
[4]盛晓风,郭莹莹,尚德荣,等. 离子选择电极法测定高氟样品中氟的方法改进[J]. 食品工业科技,2013, 34(9):285-289.
[5]蒋明,王重华,田森林,等. 氟离子选择电极测定黄磷尾气中气态氟含量[J]. 分析科学学报,2014, 30(2):244-246.
[6]杨志国, 吕牧羊. 在线超滤-离子色谱法测定牙膏中的游离氟[J]. 中国卫生检验杂志, 2010, 32(12):3 212-3 213.
[7]张红漫, 陈敬文. 二氧化钛光催化氧化-离子色谱法测定液晶材料中的氟含量[J]. 分析化学, 2010, 38(11):1 639-1 642.
[8]JEYAKUMARS,RAUTVV,RAMAKUMARKL.Simultaneousdeterminationoftraceamountsofborate,chlorideandfluorideinnuclearfuelsemployingionchromatographyaftertheirextractionbypyrohydrolysis[J].Talanta, 2008, 76 (5):1 246-1 251.
[9]ANETTAZIOA-FRANKOWSKA,MARCINFRANKOWSKI,JERZYSIEPAK,etal.Developmentofanewanalyticalmethodforonlinesimultaneousqualitativedeterminationofaluminium(freealuminiumion,aluminium-fluoridecomplexes)byHPLC-FAAS[J].Talanta, 2009, 78 (2):623-630.
[10] 李华斌, 徐向荣, 彭安. 高效液相色谱法测定茶叶和土壤中的氟[J]. 环境科学, 2008, 19(3):78-79.
[11]PAGLIANOE,MEIJAJ,DINGJ,etal.Novelethyl-derivatizationapproachforthedeterminationoffluoridebyheadspacegaschromatography/massspectrometry[J].AnalyticalChemistry, 2013, 85(2):877-881.
[12]KWONSM,SHINHS.Simpledeterminationoffluorideinbiologicalsamplesbyheadspacesolid-phasemicroextractionandgaschromatography-tandemmassspectrometry[J].JournalofChromatographyA, 2015, 1407 (1):216-221.
[13]陈文, 汪模辉, 李锡坤, 等. 单扫描极谱法测定土壤、蔬菜、水样中痕量氟[J]. 分析化学, 2007, 35(5):663-666.
[14]陈文, 李东升, 范长利, 等. 氟的单扫描极谱测定改进体系研究及分析应用[J]. 分析试验室, 2009, 28(5):11-15.
[15]MSY,HONGJI.Chromogenicandkifluorescentchemodosimeterfordetectionoffluorideinaqueoussolution[J].OrganicLetters,2007, 9(16):3 109-3 112.
[16]SUIB,KIMB,ZHANGY,etal.Organicletters,highlyselectivefluorescenceturn-onsensorforfluoridedetection[J].AppliedMaterials&Interfaces,2013, 5(8):2 920-2 923.
[17]PILLAAB,VARGHESEB,MADHUSOODANANKN.Designanddevelopmentofnovelsensorsforthedeterminationoffluorideinwater[J].EnvironmentalScience&Technology, 2012, 46(1):404-409.
[18]SARAVANANC,EASWARAMOORTHIS,WANGL.Colorimetricdetectionoffluorideionby5-arylidenebarbituricacids:dualinteractionmodeforfluorideionwithsinglereceptor[J].DaltonTransactions, 2014, 43(13): 5 151-5 157.
[19]BOKENJ,THATAIS,KHURANAP,SurendraPrasad,DineshKumar.Highlyselectivevisualmonitoringofhazardousfluorideioninaqueousmediausingthiobarbituric-cappedgoldnanoparticles[J].Talanta, 2015, 132(2):278-284.
[20]刘红梅, 侯文龙, 鲁勖琳. 阻抑动力学光度法测定桑叶中的微量氟[J]. 食品科技, 2010, 38(7):219-221.
[21]普学伟, 蒋永金, 崔庆雄, 等. 过氧化氢-钛(Ⅳ)-氟化物体系褪色光度法测定熔盐中氟[J]. 冶金分析, 2013, 33(2):42-46.
DetectionoffluorideioninfreshbynewinhibitionkineticspectrophotometryusingFe3+-hydrogenperoxide-congoredsystem
XIONGHai-tao1,2*
1(ShaanxiProvinceKeyLaboratoryofCatalyticFoundationandApplication,ShaanxiSCI-TECHUniversity,Hanzhong723000,China)2(SchoolofChemical&EnvironmentalSciences,ShaanxiSCI-TECHUniversity,Hanzhong723000,China)
Intheacidiccondition,tracefluorineioncouldobviouslyinhibitthefadingreactionbetweencongoredandH2O2catalyzedbyFe3+.Inaddition,theinhibitionde-colorationdegreewaslineartothecontentoffluorineion.Basedonthisfinding,anewinhibitionkineticspectrophotometrymethodforthedetectionoftracefluorineionwasproposed.Undertheoptimumconditions,thelinearrangeforfluorineionwas8.0×10-7~2.0×10-5mol/Lwithadetectionlimitof2.8×10-7mol/L.Theproposedmethodhasbeenappliedtoassayoffluorineioninfreshandtherecoverywasbetween95.50%and98.00%.
ironion(Ⅲ);hydrogenperoxide;congored;inhibitionkinetic;fluorideion;fresh
10.13995/j.cnki.11-1802/ts.201608033
硕士,讲师(本文通讯作者,E-mail:xionght@snut.edu.cn)。
陕西省教育厅专项科研基金项目( 16JK1131)
2015-12-29,改回日期:2016-02-16
