丙氨酰谷氨酰胺对体外培养人颊黏膜成纤维细胞生物活性的影响研究*
2016-09-16车坷科卿尚兰张熙承
车坷科,刘 鑫,卿尚兰,张熙承
(重庆市人民医院:1.药学部;2.口腔科 400014)
丙氨酰谷氨酰胺对体外培养人颊黏膜成纤维细胞生物活性的影响研究*
车坷科1,刘鑫2△,卿尚兰2,张熙承2
(重庆市人民医院:1.药学部;2.口腔科400014)
目的研究丙氨酰谷氨酰胺(Ala-Gln)溶液对体外培养的人颊黏膜成纤维细胞的生长、蛋白合成和碱性磷酸酶(ALP)活性的影响。方法实验分为对照组(N组)、Ala-Gln组(A组)和Gln组(G组),A、G组各设推荐浓度的8、4、2、1、1/2、1/4和1/8倍7个梯度浓度,在体外培养的人颊黏膜成纤维细胞中分别加入上述各组溶液。培养至12、24、36、48、60和72 h,用流式细胞仪计数细胞并绘制细胞生长曲线;用酶联免疫检测对应时段各自ALP水平,72 h时检测各组细胞蛋白水平。结果N组在72 h内细胞数量并未明显变化,ALP水平随着时间推移有所增加,但变化幅度小于A、G组(P<0.05);A、G组在24 h以内都能明显促进细胞生长,ALP的水平也明显提高(P<0.05),且以1/2倍推荐浓度组最为显著;各药物浓度组细胞蛋白水平均高于N组(P<0.05)。结论Ala-Gln能促进颊黏膜成纤维细胞生长,浓度过高或过低可影响细胞持续生长,以1/2倍推荐浓度(即Ala-Gln浓度为16.5 mg/mL)时细胞生长情况最好。
口腔黏膜;成纤维细胞;碱性磷酸酶;丙氨酰谷氨酰胺;细胞生长
口腔复发性阿弗他溃疡(recurrent aphthous ulcer,RAU)是最常见的口腔黏膜病,是以口腔黏膜自发性、复发性溃疡为特点的一种疾病,普通人群的发病率为20%左右;RAU的局部治疗目前以消炎、止痛、防止继发感染、促进愈合为原则[1]。谷氨酰胺(Glutamine,Gln)是免疫细胞及成纤维细胞等快速增殖细胞的主要能量来源[2],除了具有增加葡萄糖胺、氨基己糖、黏蛋白的生物合成和促进溃疡组织再生等生物活性外,还具有有效调节免疫应答、改善机体代谢状况、提高机体抗氧化能力等药理作用[3-4]。由于Gln在水溶液中溶解度低且不稳定[5],目前临床使用具有化学稳定性好、水溶性强、能耐受高温消毒等优点的丙氨酰谷氨酰胺(Ala-Gln)为Gln的供体,通过在细胞外发生的水解,为机体提供稳定的Gln[6]。本文就Ala-Gln对体外培养的人颊黏膜成纤维细胞(fibroblast)的生长、蛋白合成和碱性磷酸酶(alkaline phosphatase,ALP)活性进行研究,并与对应含量的Gln进行对比,以期为Ala-Gln治疗RAU的临床研究及应用提供理论依据。
1 材料与方法
1.1材料
1.1.1细胞来源标本采自重庆市人民医院口腔科在颊黏膜取送活检的组织中的正常组织,均征得患者本人及其家属同意并签署知情同意书。
1.1.2主要试剂和仪器Ala-Gln(重庆莱美药业股份有限公司,批号F151210),Gln(武汉千润生物工程有限公司赠送,批号140618),D-Hanks缓冲液(自配,含100 U/mL青霉素,100 μg/mL链霉素);DMEM 培养基、RPMI-1640培养液、胰蛋白酶、优等胎牛血清(FBS)和Ⅰ型胶原酶(美国Gibco公司);二甲基亚砜(DMSO,美国MPBIO公司);四甲基偶氮唑盐(MTT,美国Amresco公司);二氧化碳细胞恒温培养箱(美国Forma Scientic公司);CKC-TR-2W型倒置显微镜(日本Olympus公司);酶联免疫检测仪(芬兰Labsystems dragon MK3公司);YJ-875型超净化工作台(苏州净化设备厂);96孔培养板(北京中杉金桥生物技术有限公司);波形丝蛋白、角蛋白一抗及即用型SABC试剂盒(武汉博士德生物工程有限公司);二喹啉甲酸(BCA)蛋白浓度测定试剂盒(上海美季生物有限公司);碱性磷酸酶试剂盒(南京建成生物公司)。
1.2方法
1.2.1人颊黏膜成纤维细胞的原代培养、分离纯化及鉴定[7-8]无菌条件下取出颊黏膜组织,剔除坏死组织及血渍,磷酸盐缓冲液(PBS)冲洗3次,青霉素、链霉素浸泡0.5 min,PBS冲洗2次,剪成约0.5 mm×0.5 mm,加入0.25%胰蛋白酶37 ℃孵箱消化30 min,加入0.2% Ⅰ型胶原酶振荡消化30~60 min,至组织完全溶解,用含10% FBS的DMEM等体积中和,200目过滤,1 000 r/min离心5 min,弃去上清,用含15% FBS的DMEM培养基重悬细胞,接种至25 cm2培养瓶。于 37 ℃ 5% CO2饱和温度培养箱中培养。48 h后去除未贴壁细胞。此后每72小时换液1次,倒置显微镜下观察细胞形态,用机械刮出法及酶消化法去除成纤维细胞,细胞达到80%~90%汇合时,用0.25%的胰酶消化,按(4~6)×103/cm2传代。取第3代对数生长期成纤维细胞,用SABC法进行波形蛋白、角蛋白免疫组织化学染色,鉴定细胞来源。
1.2.2实验分组及处理根据加药情况,将加入Ala-Gln溶液的定为A组;加入Gln溶液的定为G组;含20% FBS的RPMI-1640培养基培养细胞作为对照,定为N组。根据Ala-Gln产品使用说明书中的推荐浓度,结合预实验结果,将Ala-Gln溶液的基础浓度定为33 mg/mL,折算Gln溶液的基础浓度为22 mg/mL,然后按加入溶质的量共设立8、4、2、1、1/2、1/4和1/8倍7个浓度梯度组,分别用A8、A4、A2、A1、A1/2、A1/4、A1/8和G8、G4、G2、G1、G1/2、G1/4、G1/8表示。
Gln溶液的配制方法:按照上述浓度梯度的设置,称取Gln原料药适量,溶于灭菌PBS(pH 7.4)中,超声助溶,配制好的储备液于0 ℃冰箱中储存。Ala-Gln溶液的配制方法同Gln。
1.2.3细胞生长情况的检测取第5代传代的成纤维细胞,胰蛋白酶消化贴壁培养的细胞,终止消化后添加15% FBS培养基,用移液管反复轻轻吹打成单细胞悬浮液,按1∶3的接种比例传代培养。将长好的贴壁细胞消化后,以细胞密度为0.75×106/mL转入摇瓶进行扩大培养。待细胞形态良好,以每瓶100 mL培养基均匀接入250 mL三角瓶中(接种密度为1.0×106/mL),按照1.2.2项的分组情况加入对应浓度的溶液,置于37 ℃培养箱内培养。每隔12 h取样,流式细胞仪计数细胞,并将本实验重复进行3次。
1.2.4细胞蛋白水平检测细胞以1×105/mL 的密度接种于96孔板,每孔1.0 mL。血清饥饿12 h后,各浓度组加入96孔板中,每种浓度加6孔;对照组加含0.5% FBS的DMEM。96孔板置于CO2培养箱中培养72 h后,弃去孔内液体,用pH 7.4的PBS冲洗3次,吸干,每孔加入150 μL 0.5% Trton X-100裂解过夜后,取200 μL裂解液按蛋白浓度试剂盒说明用酶联免疫检测仪于450 nm波长测吸光度值,根据标准曲线将吸光度值换算成蛋白水平(μg/mL)。
1.2.5细胞ALP活性检测取第5代颊黏膜成纤维细胞,以1×105/mL的细胞浓度接种于96孔培养板,10% DMEM培养基共培养4 d,弃孔内液体,加入Triton X-100,4 ℃过夜,进行如下实验:在12、24、36、48、60和72 h时,取上述各孔液体及空白对照的蒸馏水一并转入另一个96孔板。按ALP试剂盒说明依次按比例加入缓冲液、基质液,水浴,加入对硝基苯磷酸二钠(PNPP)显色剂后在酶联免疫检测仪上于405 nm波长下测吸光度值,间接反映细胞ALP活性。根据标准曲线将吸光度值换算成ALP水平(U/mgprot),并将ALP用蛋白水平进行校正。
1.3统计学处理采用SPSS17.0统计学软件进行分析,多组均数的比较采用单因素方差分析,两两之间比较用Tamhane′s T2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1体外培养的人颊黏膜成纤维细胞情况胞体呈梭型或不规则三角形,中央有卵圆形核,胞质向外伸出2~3个长短不等的突起,生长时呈放射状。经SABC法染色鉴定培养细胞表现为角蛋白染色阴性,胞质不着色,波形丝蛋白染色阳性,细胞胞质棕黄色着色,说明细胞来源于中胚层,为结缔组织源性细胞。见图1~3。
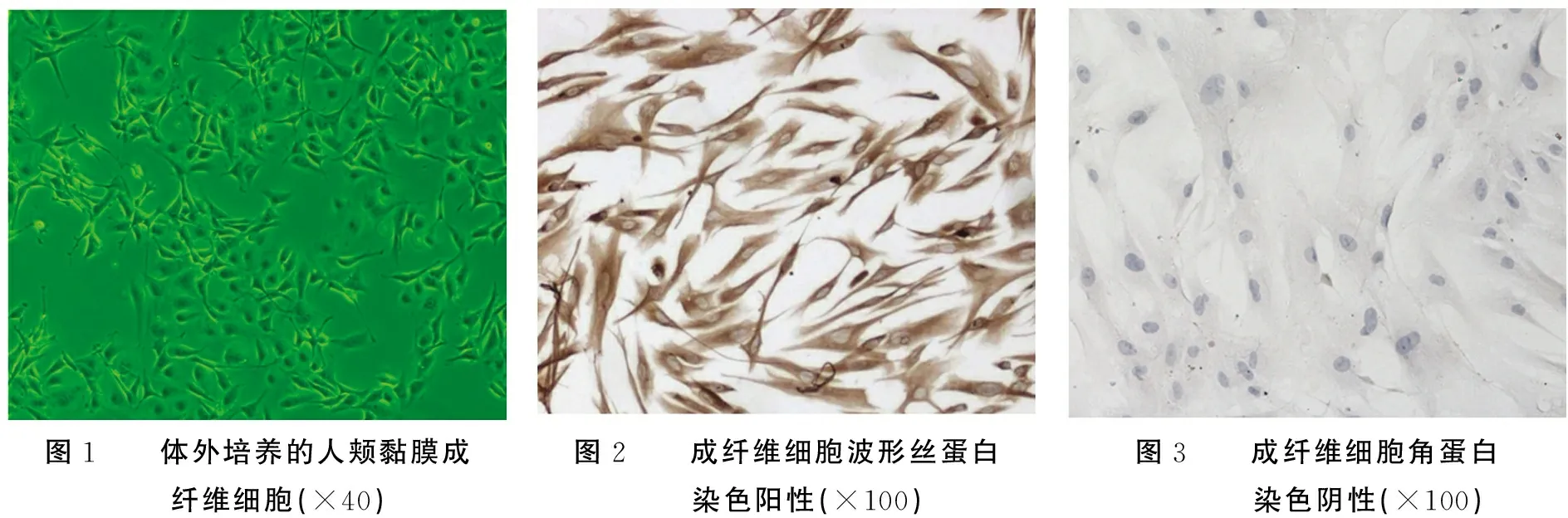
图1 体外培养的人颊黏膜成纤维细胞(×40) 图2 成纤维细胞波形丝蛋白染色阳性(×100) 图3 成纤维细胞角蛋白染色阴性(×100)
2.2细胞生长情况N组细胞的生长和凋亡处于一种平衡,细胞数并未明显变化,在(1.00~1.01)×106/mL;加入两种药物后,特别是24 h以内,都能明显促进细胞生长(P<0.05);其中,A8、A4和G8、G4从24 h后,细胞数目未明显变化;48 h后,A2和G2细胞数目增长开始逐渐减慢,而A1/8和G1/8细胞数目开始下降;60 h后,A1和G1细胞数目增长开始逐渐减慢。在整个72 h内,A1/2、A1/4和G1/2、G1/4细胞数目都能保持持续增长的状态,特别是A1/2在72 h时达到了4.20×106/mL,为本项实验数据最大值;无论是A组或者G组,1/4浓度组的生长曲线低于1/2浓度组,但A组和G组对应浓度组之间,差异无统计学意义(P>0.05)。见图4。
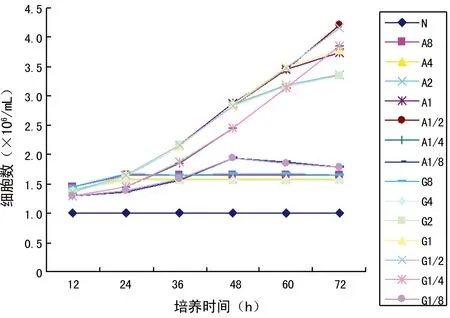
图4 各组颊黏膜成纤维细胞生长曲线
2.3细胞蛋白水平各药物浓度组细胞蛋白水平均高于N组(673.68 mg/mL),A1/2和G1/2细胞蛋白水平为各自组别最高,分别为1 407.51、1 393.35 mg/mL,而A组和G组同梯度浓度的细胞蛋白水平比较,差异无统计学意义(P>0.05)。见图5。
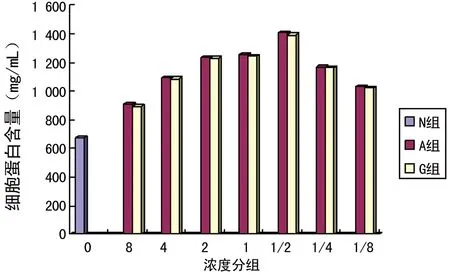
图5 各组颊黏膜成纤维细胞蛋白水平比较
2.4细胞ALP活性N组细胞的ALP水平随着时间推移有所增加,但变化幅度不如A、G组明显,在加入Ala-Gln或Gln后,特别是24 h内,ALP的水平显著提高;其中,A8、A4和G8、G4从24 h后,ALP水平未明显变化;48 h后,A2和G2 ALP增长幅度开始逐渐减慢,而A1/8和G1/8 ALP水平开始下降,但仍较N组有显著升高;60 h后,A1和G1 ALP水平增长开始逐渐减慢。72 h内A1/2、A1/4和G1/2、G1/4 ALP水平都能保持持续增长的状态,特别A1/2在72 h时达到了53.48 U/mgprot;无论是A组或G组,1/4浓度组各时间点ALP的水平都低于1/2浓度组,但A和G组同梯度浓度组之间,ALP水平差异无统计学意义(P>0.05)。见图6。
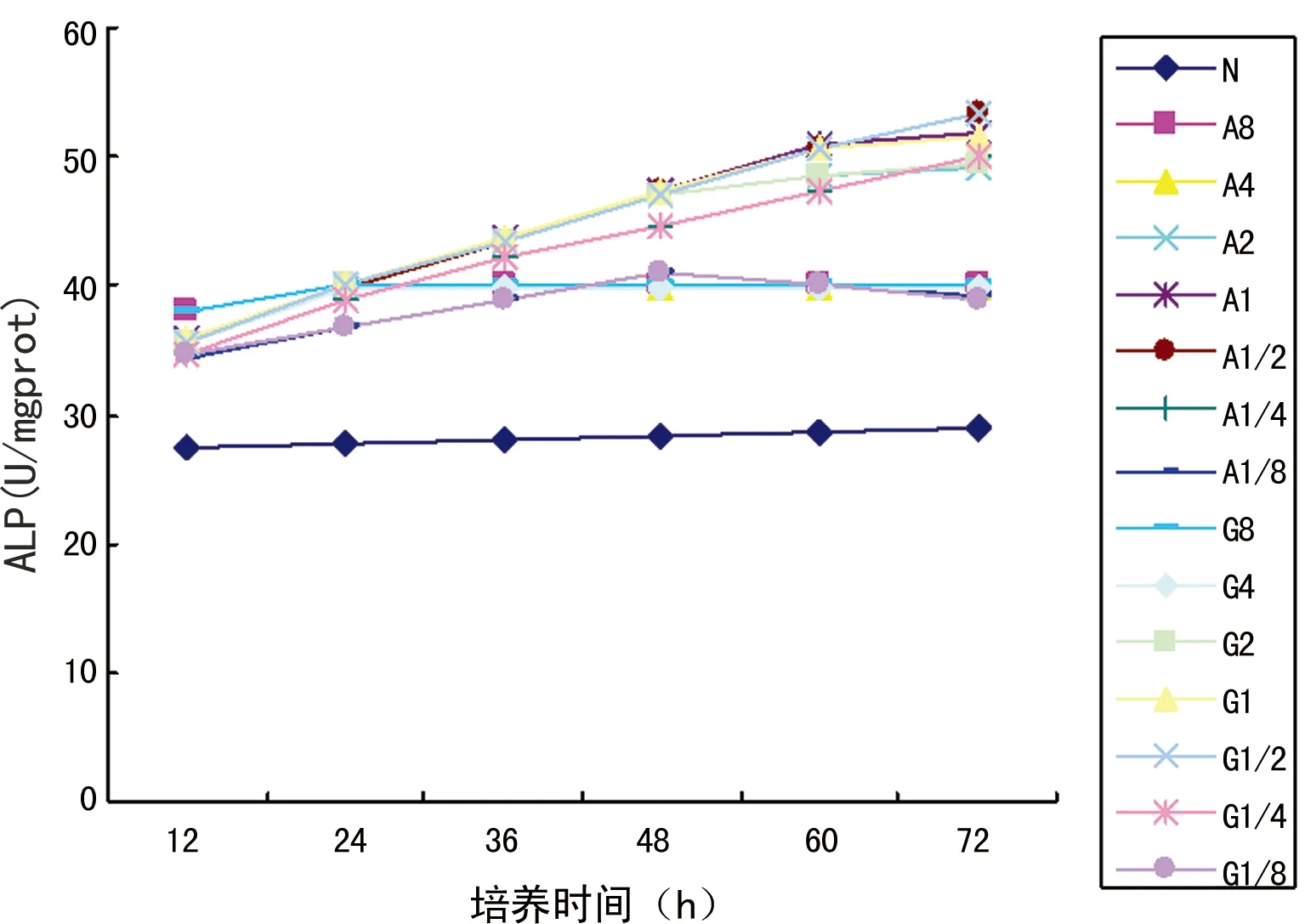
图6 各组颊黏膜成纤维细胞ALP活性比较
3 讨 论
RAU的治疗目前多采用口腔局部用药[9],常用的药物包括生长因子、中药制剂、生物制剂、人工合成药物、免疫调节剂、微量元素补充剂等,但由于病因复杂、药物价格及患者依从性等原因,其疗效和推广应用都受到了很大的限制[10]。本研究采用Ala-Gln,从促进溃疡愈合和增强黏膜局部免疫力等方面治疗RAU,从而克服目前临床上RAU治疗方面的不足。这一研究方案和初步研究成果已获得国家发明专利授权(专利号ZL 2013 1 0375582.7)。
细胞增殖是生物生长、发育、繁殖的基础,目前常用MTT法检测细胞的增殖效应,但不能较好地反映细胞活性情况;而流式细胞仪是对细胞进行自动分析和分选的装置,可以快速测量、存贮、显示悬浮在液体中的分散细胞的一系列重要的生物物理、生物化学方面的特征参量,并可以根据预选的参量范围把指定的细胞亚群从中分选出来,经过设定,可以计数活细胞和检测细胞活力[11]。蛋白水平的变化可反映细胞功能的活跃程度,细胞增殖与蛋白合成呈正相关,活细胞数量增加,其蛋白水平也应相应增多[12]。ALP是参与组织形成、代谢和再生的一种重要物质,可作为评价细胞分化和成熟的一种指标,目前已发现ALP1、ALP2、ALP3、ALP4、ALP5与ALP6 6种同工酶,而其中ALP5来自上皮和成纤维细胞[13],测定ALP活性可以评价细胞分化情况。因此,本文确定了细胞总数、蛋白水平、ALP活性3个指标综合考察Ala-Gln对人颊黏膜成纤维细胞生物活性的影响。
结果显示,A8、A4、G8和G4组,12 h内细胞数目和ALP水平均明显高于对照组,但24 h后二者几乎较12 h时无明显变化,可能由于氨的生成较多,Gln的利用受到抑制,Gln在生成谷氨酸后经过脱氢途径的量减少,更多地向转氨途径,与脱氢途径相比,细胞通过转氨途径产生的氨较少,对细胞生长产生的抑制作用也较小。这与高氨浓度抑制细胞生长、细胞需要调整能量代谢的速率与生物合成的速率相协调的观点相符;而在细胞培养过程中,氨对细胞的生长有明显的抑制作用,遵循二级抑制模型,其模型常数Ka为4.46(mmol/L)2[14]。本研究中,A2和G2组在48 h后,以及A1和G1组在60 h后出现细胞生长和分化减缓,可能与Gln分解造成的氨浓度增高有关。A1/2、A1/4、G1/8和G1/4组72 h内一直保持较好的生长曲线,48 h内细胞的生长和ALP水平与对照组比较差异有统计学意义(P<0.05);48 h后,G1/2和G1/4组的细胞生长和ALP水平相对于A1/2和A1/4组稍偏低,但其差异无统计学意义(P>0.05),推测原因为Gln在水溶液中不稳定,可能与Gln有效成分降低和Gln分解造成氨水平增高有一定关联,也应予以综合考虑。A1/8和G1/8组从一开始就生长缓慢,ALP水平偏低,与其他浓度组的差异有统计学意义(P<0.05),60 h后均停止生长并逐渐下降;而A1/2和G1/2组较A1/4和G1/4组的细胞生长好,ALP水平也较高,差异有统计学意义(P<0.05),说明Ala-Gln和Gln对细胞生长和分化的影响存在浓度依耐性。
在细胞蛋白水平方面,无论是A组还是G组,在1/8~1/2浓度,其蛋白水平呈浓度依赖性。1/2浓度组蛋白水平也明显高于1倍浓度组,而2~8倍浓度组水平明显降低,可能是Gln代谢和分解产生了高浓度的氨,对细胞的生长有抑制作用。另外,实验结果显示A组的细胞蛋白水平及
ALP水平略高于G组,估计与Ala-Gln代谢过程中产生的丙氨酸作为另一种氨基酸来源参与细胞生长有关。
综上所述,Ala-Gln可以提高人颊黏膜成纤维细胞的ALP和细胞蛋白水平,促进细胞生长,提高细胞活性,当Ala-Gln浓度过高或过低可影响细胞持续生长,以1/2倍推荐浓度(即Ala-Gln浓度为16.5 mg/mL)时细胞生长情况最好。
[1]Babaee N,Baradaran M,Mohamadi H,et al.Therapeutic effects of Zataria Multiflora essential oil on recurrent oral aphthous lesion[J].Dent Res J (Isfahan),2015,12(5):456-460.
[2]Tarakji B,Gazal G,Al-Maweri SA,et al.Guideline for the diagnosis and treatment of recurrent aphthous stomatitis for dental practitioners[J].J Int Oral Health,2015,7(5):74-80.
[3]刘寿荣,黄文豹.谷氨酰胺对急性肝功能不全大鼠的防治作用[J].中国现代应用药学杂志,2015,22(6):508-510.
[4]Pradelli L,Povero M,Muscaritoli M,et al.Updated cost-effectiveness analysis of supplemental glutamine for parenteral nutrition of intensive-care patients[J].Eur J Clin Nutr,2015,69(5):546-551.
[5]Stehle P,Kuhn KS.Glutamine:An obligatory parenteral nutrition substrate in critical care therapy[J].Biomed Res Int,2015,2015:545467.
[6]Jakopin M.Murabutide revisited:a review of its pleiotropic biological effects[J].Curr Med Chem,2013,20(16):2068-2079.
[7]章静波.组织和细胞培养技术[M].3版.北京:人民卫生出版社,2014:66.
[8]王春,向学熔,杨鑫,等.盐酸小檗碱抑制人颊黏膜成纤维细胞炎症反应的初步实验研究[J].重庆医学,2010,39(10):1222-1223.
[9]张优琴,江春霞,王智巍,等.复发性口腔溃疡的临床治疗进展[J].中国药房,2015,26(35):5030-5032.
[10]Kalaev VN,Artiukhov VG,Nechaeva MS.Micronucleus test of human oral buccal epithelium:problems,progress and prospects[J].Tsitol Genet,2014,48(6):62-80.
[11]薛雅蓉,庄重,刘智慧.设计利用现代科学仪器 紧跟科学前沿的细胞生物学实验[J].实验技术与管理,2013,30(6):163-166.
[12]Ivanov KP.Modern medical problems of energy exchange in humans[J].Vestn Ross Akad Med Nauk,2013,6(1):56-59.
[13]Bishop N.Clinical management of hypophosphatasia[J].Clin Cases Miner Bone Metab,2015,12(2):170-173.
[14]黄剑峰,王佳鸣,崔磊.氨对人表皮角质细胞生长和代谢的影响[J].中国医药生物技术,2007,2(2):123-129.
The influence of alanyl-glutamine on the bioactivity of human buccal fibroblasts in vitro*
Che Keke1,Liu Xin2△,Qing Shanglan2,Zhang Xicheng2
(1.Department of Pharmacy;2.Department of Stomatology,People′s Hospital of Chongqing,Chongqing 400014,China)
ObjectiveTo study the influence of alanyl-glutamine (Ala-Gln) on the cells growth,protein synthesis,and alkaline phosphatase (ALP) bioactivity of human buccal fibroblasts in vitro.MethodsThe human buccal fibroblasts in vitro were divided into the control group(group N ),Ala-Gln group (group A) and Gln group (group G).Group A and G set up 7 gradient concentrations(8,4,2,1,1/2,1/4,1/8 times recommended concentration) respectively,then cultured for 12,24,36,48,60 and 72 h.Flow cytometry was used to count cells,and drew cell growth curve as well.In addition,the ALP concentration in the corresponding period was detected by using euzymelinked immunosorbent assay,the total protein content of the cells was detected after 72 h.ResultsThe amount of cells in group N did not change obviously within 72 h,ALP contents increased over time but the changes in group A and G were more significant(P<0.05).The cell growths in group A,G were obviously accelerated within 24 h,and the content of ALP also increased significantly (P<0.05).The change of 1/2 times recommended concentration group was significantly better than that of other concentration groups.The cell protein contents of each drug concentration group were higher than group N(P<0.05).ConclusionAla-Gln can accelerate the growth of buccal fibroblasts.However,when the concentration is too high or too low,the sustaining growth of cells is depressed.The 1/2 times recommended concentration of Ala-Gln(16.5 mg/mL) is more reasonable.
mouth mucosa;fibroblasts;alkaline phosphatase;alanyl-glutamine;cell growth
重庆市卫生和计划生育委员会医学科研项目(2013-02-098,2015MSXM067)。作者简介:车坷科(1981-),主管药师,在读博士,主要从事临床药物治疗学与生物药剂学研究。△
,E-mail:ares_young@163.com。
论著·基础研究10.3969/j.issn.1671-8348.2016.22.002
R963
A
1671-8348(2016)22-3028-03
2016-02-08
2016-03-15)
