熔盐法制备Mn掺杂TiO2纳米线及其光催化性能
2016-09-15崔伟豪欧阳申珅
崔伟豪,欧阳申珅,王 騊,王 晟
(浙江理工大学先进纺织材料与制备技术教育部重点实验室,杭州 310018)
熔盐法制备Mn掺杂TiO2纳米线及其光催化性能
崔伟豪,欧阳申珅,王騊,王晟
(浙江理工大学先进纺织材料与制备技术教育部重点实验室,杭州 310018)
以硝酸锰(Mn(NO3)2)为锰源,P25纳米粒子为钛源,采用熔盐法制备掺杂锰的金红石TiO2光催化剂。使用SEM、TEM、XRD、EDS等手段对其形貌、结构、物相进行表征,并以罗丹明B为目标污染物,通过调节Mn的掺杂量,探索Mn的掺杂量对可见光催化降解罗丹明B的影响。结果表明:Mn/Ti原子比为1/50的样品(10-Mn-TiO2)对罗丹明B降解作用最好,该样品为一维线状结构,结晶度高,且直径分布均一,纵横比高达400以上,其有效催化面积最大。
熔盐法;Mn-TiO2复合物;可见光催化
0 引 言
纳米TiO2光催化剂由于其化学性质稳定、催化活性高、热稳定性好,且具有反应条件温和,成本低廉,彻底降解产物多(产物为CO2、H2O等简单的小分子化合物)等优点,在空气净化,水处理等领域被认为具有潜在应用价值。
然而,纳米TiO2作为一种半导体材料,其禁带宽度较大,只有在紫外光激发下才具有光催化活性;此外,由于光生电子和空穴易复合,从而使光催化效率降低。以上因素极大地限制了TiO2光催化剂的使用范围。
为了改善TiO2光催化剂的性能,人们做了大量的探索,对TiO2光催化剂[1-3]的改性方法主要有:贵金属沉积[4-6]、过渡金属离子掺杂[7-9]、复合半导体[10-11]、提高比表面积、表面酸化处理等。以上改性工作都使纳米TiO2的光催化活性有一定程度的提高。在以上方法中,过渡金属离子掺杂被认为是最有效方法之一,并且备受关注。已有文献报道,使用Fe、Cr、Co、Ni、V、Mn等过渡金属离子掺杂后可以使纳米TiO2光催化剂在可见光区的催化活性明显提高[12]。过渡金属离子掺杂的作用机理为:在TiO2晶格中掺入一定量的过渡金属离子,会改变TiO2的结晶度或使其表面产生缺陷,成为光生电子-空穴对的浅势捕获阱,延长电子-空穴的复合时间,从而提高催化性能。通过过渡金属离子掺杂,也可以改善TiO2光催化剂对反应物的吸附性能,提高催化效率。锰是一种常见的过渡金属元素,具有独特的电子结构,是过渡金属离子掺杂改性TiO2光催化剂经常使用的一种元素。通过掺杂改性使Mn2+进入TiO2的晶格内,可以引入新能级,降低电子跃迁的能垒,并且使金红石型TiO2晶体表面产生更多氧空位,有利于提高TiO2的光催化性能[13]。
金属离子掺杂TiO2的方法有很多,采用不同的方法得到的催化剂的尺寸大小、表观形貌、结晶度等性质均有不同,所以光催化活性也有很大的不同。常用的掺杂方法主要有沉淀法[14-16]、浸渍法[17-18]、离子注入法[19]、化学气相沉积法、等离子体火焰法等。熔盐法是将一种或多种低熔点的盐类作为反应介质,合成过程中盐类熔化为液相,反应物在其中有一定的溶解度,在熔盐状态的离子迁移率比在固体中高约1010倍,使反应物在液相中以原子尺度混合,使反应由固-固反应转化为固-液反应。与传统的沉淀法、浸渍法及离子注入法相比,该方法具有技术难度要求低、制备成本低、方法简单、反应体系纯净、易于控制等优点。
根据文献报道,质量分数80%NaCl(熔点801 ℃)和质量分数20%Na2HPO4(熔点985 ℃)的低共熔温度约为735 ℃[20-21]。实验基于熔盐法制备TiO2纳米线的思路,以Mn(NO3)2为锰源,NaCl和Na2HPO4的共熔盐为反应介质,P25为钛源,为提高离子扩散速率,升温至825 ℃,在NaCl和Na2HPO4的共熔体系中制备Mn-TiO2复合光催化剂。将光催化剂的光响应范围拓展至可见光区,并通过降解罗丹明B来研究其光催化性能。
1 实验部分
1.1实验试剂
P25(混晶型TiO2,锐钛矿型与金红石型重量比约为7∶3,德国Degussa公司);氯化钠(NaCl,AR,上海试四赫维化工有限公司);磷酸氢二钠(Na2HPO4,AR,湖州湖试化学试剂有限公司);硝酸锰(Mn(NO3)2,AR,国药集团化学试剂有限公司);罗丹明B(TP,东京化成工业株式会社)。
1.2实验仪器
马弗炉(SXL-1008型,上海精宏实验设备有限公司);光化学反应仪(XPA-2,南京胥江机电厂,350W氙灯,插入滤光片滤掉波长在420 nm以下的光源)。
1.3TiO2纳米线的制备
称取100 mg P25、400 mg NaCl和100 mg Na2HPO4,混合,在玛瑙研钵中充分研磨,使其分布均匀。将研磨后的混合物置于马弗炉中煅烧(升温速率10 ℃/min,升温至825 ℃,保持8 h,降温速率5 ℃/min),冷却至室温后,取出煅烧产物。用煮沸的去离子水反复洗涤,除去残余的可溶盐,过滤,80 ℃烘干,即得到TiO2纳米线,记为p-TiO2。
1.4Mn-TiO2光催化剂的制备
以Mn(NO3)2为锰源制备Mn-TiO2光催化剂,称取100 mg P25、400 mg NaCl和100 mg Na2HPO4,再加入一定量的Mn(NO3)2,混合,在玛瑙研钵中充分研磨,使其分布均匀。将研磨后的混合物置于马弗炉中煅烧(升温速率10 ℃/min,升温至825 ℃,保持8 h,降温速率5 ℃/min),冷却至室温后,取出煅烧产物。用煮沸的去离子水反复洗涤,除去残余的可溶盐,过滤,80 ℃烘干,即得到所需样品。其中,在制备过程中加入Mn(NO3)2的量为10、15、20 mg所得的样品记为10-Mn-TiO2、15-Mn-TiO2、20-Mn-TiO2。
1.5测试与表征
采用场发射扫描电子显微镜(FESEM,S-4800,HITACHI公司)和透射电子显微镜(TEM-2010(HR),日本电子公司)观察Mn-TiO2催化剂的微观形貌;采用电子能谱仪(INGA-ENERGY 200,英国OXFORD公司)分析Mn-TiO2催化剂的元素组成;采用X射线粉末衍射仪(XRD,美国热电ARL公司)对产物中元素的存在形式进行成分分析(工作电压:40 kV;工作电流:40 mA;扫描范围:10~80°;扫描速度:2°/min);采用紫外-可见分光光度计(752(UV-2000),上海菁华科技仪器有限公司)对Mn-TiO2光催化剂降解罗丹明B溶液后的吸光度进行测试;使用紫外可见分光光度计(BWS003,必达泰克光电科技有限公司)以KBr为背景测得样品的紫外-可见漫反射光谱。
1.6Mn-TiO2光催化剂降解罗丹明B
采用可见光光催化降解罗丹明B溶液,以罗丹明B溶液降解的程度来评价Mn-TiO2光催化剂的可见光光催化活性。可见光光催化降解使用的罗丹明B溶液的浓度为1×10-6mol/L,使用350 W氙灯作为反应光源(插入滤光片,滤掉波长在420 nm以下的光源)。将20 mg P25及p-TiO2、10-Mn-TiO2、15-Mn-TiO2、20-Mn-TiO2的Mn-TiO2复合物分别加入20 ml 1.0×10-6mol/L的罗丹明B溶液中,遮光超声分散10 min,在暗处搅拌10 h,使均匀分散,并达到吸附、脱附平衡。在350 W氙灯可见光照下进行催化降解,在反应过程中每隔1 h进行取样,离心得到上清液,并使用紫外-可见分光光度计测定所得上清液的吸光度。
2 结果与讨论
2.1熔盐法制备TiO2纳米线的反应机理
实验采用NaCl和Na2HPO4作为共熔盐,P25为钛源,制备TiO2纳米线,其反应机理如下:
(1)

(2)

(3)
Na2HPO4不稳定,当体系温度高于215 ℃时,Na2HPO4会分解为Na4P2O7和H2O,如式(1)所示;当温度高于600 ℃时,反应体系中亚稳相的锐钛矿型TiO2与Na4P2O7反应,生成中间产物Na4TiP2O9,如式(2)所示,同时处于热力学稳定状态的金红石型TiO2不参与此反应;随着温度继续升高,中间产物Na4TiP2O9分解,形成金红石型TiO2,如式(3)所示。因此,中间产物Na4TiP2O9的存在至关重要,使反应体系中钛矿型TiO2不断转变为金红石型TiO2。由纯锐钛矿TiO2反应生成的纳米线尺寸分布不均一,而P25同时含有锐钛矿相和金红石相TiO2,它既可以成为金红石相纳米线的晶种,又可以作为纳米线生长过程所需的补充物,因此生成的纳米线尺寸分布较均一。
2.2样品的微观形态及元素分析
图1是TiO2纳米线以及不同掺杂比例的Mn-TiO2复合物的SEM图。由图1(a)(b)可知,p-TiO2和10-Mn-TiO2形貌特征为一维线状,其直径分布均一,约为100 nm,长度约为5~40 μm,纵横比高达400,为典型的一维线状的结构。图1(e)是10-Mn-TiO2在低倍数下的SEM图,可以明显的看出其一维线状的形貌。随着锰掺杂量的提高,15-Mn-TiO2的形貌已经开始发生变化,这从图1(c)中可以看出,相比于样品10-Mn-TiO2,样品15-Mn-TiO2的形貌变得杂乱,单根样品在变粗变短,纵横比下降。继续提高锰掺杂量,一维线状结构被彻底破坏,取而代之的是大量的杆状、短棒状结构,如图1(d)(f)所示。
根据X射线能谱(EDS)的测试结果,10-Mn-TiO2、15-Mn-TiO2、20-Mn-TiO23个样品中Mn/Ti的原子比分别约为1/50、2/50、3/50。随着过渡金属前驱体添加量增加,产物掺杂量也有所增加。10-Mn-TiO2的形貌规整,尺寸均匀,与p-TiO2相差不大,均为一维线状结构。样品15-Mn-TiO2与20-Mn-TiO2中锰的掺杂量虽然得到提高,但产物形貌杂乱,尺寸增大,纵横比下降。

图1 不同掺杂比例Mn-TiO2复合物的扫描电镜照片
图2是单根10-Mn-TiO2纳米线的TEM图;图3(a)和图3(b)分别是p-TiO2和10-Mn-TiO2的X射线光电子能谱图。由图2(a)可清晰的看出,单根TiO2纳米线直径约为100 nm,纳米线的顶端为圆锥形,圆锥顶角约为114°。图2(b)是单根10-Mn-TiO2纳米线表面的局部高分辨率透射图,从中可以看出,纳米线的位错和缺陷很少,高度结晶。由X射线衍射谱图(图4)可知,所制备的Mn-TiO2复合物结晶性良好且均为金红石型,图2(b)很好地证实了这一点。根据晶格条纹进行测量,10-Mn-TiO2纳米线晶格间距约为0.33 nm,与金红石(110)晶面间距相比略有增大,这可能是Mn的掺杂一定程度上影响了TiO2的晶体结构[22]。图3可见,p-TiO2中主要为元素Ti和O,10-Mn-TiO2中主要为元素Ti、O和Mn,Mn/Ti原子比约为1/50,图3(b)进一步证明了TiO2纳米线中Mn元素的存在。

图2 10-Mn-TiO2纳米线的透射电镜照片
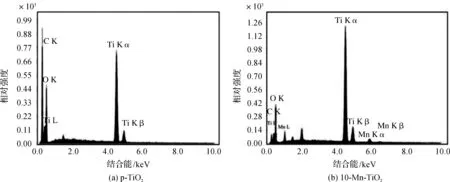
图3 X射线光电子能谱图
2.3晶型分析
图4是不同TiO2催化剂样品的X射线衍射谱图。从图4可以看出,以熔盐法制备的TiO2催化剂均显示出TiO2金红石的(110)、(101)、(200)、(111)、(210)、(211)、(220)、(002)、(310)、(301)和(112)晶面的特征峰,与之对应的2θ值分别为27.44°、36.10°、39.16°、41.24°、44.04°、54.36°、56.66°、62.78°、64.10°、69.08°和69.88°。各个衍射峰与金红石标准卡片一致,且无锐钛矿衍射峰存在。图中的衍射峰高且尖锐,说明金红石相的结晶度很高。与p-TiO2相比,掺杂Mn后,TiO2晶型并未发生变化。样品15-Mn-TiO2和20-Mn-TiO2在2θ为48.14°处有一小峰,对应的是金属Mn的(110)晶面。但是样品10-Mn-TiO2未发现Mn的衍射峰,这可能是由于Mn在TiO2中掺杂得较均匀,且掺杂量比较小所导致的。
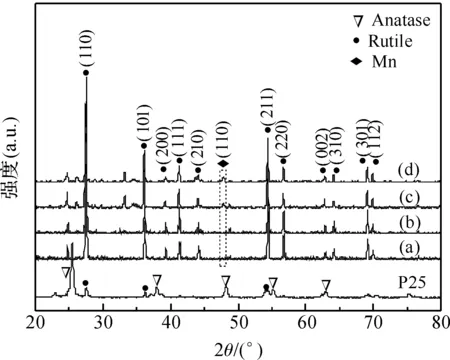
(a)p-TiO2;(b)10-Mn-TiO2;(c)15-Mn-TiO2;(d)20-Mn-TiO2图4 P25和不同TiO2催化剂样品的X射线衍射谱图
2.4紫外可见漫反射光谱分析
图5(a)是不同TiO2催化剂样品的紫外可见漫反射光谱,图5(b)是不同TiO2催化剂样品的照片。在波长小于400 nm的紫外光区,P25光催化剂有很强的吸收,但在可见光区的吸收非常弱。未掺杂Mn的p-TiO2纳米线在可见光区吸收较弱,在紫外光区吸收减弱的原因可能是由于p-TiO2纳米线的尺寸远大于P25(平均粒径21 nm)光催化剂,使得吸收光的有效面积减小的缘故。随着锰掺杂量的增加,样品可见光的吸收明显增强。在可见光区,Mn掺杂的TiO2样品10-Mn-TiO2、15-Mn-TiO2、20-Mn-TiO2都比P25有着更好的吸收。这可能是因为Mn2+掺杂进入了TiO2的晶格之中或存在于晶粒间隙,成为电子-空穴对的浅势俘获阱,使电子与空穴的复合时间延长。同时,引入Mn2+,改变了TiO2的能级结构,使得电子跃迁由原来的一步完成变为两步或多步完成,激发电子跃迁所需的能量降低至可见光区域,从而提高了TiO2的可见光光催化性能[13]。

(a)p-TiO2;(b)10-Mn-TiO2;(c)15-Mn-TiO2;(d)20-Mn-TiO2图5 不同TiO2催化剂样品的紫外可见漫反射光谱和照片
2.5光催化活性分析
图6为不同Mn-TiO2催化剂在可见光下对罗丹明B溶液的降解曲线。图6可见,经可见光照12 h后,加入P25和p-TiO2的体系中罗丹明B浓度小幅降低。这可能是因为罗丹明B具有可见光吸收,且当其吸附在催化剂表面时激发态的罗丹明B将电子转移到催化剂上,产生了光敏化作用自降解所致[23]。相比于P25及p-TiO2,Mn-TiO2催化剂的可见光光催化效果显著。12 h光照后,10-Mn-TiO2、15-Mn-TiO2、20-Mn-TiO2对罗丹明的降解率分别达到87%、75%、57%。其中,10-Mn-TiO2的光催化效率最好。随着Mn掺杂量的提高,15-Mn-TiO2和20-Mn-TiO2的光催化降解能力反而逐步降低。通过对图1中不同掺杂比例的Mn-TiO2复合物SEM图进行分析,10-Mn-TiO2与p-TiO2均为一维线状结构,纵横比高达400以上,15-Mn-TiO2和20-Mn-TiO2的纵横比均有不同程度的降低,即相同质量催化剂的有效催化面积减小,降低了催化效率。综合实验结果,Mn/Ti原子比为1/50的样品10-Mn-TiO2可见光催化性能最好。
由光催化实验可知,使用熔盐法制备过渡金属Mn掺杂的Mn-TiO2催化剂,在可见光区的催化性能有了明显的提高,拓宽了TiO2光响应范围至可见光区域。这是因为,Mn2+的引入,改变了TiO2的能级结构,使得电子跃迁由原来的一步完成变为两步或多步完成,激发电子跃迁所需能量的降低,同时,掺杂的Mn2+成为了光电子的浅势俘获阱,使光生电子-空穴有效分离,电子与空穴的复合时间延长。

图6 不同TiO2催化剂样品可见光降解罗丹明B速率曲线
3 结 论
以熔盐法制备了具有可见光响应的Mn-TiO2复合物,并对其可见光催化性能进行了研究。所制备的Mn-TiO2复合物均为金红石相,高度结晶。适量Mn掺杂的Mn-TiO2为一维线状结构,过量Mn掺杂的Mn-TiO2为杆状或短棒状。在可见光下,所有Mn-TiO2复合物对罗丹明B均有可见光降解效果,其中具有一维线状结构的10-Mn-TiO2对罗丹明B降解效果最好。
[1] 贺飞, 唐怀军. 纳米TiO2光催化剂负载技术研究[J]. 环境污染治理技术与设备, 2001, 2(2): 47-58.
[2] 廖振华, 陈建军, 姚可夫, 等. 纳米TiO2光催化剂负载化的研究进展[J]. 无机材料学报, 2004, 19(1): 17-24.
[3] KIM S, HWANG S J, CHOI W. Visible light active platinum-ion-doped TiO2photocatalyst[J]. The Journal of Physical Chemistry B, 2005, 109(51): 24260-24267.
[4] 刘秀华, 邓义, 龙素群, 等. Pt/TiO2纳米粒子的制备及其光催化性能研究[J]. 功能材料, 2008, 38(A07): 2407-2411.
[5] 姜艳丽, 刘惠玲, 田玫, 等. 离子溅射沉积法制备Pt-TiO2/Ti催化剂及其性能研究[J]. 功能材料, 2007, 38(A07): 2412-2414.
[6] KIYONAGA T, MITSUI T, TORIKOSHI M, et al. Ultrafast photosynthetic reduction of elemental sulfur by Au nanoparticle-loaded TiO2[J]. The Journal of Physical Chemistry B, 2006, 110(22): 10771-10778.
[7] 姜丽娜, 刘金华, 孟德营. 二氧化钛光催化技术的应用[J]. 山东陶瓷, 2009, 32(5): 34-36.
[8] VAMATHEVAN V, TSE H, AMAL R, et al. Effects of Fe3+and Ag+ions on the photocatalytic degradation of sucrose in water [J]. Catal Today, 2001, 68: 201-208.
[9] FRANK S N, BARD A J. Heterogeneous photocatalytic oxidation of cyanide ion in aqueous solutions at titanium dioxide powder[J]. Journal of the American Chemical Society, 1977, 99(1): 303-304.
[10] PUMA G L. Novel one step hydrothermal synthesis of TiO2/WO3nanocomposites with enhanced photocatalytic activity[J]. Chemical Communications, 2007, 45: 4749-4751.
[11] KOMINAMI H, KATO J, MURAKAMI S, et al. Solvothermal syntheses of semiconductor photocatalysts of ultra-high activities[J]. Catalysis Today, 2003, 84(3): 181-189.
[12] JO W K, KANG H J. Polyacrylonitrile-TiO2fibers for control of gaseous aromatic compounds[J]. Ind Eng Chem Res, 2013, 52(12): 4475-4483.
[13] 张立艳, 张英锋, 马子川. 锰在光催化中的作用与影响[J]. 化学教育, 2011(1): 4-15.
[14] ZHANG Y H, RELLER A. Phase transformation and grain growth of doped nanosized titania[J]. Materials Science and Engineering: C, 2002, 19(1): 323-326.
[15] WANG S M, SUN X J. Discussion on solar photocatalytic degradation of treated leachate using transition metal-nonmetal Co-doped TiO2[J]. Advanced Materials Research, 2013, 781: 1954-1957.
[17] LI X Z, LI F B, YANG C L, et al. Photocatalytic activity of WOx-TiO2under visible light irradiation[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2001, 141(2): 209-217.
[18] XU A W, GAO Y, LIU H Q. The preparation, characterization, and their photocatalytic activities of rare-earth-doped TiO2nanoparticles[J]. Journal of Catalysis, 2002, 207(2): 151-157.
[19] MARDARE D, TASCA M, DELIBAS M, et al. On the structural properties and optical transmittance of TiO2rf sputtered thin films[J]. Applied Surface Science, 2000, 156(1): 200-206.
[20] ROY B, AHRENKIEL S P, FUIERER P A. Controlling the size and morphology of TiO2powder by molten and solid salt synthesis[J]. Journal of the American Ceramic Society, 2008, 91(8): 2455-2463.
[21] ROY B, FUIERER P A. Influence of sodium chloride and dibasic sodium phosphate salt matrices on the anatase-rutile phase transformation and particle size of titanium dioxide powder[J]. Journal of the American Ceramic Society, 2010, 93(2): 436-444.
[22] 刘文军, 薛成山, 石锋, 等. Mn掺杂GaN纳米条的制备和性质的研究[J]. 山东科学, 2010, 23(1): 28-31.
[23] YAN X, OHNO T, NISHIJIMA K, et al. Is methylene blue an appropriate substrate for a photocatalytic activity test? A study with visible-light responsive titania[J]. Chemical Physics Letters, 2006, 429(4): 606-610.
(责任编辑: 张祖尧)
Preparation of Mn-doped TiO2Nanowire by Molten Salt Synthesis and Its Photocatalytic Performance
CUIWeihao,OUYANGShenshen,WANGTao,WANGSheng
(Key Laboratory of Advanced Textile Materials and Manufacturing Technology, Ministry of Education of PRC, Zhejiang Sci-Tech University, Hangzhou 310018, China)
Mn-doped rutile TiO2photocatalysts were prepared with molten salt synthesis by using Mn(NO3)2as manganese source and P25 nanoparticles as titanium source. The morphology, structure and phase of photocatalyst were characterized by SEM, TEM, XRD and EDS. Rhodamine B was used as a target pollutant. The effects of various Mn doping concentrations on the photodecomposition of Rhodamine B under visible light irradiation were investigated. The results indicate that when the atomic ratio of Mn/Ti is 1∶50 (sample 10-Mn-TiO2), the degradation of Rhodamine B is the best; the sample shows one-dimensional linear structure, uniform diameter distribution and high degree of crystallinity; the aspect ratio is as high as 400; the effective catalysis area is the largest.
molten salt synthesis; Mn-TiO2compound; visible light photocatalysis
10.3969/j.issn.1673-3851.2016.01.006
2015-02-03
国家自然科学基金项目(51372227,51471153);浙江省自然科学基金项目(LY14E020011)
崔伟豪(1993-),男,安徽蚌埠人,硕士研究生,主要从事纳米材料方面的研究。
王晟,E-mail:wangsheng571@hotmail.com
O649.1
A
1673- 3851 (2016) 01- 0035- 06 引用页码: 010203
