排水法收集二氧化碳可行性的实验探究
2016-09-05洪碧瑜
洪碧瑜
摘要:从不同浓度稀盐酸与石灰石反应、用排水法收集二氧化碳的实验中获取实证数据,结合手持技术对二氧化碳浓度进行测定,以优化稀盐酸浓度的视角,从二氧化碳收集数量、速率、收集率及所达到的浓度等方面,探讨了排水法收集二氧化碳的可行性。
关键词:排水法集气;二氧化碳浓度测定;手持技术;可行性;实验探究
文章编号:1005–6629(2016)7–0065–03 中图分类号:G633.8 文献标识码:B
1 问题的提出
初中化学教材中二氧化碳气体只提到用向上排空气法收集[1],许多老师在进行这部分知识的教学时,也认为二氧化碳可溶于水,因此不宜用排水法收集。但近年来,对此看法的质疑日渐增多,并有一些老师撰文对排水法收集的可行性进行了论证。这些文章更多的是从气体收集的可行性角度,如二氧化碳水溶液中微粒的存在形式[2]、二氧化碳溶解时在水中的扩散速率[3]、二氧化碳溶解于水的速度实验[4]及不同方法收集二氧化碳的纯度比较[5]等方面进行论证;而涉及气体发生的可行性,如实验时所选择石灰石形状、稀盐酸浓度的不同对排水法收集二氧化碳会造成怎样影响等等的研究则相对较少。本文尝试从反应物选择的角度,从另一侧面对排水法收集二氧化碳的可行性进行论证。
2 问题研究
2.1 排水法收集二氧化碳的实验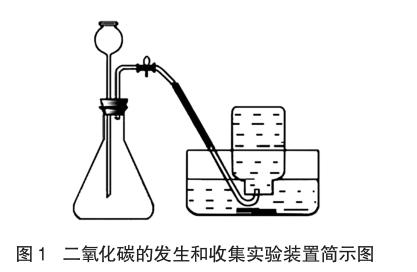
利用图1所示的装置制取和收集二氧化碳(集气瓶容积为145mL,锥形瓶容积为165mL)。
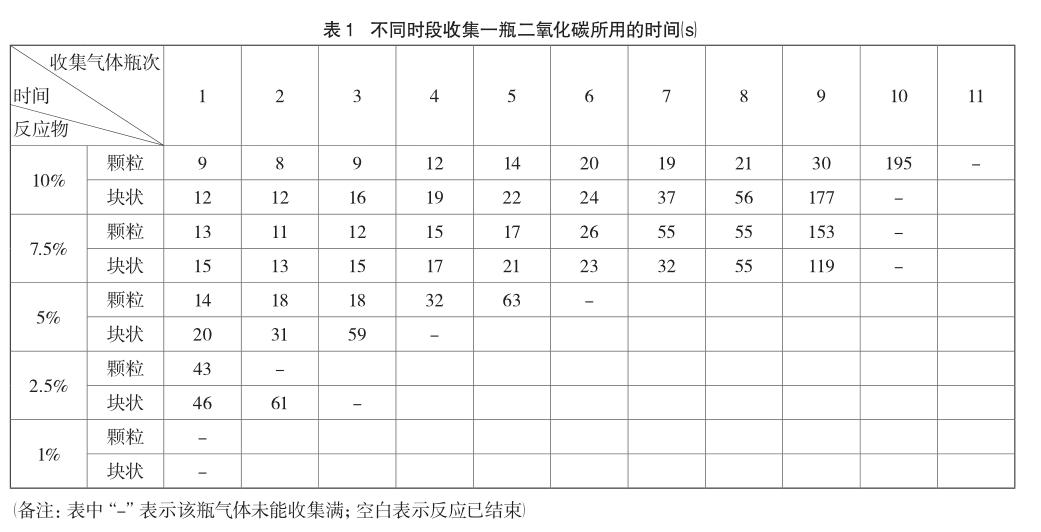
选用同批次的颗粒状与块状石灰石分别与浓度为10%、7.5%、5%、2.5%、1%的稀盐酸(每次用量均取70mL)进行实验。每次制取实验用容积为145mL的集气瓶连续收集反应产生的气体,并记录收集每瓶气体所用的时间,所得数据如表1所示。
就本实验获取的数据来看,浓度为1%的稀盐酸不能完成气体的收集,浓度为2.5%的稀盐酸收集的气体偏少且耗时较长,因此,实验制取时不宜采用这两种浓度的稀盐酸。仅从收集气体的数量来看,其他三种溶质质量分数稀盐酸均可用于制取二氧化碳的实验。
用排水法收集气体,还存在着一个收集率的问题。从理论上计算,70mL 10%、7.5%、5%的稀盐酸最多产生二氧化碳的体积分别约为2241mL、1649mL、1099mL(二氧化碳的密度取1.429 g·L-1)。就表1的数据分析,各组实验实际收集的二氧化碳与理论值之间存在的差异不尽相同(实验收集到二氧化碳的瓶数乘以实验用集气瓶的容积即为实际收集的二氧化碳体积,没有收集满的一瓶没有列入统计),具体情况如表2所示。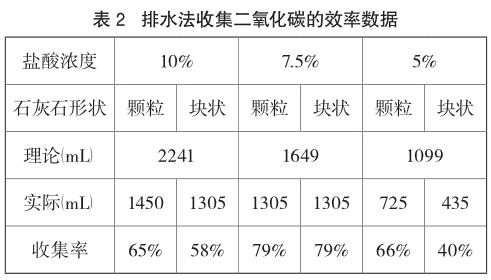
各组实验相比而言,7.5%的稀盐酸与颗粒状或块状的石灰石反应产生气体的收集率都达到了79%左右,气体利用率符合气体制取实验的要求。从另一个角度上看,这两组实验,收集前6瓶气体的平均用时分别为每瓶15.7秒和17秒,这与稀盐酸浓度10%的两组实验相差不大,而且这样的速度也达到气体收集实验的要求。
2.2 二氧化碳的浓度测定实验
为进一步验证排水法收集二氧化碳的可行性,以溶质质量分数7.5%的稀盐酸和块状石灰石为反应试剂产生二氧化碳,利用浓度传感器测定不同时刻从反应容器排出的气体中二氧化碳的浓度,并通过数据采集器和计算机绘制浓度变化曲线,从而获取实验所需的相关数据,实验装置如图2所示。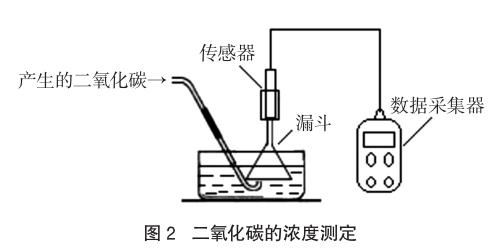
实验过程中产生的二氧化碳通过一个倒置在水中的漏斗收集。石灰石与稀盐酸反应的时间与对应排出气体中二氧化碳浓度的数据通过与漏斗相连的传感器进行测定,所得数据的图像如图3所示。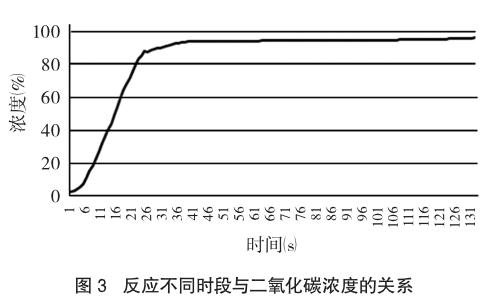
图3显示,反应过程中二氧化碳浓度的变化呈现四个主要时段:反应初期,二氧化碳浓度逐渐增大(每秒增加0.5%~1%);接着快速增大(每秒递增4%~5%);然后又逐渐变缓(每秒增加0.5%~ 1%),最后趋于稳定。结合实验过程观察到每一时段气泡冒出的情况,将相关信息归纳如表3所示。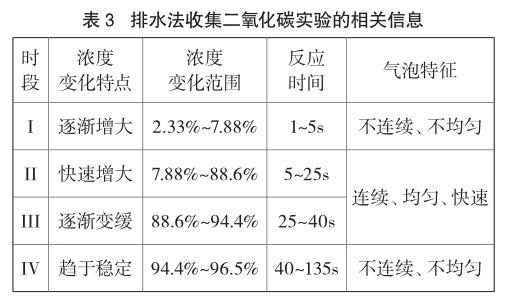
从表3可以看出,采用浓度7.5%的稀盐酸和石灰石反应制取二氧化碳,用排水法收集到的气体中二氧化碳的浓度最高可达到96.5%。为此,说明只有选择合适浓度的稀盐酸为反应物,采用排水法收集二氧化碳是完全可行的。利用浓度传感器对浓度7.5%的稀盐酸和块状石灰石反应并用排水法收集到的前四瓶气体中CO2的浓度进行测定(所得数据如表4所示),数据表明即使是第一瓶收集的二氧化碳,其浓度也达到了52.6%,对于初中二氧化碳性质实验而言,该浓度数值足够满足实验要求。为证明这一点,继续进行一组对照实验,分别采用向上排空气法和排水法进行收集二氧化碳,当收集15秒(排水法收集第一瓶二氧化碳的用时)后,用燃着的木条放在瓶口检验,发现采用排空气法收集的二氧化碳没能让燃着的木条熄灭,而用排水法收集的能使燃着的木条熄灭。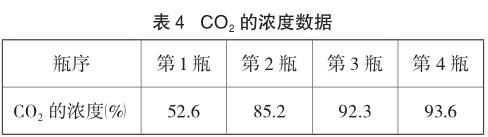
2.3 结果与讨论
2.3.1 制取二氧化碳稀盐酸浓度的选择
从表1看,并不是所有浓度的稀盐酸可以用于实验室制取二氧化碳,根据实际收集二氧化碳的数量来看,浓度1%和2.5%的稀盐酸均不适合于实验;浓度5%的稀盐酸,只有采用与颗粒状的石灰石反应,才勉强符合要求;而浓度为10%和7.5%的稀盐酸,无论是与块状或颗粒状的石灰石反应,均可满足要求,且收集二氧化碳的速率二者差别不大。表2显示,利用7.5%的稀盐酸制取二氧化碳的收集率比10%的稀盐酸高。结合考虑稀盐酸浓度对氯化氢挥发的影响及原料的利用率等因素,浓度在7.5%左右(大小偏差约为1%)的稀盐酸应是制取二氧化碳较为理想的反应试剂。这一结论的可靠性从表4的数据中也能得到证实,该数据显示,利用7.5%的稀盐酸制取并收集的二氧化碳,其浓度最少也能达到52.6%。
2.3.2 排水法收集二氧化碳的适宜时机
对于排水法收集气体,还应考虑气体发生装置中的空气是否对收集的气体会造成影响,从而选择开始收集气体的时机。在氧气的排水法收集中,有将气泡连续均匀冒出25s定为收集氧气适宜时机的研究[6]。从表3数据看,排水法收集二氧化碳,气泡刚连续均匀冒出时,气体的浓度并不高,只有7.88%,但在较短的时间内,浓度迅速增大到(88.6%),刚好与收集一瓶二氧化碳(145mL)的用时差不多。结合表4数据来看,即使是反应一开始就收集,得到的第一瓶二氧化碳仍符合实验要求,我们可以推断将气泡连续均匀冒出确定为收集二氧化碳的时机是完全可行的。
2.3.3 有关实验操作误差的讨论
在具体的实验操作过程中,石灰石的产地、石灰石形状及大小,加入稀盐酸的方式、发生装置中锥形瓶大小和导气管长短等因素各不相同,对制取二氧化碳反应的速率、排尽发生装置中空气的时间等会造成一定影响,从而可能使该实验所测得的数据存在一定的偏差。
3 结论
实验表明,排水法收集二氧化碳是可行的,但对于制取二氧化碳的反应物有一定的条件要求。若采用块状或颗粒状的石灰石与稀盐酸反应制取二氧化碳,稀盐酸的浓度不宜太小,选择浓度7.5%(±1%)左右的稀盐酸进行实验效果较为理想。
参考文献:
[1]王祖浩主编.义务教育课程标准实验教科书·化学(九年级上册)[M].上海:上海教育出版社,2014:43.
[2]陈明元.中学化学中二氧化碳溶于水的问题[J].化学教学,2014,(9):93.
[3]郑萍,陈明元.相平衡与二氧化碳在水中的扩散速率[J].贵州教育学院学报(自然科学版),2004,15(2):70.
[4][5]郁学梅.实验室二氧化碳气体的收集及检测方法再研究[J].化学教学,2014,(7):65.
[6]张章录.排水法收集氧气时机选择的实验探究[J].化学教学,2015,(8):75.
