透脓散醇提物急性毒性实验研究※
2016-09-03房良华刘沈林王瑞平胡守友
房良华 刘沈林 王瑞平 胡守友
(江苏省中医院肿瘤内科,江苏 南京 210029)
透脓散醇提物急性毒性实验研究※
房良华刘沈林王瑞平△胡守友
(江苏省中医院肿瘤内科,江苏南京210029)
目的探讨透脓散醇提物对小鼠的急性毒性反应。方法先进行预实验,取12只SPF级昆明种小鼠(雌雄各半),随机分为3组,即透脓散醇提物高、中、低剂量组,每组各4只,分别予透脓散醇提物1.00、0.75、0.50 g/mL浓度药液0.04 mL/只,每日2次灌胃给药,连续观察5 d,拟找出100%致死量(LD100)、最大全不致死量(LD0)和相应的剂量组间距r值。另取小鼠40只(雌雄各半),随机分为2组,即实验组及对照组,每组各20只,进行最大给药量实验。实验组小鼠予高浓度透脓散醇提物(1.00 g/mL)0.04 mL,对照组予0.9%氯化钠注射液0.04 mL/只,均每日2次灌胃,连续14 d。给药期间每隔2 d测实验组及对照组小鼠体质量,记录给药后2组小鼠活动、饮食情况、精神状态、不良反应情况及死亡数量、死亡时间。末次给药后测定小鼠肝、肾功能变化,然后2组小鼠全部脱颈处死、解剖,肉眼观察心、肝、脾、肺、肾、脑等各脏器有无异常。结果预实验期间透脓散醇提物高、中、低剂量组小鼠生命状况良好,无死亡现象,无法测出该药的半数致死量(LD50)。最大给药量实验观察期14 d内,实验组及对照组小鼠毛色、饮食、粪便、活动均未见异常,肝、肾功能指标正常,未见任何中毒表现,无死亡,尸检各脏器无异常。结论小鼠对透脓散醇提物的最大耐受量为40 g/kg,该量为临床用量0.625 g/kg的64倍,可以认为临床用药安全。
急性毒性试验;中草药;小鼠
透脓散是《外科正宗》中常用的托毒排脓方剂,由生黄芪、当归、川芎、炮穿山甲、皂角刺5味中药组成,具有补气托毒、养血散瘀、软坚溃膜等功效。临床主要用于正虚不能托毒、内已成脓、外不易溃、漫肿无头之痈疡。有研究表明,透脓散还有良好的抗感染[1-2]和抗肿瘤作用[3-4]。本实验通过对昆明种小鼠灌胃给药,观察透脓散醇提物的急性毒性,初步评价其在肿瘤治疗中的安全性,确定其主要的毒性反应症状,为进一步的研究提供科学依据。
1 材料与方法
1.1材料
1.1.1实验动物SPF级昆明种小鼠52只,体质量18~22 g,雌雄各半,由中国人民解放军军事医学科学院实验动物中心提供。实验动物质量合格证SCXK(军)2007-004,合格证编号0024645,实验动物使用许可证SYXK(军)2007-030。放入实验室环境中分笼饲养,每笼5只,保持环境温度20~25 ℃,湿度40%~70%,饲以实验动物用配合饲料,自由进食、饮水。
1.1.2主要药物与试剂透脓散:透脓散中5种药材黄芪、当归、皂角刺、川芎及炮穿山甲均由江苏省中医院提供。其名称、产地、产品批号、生产日期和用量详见表1。取10倍量的药材共375 g,经粉碎过40目筛后用80%乙醇煎煮2次,第1次加入10倍量80%乙醇回流提取2 h,第2次加入8倍量80%乙醇回流提取1.5 h,合并2次提取物,70 ℃减压浓缩回收至无醇并浓缩至1 g生药/mL,-20 ℃冰箱保存备用。
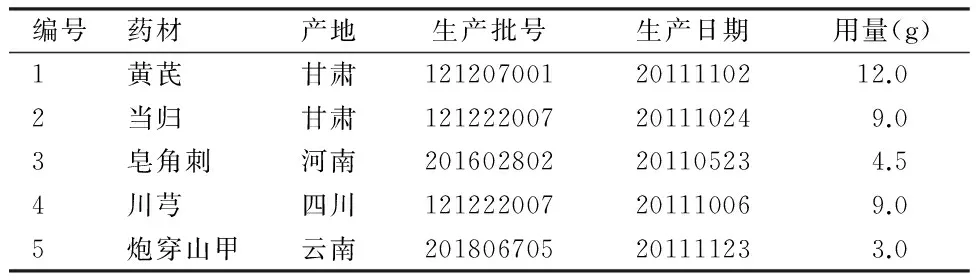
表1 透脓散药材信息
1.2实验方法1.2.1预实验取12只小鼠(雌雄各半),适应性喂养3 d后,禁食12 h,不禁水,随机分为3组,即透脓散醇提物高、中、低剂量组,每组各4只。按照受试物的配制方法,配制成透脓散醇提物1.00、0.75、0.50 g/mL(高、中、低)3个浓度的药液,以0.04 mL/g每日分2次给各对应组小鼠灌胃给药,连续观察5 d,拟找出100%致死量(100% lethal dose,LD100)、最大不全致死量(LD0)和相应的剂量组间距r值。1.2.2最大给药量实验另取小鼠40只(雌雄各半),适应性喂养3 d后,禁食12 h,不禁水,随机分为2组,即实验组及对照组,每组各20只。实验组小鼠予高浓度透脓散醇(1.00 g/mL)0.04 mL,每日2次灌胃给药,连续14 d。对照组小鼠予0.9%氯化钠注射液0.04 mL,每日2次灌胃,连续14 d。
1.3观察项目最大给药量实验给药期间每隔2 d测实验组及对照组小鼠体质量,记录给药后2组小鼠活动、饮食情况、精神状态、不良反应情况及死亡数量、死亡时间[5]。末次给药后24 h眼眶静脉丛采血,测定小鼠肝、肾功能[主要指标为丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、尿素氮(BUN)、血肌酐(Cr)]变化。然后2组小鼠全部脱颈处死、解剖,肉眼观察心、肝、脾、肺、肾、脑等各脏器有无异常[6]。

2 结 果
2.1预实验结果预实验期间透脓散醇提物高、中、低剂量组小鼠生命状况良好,无死亡现象,因而无法测出该药的LD50,故进行最大给药量实验。2.2最大给药量实验结果
2.2.1小鼠一般情况观察期14 d内,实验组及对照组小鼠毛色、饮食、粪便、活动均未见异常,无小鼠死亡。
2.2.22组小鼠体质量变化情况比较见表2。
表2 2组小鼠体质量变化情况比较 ±s
由表2可见,随着用药时间的延长,实验组和对照组小鼠体质量均呈上升趋势,但2组间小鼠体质量变化比较差异无统计学意义(P>0.05)。2组给药后14 d小鼠体质量与本组给药前比较差异均无统计学意义(P>0.05)。
2.2.32组小鼠肝、肾功能指标比较见表3。
表32组小鼠肝、肾功能指标比较

±s
由表3可见,与对照组比较,实验组小鼠肝、肾功能无明显变化,比较差异无统计学意义(P>0.05)。
2.2.42组小鼠主要脏器变化经解剖肉眼观察,2组小鼠心、肝、脾、肺、肾、脑等主要器官未见明显异常。
3 讨 论
透脓散方以生黄芪为君药,善于走表,敛汗托毒消肿,兼升阳举陷;皂角刺消肿散结,拔毒透脓,与穿山甲相须为用,使脓外达;川芎、当归养血活血,扶助正气,助脓托出,用于正虚不能托毒、内已成脓、外不易溃、漫肿无头之痈疡。前期实验表明,透脓散具有良好的抗肿瘤作用,且随着剂量的增大作用增强[3,7]。目前透脓散在临床无毒性反应的报道,但由于该方常规用于痈疡的治疗,剂量较小。而用于肿瘤的治疗需要提高剂量,且基础实验研究表明其抗肿瘤作用具有明显的量效关系。因此,我们进行该药物的毒性反应实验,为后续临床使用透脓散进行抗肿瘤剂量的选择和观察指标的设计提供参考信息。本实验结果表明,小鼠对透脓散醇提物的最大耐受量为40 g/kg,该量已为临床用量0.625 g/kg的64倍,为临床提供了用药安全的依据。
中药、天然药物的急性毒性往往难以表现出来,即使在采用大剂量时能观察到动物死亡情况,但该剂量可能与有效剂量或拟临床用量相差很大,其毒性反应对其他安全性试验及临床的指导意义已不大。国家食品药品监督管理局1999年颁布的《中药新药药理毒理研究的技术要求》明确规定,因受试物的浓度或体积限制,无法测出半数致死量(LD50)时,可做最大给药量实验进行中药急性毒性实验。本研究预实验的目的有2个:①观察3个剂量对小鼠的致死率分别是多少,选择最佳剂量进行后续的正式实验。②如果3个剂量都没有出现致死,那么就选择最高剂量进行后续实验。本实验在预实验期间对实验小鼠予透脓散醇提物1.00、0.75、0.50 g/mL 3个浓度的药液灌胃,均未有小鼠死亡,未得到LD50值,故以透脓散醇提物最高浓度1.00 g/mL给药,证实小鼠完全耐受,未出现任何毒性反应,其用量相当于成人临床日用量的64倍。说明透脓散醇提取液安全,急性毒性小,LD50远远大于40 g/kg的剂量。但此实验观察时间较短,还需要结合长期毒性实验进一步观察此药物的毒性。
[1]王筠,罗燕.程氏透脓散治疗急性化脓性扁桃体炎50例[J].中国中医急症,2003,12(3):277-278.
[2]周玉霞,于君平,刘秋.透脓散治疗耳前瘘管感染70例分析[J].实用中医内科杂志,2003,17(3):206.
[3]Fang LH, Wang RP, Hu SY,et al.Tounongsan extract induces apoptosis in cultured Raji cells[J].Chin J Integr Med,2012,18(7):522-528.
[4]房良华,刘沈林,王瑞平,等.透脓散为主方治愈霍奇金淋巴瘤1例[J].中国中西医结合杂志,2013,33 (6):847-848.
[5]许迪,叶明霞,熊美云,等.WHPI经腹腔注射和静脉注射对小鼠的急性毒性研究[J].实验动物科学,2011,28(5):66-68.
[6]符翠莉,蒙大平,荣延平,等.广西苦丁茶老叶水提取物的急性毒性作用研究[J].中国临床新医学,2011,4(4):298-300.
[7]Fang LH,Wang RP,Hu SY,et al.The effect of tou nong san on transplanted tumor growth in nude mice[J].Evid Based Complement Alternat Med,2015:518454.
(本文编辑:曹志娟)
Experimental study of acute toxicity of the alcohol extraction of Tou-nong powder
FANGLianghua,LIUShenlin,WANGRuiping,etal.
DepartmentofMedicalOncology,HospitalofTraditionalChineseMedicineinJiangsuProvince,Jiangsu,Nanjing210029
Objective To study the acute toxicity reaction of alcohol extraction of Tou-nong powder in mice. Methods 12 SPF Konmin mice (half male and female) were randomly divided into three groups that Tou-nong powder-alcohol extraction high, middle and low dose groups, 4 mice in each group. Mice in high, middle and low dose groups were received Tou-nong powder-alcohol extraction at concentration of 1.00,0.75,0.50 g/mL respectively, intragastric administration of 0.04 mL/mouse, twice per day for 5 d. To find out the 100% lethal dose (LD100), lethal dose-0 (LD0) dose and the r-value of corresponding dose. The other 40 mice (half male and female) were randomly divided into experimental group and control group. Mice in experimental group received high concentration (1 g/mL) of Tou-nong powder-alcohol extraction (0.04 mL/mouse). Mice in control group received 0.9% sodium chloride injection (0.04 mL/mouse), intragastric administration twice per day for 14 d. The body mass of mice were detected every 2 d during experimental period in experimental and control groups. The activity, diet condition, mental state, adverse reaction, the number and time of deaths after administration were recorded in two groups. The changes of liver and kidney functions were mesured after final administration. Then, all mice were decapitated. The organ conditions such as heart, liver, spleen, pulmonary, kidney and brain were observed by dissection. Results Mice life indication stabilize in Tou-nong powder-alcohol extraction high, middle and low dose groups during preliminary experiments, without death, and the medianl lethal dose(LD50) could not be detected. During observation period of themaximum dosage experiment (14 d), there were no abnormal changes about coat color, eating, drinking, faeces and activity in experimental and control groups that with normal serum liver and kidney function indexes and without intoxicating phenomenon and death. Mice were sacrificed after 14 days and postmortem examination showed that there were no abnormal changes in organs. Conclusion The maximum tolerance dose of Tou-nong powder-alcohol extraction is 40 g/kg in mice which is more than 640 percent than clinical dosage (0.625 g/kg), can be considered clinical medication safety.
Acute toxicity test; Chinese herbal medicine; Mice
10.3969/j.issn.1002-2619.2016.01.026
△江苏省中医院肿瘤内科,江苏南京210029
房良华(1976—),女,副主任医师,硕士研究生导师,博士,博士后。从事肿瘤的中西医结合治疗和免疫治疗。
R285.5;R994.13
A
1002-2619(2016)01-0085-03
2014-07-15)
※ 项目来源:江苏省财政厅 江苏省科学技术厅2014年省级自然科学基金(青年科技人才专项资金)项目(编号:BK20141034);江苏省人民政府办公厅江苏高校优势学科建设工程项目(编号:NO.012062003010);江苏省六大人才高峰项目(编号:NO.2011-WS-049)
