差热分析装置改进及在物理化学实验教学中的应用
2016-08-29许新华吴梅芬肖寒霜王晓岗
许新华, 吴梅芬, 肖寒霜, 王晓岗
(同济大学 化学系, 上海 200092)
差热分析装置改进及在物理化学实验教学中的应用
许新华, 吴梅芬, 肖寒霜, 王晓岗
(同济大学 化学系, 上海200092)
介绍了用简单材料制作风冷系统,并将其用于改造实验教学用的差热分析仪。测试表明,采用风冷系统后可以大大提高差热分析仪电炉的降温速率,在常规实验条件下,一般15 min内可以将加热后的炉体温度降低到40 ℃以下,显著减少了实验中的无效等待时间,为在基础物理化学实验课程中开展综合性的差热分析实验项目创造了条件。用改造后的差热分析仪测定了KNO3-NaNO3二元熔盐体系的液固平衡相图,该熔盐组份在加热过程中经历固态晶相转变和固-液相转化,且转变温度随熔盐组成连续变化,与传统的简单二元体系相图有很大差别。采用改造后的差热分析仪可以在常规实验课时内较完整地测得该复杂体系相图,实验教学效果良好。
差热分析; 物理化学实验; 二元熔盐体系; 相图
差热分析技术是现代热分析的主流实验技术,在材料科学、物理学、化学及生命科学等领域有广泛的应用。差热分析实验是物理化学实验教学中的经典实验项目,通常以CuSO4·5H2O的脱水过程为研究对象[1-3],也有将差热分析应用于CaC2O4·2H2O脱水及分解反应[4]、铅-锡合金相图测定[5-6]、CaC2O4·H2O脱水反应动力学[6]以及层状材料热稳定性测量[7]等实验教学的研究。但是,差热分析实验教学的一个主要问题就是单次测量耗时较长,尤其是线性升温后,仪器降温过程的无效实验时间过长,导致无法在有限的实验教学课时内完成多批次测定,因此差热分析法的一些重要应用性实验项目,如相图测定或者热动力学分析等,往往无法在4课时内完成,甚至8课时完成也非常困难。差热分析仪属于比较昂贵的基础物理化学实验仪器,如果只能在实验教学中进行简单的定性观察和测量,显然是极大的浪费。有鉴于此,我们从商品化的教学型差热分析仪改造入手,通过添加简单附件,有效加快了仪器的降温速率,缩短了无效实验时间,并在经过改造的仪器上进行二元熔盐KNO3-NaNO3体系复杂相图的测定实验,取得良好的教学效果。
1 教学型差热分析仪的改造
教学型差热分析仪采用南京桑力电子设备厂的ZCR差热实验装置(见图1),该型差热分析仪控温范围为室温~1 100 ℃、升温速率1~20 ℃/min、DTA分析仪的分辨率为1V、量程为2 000V[8],能满足基础实验教学的要求。
为提高炉体的冷却速率,在仪器上加装一个风冷系统,使用微型无电刷直流风扇NMB 3100KL-04 W(80 mm×80 mm×25 mm),风扇固定在用工程塑料加工的圆环外罩上,由按钮开关控制风扇启动,由差热实验装置的控温仪提供12 V、0.15 A直流电。差热曲线测量完成后,取下加热炉顶盖及隔热盖片,将加热炉提升后,把风冷系统密贴放置在加热炉保护网罩顶端的定型卡环上(见图2),风扇产生的轴流冷风自上而下同时吹过加热炉体的炉膛内外,产生很好的冷却效果。

图1 ZCR差热实验装置加热炉体及冷却风扇附件
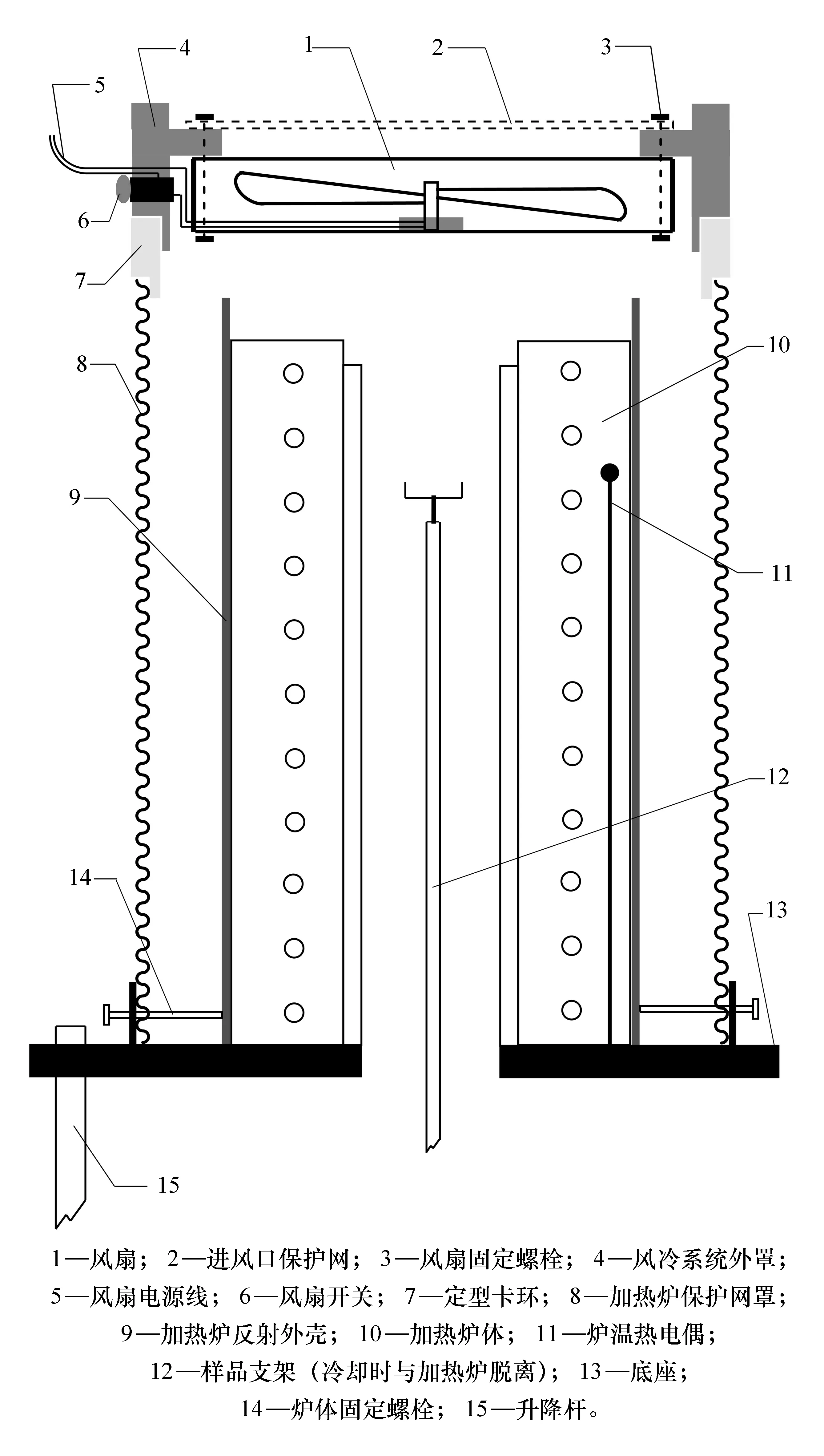
图2 风冷系统与差热加热炉装配结构图
ZCR差热实验装置的加热炉在自然冷却状态和风冷状态下的降温曲线见图3,可以看出加装风冷系统后,差热装置的加热炉能够在30 min以内自350 ℃降温至40 ℃以下,比较合理;而在自然冷却状态下,同样的降温过程耗时超过90 min,相当于2个实验课时的时间。换句话说,如果没有风冷系统,一个常规的4课时实验,除去实验指导时间和加热炉降温时间后,剩下的真正进行差热曲线测量的时间内只能完成1次差热曲线的测量,即使8课时实验也只能最多完成3次差热曲线的测量,要在有限的实验课时内完成诸如热动力学分析或者相图测定等综合性实验内容几乎是不可能的。
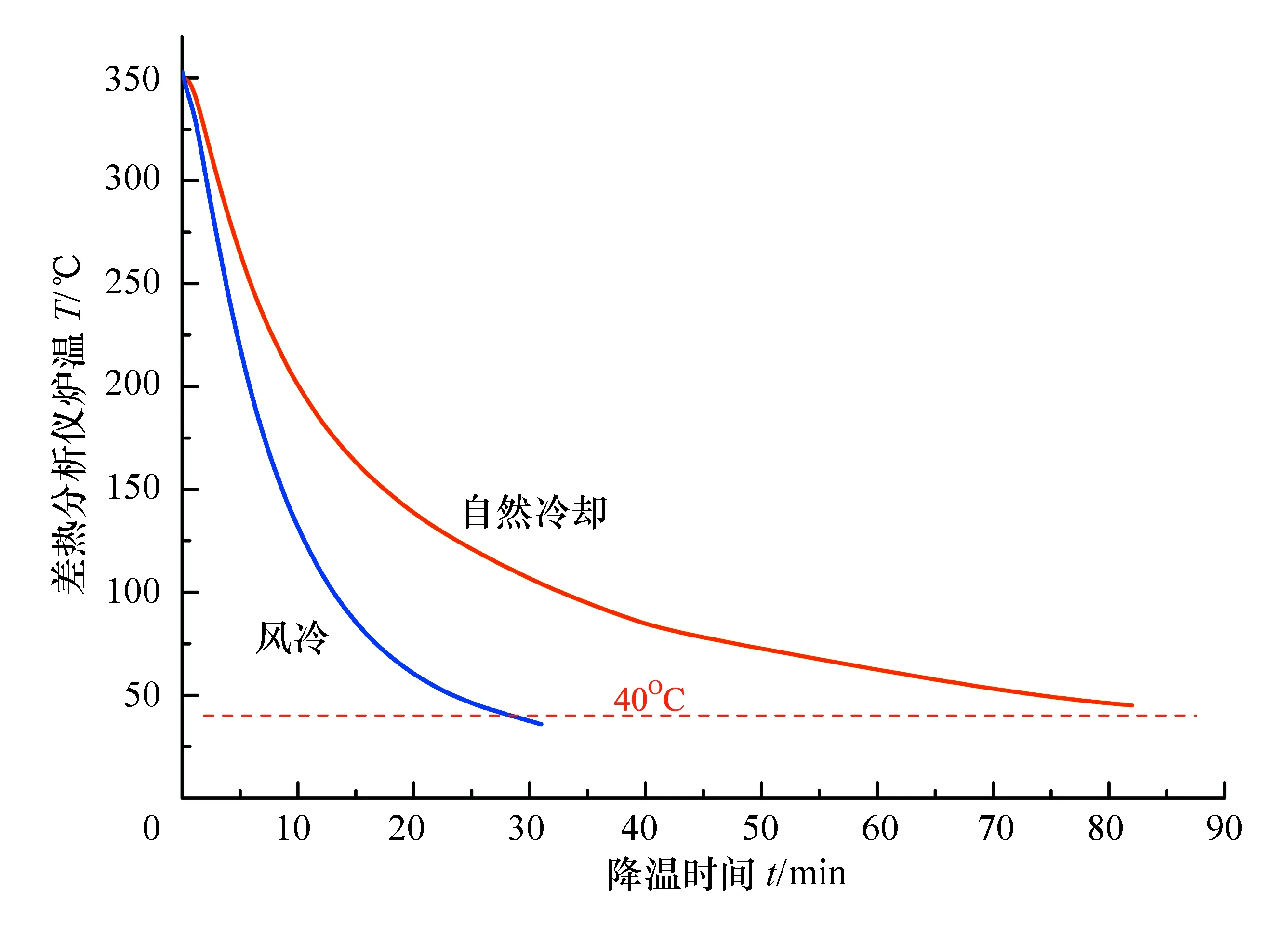
图3 自然冷却与风冷的降温曲线对比
在基础物理化学实验课程中,差热分析的实验温度一般低于350 ℃,由于加热炉外壳采用反射材料,样品托盘所在的炉膛中心温度往往高于炉体温度,两者相差约100 ℃。在风冷条件下,加热炉自250 ℃左右冷却至40 ℃以下所需时间大约20 min以内,因此完成一次差热分析测试的周期约为50 min,这就为在有限的实验课时内进行多次测量创造了条件。
2 KNO3-NaNO3熔盐体系复杂相图的差热分析测定
2.1实验简介
KNO3-NaNO3二元熔盐体系是一个涉及固相晶型转变的液固平衡体系,相图[9]见图4,其中A区为熔融液态单相区,B区为液固平衡二相区,C区为Na,K//NO3三方晶系固体单相区,D区为固溶体+Na,K//NO3三方晶系固体二相区,E区为固体NaNO3+ Na,K//NO3三方晶系固体二相区,F区为NaNO3溶于KNO3中形成的固溶体单相区,G区为固溶体+NaNO3固体二相区。纯净的KNO3和NaNO3分别在130 ℃和277 ℃发生由斜方晶系向三方晶系的转变。形成二元熔盐体系后,其晶系转变温度降低至109 ℃附近,随后的升温过程伴随有复杂的固相转变融合过程,在223 ℃以上开始部分熔融,直至达到液线温度。
熔融盐是非常优良的储热材料,采用熔盐作为光热发电的传热和储热工质,可显著提高光热发电系统的热效率、系统的可靠性和经济性,帮助光热发电站实现持续稳定运行[10-12]。光热发电领域目前经商业化应用验证的成熟熔盐产品的成分组成为60%NaNO3和40%的KNO3二元混合熔盐,它利用相变材料在相变过程中吸收(释放)大量热量而实现能量转换,能将太阳辐射能存储起来,在需要能量时再将其释放,从而解决了太阳能间歇性、波动性的特点。大多数硝酸盐的熔点在300 ℃左右,其突出的优点是价格低、腐蚀性小及在500 ℃以下不会分解。与其他熔盐(如碳酸盐、氯化盐、氟化盐)相比,硝酸盐具有很大的优势。
测定KNO3-NaNO3二元熔盐体系的液-固平衡相图,对于理解涉及固-固、液-固相间转化的规律,以及判断熔盐体系作为储热材料的使用条件,都有重要的意义。
2.2仪器与试剂
试剂:KNO3(A.R.),NaNO3(A.R.),-Al2O3粉末。
仪器:ZCR-III型差热分析仪,φ5 mm×4 mm铝坩埚。
2.3相图测定方法和实验组织
2.3.1样品制备
将KNO3和NaNO3在105 ℃干燥4 h,然后置于干燥器中冷却待用;按组成配比称取适量的KNO3和NaNO3混合物,总质量约10 g,研磨搅拌均匀后置于具塞玻璃试管中,10 ℃/min程序升温至380 ℃,保温30 min,并用细玻璃棒不时搅拌;以5 ℃/min的降温速率冷却至100 ℃左右,再将样品试管置于干燥器中冷却至室温;将KNO3-NaNO3熔融体机械粉碎,在玛瑙研钵中研磨,过80~120目筛,所得熔盐粉末装入密封试剂瓶中,置于干燥器中保存。共制得20个不同组成的熔盐样品,另加2个纯组分。样品制备工作在实验前预先完成。
2.3.2KNO3-NaNO3熔盐材料的差热分析(DTA)曲线测定
2.3.3实验组织
对于8课时实验,可安排2套差热实验装置合作共同测定一套完整相图实验数据,学生可选择约15个不同组成的样品,测量其DTA曲线。对于4课时实验,可安排3套差热实验装置合作,测定约10条DTA曲线,虽然实验点稍稀疏,仍足以勾勒出相图的轮廓。
2.4结果与讨论
不同组成的KNO3-NaNO3二元熔盐样品的DTA曲线呈现出多种形态,且峰型各异,部分典型的DTA曲线如图5所示。可以看出,每条DTA曲线上都有两类峰,其一位于150 ℃以下,其二位于220 ℃以上,前者对应于硝酸盐晶体由斜方晶系向三方晶系转变过程,后者则是固体熔盐的融化过程,这两个过程都是吸热过程。
KNO3-NaNO3二元熔盐样品的组成-相转变温度关系数据见表1。

图5 不同组成KNO3-NaNO3熔盐的DTA曲线(升温速率10 ℃/min)

硝酸钠摩尔分数xNaNO3晶相转变温度TCT/℃固态转变温度T/℃*固线温度TS/℃液线温度TL/℃**0.0000126.77/338.71338.710.0186119.12/298.58333.050.0412119.55/271.94324.280.0727117.75/262.31315.520.1387106.66/249.08295.920.2122109.49/220.88277.010.2276108.29/218.48271.850.3340109.07/220.88241.940.3795109.84/221.31233.520.4473111.47/222.09226.730.4983114.31/222.52222.520.5492115.94/220.37227.760.6200108.64/222.09231.890.6632113.88/221.31237.990.7223110.27/222.09254.410.8066113.88/220.11269.360.8767110.7/253.20285.010.8789110.7/265.00284.660.9151105.46/274.47293.080.9496111.47249.71289.30301.940.9807/264.03299.70307.271.0000/277.32309.76309.76
注:*大部分样品无法确认图4相图中C区与D区、C区与E区的分界线温度;**已经过校正。
在程序升温测定的差热曲线上,以各峰前缘的斜率最大点的切线与基线的交点对应的温度作为过程的始点温度,分别得到固态熔盐的晶相转变温度TCT和起始熔融温度(即固线温度)TS。在程序升温差热曲线上确定熔融过程结束时的温度(即液线温度)TL的标准不一,有以峰顶温度为据的,也有以熔融峰后缘上斜率最大点的切线与基线的交点对应的温度为据的,甚至有以曲线回归基线点的温度为据的,其选择原则根据所用仪器、实验条件和测量对象不同而有所取舍。本实验采用经过校正的以熔融峰后缘上斜率最大点的切线与基线的交点对应的温度作为液线温度TL。当然,液线温度的准确测定应以程序降温测定的DTA曲线上结晶过程的始点温度为准,但是由于课时和仪器性能的限制,无法在基础实验课程中广泛采用。由各样品DTA曲线测得的相转变温度数据列于表1中,图6是根据表1数据绘制的相图。
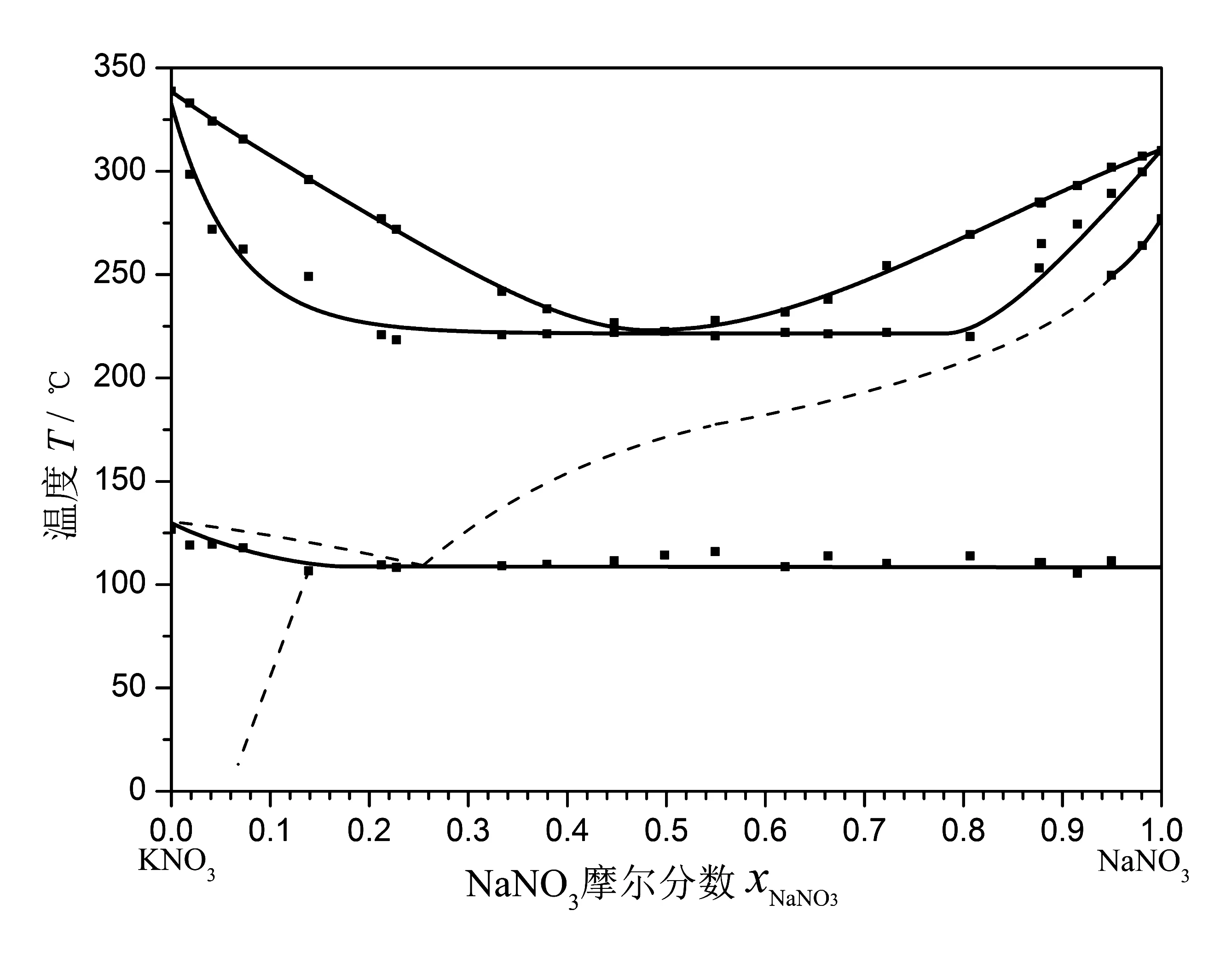
图6 差热分析法实验测定的KNO3—NaNO3二元熔盐体系液固平衡相图
从图6看出,程序升温差热分析数据可以较清晰地标示出硝酸盐熔盐体系由斜方晶系转变为三方晶系的温度,在NaNO3的摩尔分数xNaNO3大于0.13时,该转变温度基本稳定,平均值为108.3 ℃,与文献值(109 ℃)非常接近。熔盐体系的固-液转变过程在差热分析曲线上也能够较清晰地分辨出来,当xNaNO3在0.20~0.80范围内,固线近似水平,液线形状与文献相图(见图4)基本相符。液线与固线在xNaNO3≈0.49处相交,形成最低点,温度为221 ℃,略低于文献值的223 ℃。文献相图表明,固线温度自xNaNO3=0.20时的232 ℃,经过最低点xNaNO3=0.49时的223 ℃,在xNaNO3=0.80时达到235 ℃,形成一个明显的浅弧线;而实验测得的固线在此组成范围内形状更加平直,近似直线,这个结果与差示扫描热分析(DSC)实验的结果相似[15]。值得注意的是,除了在靠近NaNO3端的极少部分样品外,文献相图中的C区与D、E区的分界线在DTA曲线上基本无法明确标示,虽然可以在不少实验曲线上观察到DTA曲线偏离基线的情况,但是不能确定为固态多晶相混合物转变为单一晶相的Na,K//NO3三方晶系固体的过程,文献[15]采用X-射线衍射技术对不同组成的KNO3-NaNO3二元熔盐样品进行分析,均仅测得KNO3、NaNO3两种晶体的特征衍射峰的叠加谱,而没有得到单一晶相的Na,K//NO3三方晶系固体的特征衍射峰,因此在DTA曲线上无法观测到连续的固态晶相转变过程似也合理。
平直的固线往往意味着存在最低共熔点混合物,但是研究表明[15-18]KNO3-NaNO3二元熔盐体系却是不存在最低共熔点混合物的,这与经典物理化学实验中简单二元液固平衡相图实验体系(如铅-锡合金或锡-铋合金)有很大区别,这对学生拓宽知识面,全面理解相平衡理论和相图结构具有重要意义。图7绘出了xNaNO3=0.20~0.80范围内220 ℃以上固-液转化过程的DTA曲线,可以看出随着样品组成向xNaNO3=0.49的两侧发生改变,熔融过程的DTA峰位也随之发生连续变化,且峰型变宽、峰高变低,以液线最低点样品的峰顶温度为基准,在其左右两侧样品的峰顶温度移动均达到约50 ℃,这与形成低共熔点混合物体系的DTA曲线有明显差别,后者随着样品组成变化只会有峰高的变化,峰型和峰温基本不变。
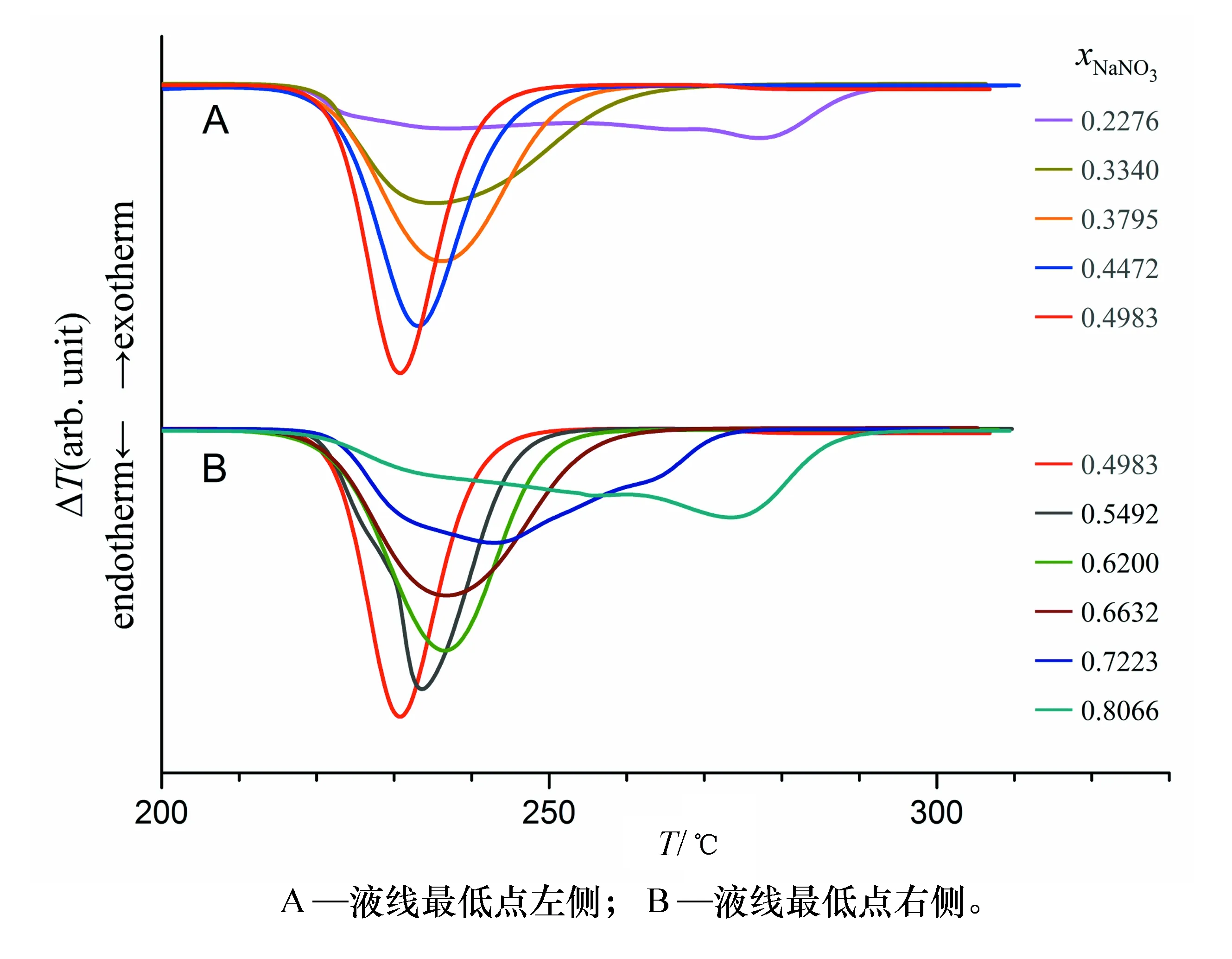
图7 KNO3-NaNO3二元熔盐体系固-液转化过程的DTA曲线
3 结论
采用电脑冷却用的无电刷风扇,经过简单加工和装配,制成与教学型差热分析仪配套使用的风冷系统,能够快速冷却实验仪器,保证在有限的实验课时内完成多轮次的差热分析曲线测定,为开展综合性差热分析实验教学创造了条件。在此基础上,开发了用差热分析法研究KNO3-NaNO3二元熔盐体系液固平衡相图的实验教学项目。与传统的简单二元体系液固平衡相图实验相比,该实验试剂价廉易得,安全无毒,且用量极少;相变过程包括固态晶相转化和固-液转化,相图结构中包含类似低共熔点形态,但是二组分间实际上又没有形成低共熔点混合物,体现了相平衡和相变过程的多样性和复杂性。
本实验项目可以培养学生的独立思考能力,根据实际情况具体分析问题,而不是盲从书本知识。通过改造实验仪器,将差热分析法用于测定复杂相变体系的相图,填补了物理化学实验相关内容的空白,对学生全面理解和掌握相平衡理论和概念有积极帮助,实验教学效果良好。
References)
[1] 复旦大学. 物理化学实验[M].2版.北京:高等教育出版社,1993.
[2] 北京大学化学学院物理化学实验教学组. 物理化学实验[M].4版.北京:北京大学出版社,2010.
[3] 罗士平. 物理化学实验[M].2版.北京:化学工业出版社,2010.
[4] 于文生,吕英士,王进贤. 差热分析实验的改进[J]. 科技资讯,2008(32):3.
[5] 许新华,王晓岗,吴梅芬. 简易差热装置在合金相图测定实验中的应用[J]. 实验技术与管理,2013,30(12):72-76,86.
[6] 陈良坦,董振荣,黄泰山. 差热分析在物化实验中的应用[J]. 实验室研究与探索,2001,20(2):96-98.
[7] 汤颖,孟梅,徐敬芳,等. 一个物理化学综合实验的设计与实践[J]. 实验室科学,2010,13(2):98-99.
[8] 南京桑力电子设备厂. ZCR 差热实验装置使用说明书[EB/OL].(2012-01-16)[2015-04-28]. http://www.sangli.com.cn/end.asp?id=163.
[9] Centre for Research in Computational Thermochemistry(CRCT). FACT Compound and Solution Database[EB/OL]. [2015-04-28]. http://www.crct.polymtl.ca/FACT/phase_diagram.php?file=KNO3-NaNO3.jpg&dir=FTsalt.
[10] 彭强,丁静,魏小兰,等. 硝酸熔盐体系在能源利用中的研究进展[J]. 现代化工,2009,29(6):17-22,24.
[11] 路阳,彭国伟,王智平,等. 熔融盐相变储热材料的研究现状及发展趋势[J]. 材料导报,2011,25(11):38-42.
[12] 葛志伟,叶锋,Mathieu Lasfargues,等. 中高温储热材料的研究现状与展望[J]. 储能科学与技术,2012,1(2):89-102.
[13] 刘振海,畠山立子. 分析化学手册:第八分册 热分析[M].2版.北京:化学工业出版社,1999.
[14] Pope M I, Judd M D. Differential Thermal Analysis[M]. London:Heyden and Son Ltd,1977.
[15] Kramer C M, Wilson C J. The Phase Diagram of NaNO3-KNO3[J]. Thermochim Acta,1980,42:253-264.
[16] Zamali H, Jemal M. Diagrammes de Phase des Systemes Binaries KNO3-CsNO3et KNO3-NaNO3[J]. J Therm Anal,1994,41:1091-1099.
[17] Jriri T, Rogez J, Mathieu J C, et al. Thermodynamic Analysis of the CsNO3-KNO3-NaNO3System[J]. J Phase Equil,1999,20(5):515-525.
[18] Sangster J. Thermodynamics and Phase Diagrams of 32 Binary Common-Ion Systems of the Group Li,Na,K,Rb,Cs//F,Cl,Br,I,OH,NO3[J]. J Phase Equil, 2000,21(3):241-268.
Improvement of DTA apparatus and its application in physical chemistry experimental teaching
Xu Xinhua, Wu Meifen, Xiao Hanshuang, Wang Xiaogang
(Department of Chemistry, Tongji University, Shanghai 200092, China)
The air-cooling system (fan) was fabricated with simple assemblies to improve the commercial DTA apparatus for experimental teaching. It was proved that the cooling rate of the DTA furnace could be increased greatly by using this fan. Under ordinary experiment conditions, the heated furnace could be cooled down to the temperature below 40 ℃ within 15 min. By reducing the useless waiting time, it is possible to conduct the comprehensive DTA experiments in the basic physical chemistry experiment curriculum. By using the improved DTA apparatus, the solid-liquid phase diagram of KNO3-NaNO3binary fused salt system was measured. Both the transition between solid crystal phases and the transition from solid to liquid can be observed in this system, and the transition temperatures vary with the sample compositions. This is quite different from that for simple eutectic binary systems. The experiment can be finished in the reasonable laboratory time, and the results in experimental teaching are better.
DTA(differential thermal analysis); physical chemistry experiment; binary fused salt system; phase diagram
DOI:10.16791/j.cnki.sjg.2016.01.017
2015- 05- 04修改日期:2015- 06- 22
同济大学第七期精品实验建设项目(1380104077)
许新华(1967—),男,浙江黄岩,博士,副教授,从事物理化学及实验的教学工作
E-mail:xxh01@tongji.edu.cn
王晓岗(1965—),男,江苏盐城,博士,教授,同济大学化学实验教学示范中心主任,研究方向为纳米电化学.
O657.99; O64-33
B
1002-4956(2016)1- 0067- 05
仪器设备研制与应用
