Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图研究及其应用*
2016-08-05巩学敏张嘉勇曹吉林
巩学敏 张嘉勇 曹吉林
(1.河北工业大学化工学院,河北省绿色化工与高效节能重点实验室 天津 300130;2.华北理工大学 河北唐山 063009)
环境管理与咨询
Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图研究及其应用*
巩学敏1,2张嘉勇2曹吉林1
(1.河北工业大学化工学院,河北省绿色化工与高效节能重点实验室天津 300130;2.华北理工大学河北唐山 063009)
根据不同温度下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图的绘制,分析了该四元体系相图受温度影响的相图特征,设计了以硫酸铵为盐析剂加工分离白钠镁矾的最佳生产工艺。新工艺具有反应时间短,操作简单,可以生产得到氮镁复肥和无水硫酸钠等优点。此工艺对于克服白钠镁矾的加工分离困难,实现白钠镁矾资源的综合开发和利用具有重要的现实意义。
白钠镁矾硫酸铵盐析法相图
0 引言
我国白钠镁矾矿产资源储量十分丰富,主要分布在我国西部和北部的西藏、青海、新疆、内蒙古、山西等地[1-2]。然而采用物理化学法或结晶沉淀等传统工艺都很难实现白钠镁矾的合理开发和综合利用。如何有效分离白钠镁矾矿物,实现白钠镁矾资源的合理开发和综合利用具有重要的现实意义。
水盐体系相图是描述盐类物质在水中溶解度变化的特征图形,在盐矿物的分离和提纯[3-4]方面得到了广泛的应用。采用水盐体系相图特征用于指导盐矿资源的开采工艺,可以减少传统物理或化学法产生废弃物或副产物对环境污染的影响,实现低能环保和工艺循环利用的目的[5-6]。文献可查到各温度条件下Na2SO4-MgSO4-H2O三元体系相平衡数据[7],通过分析相图特征可知,采用传统低温结晶,高温蒸发的方法很难有效加工分离白钠镁钒矿物。因此,针对白钠镁矾盐矿的合理开采和综合利用出现了一些新的研究,黄雪莉等[8]采用氯化钾与白钠镁矾反应,通过相关相图分析,研究制备硫酸钾等产品,兰天洋等[9]进行了尿素盐析法对白钠镁矾进行加工分离的研究。目前,对于Na2SO4-MgSO4-(NH4)2SO4-H2O体系相平衡的研究及其应用较为全面[10-13],然而,对于白钠镁矾的工业综合开发和利用,这些方法均不同程度上存在问题。综合分析各温度条件下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图特征,文章设计了以硫酸铵为盐析剂,白钠镁矾为原料,25 ℃时生产氮镁复肥,60 ℃时升温生产硫酸钠的生产工艺。该工艺具有反应时间短,操作简单,可生产得到氮镁复肥和无水硫酸钠,环保节能等优点。
1 各温度条件下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图
Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系达到相平衡的时间随温度升高逐渐缩短,即高温条件更有利于该四元体系达到相平衡状态[10-13]。对于研究该四元体系相图,以硫酸铵为盐析剂,对白钠镁矾进行加工分离的工艺来说,很大程度上节省了工艺运行时间,提高了工艺生产效率。
为便于研究,在0 ℃条件下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系完整相图的基础上,对25,35,60 ℃条件下该四元体系相图进行描绘,如图1所示。图中各干盐点的组成均为以Na2SO4,MgSO4,(NH4)2SO43种盐物质含量组成之和等于100 g时为基准的干基组成百分含量。从生产氮镁复肥的工艺角度考虑,各温度条件下的四元体系相图只是绘制了MgSO4·(NH4)2SO4·6H2O和硫酸钠结晶区的部分两盐共饱曲线。
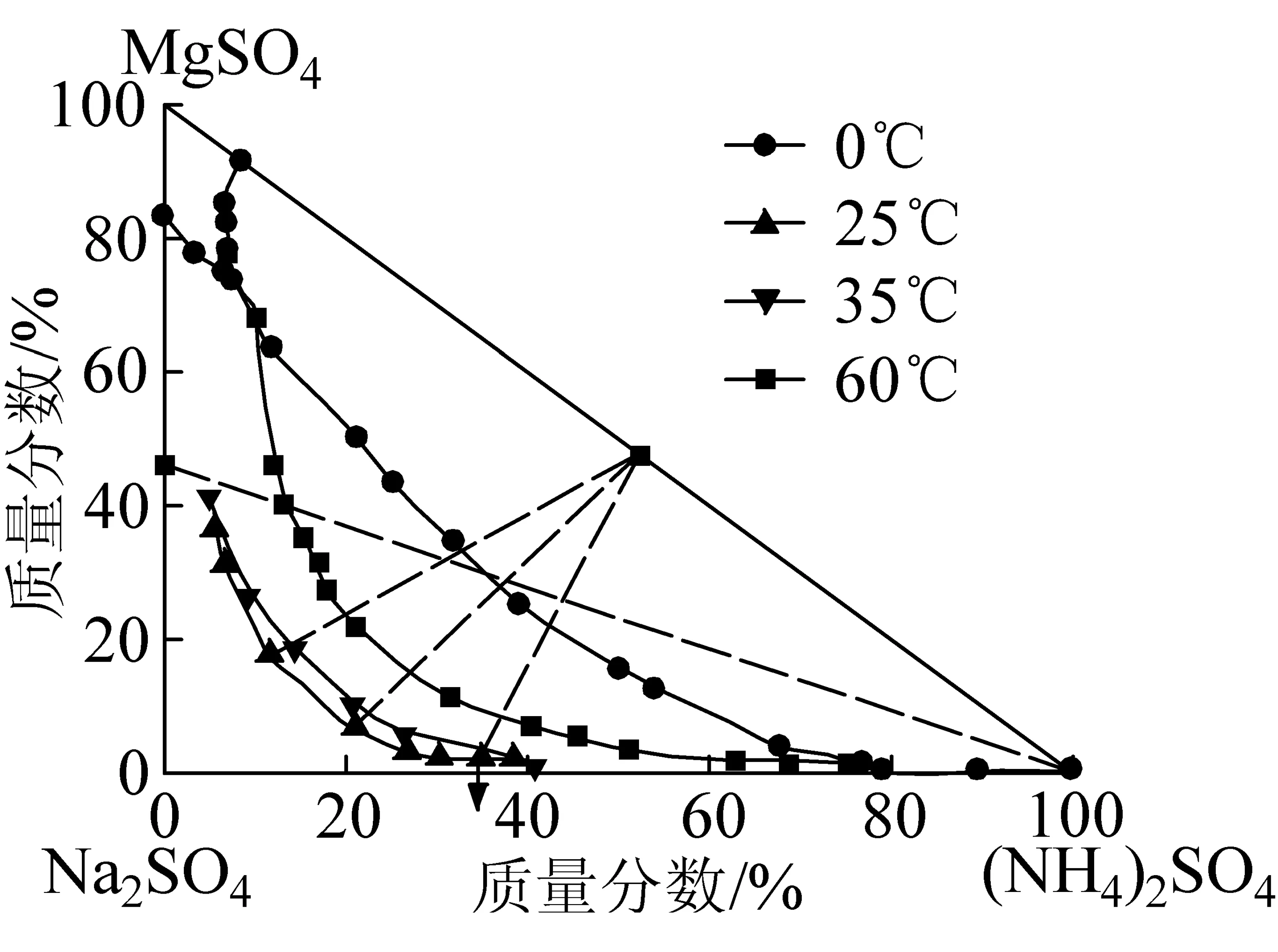
图1 各温度下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图
通过分析相图的等温共饱点和结晶区可知,各温度的共饱点和结晶固相物质组成均有所差别。0 ℃时,不存在MgSO4·NaSO4·4H2O的结晶区,MgSO4·(NH4)2SO4·6H2O结晶区较小,且形成较大的Na2SO4·10H2O结晶区。25 ℃时,存在较大的MgSO4·(NH4)2SO4·6H2O复盐结晶区,形成Na2SO4·10H2O结晶区,且面积较小。35 ℃时,存在较大的MgSO4·(NH4)2SO4·6H2O复盐结晶区(较25 ℃时略小),不存在Na2SO4·10H2O结晶区,但无水Na2SO4结晶区面积较小。60 ℃时 Na2SO4·(NH4)2SO4·4H2O复盐结晶区消失,存在较大的MgSO4·(NH4)2SO4·6H2O复盐结晶区(比25 ℃和35 ℃略小),形成无水Na2SO4结晶区,且面积较大。
由图1各温度条件下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图特征,可以设计在不同温度条件下白钠镁矾的加工分离工艺:一定配比量的白钠镁矾、硫酸铵和水的混合液充分溶解反应后,将有氮镁复肥结晶析出后,分离氮镁复肥固相后,对应的剩余母液分别落在各自温度相图的MgSO4·(NH4)2SO4·6H2O和硫酸钠结晶区的两盐共饱曲线上,调节温度至合适的结晶区范围,可进行结晶析出硫酸钠产品的生产工艺。
针对0,25,35和60 ℃条件下Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系的相图特征,选择最适宜的生产工艺。从生产氮镁复肥的角度考虑,25 ℃条件下,氮镁复肥的结晶区面积最大。如图1所示,由杠杆定理可知,当原料加入点相同时,25 ℃时氮镁复肥的产量最大。生产氮镁复肥的母液用于生产硫酸钠时,从生产物质和产量角度来考虑,生产母液升温至60 ℃时,产生的无水Na2SO4产量较高,且不含结晶水,减少了硫酸钠结晶水的脱水热分解过程。由此可以设计以白钠镁矾为原料,硫酸铵为盐析剂,25 ℃条件下生产制备氮镁复肥,剩余母液升温至60 ℃时又可生产无水硫酸钠,生产母液加入一定配比量的硫酸铵和白钠镁矾还可实现工艺的循环生产。
2 60 ℃时Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图的应用
2.1基于相图的工艺设计
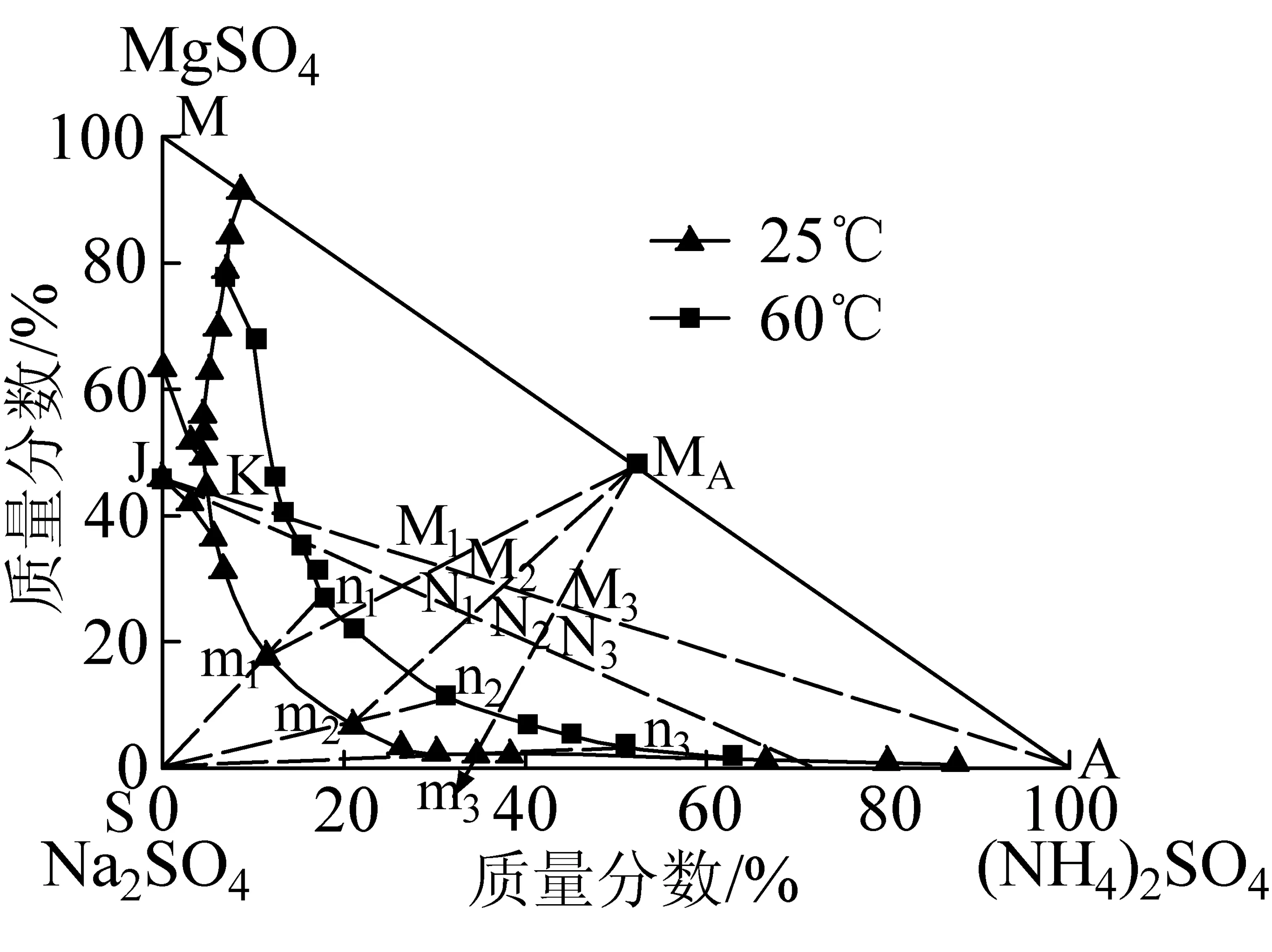
图2 硫酸铵盐析法生产氮镁复肥和硫酸钠的工艺相图
图2为硫酸铵盐析法生产氮镁复肥和硫酸钠的工艺相图。从生产工艺角度考虑,只绘制了25 ℃时Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图与60 ℃时该体系的Mg-N复肥和硫酸钠结晶区两盐共饱曲线的部分相图。图中实线和虚线分别表示结晶区域边界线和工艺技术线,白钠镁矾组成分别为:硫酸钠42.47%,硫酸镁35.99%,水21.54%,该组成点在图2中为J点。MA点代表Mg-N复肥,其组成分别为:硫酸铵36.64%,硫酸镁33.38%,水29.98%。如图2所示,25 ℃时Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图的MgSO4·(NH4)2SO4·6H2O 与Na2SO4·10H2O的两盐共饱线部分落在60 ℃该体系相图的Na2SO4结晶区内。
25 ℃条件下,当向J体系点中逐渐加入(NH4)2SO4和H2O时,混合体系的干盐组成点将随着加入量的增加沿JA线且由J点向A点移动。当加入的混合体系点落在相图中KA线上时,Mg-N复盐将会结晶析出,K点是JA线与25 ℃时四元体系相图的交点。
对KA线上3个混合体系点M1,M2和M3进行比较,由杠杆规则和物料平衡计算分析可知,当初始加入量相同时,析出复盐Mg-N复肥的量由大到小的顺序为M3>M2>M1,分离出复肥后剩余母液组成分别为m1,m2和m3点,它们分别是MAM1,MAM2和MAM3延长线与25 ℃时该相图共饱线的交点。
此时,剩余母液点m1,m2和m3点均落在60 ℃Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图Na2SO4结晶区内,当混合体系升温至60 ℃时,无水Na2SO4将结晶析出,分离Na2SO4结晶固相后,剩余母液组成点分别为n1,n2和n3,它们分别是Sm1,Sm2和Sm3延长线与60 ℃时该体系相图共饱线的交点。根据杠杆规则和物料平衡计算分析,析出Na2SO4的量从大到小顺序为:m1>m2>m3。分离Na2SO4固相后,剩余母液含一定量的(NH4)2SO4,MgSO4和Na2SO4可以与原料混合进行循环生产。当向剩余母液中加入一定配比量的白钠镁矾、硫酸铵和水时,混合体系点可分别落在MAM1m1,MAM2m2和MAM3m3线上,调节温度至25 ℃时,复盐MgSO4·(NH4)2SO4·6H2O又将会析出,得到相应的剩余母液组成点分别为m1,m2和m3,按照上述步骤,剩余母液可实现下一个循环生产。这样通过调节温度和水量就可以实现Mg-N复肥和无水硫酸钠的循环生产。以白钠镁矾为原料,硫酸铵盐析法加工制备Mg-N复肥和硫酸钠工艺流程如图3所示。
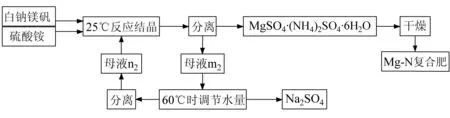
图3 白钠镁矾为原料加工制备氮镁复肥和硫酸钠工艺流程图
2.2基于相图的工艺计算
以1 000 kg白钠镁矾为基本加工量,依据杠杆规则和物料平衡定理,对2.1节所述原料混合体系点M2进行生产的相图计算和分析,计算结果如表1所示。
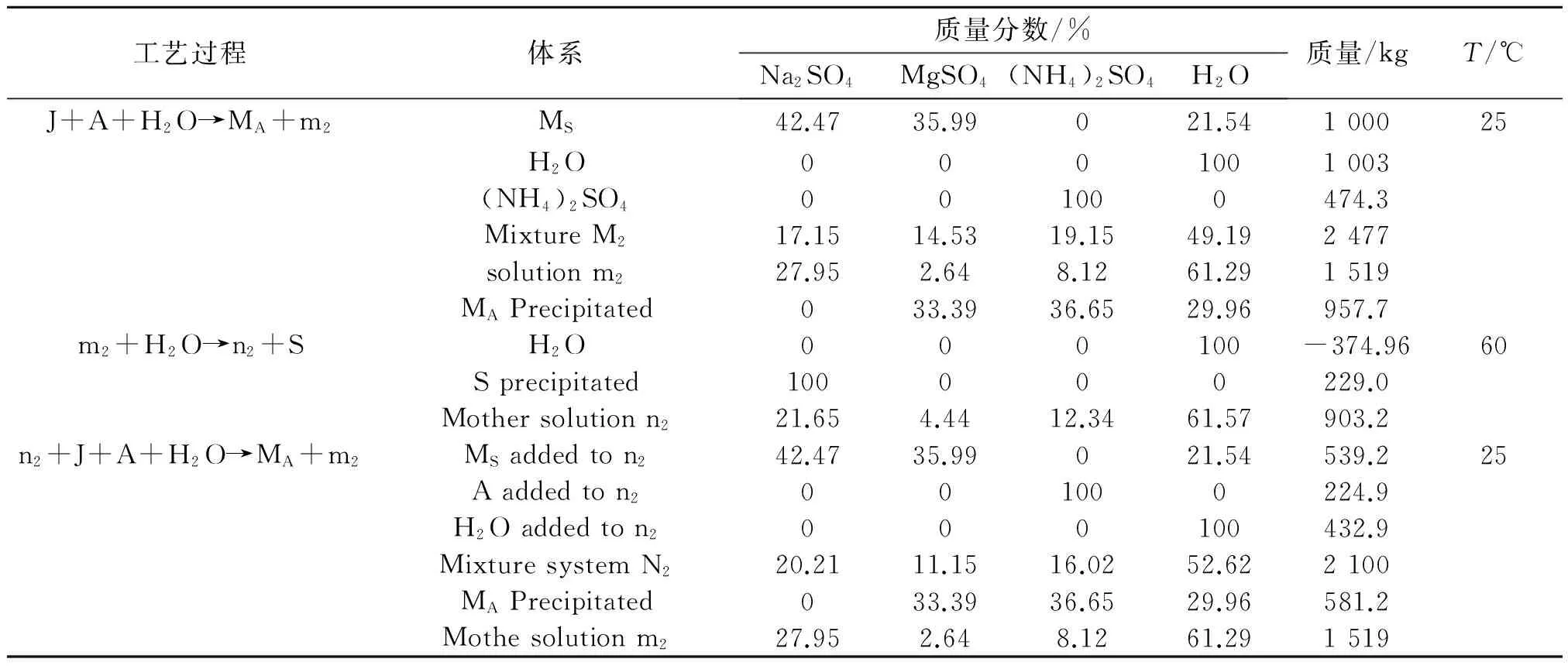
表1 白钠镁矾为原料加工制备氮镁复肥和硫酸钠工艺计算
在25 ℃时,当向1 000 kg白钠镁矾J点中加入1 003 kg水和474.3 kg硫酸铵时,系统落在M2点,这时有957.7 kg氮镁复肥和1 519 kg剩余母液m2产生。此时将剩余母液升温至60 ℃时,同时蒸发母液点m2中374.9 kg水,将沉淀析出229.0 kg Na2SO4,产生剩余母液n2903.2 kg。分离Na2SO4后,向剩余母液n2中加入539.2 kg白钠镁矾、224.9 kg硫酸铵和432.9 kg H2O,将又得到2 100 kg的混合液,这时系统点为图2的N2点,25 ℃条件下又将产生581.2 kg氮镁复肥和1 519 kg母液m2。按照以上工艺步骤,m2点进行下一个循环生产。
综合比较M1,M2,M3混合体系点,析出复盐MgSO4·(NH4)2SO4·6H2O量大小顺序为M3>M2>M1,析出Na2SO4的量大小顺序为:m1>m2>m3。综合比较选取适宜最初加料点,可按照生产需求决定。
3 结论
(1)通过分析0,25,35和60 ℃时Na2SO4-MgSO4-(NH4)2SO4-H2O四元体系相图可知,各温度的共饱点和结晶固相物质组成均有所差别,确定最佳生产氮镁复肥和硫酸钠的工艺技术。
(2) 依据相图分析和计算,设计了硫酸铵盐析法加工分离白钠镁矾的生产工艺:先在25 ℃条件下反应制备氮镁复肥MgSO4·(NH4)2SO4·6H2O,然后升温至60 ℃制备硫酸钠,分离硫酸钠后的剩余母液返回与白钠镁矾混合可实现循环生产。
[1]高世扬. 运城盐湖制盐工艺过程及其制盐史的研究[J].盐湖研究,1997,5(3/4):1-15.
[2]崔峤.甘肃玉门发现白钠镁矾[J].甘肃科学学报,1996,8(1):89-91.
[3]梁保民.水盐体系相图原理及应用[M].北京:轻工业出版社,1996:13-14,551-559.
[4]牛自得,程芳琴.水盐体系相图及其应用[M].天津:天津大学出版社,2002:551-575.
[5]杨红梅,李旭兵.水盐体系相平衡与相图研究现状[J].海湖盐与化工,2002,5(3):14-19.
[6]刘俊梅.水盐体系相平衡实验研究现状[J].化学工程与装备,2010(1):144-145.
[7]HOWARD S. Solubilities of Inorganic and Organic Compounds[M]. Oxford: New York Pergamon Press, 1979.
[8]黄雪莉,高飞,迪木拉提.钠镁矾类矿制取硫酸钾工艺开发研究[J].海湖盐与化工,2001,30(5):8-11.
[9]LAN Tianyang, CAO Jilin, JIN Huaiyong, et al. Phase Diagrams of Na2SO4-MgSO4-CO(NH2)2-H2O System at 25 ℃ and Their Application[J]. Journal of Chemical & Engineering Data,2012,57(2):389-393.
[10]GUO H F, CAO J L, WANG J J, et al. Phase Diagrams of Na2SO4-MgSO4-(NH4)2SO4-H2O System at 25 ℃ and Their Application[J]. Fluid Phase Equilib, 2014,367:79-84.
[11]GONG X M, ZHAO B, ZHANG J Y, et al. Phase Diagrams of the Na2SO4-MgSO4-(NH4)2SO4-H2O System at 60 ℃ and Their Application[J]. Journal of Chemical & Engineering Data, 2015,60(4):1048-1055.
[12]ZHANG Jing, GUO Hongfei, CAO jilin. Phase Equilibrium of the Quaternary System Na2SO4-MgSO4-(NH4)2SO4-H2O at 0 ℃[J]. Journal of Chemical & Engineering Data, 2013,58(9):2622-2628.
[13]郭宏飞,郭宝曼,张菁,等. 35 ℃时Na2SO4-MgSO4--(NH4)2SO4-H2O体系相图及其应用[J]. 高校化学工程学报,2015,29(2):264-269.
Study on the Phase Diagram of Na2SO4-MgSO4-(NH4)2SO4-H2O System and Their Application
GONG Xuemin1,2ZHANG Jiayong2CAO Jilin1
(1.HebeiProvincialKeyLabofGreenChemicalTechnologyandHighEfficientEnergySaving,CollegeofChemicalEngineeringandTechnology,HebeiUniversityofTechnology,Tianjin300130)
Based on the phase diagram of Na2SO4-MgSO4-(NH4)2SO4-H2O quaternary system, the characteristics of the phase diagram affected by temperature is explained in detail. An optimum process is designed to separate bloedite using (NH4)2SO4as salting-out agent. The technology is fast to reach phases equilibrium, easy to operate, and can gain Mg-N compound fertilizers and anhydrous Na2SO4directly. New process has a very important practical significance in exploiting and using bloedite comprehensively.
bloediteammonium sulfatesalting-out agentphase diagram
2016-04-21)
国家自然科学基金(21076057)。
巩学敏,1979年生,女,讲师,博士研究生,主要从事无机盐化工等方面的教学和科研工作。
