培美曲塞与铂类联合应用对晚期非小细胞肺癌疗效及安全性
2016-07-10陈倩潘超
陈倩,潘超
(浙江省肿瘤医院 胸部肿瘤外科,浙江 杭州 310022)
培美曲塞与铂类联合应用对晚期非小细胞肺癌疗效及安全性
陈倩Δ,潘超
(浙江省肿瘤医院 胸部肿瘤外科,浙江 杭州 310022)
目的 观察培美曲塞与铂类联用对晚期非小细胞肺癌的治疗效果,并分析其安全性。方法 回顾性分析2013年 8月~ 2015年8月在浙江省肿瘤医院胸部肿瘤外科接受化疗的晚期非小细胞肺癌患者的临床资料,根据其化疗方式分为顺铂联合紫杉醇化疗组和顺铂联合培美曲塞化疗组。观察2组患者的治疗效果,比较2组患者治疗前后肿瘤标志物水平、生活质量和毒副作用发生率的差异。结果 顺铂联合培美曲塞化疗组治疗的有效率为98.2%,明显高于顺铂联合紫杉醇化疗组(82.5%)(P<0.05);治疗前2组患者肿瘤标志物水平无明显差异,治疗后2组患者各项肿瘤标志物水平较治疗前均降低,且顺铂联合培美曲塞化疗组降低更明显(P<0.05);2组患者血液系统毒性,消化道毒性、肝、肾功能损害发生率无明显差异;2组患者治疗前生活质量得分无明显差异,治疗后2组患者生活质量均较治疗前改善,且顺铂联合培美曲塞化疗组改善更明显(P<0.05)。结论 培美曲塞与铂类联用对晚期非小细胞肺癌有较好的治疗效果,可明显提高患者的生活质量。
培美曲塞;铂类;非小细胞肺癌;生活质量
肺癌是临床上较为常见的呼吸系统恶性肿瘤,在病死率较高的恶性肿瘤中排名前3位。相关研究显示,我国现阶段每年的肺癌新发病例可达15万以上,且近年来呈现出了一定的上升趋势[1]。
晚期肺癌患者往往失去了手术机会,其中非小细胞肺癌(non-small celll ung cancer,NSCLC)占到了各种完全肺癌患者的25%以上。通过静脉化疗的方式可以提高完全肺癌患者的临床治疗有效率,抑制病情进展率,并延长中位生存时间[2]。但迄今为止对于完全NSCLC患者的静脉化疗方案的研究较多,其中紫杉醇联合顺铂的静脉化疗方案的效果较为肯定,但其化疗的总体有效率仍然不足45%[3-4]。培美曲塞是新型的抗叶酸代谢药物,可以显著抑制肿瘤细胞的增殖活性,本研究回顾性分析2013年8月~2015年8月在本院接受化疗的NSCLC临床资料,探讨了不同化疗方案的化疗效果,报道如下。
1 资料与方法
1.1 一般资料 选取2013年8月~2015年8月在浙江省肿瘤医院胸部肿瘤外科接受化疗的晚期非小细胞肺癌患者为研究对象。纳入标准:年龄≥18岁;确诊为晚期非小细胞(Ⅲ期、Ⅳ期);不能耐受手术者。排除标准:临床资料不全者;肝肾功能严重异常,不能耐受化疗者。根据纳入排除标准共纳入研究对象95例,其中顺铂联合紫杉醇化疗组40例,男31例,女9例,年龄52~78岁,平均(65.35±5.82)岁,Ⅲ期者18例,Ⅳ期者22例;顺铂联合培美曲塞化疗组55例,男42例,女13例,年龄55~79岁,平均(65.29±5.79)岁,Ⅲ期者21例,Ⅳ期者34例。2组患者在年龄、性别和肿瘤分期等一般资料方面比较差异无统计学意义,具有可比性,且本项研究经医院伦理委员会评审通过。
1.2 方法
1.2.1 治疗方法:观察组:培美曲塞(江苏豪森药业股份有限公司,国药准字:H20051288),500 mg,静脉滴注,第1天,顺铂(江苏豪森药业股份有限公司,国药准字:H20040812)75 mg/m2,静脉滴注,第3天,化疗前常规给予哌替啶、地塞米松抗过敏和止吐治疗,并给予水化、保肝等治疗,21 d为1个疗程,连续化疗3个疗程。
对照组:紫杉醇(南京绿叶思科药业有限公司,国药准字:H20030357),175 mg/m2,第1天,静脉滴注,顺铂(江苏豪森药业股份有限公司,国药准字:H20040812)75 mg/m2,静脉滴注,第2天,并给予补液、止吐、保肝等治疗,21 d为1个疗程,连续化疗3个疗程。
1.2.2 评价指标:观察2组患者的治疗效果,比较2组患者治疗前后肿瘤标志物水平、生活质量和毒副作用发生率的差异。完全缓解(CR):全部病灶完全消失,至少维持4w以上;部分缓解(PR):基线病灶长径总和缩小≥30%,至少维持4 w以上;疾病稳定(SD):基线病灶长径总和有所缩小但未达PR或有所增加但未达PD。疾病进展(PD):基线病灶长径总和增加≥20%或出现新病灶。治疗的有效率=(CR+PR+SD)/总例数。
1.2.3 检测方法:清晨采集空腹静脉血,按照10000 r/min的离心速度进行离心分离血清,-20 ℃保存待测,采集标本后1 w内检测神经元特异性烯醇化酶(neuron specific enolase,NSE)、癌胚抗原(carcino embryonie antigen,CEA)、糖类抗原125(carbohydrate antigen 125 ,CA125)、糖类抗原CA19-9(CA19-9),采用瑞士罗氏全自动生化分析仪E170模块进行检测,检测试剂盒购自上海泰康生物科技有限公司。具体检测方法参照试剂盒说明书,试剂盒内配有质控血清或质控标准品,所有操作严格按照操作说明完成。
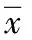
2 结果
2.1 2组患者治疗效果的比较 顺铂联合培美曲塞化疗组治疗的有效率为98.2%,明显高于顺铂联合紫杉醇化疗组(82.5%)(χ2=7.385,P<0.05)。见表1。

表1 2组患者治疗效果的比较
#P<0.05,与对照组比较,compared with control group
2.2 2组患者治疗前后肿瘤标志物水平的比较 治疗前2组患者肿瘤标志物水平无明显差异,治疗后2组患者各项肿瘤标志物水平较治疗前均降低,且顺铂联合培美曲塞化疗组降低更明显(P<0.05)。见表2。
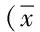
表2 2组患者治疗前后肿瘤标志物水平的对比±s)
*P<0.05,与同组治疗前比较,compared with the same group pre-treatment;#P<0.05,与对照组治疗后比较,compared with control group post-treatment
2.3 2组患者不良反应发生率的比较 2组患者血液系统毒性,消化道毒性、肝、肾功能损害发生率无明显差异(χ2=1.080,P>0.05)。见表3。

表3 2组不良反应发生率的比较(n)
2.4 2组患者治疗前后生活质量的比较 治疗前2组患者生活质量得分无明显差别,治疗后2组患者生活质量均较治疗前改善,且顺铂联合培美曲塞化疗组改善更明显(P<0.05)。见表4。

表4 2组患者治疗前后生活质量的比较±s)
*P<0.05,与同组治疗前比较,compared with the same group pre-treatment;#P<0.05,与对照组治疗后比较,compared with control group post-treatment
3 讨论
吸烟、遗传易感因素、空气污染等,均可以促进NSCLC的发生发展,特别是在年龄大于45岁的吸烟人群中,NSCLC的发病率更高,可较普通对照人群上升3~4倍[5]。NSCLC患者多数已发生了明显的淋巴结及远处转移,中位生存时间不足34个月,5年生存率不足45%,临床预后生存指标较差[6-7]。静脉化疗可以通过抑制肿瘤细胞增殖,促进肿瘤细胞凋亡等机制,进而改善患者的远期生存指标,延长NSCLC患者的生存时间。但一项汇集了176例NSCLC患者的化疗效果的随访研究可以,紫杉醇联合顺铂等化疗方案化疗后的无瘤生存时间改善并不明显,患者的5年生存率等指标仍然较低,病情缓解率不足35%[8]。
培美曲塞是叶酸靶点作用药物,可以通过拮抗细胞内的胸苷酸酶、叶酸合成酶及二氢叶酸还原酶等,抑制肿瘤细胞的嘌呤和嘧啶等核酸物质的合成,导致肿瘤细胞降解凋亡。培美曲塞联合顺铂化疗,可以在拮抗嘌呤和嘧啶合成的同时,进一步抑制肿瘤细胞DNA的扩增,降低肿瘤细胞复制和增殖的活性,提高化疗效果[9-11]。已有的研究探讨了培美曲塞单用及联合铂类化疗药物静脉化疗的临床效果,认为培美曲塞联合顺铂化疗具有良好的病情缓解率和中位生存时间[12- 13]。但迄今为止对于以铂类为基础的联合化疗方案的对比研究不足,本研究的创新点在于探讨了培美曲塞联合顺铂化疗效果的同时,揭示了NSCLC患者血清肿瘤指标的变化。
本研究发现,培美曲塞联合顺铂化疗后的总体有效率明显高于对照组,差异具有统计学意义(P<0.05),表明在顺铂的基础上联合培美曲塞化疗可以进一步提高静脉化疗的效果。培美曲塞对于细胞内核酸物质合成的抑制作用可以促进肿瘤病灶的萎缩,提高顺铂化疗的敏感性。Tomasini等[14]研究者通过前瞻性分析了83例样本量的NSCL患者化疗的临床资料,发现培美曲塞联合顺铂化疗3个疗程后的总体有效率可达65%以上,这与本研究的结论较为一致。血清肿瘤学指标在NSCLC患者临床预后评估中具有重要的意义,CEA、NSE等肿瘤指标的下降是晚期肺癌患者预后改善的保护性因素,本研究中顺铂联合培美曲塞组化疗后的CEA、NSE等指标明显低于顺铂联合紫杉醇组,下降程度较为明显(P<0.05),进一步提示了培美曲塞化疗的临床效果。但需要注意的是,Tomasini等[14-15]研究者的研究中并未发现血清CEA、NSE等肿瘤指标的改善,考虑样本量的不足、临床资料的收集偏移及检测方法的不统一等,均可能导致了结论的差别。培美曲塞化疗组化疗后肺癌患者的生活质量更高,患者的躯体角色、社会功能、精神健康等评分均明显改善(P<0.05),其机制考虑可能与培美曲塞联合顺铂化疗对于完全肺癌患者肿瘤负荷的解除有关。临床安全性的分析也可见,培美曲塞并不会增加肝肾功能损伤及血液系统毒性等的发生,临床安全性较为可靠。
综上所述,培美曲塞联合顺铂化疗的临床效果更为显著,化疗的总体有效率更高,化疗后患者的血清肿瘤学指标明显改善,且患者的生活质量得到了提高。本研究仍然存在一定的局限性:样本量不足,缺乏多中心的临床研究;对于培美曲塞化疗后的远期生存指标的分析不足。
[1] 赵玲娣,李威,王子兵,等. 晚期非小细胞肺癌中二线比较多西他赛和培美曲塞疗效的临床研究[J]. 中华临床医师杂志(电子版),2015,22(18):3448-3450.
[2]宿濛,秦宝丽. DC-CIK技术联合奥沙利铂、吉西他滨化疗治疗进展期中央型非小细胞肺癌的临床研究[J]. 现代仪器与医疗,2015,21(2):31-34.
[3]太祥,陈满军,洪文娟,等. 培美曲塞和紫杉醇分别联合奥沙利铂用于非小细胞肺癌术后辅助化学治疗疗效比较[J]. 重庆医学,2015,24(35):4936-4939.
[4]许涛,景红霞,李林均,等. 培美曲塞/卡铂同步放化疗联合DC-CIK对局部晚期非鳞癌非小细胞肺癌的疗效[J]. 广东医学,2016,32(7):1070-1074.
[5]彭东旭,方晓娟,杜均详,等. 培美曲塞联合顺铂化疗对晚期非小细胞肺癌患者血清肿瘤标志物的影响[J]. 临床肺科杂志,2016,32(7):1306-1309.
[6]Cheng Y, Murakami H, Yang PC, et al. Randomized Phase II Trial of Gefitinib With and Without Pemetrexed as First-Line Therapy in Patients With Advanced Nonsquamous Non-Small-Cell Lung Cancer With Activating Epidermal Growth Factor Receptor Mutations[J]. J Clin Oncol,2016,25(6):90-93.
[7]Kentepozidis N, Economopoulou P, Christofyllakis C, et al. Salvage treatment with irinotecan/cisplatin versus pemetrexed/cisplatin in patients with non-small cell lung cancer pre-treated with a non-platinum-based regimen in the first-line setting: a randomized phase II study of the Hellenic Oncology Research Group (HORG)[J]. Clin Transl Oncol,2016,25(6):103-105.
[8]Ma D, Hao X, Wang Y, et al. Clinical effect of pemetrexed as the first-line treatment in Chinese patients with advanced anaplastic lymphoma kinase-positive non-small cell lung cancer[J]. Thorac Cancer,2016,7(4):452-458.
[9] 石远凯,孙燕,于金明,等. 中国晚期原发性肺癌诊治专家共识(2016年版)[J]. 中国肺癌杂志,2016,22(01):1-15.
[10]陆国权,周晓红,陈红,等. 培美曲塞联合顺铂与多西他赛联合顺铂治疗非小细胞肺癌的疗效对比[J]. 中国生化药物杂志,2015,32(8):143-145.
[11]刘雨桃,胡兴胜,李峻岭,等. 培美曲塞联合铂类药物治疗老年晚期肺腺癌的疗效与安全性分析[J]. 临床药物治疗杂志,2015,24(5):24-28.
[12]李蕊,杜美春,闫可颐. 探析培美曲塞及顺铂化疗在晚期非小细胞肺癌治疗中的效果[J]. 中国现代药物应用,2016,25(8):166-167.
[13]李海丽,王轶楠,肖建波,等. 培美曲塞联合铂类化疗对晚期非小细胞肺癌患者外周血TGF-β1、MMP2的影响[J]. 现代肿瘤医学,2015,32(23):3439-3442.
[14]Tomasini P, Barlesi F, Mascaux C, et al. Pemetrexed for advanced stage nonsquamous non-small cell lung cancer: latest evidence about its extended use and outcomes[J]. Ther Adv Med Oncol,2016,8(3):198-208.
[15]Grossi F, Bennouna J, Havel L, et al. Oral vinorelbine plus cisplatin versus pemetrexed plus cisplatin as first-line treatment of advanced non-squamous non-small-cell lung cancer: cost minimization analysis in 12 European countries[J]. Curr Med Res Opin,2016,22(5):1-8.
(编校:王俨俨)
Effect and safty of pemetrexed combined with platinum drug in advanced non-small-cell lung cancer
CHEN QianΔ, PAN Chao
(Department of Thoracic Oncology, Tumor Hospital of Zhejiang Province, Hangzhou 310022, China)
ObjectiveTo observe the therapeutic effect of pemetrexed combined with platinum drug in advanced non-small-cell lung cancer and its safety.MethodsThe clinical data of patients with advanced non-small-cell lung cancer who
chemotherapy in our hospital from August 2013 to August 2015 were retrospectively analyzed. According to the method, the chemotherapy were divided into the cisplatin combined with paclitaxel chemotherapy group and the cisplatin combined with pemetrexed chemotherapy. The therapeutic effects of two groups were observed and the differences of tumor markers levels, quality of life and the incidence of side effects between the two groups before and after treatment were compared.ResultsThe effective rate of cisplatin combined with pemetrexed chemotherapy was 98.2%, which was significantly higher than that in control group (82.5%) (P<0.05). There was no significant difference in the levels of tumor markers between the two groups before treatment, the levels of tumor markers in the two groups after treatment was lower than before treatment, and the cisplatin combined with pemetrexed chemotherapy decreased more significantly(P<0.05). There was no significant difference in the incidence of systemic toxicity, gastrointestinal toxicity, liver and renal function between the two groups. There was no significant difference in quality of life between the two groups before treatment. After treatment, the quality of life of the two groups improved after treatment, and the improvement of the cisplatin combined with pemetrexed chemotherapy was more obvious (P<0.05).ConclusionThe combination of the pemetrexed and platinum drug in the treatment of advanced non-small-cell lung cancer has a good effect, could significantly improve the quality of life of patients.
pemetrexed; platinum drug; advanced non-small-cell lung cancer; quality of life
10.3969/j.issn.1005-1678.2016.07.17
陈倩,通信作者,男,博士,住院医师,研究方向:胸外科疾病诊断及治疗,E-mail:chenqianys@163.com。
R734.2
A
