由粉煤灰制备MCM-41及其负载纳米TiO2的光催化性能研究
2016-06-05李增和陈光岩
靳 琳,李增和*,李 歌,陈光岩
(1.北京化工大学 理学院,北京 100029;2.中国石油吉林石化公司 研究院,吉林 吉林 132021)
近年来染料被广泛使用在纺织、皮革和造纸等工业[1],由染料引发的环境污染也日益显著。而TiO2纳米制备技术的发展为染料的光催化降解提供了有效途径。TiO2在受到高能量光照射时,价带电子发生跃迁并移至表面,促进生成高活性的·OH,从而降解染料[2]。TiO2由于光催化效率高、氧化能力强、成本低、稳定性高等性能而备受研究者青睐[3]。由于量子尺寸效应,TiO2颗粒越小越有利于提高光催化性能。然而小粒径会造成TiO2的严重团聚并且不利于工业回收利用,造成浪费[4-5]。为了解决这一问题人们关注于将纳米TiO2负载于不同载体上。比如:介孔分子筛SBA-15、SBA-16、MCM-41等[6],黏土[7],高分子膜[8],活性炭[9]等。在这些载体之中介孔分子筛由于可为纳米TiO2的生长提供特殊的孔道环境,有效抑制团聚和粒径增长,并且为TiO2提供大的比表面积使其更有利于反应物与光催化中心的接近而备受青睐。其中MCM-41由于孔径均匀,吸附容量大,水热稳定性好,具有有序的二维六方孔道结构以及易于修饰而被视为理想载体[10]。一般来说,纯TiO2在激发波长小于387.5 nm的紫外光源下才有光催化活性[11]。但在吸附染料的情况下,染料可以作为敏化剂吸收可见光辐射从而被激发将电子转移到TiO2,使其在可见光区也有响应[12]。Lachheb H[13]等人研究了TiO2-SBA-15在可见光下的催化性能。作者考察了TiO2/MCM-41在氙灯模拟日光光源下的光催化活性,并且讨论了TiO2负载量、pH值与温度对于光催化的影响。
1 实验部分
1.1 试剂与仪器
钛酸四丁酯:分析纯,天津市福晨化学试剂厂;亚甲基蓝:分析纯,天津光复精细化工;无水乙醇、硝酸、过氧化氢、NaOH、HCl:分析纯,北京化工厂;十六烷基三甲基溴化铵(CTAB):分析纯,梯希爱(上海)化成工业;去离子水:自制。
X射线衍射仪:2500VB2+PC型,日本理学株式会社;傅立叶红外光谱仪:Nicoeit 8700,美国热电公司;紫外-可见光谱仪:UV-3600型,日本岛津公司;透射电子显微镜:23200N型、扫描电镜:S-4700型,日本日立公司。拉曼光谱仪:RenishawInVia,英国雷尼绍公司;可见分光光度计:722型,南京宁博分析仪器有限公司;光催化装置:特制,北京光电研究所。
1.2 催化剂的制备
1.2.1 MCM-41的制备
将北京市石景山区热电厂粉煤灰10 g放入烧瓶中,加入100 mL、2 mol/L HCl在80 ℃下搅拌2 h除铁,抽滤、洗涤,滤饼95 ℃干燥。再加入7.7 g NaOH及20 mL水,置于有聚四氟乙烯内衬的反应釜,95 ℃碱溶4 h后取上清液。将3.204 6 g CTAB溶于63 mL水中,35 ℃下搅拌2 h。加入粉煤灰前处理过程中所得清液,调节pH值至10.5,25 ℃下搅拌2 h。所得溶液倒入有聚四氟乙烯内衬的反应釜中。100 ℃下晶化72 h。抽滤洗涤,将产物100 ℃干燥8 h,550 ℃煅烧,得到MCM-41型介孔分子筛。
1.2.2 TiO2/MCM-41的制备
将5 mL无水乙醇和2 mL钛酸四丁酯混合制成A液。15 mL无水乙醇中加入0.8 mL水,在磁力搅拌下缓慢加入0.2 mL浓硝酸,再分别加入0,0.935,1.168 8,1.558 3,2.337 8和4.675 0 g MCM-41超声10 min,搅拌30 min制得B液。25 ℃水浴下将A液缓慢滴加入溶液B,搅拌1 h,静置待其形成凝胶。将凝胶放入100 ℃烘箱中干燥20 h后,置于马弗炉中550 ℃煅烧4 h。研磨后得到纯TiO2及TiO2质量分数分别为20%、40%、60%和80%的TiO2/MCM-41样品,表示为20%TiO2/MCM-41、40%TiO2/MCM-41、60%TiO2/MCM-41、80%TiO2/MCM-41。
1.3 样品的表征
XRD测试条件:Cu Kα波长为0.154 06 nm,扫描范围为1°~ 7°和15°~90°。FT-IR光谱采用KBr压片法,测量范围为400~4 000 cm-1。固体紫外可见光谱,扫描范围为200~800 nm,BaSO4作为基体。样品形貌与孔道结构分别使用扫描和透射电子显微镜观察。
1.4 光催化性能的测定
光催化装置以500 W氙灯为光源。取100 mL、35 mg/L亚甲基蓝溶液,加入0.02 g TiO2或TiO2/MCM-41催化剂。超声10 min,加入双氧水30.6 μL,用1 mol/L的NaOH和HCl溶液调节pH值。然后暗反应至吸附平衡。打开光源进行光催化反应,每隔一定的时间取适量反应液,用0.22 μm针头滤器过滤,测定在665 nm处的吸光度,与标准曲线对比确定其浓度。催化剂稳定性通过循环实验来考察。将光催化后的催化剂离心分离,乙醇清洗,120 ℃烘干,300 ℃煅烧3 h。然后在相同条件下测试其光催化性能。
2 结果与讨论
2.1 XRD分析
不同TiO2质量分数的催化剂XRD分析结果见图1、图2。
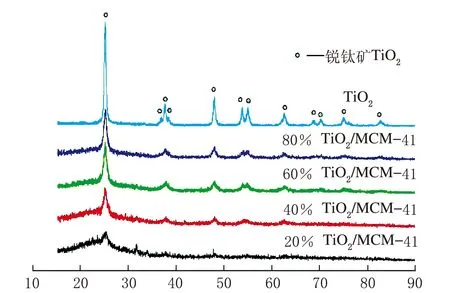
2θ/(°)图1 不同负载量TiO2/MCM-41的XRD图
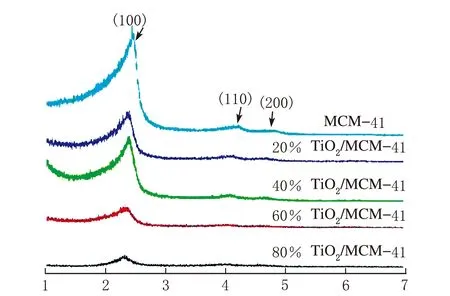
2θ/(°)图2 不同负载量TiO2/MCM-41的SA-XRD图
由图1可见,采用溶胶凝胶法制备的纯TiO2在2θ为25.3°,37.7°,48.0°,53.8°,55.0°和62.7°处均出现了衍射峰,而这些峰是锐钛矿的特征衍射峰分别对应其(101),(004),(200),(105),(211)和(204)晶面。而锐钛矿峰强度随着TiO2质量分数的减小而减小。由图2可以看出,MCM-41在1°~7°有3个特征峰,分别属于(100)、(110)和(200)晶面。这些都属于典型的二维六方介孔结构的特征衍射峰。随着TiO2掺杂量的增加MCM-41的特征峰强度有所下降,这可能是因为掺杂导致MCM-41孔道有序性下降所致。虽然特征峰强度有所下降但其各晶面衍射峰一直存在说明即使掺杂TiO2,催化剂的孔道结构依然稳定。
2.2 FT-IR分析
为了证明在催化剂的框架结构中是否掺杂进了TiO2,对催化剂进行了FT-IR分析,结果见图3。
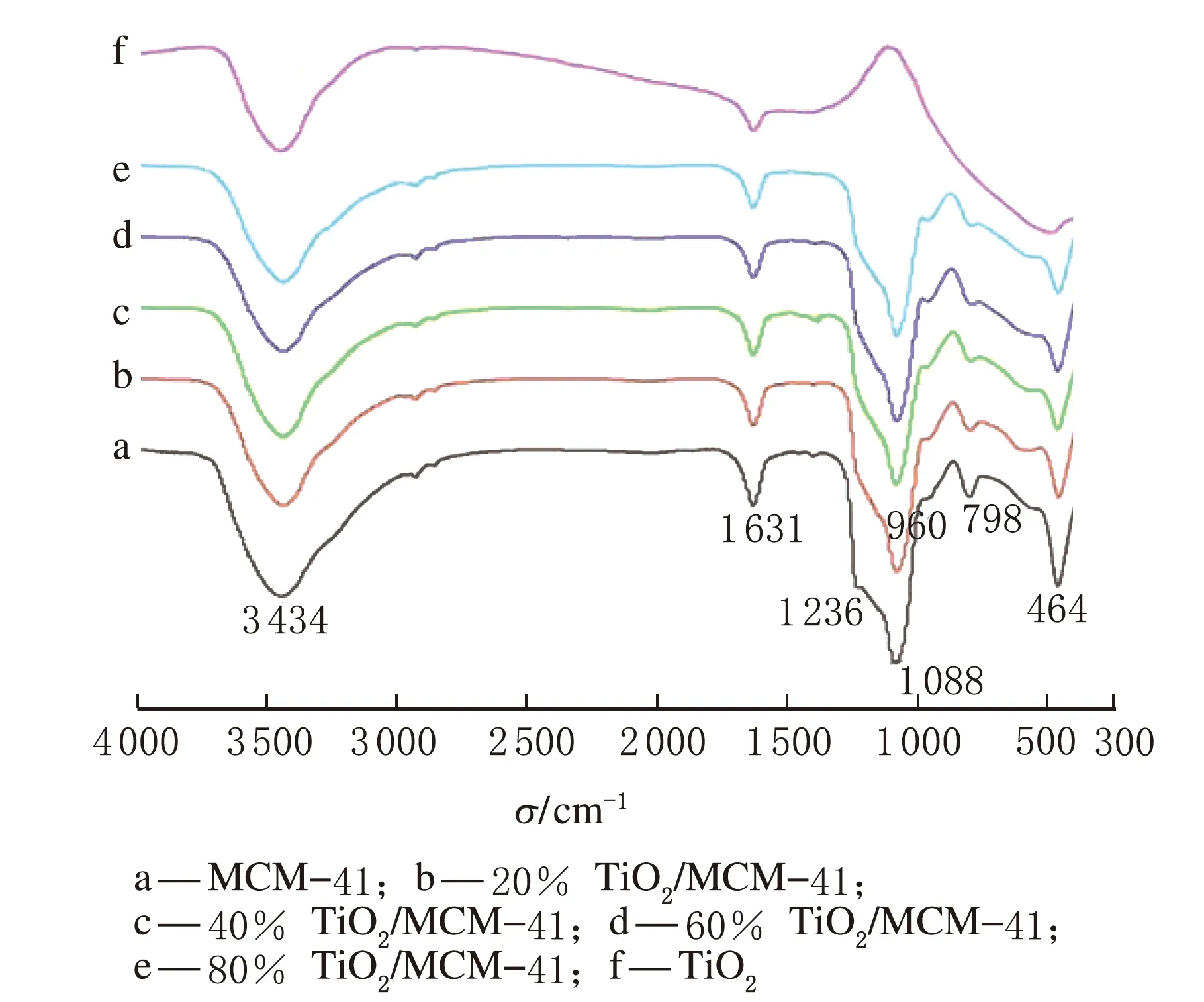
图3 催化剂的FT-IR图
图3中3 434和1 631 cm-1处的吸收峰分别为样品所吸附水中O—H键的伸缩和弯曲振动吸收峰。TiO2中400~600 cm-1处的宽吸收峰为典型的Ti—O—Ti的振动吸收峰。而在分子筛中464 cm-1处的吸收峰为Si—O—Si键的弯曲振动吸收峰。两者在464 cm-1处出现了重叠。798和1 081 cm-1处的吸收峰分别为Si—O—Si键的对称和反对称伸缩振动峰。1 081 cm-1处及其在1 236 cm-1处的肩峰是SiO4四面体结构单元的特征吸收峰。960 cm-1处的吸收峰是含Ti分子筛的一个重要的吸收峰,为Ti—O—Si键的伸缩振动吸收峰。它是Si—O键伸缩振动时被相邻的Ti金属离子干扰所形成的。这证明了Ti进入了分子筛骨架之中[14]。此外在图3中可以看出随着TiO2负载量的增加960 cm-1处的吸收峰强度增加。
2.3 紫外-可见光谱分析
不同负载量的催化剂紫外-可见光谱表征结果见图4。
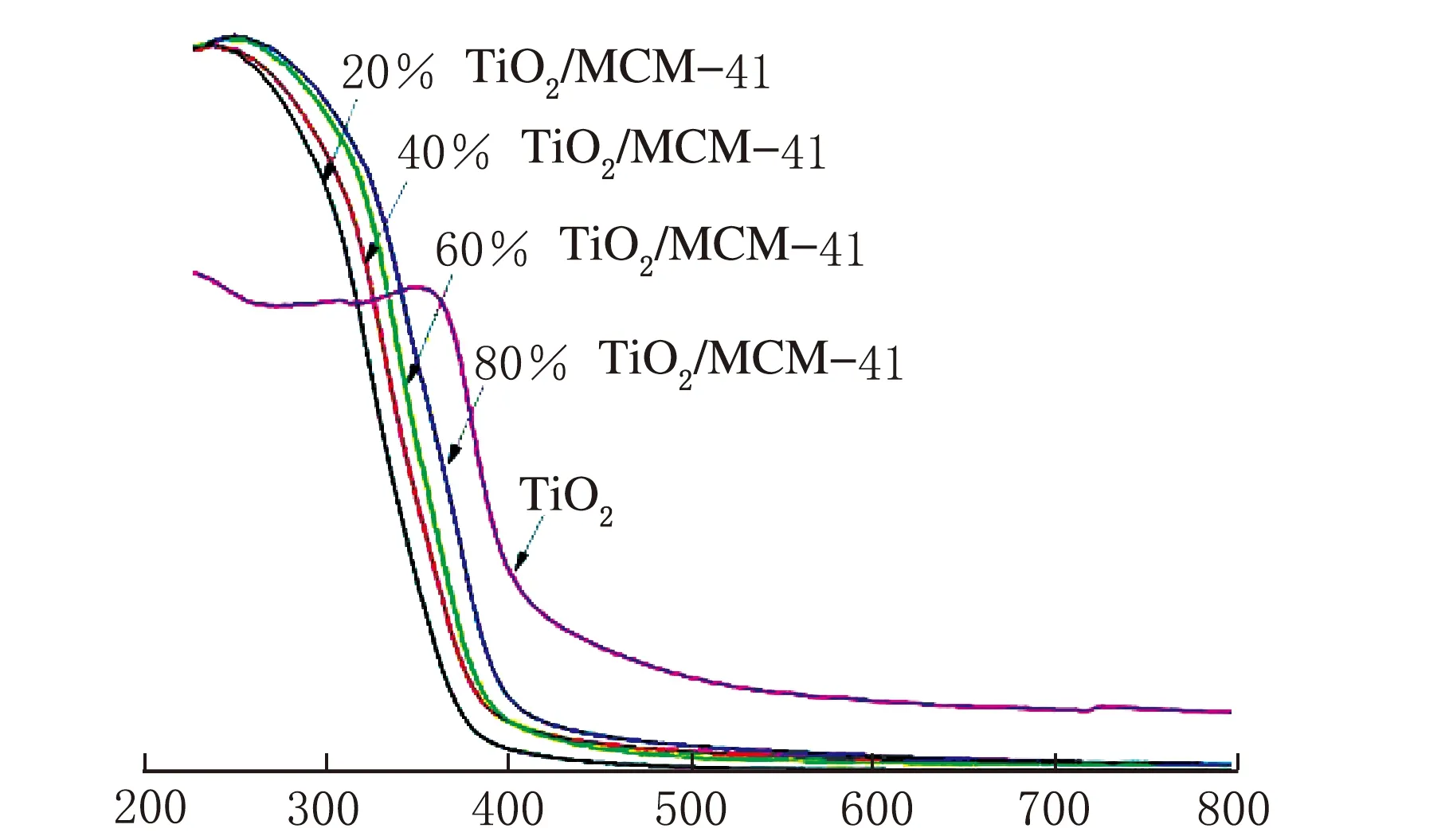
λ/nm图4 不同负载量的催化剂紫外-可见光谱
图4中样品的紫外-可见光光谱图与纯TiO2的吸收带相比掺杂后的样品吸收带发生了蓝移。而导致这一现象的是量子限制效应。MCM-41的孔道结构为TiO2提供了生长的环境,这些孔道可以有效地防止TiO2粒子的聚集,也控制其粒径。由于TiO2粒径的减小使得吸收带发生蓝移[15]。图中还可以看出复合催化剂蓝移的程度随着TiO2负载量的增加而减少,这有可能是因为在合成过程中随着Ti4+浓度的增加TiO2粒子直径增加从而禁带间隙减小的缘故[16]。
2.4 SEM与TEM分析
样品的SEM和TEM表征结果见图5、图6。
从图5a中可以看出所制备的TiO2直径约为20~30 nm且团聚严重,这会影响其光催化性能。相较MCM-41负载TiO2前,负载后其颗粒表面明显变得没有之前光滑(见图5b)。为了对于MCM-41负载TiO2后的孔道结构及负载情况进行分析,对样品进行了TEM表征,见图6。由图6a可以看出MCM-41是有序的六边形纳米孔道。在掺杂后(图6b),TiO2微粒在MCM-41中均匀分布,且粒径明显较图6a中小,约为10 nm。这与紫外-可见吸收光谱分析结果一致。可见TiO2掺杂入介孔分子筛有利于控制粒径,增大比表面积。而掺杂TiO2后MCM-41的二维六方介孔结构依旧完好,说明掺杂并未改变介孔结构。只是有序度较之前有所降低,这与SA-XRD图结论一致。

a TiO2

b 60% TiO2/MCM-41图5 样品透射电镜图

a MCM-41

b 60% TiO2/MCM-41图6 样品扫描电镜图
2.5 光催化性能分析
2.5.1 TiO2负载量对于光催化性能的影响
不同TiO2负载量的TiO2/MCM-41因其TiO2颗粒大小、比表面积及孔道容积不同,会影响催化剂的光催化活性。反应温度15 ℃,其光催化结果见图7。

t/min图7 TiO2和不同TiO2负载量催化剂对亚甲基蓝的光催化性能
由图7可以看出光催化过程分为黑暗条件下的吸附过程和光催化降解过程。催化剂暗反应40 min达吸附平衡,TiO2对于亚甲基蓝的吸附仅为1.7%,远低于TiO2/MCM-41。而TiO2负载量越低吸附效果越好。其中20%TiO2/MCM-41的吸附量达到66.7%。这归因于介孔分子筛含量的增加,使催化剂吸附位点增多。而吸附有利于反应物与光催化活性位点的接触。为了更直观的表达催化剂降解性能,做出了降解率随时间的变化曲线,见图8。从图8可以看出,在光照条件下TiO2的催化效果低于TiO2/MCM-41。这可归因为TiO2/MCM-41中TiO2粒径更小且分散,提高了单位质量的光催化活性位点个数。此外,当负载量过大时,分子筛对TiO2的抑制作用降低可能会出现不同程度的团聚,阻塞孔道造成光催化性能减小。当负载量为60%时催化剂光催化性能最好。
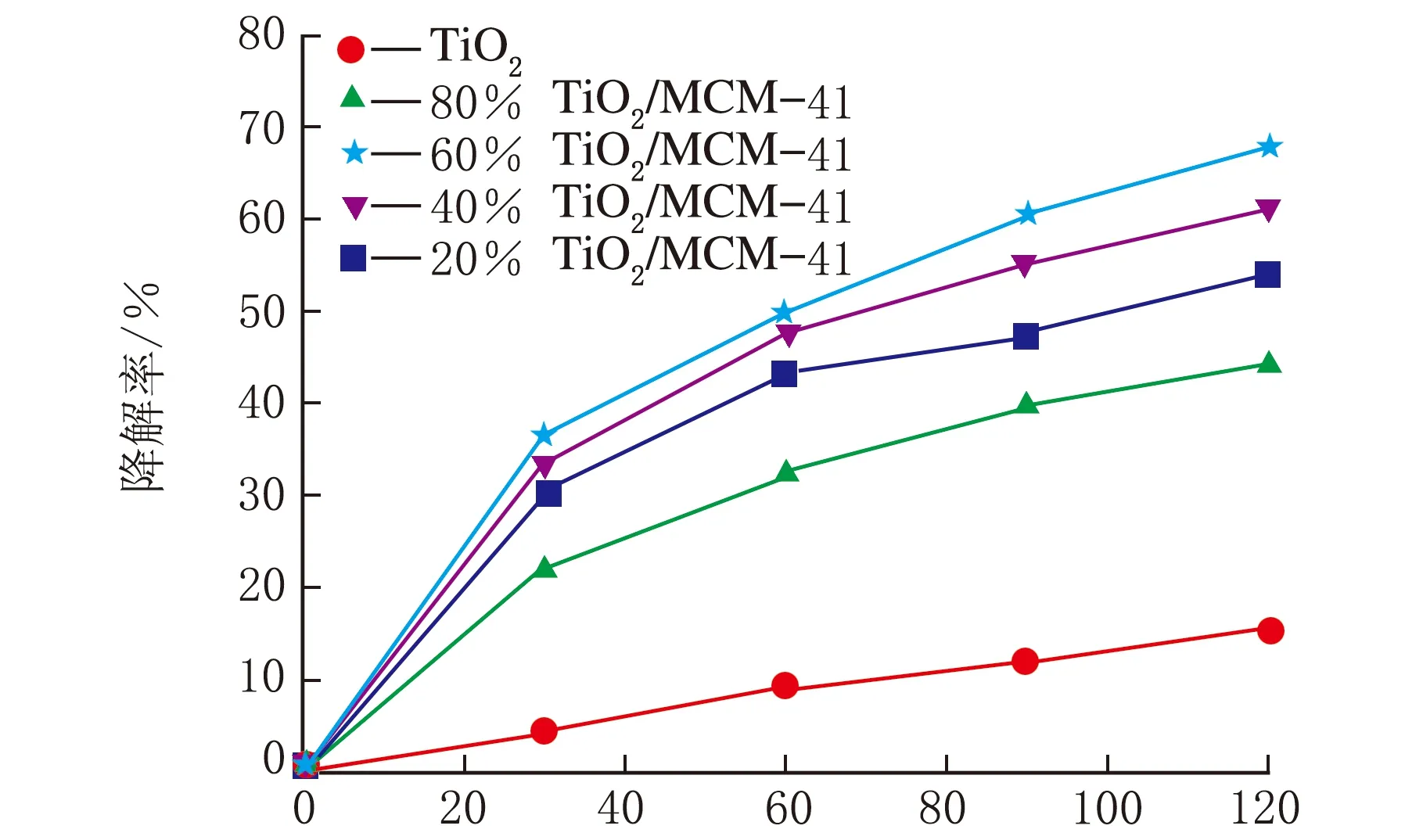
t/min图8 不同TiO2负载量对亚甲基蓝光催化降解率的影响
为了更好的考察催化剂光催化性能,进行了动力学研究。一般认为染料的光催化降解符合一级动力学反应特征[17],见下式。
lnc0/ct=kt
式中,c0为初始浓度,ct为t时间所对应的反应液浓度。以ln(c0/ct)为Y轴,t为X轴作图,见图9。
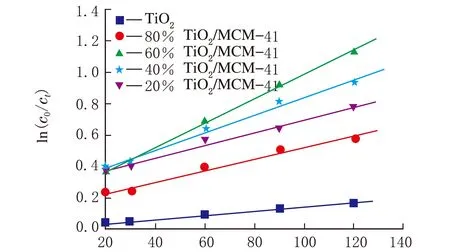
t/min图9 TiO2和不同TiO2负载量催化剂光催化降解亚甲基蓝的ln(c0/ct)-t动力学曲线
由图9可以看出ln(c0/ct)与t呈线性关系说明反应属于一级动力学反应。经拟合TiO2和(80%,60%,40%,20%)的TiO2/MCM-41反应速率常数分别为:0.001 4,0.003 7,0.007 8,0.005 6和0.004 min-1。可以看出MCM-41的加入明显提高了TiO2的光催化活性,且与负载量多少有关。其中60% TiO2/MCM-41光催化活性最高,而TiO2的光催化活性最低,这与图8结果一致。
2.5.2 pH值对于光催化性能的影响
用HCl和NaOH调节反应溶液初始pH=3、5、7、9和11,在15 ℃下使用60% TiO2/MCM-41进行光催化研究,结果见图10。
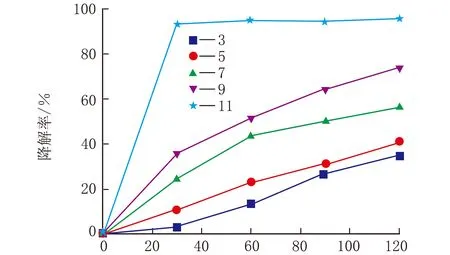
t/min图10 pH值对于亚甲基蓝光催化降解率的影响
由图10可以看出,降解率随着pH值的增加而增大。当pH=11时降解率在120 min可达95.5%,当pH=3时降解率只有35%。这归因为pH值增大OH-浓度增加,有利于形成羟基自由基,而羟基自由基可避免光生电子和光生空穴的结合。所以pH=3~11范围增加有利于光催化性能的提高。
2.5.3 温度对于光催化性能的影响
使用60%TiO2/MCM-41,在pH=7条件下降解60 min,研究温度对于亚甲基蓝光催化性能的影响,结果见图11。
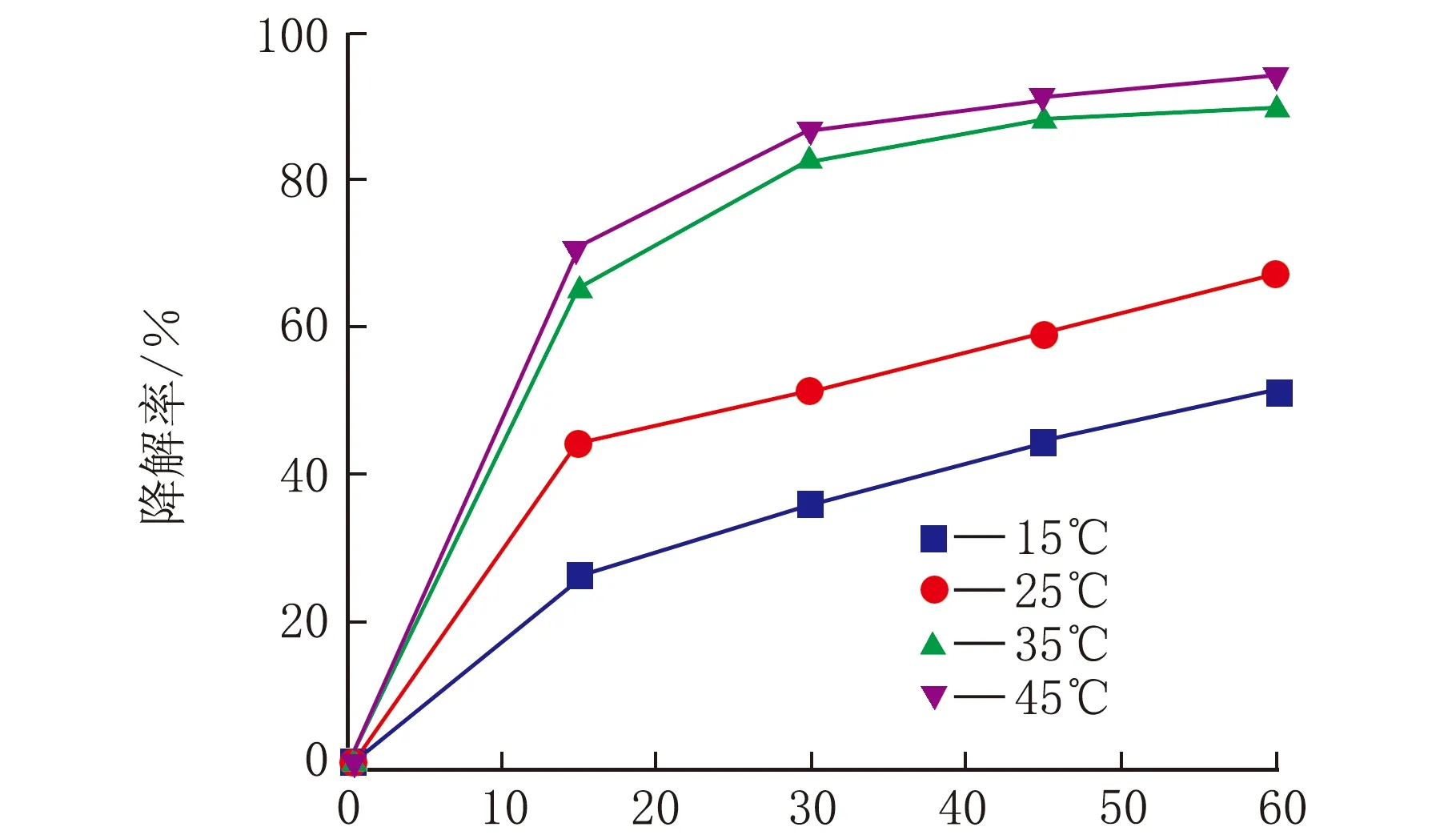
t/min图11 温度对于亚甲基蓝光催化降解率的影响
由图11可知,随着温度的升高降解率升高。在45 ℃,60 min光催化降解率便可达到94.05%。由于已经证明此光催化反应为一级动力学反应。对15、25、35和45 ℃分别做ln(c0/ct)-t图,得反应速率k分别0.009 3,0.011 6,0.026 8和0.034 4 min-1。由Arrhenius公式lnk=-Ea/(RT)+B,做lnk-1/T图,斜率为Ea/R,经拟合得Ea/R=4 356,R为摩尔气体常量,所以活化能Ea为36.2 kJ/mol。可知光催化降解所需活化能较高,因而温度对其影响较大,温度越高光催化活性越大。
2.5.4 TiO2/MCM-41催化剂的稳定性
为了研究催化剂的稳定性,对于光催化回收的60% TiO2/MCM-41催化剂经过洗涤、干燥、煅烧后相同条件下进行了循环使用下吸附及光催化降解性能变化的研究,设第1次的效率为100%,比较循环使用后效率的相对变化。结果见图12。
由图12可见,相较于第1次使用,除了第2次吸附率有所升高外,3、4次均有所下降。第4次使用较新鲜催化剂吸附性率下降了3.59%。而第2、3、4次光催化降解率分别为第1次光催化降解率的95.42%,93.83%和91.64%。随着催化剂使用次数的增加降解率有所下降,但幅度均不大,可见60% TiO2/MCM-41催化剂结构较为稳定,可多次重复使用。经过4个周期后吸附率下降了3.59%,降解率下降了8.36%。

循环次数图12 60% TiO2/MCM-41在不同光催化周期降解率较新鲜催化剂变化情况
3 结 论
通过由粉煤灰制备的MCM-41与钛酸四丁酯溶胶-凝胶制备了不同TiO2负载量的TiO2/MCM-41催化剂。对于所制备催化剂进行了相关表征和光催化亚甲基蓝性能探究。结果发现,TiO2均匀掺杂进入了MCM-41孔道有效抑制了团聚和粒径的增加。TiO2/MCM-41光催化性能也优于纯TiO2,当TiO2负载量为60%时光催化性能最高,反应属于动力学一级反应。此外,pH值和温度的增加都有利于光催化的进行。
参 考 文 献:
[1] HAMDAOUI O,SAOUDI F,CHIHA M,et al.Sorption of malachite green by a novel sorbent,dead leaves of plane tree:equilibrium and kinetic modeling[J].Chemical Engineering Journal,2008,143(1):73-84.
[2] HAN T Y,WU C F,Hsieh C T.Hydrothermal synthesis and visible light photocatalysis of metal-doped titania nanoparticles[J].Journal of Vacuum Science & Technology,B:Microelectronics and Nanometer Structures--Processing,Measurement,and Phenomena,2007,25(2):430-435.
[3] NEATU S,SACALIUC-PARVULESCU E,LEVY F,et al.Photocatalyticdecomposition of acetone over dc-magnetron sputteringsupported vanadia/TiO2catalysts[J].Catalysis Today,2009,142(3/4):165-169.
[4] ACOSTA-SILVAY J,NAVAR,HERNNDEZ-MORALESV,et al.Methylene blue photodegradation over titania-decorated SBA-15[J].Applied Catalysis B:Environmental,2011,110:108-117.
[5] ZANJANCHI M A,GOLMOJDEH H,ARVAND M.Enhanced adsorptive and photocatalytic achievements in removal of methylene blue by incorporating tungstophosphoric acid-TiO2into MCM-41[J].Microp Journal of Hazardous Materials,2009,169:233-239.
[6] BINITA NANDA,AMARESH C PRADHAN,PARIDA K M.A comparative study on adsorption and photocatalytic dye degradation under visible light irradiation by mesoporous MnO2modified MCM-41 nanocomposite[J].Microporous and Mesoporous Materials,2016,226:229-242.
[7] SHIMIZU K,KANEKO T,FUJISHIMA T,et al.Selectiveoxidation of liquid hydrocarbons over photoirradiated TiO2pillared clays[J].Applied Catalysis,A:General,2002,225(1/2):185-191.
[8] DHANANJEYAN M R,KIWI J,THAMPI K R.Photocatalytic performance of TiO2and Fe2O3immobilized on derivatized polymer films for mineralisation of pollutants[J].Chemical Communications(Cambridge),2000(15):1443-1444.
[9] HERMANN J,MATOS J,DDISDIER J,et al.Solar photocatalytic degradation of 4-chlorophenol using the synergistic effectbetween titania and activated carbon in aqueous suspension[J].Catalysis Today,1999,54(2/3):255-265.
[10] 冯利利,赵威,刘洋,等.MCM-41分子筛担载纳米TiO2复合材料光催化降解罗丹明B[J].物理化学学报,2009,25(7):1347-1351.
[11] SADJADI M S,MOZAFFARI M,ENHESSARI M,et al.Effects of NiTiO3nanoparticles supported by mesoporous MCM-41 on photoreduction of methylene blue under UV and visible light irradiation[J].Superlattices and Microstructures,2010,47(6):685-694.
[12] DING H,SUN H,SHAN Y.Preparation and characterization of mesoporous SBA-15 supported dye-sensitized TiO2photocatalyst[J].Journal of Photochemistry and Photobiology A:Chemistry,2005,169(1):101-107.
[13] LACHHEB H,AHMED O,HOUAS A,et al.Photocatalytic activity of TiO2-SBA-15 under UV and visible light[J].Journal of Photochemistry and Photobiology A:Chemistry,2011,226(1):1-8.
[14] MA L N,JI J B,YU F W,et al.Post-synthesis of TiO2/MCM-41 from aqueous TiCl4solution:structure characteristics and epoxy catalytic activity[J].Microporous and Mesoporous Materials,2013,165:6-13.
[15] YANG H M,DENGY H,DU C F.Synthesis and optical properties of mesoporous MCM-41 containing doped TiO2nanoparticles[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2009,339:111-117.
[16] SOROLLA M G,DALIDA M L,KHEMTHONG P,et al.Photocatalytic degradation of paraquat using nano-sized Cu-TiO2/SBA-15 under UV and visible light[J].Journal of Environmental Sciences,2012,24:1125-1132.
[17] KUO C S,LIN C F,HONG P K.Photocatalytic degradation of methampheta mine by UV/TiO2kinetics,intermediates,and products[J].Water Research,2015,74:1-9.
