银缓释载银杀菌活性炭的低温水热炭化法制备*
2016-05-17孔祥千豆彩霞柴源涛李寿旺李秋岩刘守新
孔祥千,豆彩霞,柴源涛,李寿旺,李秋岩,刘守新
(东北林业大学 材料科学与工程学院, 哈尔滨 150040)
银缓释载银杀菌活性炭的低温水热炭化法制备*
孔祥千,豆彩霞,柴源涛,李寿旺,李秋岩,刘守新
(东北林业大学 材料科学与工程学院, 哈尔滨 150040)
摘要:采用低温水热炭化法制备了载银活性炭(Ag/AC),以大肠杆菌(E.coli)为实验菌种,考察了不同载银量活性炭的灭菌性能和抗银流失性能。利用X射线衍射(XRD)、扫描电子显微镜(SEM)以及低温液氮吸附对载银活性炭进行表征。结果表明,负载银对活性炭的石墨微晶结构无影响。随着载银量的增加,负载到活性炭上的银晶粒变大,比表面积、孔容积和孔径均变小,抗菌性能提高,银流失量变化不明显,抗流失天数增多。经分析,载银量为1.54%(质量分数)Ag/AC3样品,比表面积为813.35 m2/g,100 min之内杀灭107 CFU/mL的大肠杆菌,9 d内银流失量约为2.9%,可见,在保持较高比表面积的基础上,具备良好的抗菌性能和抗银流失性能。
关键词:低温水热;载银活性炭;抗菌;银缓释
1引言
椰壳活性炭是一种性质优良的非极性吸附剂,具有独特的孔隙结构和表面活性官能团,化学性质稳定,机械强度高,耐酸、耐碱、耐热,不溶于水和有机溶剂,使用失效后可以再生[1],被广泛应用于饮用水净化[2-3]。椰壳活性炭在净水过程中由于其本身良好的生物相容性,在吸附、富集水中的有机物后,极易成为细菌生长繁殖的温床,从而导致水体中微生物数量增加,并生成致突变物质亚硝酸盐,造成出口水质变坏[4]。
为克服此缺点,通常将具有杀菌性能的物质负载在AC表面,以消除饮用水深度净化过程中微生物繁殖所带来的二次污染。当银离子与微生物接触后,能强烈吸附微生物细胞,并与细胞机体中酶蛋白的巯基(-SH)反应, 使微生物蛋白质凝固,然后致其失活[5],银离子具有抗菌广谱、杀菌效率高、不易产生抗药性等优点,可以用来杀死或者抑制细菌、病毒、藻类和真菌[6]。实验表明,人体组织中银含量小于0.01% mg,多余银可通过消化道很快排除,不会引起人体器官和组织的病理变化[7]。目前,国内外饮用水深度净化活性炭的抗菌成分主要以担载银为主。此外,目前市售Ag/AC的制备方法主要以浸渍法为主,但活性炭对银主要是物理吸附,银极易流失,不能达到持久杀菌的效果,并且短时间内释放的银离子浓度较高,对人体造成伤害[8-10]。因此在保持高抗菌活性下实现银的缓释具有重要意义。
本文将多孔性活性炭浸渍在AgNO3溶液中,然后通过低温(120 ℃)水热反应,将金属Ag负载到活性炭上,得到杀菌功能Ag/AC。利用XRD、SEM、低温液氮吸附等手段对Ag/AC进行表征,通过对E.coli的杀菌实验和恒温震荡法测量Ag/AC的抗菌性能和抗银流失性能。
2实验
2.1原料和试剂
活性炭(苏州美净活性炭厂);硝酸银(天津市禹名化学试剂厂,分析纯);氢氧化钠(哈尔滨化学化工试剂厂,分析纯);硫酸铁(Ⅲ)铵(天津石英钟厂霸州市化工分厂,分析纯);硫氰酸钠(温州市化学用料厂,分析纯);浓硝酸(锦州市宏远市机厂,分析纯);营养琼脂(北京奥博星生物技术有限责任公司,生化试剂);大肠杆菌(黑龙江省应用微生物研究所)。
2.2载银活性炭的制备
以苏州美净活性炭厂的椰壳活性炭为原料。使用前蒸馏水洗除去其表面浮尘和杂质,在105 ℃恒温干燥12 h后储于干燥器中备用(标为ACraw)。将一定量的ACraw分别与一定量的浓度为1.0,2.0,4.0和8.0 g/L的AgNO3溶液放置反应釜中120 ℃反应6 h,之后用蒸馏水洗涤直至无银离子检出。然后将上述活性炭置于70 ℃真空干燥箱中烘4 h,在氮气保护下,500 ℃煅烧2 h,制得Ag/AC。按照所采用硝酸银溶液浓度的不同,分别标记为Ag/AC1、Ag/AC2、Ag/AC3、Ag/AC4。
2.3材料表征
SEM测试在QUATA200型扫描电子显微镜(荷兰FEI 公司)上进行;XRD测试在日本理学D/max-rB型X射线衍射仪上进行,室温,CuKα射线,管电压40 kV,管电流30 mA,根据Scherrer公式计算晶粒大小;FT-IR测试在Nicolet-560型傅立叶变换红外光谱仪(美国尼高力)上进行,KBr压片;比表面积测定在ASAP2020自动吸附仪(美国麦克公司)上进行,采用低温液氮(77 K)吸附法,相对压力(p/p0)范围为0.01~1. 0,所有样品测试前均在300 ℃脱气10 h。
2.4银含量测定
载银活性炭的载银量分析参照HAN Ping等文献[11]所述方法测定。
2.5抗菌性能测试
配置大肠杆菌的肉汤培养基(牛肉膏、蛋白胨、琼脂、NaCl、水、pH值为7.2~7.4)。移取100 mL蒸馏水到锥形瓶中,加入少量肉汤培养基,再加入2.0 g的Ag/AC,用高压灭菌锅灭菌后,冷却至室温。然后在锥形瓶中接入实验菌种,并每隔一段时间测一次细菌浓度。细菌浓度用稀释平板法测定(条件:37 ℃,培养48 h)。每次抗菌实验均同时进行空白和平行对照实验[12]。
2.6抗银流失性能测试
取100 mL蒸馏水和2.0 g载银活性炭放入250 mL的锥形瓶中,于25 ℃条件下以150 r/min恒温振荡,并每隔一段时间测一次水中银的浓度,银的浓度通过双硫腙分光光度法于TU-900型紫外-可见分光光度计上测量[13-14]。
3结果与讨论
3.1载银量及结构分析
银离子与活性炭在水溶液中可以发生氧化还原反应,银离子被还原成单质银而附着在活性炭表面[15]。不同载银活性炭的结构参数如表1所示。
表1不同条件下制备载银活性炭的结构参数
Table 1 Structure parameters of Ag/AC prepared under different conditions

样品银含量/wt%BET比表面积/m2·g-1总孔容/cm3·g-1平均孔径/nmACraw01106.080.422.46Ag/AC10.15860.470.482.18Ag/AC20.60842.150.342.00Ag/AC31.54813.350.341.96Ag/AC42.29751.890.281.73
ACraw的比表面积为1 106.08 m2/g,孔容积为0.42 cm3/g,通过对活性炭载银实验发现,载银活性炭的比表面积比ACraw的比表面积低,同时,随着AgNO3溶液浓度的增加,Ag/AC的银含量随之增加,比表面积、总孔容和平均孔径呈现降低趋势。Ag/AC1的总孔容达到最大值0.48 cm3/g,这可能是因为AC在500 ℃煅烧时,AC发生再活化使Ag/AC的总孔容变大。然而,在银颗粒沉积于载体过程中,由于银对氧有独特的亲和力,只需很少能量就能克服银与氧的排斥力,因此氧原子很容易通过银的晶格,填充在银的八面体空穴中[16-17],成为银生长的晶核,并成长为银颗粒负载而堵塞AC孔隙,导致AC比表面积、平均孔径随着载银量的增加而逐渐降低。
3.2SEM分析结果
低温水热法制备的载银活性炭的SEM图如图1所示。

图1载银活性炭的SEM图
Fig 1 SEM images of the prepared Ag/AC
银颗粒粒径为200~800 nm,大部分分布于活性炭表面,极少量分布于大孔孔道入口处。由图1可知,银颗粒的尺寸和分布与浸渍的AgNO3浓度有关。Ag/AC1表面所载银颗粒数量很少,粒径约为200~400 nm,分布比较均一;Ag/AC2表面所载银颗粒数量明显增加,粒径增加不明显,仍为200~400 nm,分布很均一;Ag/AC3所载银颗粒数量略微增加,粒径也有所增加,约为500 nm;Ag/AC4银颗粒数量显著增加,粒径尺寸分布明显变宽,粒径约为600~800 nm,颗粒聚集现象较为严重。
3.3XRD分析结果
图2为Ag/AC的XRD图。2θ值在20~30°之间的宽峰对应的是石墨微晶(002)乱层结构。经载银煅烧后,该衍射峰的强度稍有增加,但(002)晶面对应峰的衍射角基本无变化,由此表明经载银煅烧后,不改变活性炭的石墨微晶结构。同时样品Ag/AC3、Ag/AC4的XRD谱图中2θ值为38.1,44.2和64.4°的衍射峰分别对应了Ag(111)、Ag(200)、Ag(220)晶面,与纯银的标准XRD谱图(JCPDS卡片04-0783)相对应[18-19],且随着载银量的增加衍射峰强度增强;相对而言,Ag/AC1、Ag/AC2在银处的衍射峰较弱,衍射峰不明显。结果表明,在AgNO3浓度含量为4%和8%时,载银效果明显。

图2 载银活性炭的XRD图
3.4抗菌性能
Ag/AC的抗菌测试结果如图3所示。随着载银量的增加,Ag/AC表现出由无活性、抑菌到杀菌活性的变化规律。对于载银量分别为0.15%和0.60%的Ag/AC1、Ag/AC2,溶液培养24 h后E.coli浓度基本不变,表明它对大肠杆菌只能起到抑制而无杀灭作用。对于载银量为1.54%(质量分数)的Ag/AC3样品能在100 min内杀灭107CFU/mL浓度的E.coli。而载银量2.29%(质量分数)Ag/AC4表现出很强的杀菌性能,在40 min内杀灭107CFU/mL浓度的E.coli。综合对样品的比表面积和杀菌性能分析,为了兼顾Ag/AC吸附性能和杀菌功能,Ag的担载存在最佳担载量,我们选定Ag/AC3样品为最佳。
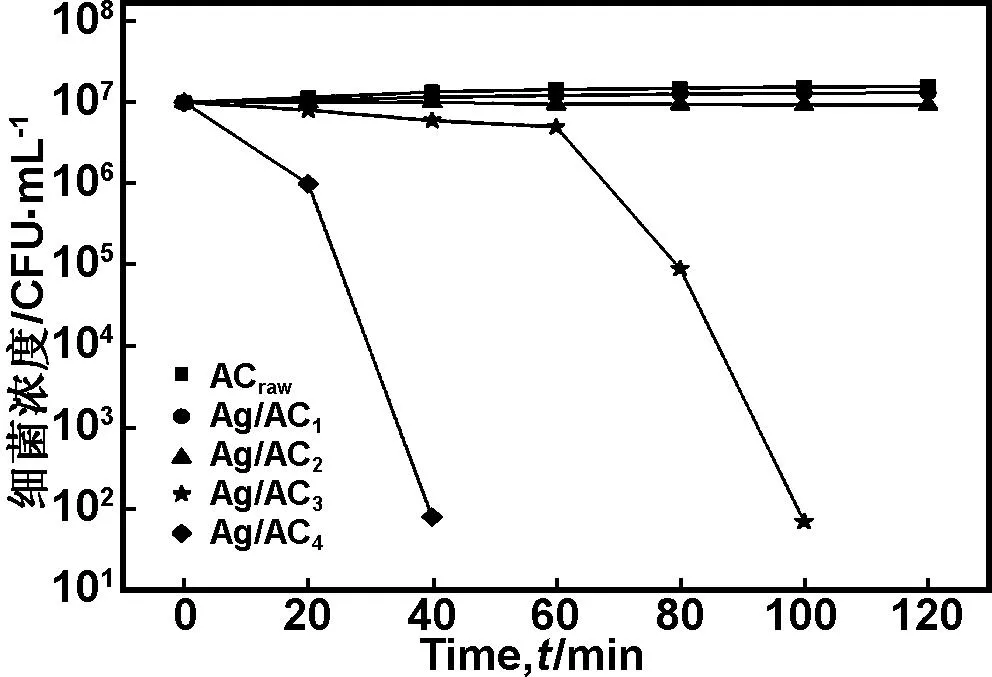
图3 载银活性炭对大肠杆菌的抗菌性能
Fig 3 Anti-bacterial performance towards E. coil of the prepared Ag/AC
3.5抗银流失性能
抗银流失性能的测试结果如图4所示,低温水热法制备的Ag/AC在恒温水浴震荡的条件下,第一天的银流失量较多,约为0.059%,从第二天开始每天的银流失量大概为0.0094%,活性炭中的银缓慢的释放出来,Ag/AC2在前9 d的流失量约为2.7%,不同载银量的活性炭银释放的速度相近。从中可以看出本文方法的一个显著优点,抗银流失性能并不与载银量呈正相关。由此证明,水热反应法制备的Ag/AC,AC与银之间的结合力很强,抗银流失性能好,可以实现银的缓释。
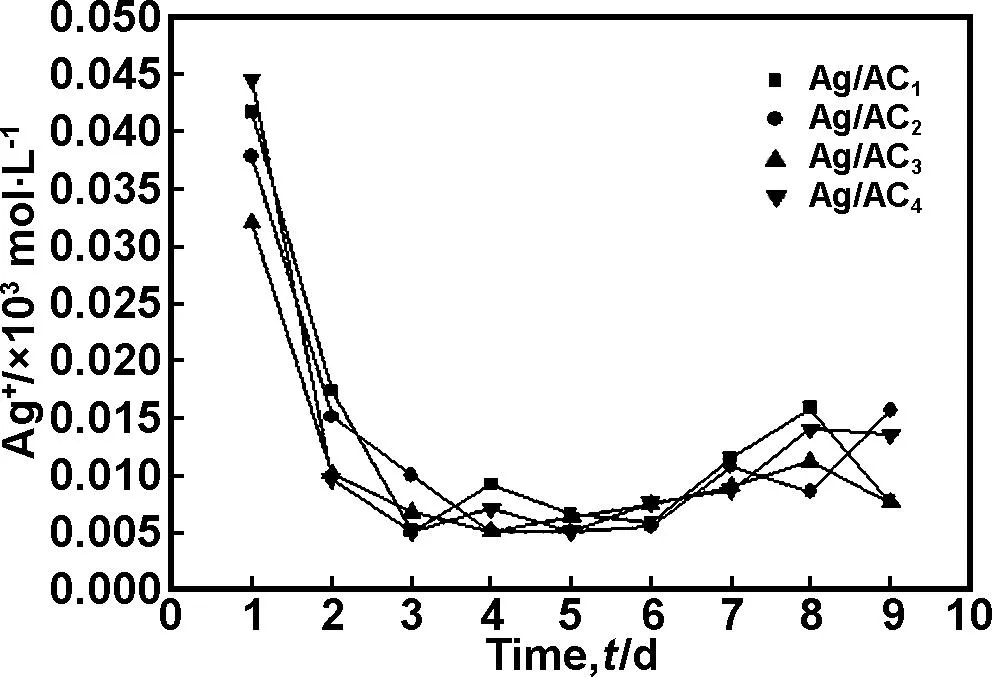
图4 载银活性炭的银离子流失与时间的关系
4结论
低温水热法是一种制备具有银缓释杀菌功能活性炭的适宜方法。随着载银量的增加,所制备活性炭表现出由无活性、抑菌到杀菌活性的变化规律。载银量为2. 28%时,本文制备的活性炭展示出高抗菌活性,但其抗银流失性能较之其它浓度相差不大,流失量较少。由此可见,水热法制备的载银活性炭在保持较高杀菌活性前提下,可以实现银的缓释。低温水热法制备的载银活性炭的载银量、比表面积、生成单质银颗粒的粒径及分布取决于AgNO3溶液浓度。
参考文献:
[1]Zhang H S, Wang Z Q, Wang R, et al. Preparation and characterization of visible-light response activated carbon with antibacterial behavior [J]. Environmental Science, 2011, 32(1): 140-144.
[2]Tang H Q, Feng H J, Zheng J H, et al. A study on antibacterial properties of Ag+-implanted pyrolytic carbon [J]. Surface and Coatings Technology, 2007, 201(9-11): 5633-5636.
[3]Xia G H, Zhao X D, Liao R H. Study on magnetic/active carbon composite coating modification for porous suspension ceramsite [J]. Journal of Functional Materials, 2013, 44(7): 1024-1028.
[4]Pape H L, Solano-Serena F, Contini P, et al. Involvement of reactive oxygen species in the bactericidal activity of activated carbon fiber supporting silver: bactericidal of ACF(Ag) mediated by ROS [J]. Journal of Inorganic Biochemistry, 2004, 98(6): 1054-1060.
[5]Wan Y Z, Wang Y L, Dong X H. Comparison of bacterial adsorption and antibacterial properties between AC and AC(Ag) [J]. Chinese Journal of Biomedical Engineering, 2000, 19(3): 294-299.
[6]Wang G J, Zhang J K. Studies of adsorbent preparation of activated carbon loaded silver for removal of benzothiophene [J]. Journal of Functional Materials, 2013, 44(7): 949-953.
[7]Wang B S, Hu X H. Bacteria "killer"-silver [J]. Metal World, 1995, 5: 21.
[8]Wang Y L, Wan Y Z, Dong X H, et al. Preparation and characterization of antibacterial viscose-based activated carbon fiber supporting silver [J]. Carbon, 1998, 36(11): 1567-1571.
[9]Kim B J, Park S J. Antibacterial behavior of transition-metals-decorated activated carbon fibers [J]. Journal of Colloid Interface Science, 2008,325: 297-299.
[10]Park S J, Jane Y S. Preparation and characterization of activated carbon fibers supported with silver metal for antibacterial behavior [J]. Journal of Colloid Interface Science, 2003, 261 (2): 238-243.
[11]Han P. Analysis of the amount of silver supported in activated carbon [J]. Chemical World, 1999, 11: 606-608.
[12]Quiroga E N, Sampietro A R, Vattuone M A. Screeningantifungal activities of selected medicinal plants [J]. Journal of Ethnopharmacol, 2001, 74(1): 89-96.
[13]Wan L Y. The determination of silver by dith zone-carbon tetrachloride extracted spectrophotomety [J]. Gold, 2006, 27(6): 54-56.
[14]Cao Y F. Determination of Ag+content in Ag-loaded activated carbon by UV method [J]. Coal Chemical Industry, 2006, 3: 50-52.
[15]Chen S X, Zeng H M. Improvement of the reduction capacity of activated carbon fiber[J]. Carbon, 2003, 41(6): 1265-1271.
[16]Outlaw R A, Wu D, Davidson M R, et al. Study of the oxygen transport through Ag (110), Ag (poly), and Ag 2.0 Zr[J]. Journal of Vacuum Science and Technology A, 1992, 10(4): 1497-1502.
[17]Eberhart M E, Donovan M M, Outlaw R A. Ab initio calculations of oxygen diffusivity in group-IB transition metals[J]. Physical Review B: Condensed Matter, 1992, 46(19): 12744-12747.
[18]Grunwaldt J D, Atamny F, Gobel U, et al. Preparation of thin silver films on mica studied by XRD and AFM[J]. Applied Surface Science, 1996, 99(4): 353-359.
[19]Liu S W, Huang W P, Chen S G, et al. Synthesis of X-ray amorphous silver nanoparticles by the pulse sonoelectrochemical method[J]. Journal of Non-Cryst Solids, 2001, 283(1-3): 231-236.
Activated carbon with silver control release and antibacterial behavior by low temperature hydrothermal method
KONG Xiangqian, DOU Caixia, CHAI Yuantao, LI Shouwang, LI Qiuyan, LIU Shouxin
(College of Material Science and Engineering,Northeast Forestry University,Harbin 150040,China)
Abstract:Silver-loaded activated carbons (Ag/AC) were prepared by low temperature hydrothermal carbonization method, Using E.coli as the experimental strains, investigates the antibacterial properties and anti silver loss of different silver content. X-ray diffraction (XRD), scanning electron microscopy and N2 sorption were used to characterize the Ag/AC. The results showed that the content of the silver had no influence on the graphite crystallite structure of the Ag/AC. With the increase of the sliver content, the particle size of the silver doped AC became larger, while the surface area, pore volume and pore size of the carbons decreased. Meanwhile, the antibacterial activity improved as the increase of the sliver content, and the loss of the silver content had not a significant change, thus the performance of silver leaching resistance increased. According to the analysis of the antibacterial experiments, the sample Ag/AC3 with the low silver content of 1.5430wt% and high surface area of 813.3548 m2/g exhibited the high antibacterial activity, which can thoroughly kill the E. coil (107 CFU/mL) in 100 min. Furthermore, the loss percent of the silver was as low as 2.9% after 9 days, which indicated high antibacterial activity and silver leaching resistance.
Key words:low-temperature hydrothermal reaction; silver-loaded activated carbons; antibacterial activity; control release
DOI:10.3969/j.issn.1001-9731.2016.01.043
文献标识码:A
中图分类号:TQ424.1
作者简介:孔祥千(1994-),女,山东曲阜人,师承刘守新教授,从事生物质炭材料研究。
基金项目:中央高校基本科研业务费专项资金资助项目(2572014EB01);国家自然科学基金资助项目(31170545);在校本科生国家创新实验资助项目(201410225012)
文章编号:1001-9731(2016)01-01203-04
收到初稿日期:2015-01-19 收到修改稿日期:2015-10-10 通讯作者:刘守新,E-mail: liushouxin@126.com
