十六烷基三甲基溴化铵修饰P型沸石吸附水中直链烷基苯磺酸钠的研究
2016-04-08谭文渊
谭文渊, 徐 曼, 曾 英
(1. 成都理工大学材料与化学化工学院, 成都 610059;
2. 四川理工学院分析测试中心, 自贡 643000)
十六烷基三甲基溴化铵修饰P型沸石吸附水中直链烷基苯磺酸钠的研究
谭文渊1,2, 徐曼2, 曾英1
(1. 成都理工大学材料与化学化工学院, 成都 610059;
2. 四川理工学院分析测试中心, 自贡 643000)
摘要通过使用碱液对天然斜发沸石(Z)进行处理制得P型沸石(PZ), 再用十六烷基三甲基溴化铵(CTMAB)对Z和PZ进行修饰, 制得有机改性沸石ZC和PZC, 对比考察了ZC和PZC对直链烷基苯磺酸钠(LAS)的吸附性能. 实验结果表明, 制得的PZ硅/铝比为2, 比Z(4.85)降低58.8%; PZ的零净电荷点、比表面积、孔径和孔容均高于Z; 吸附平衡时间为4 h. 当pH=2时, ZC和PZC对LAS吸附量达到最高, 吸附数据符合Langmuir准二级动力学方程和Langmuir等温吸附方程, 饱和吸附量(qm)分别为12.658和27.100 mg/g, 吸附过程主要为单分子层的化学吸附, PZC的吸附速率常数大于ZC, 具有更好的动力学性能.
关键词P型沸石; 十六烷基三甲基溴化铵; 直链烷基苯磺酸钠; 吸附
直链烷基苯磺酸钠(LAS)是一种重要的阴离子表面活性剂, 每年我国消耗的LAS总量超过100万吨. 大量的LAS进入水体会在环境和生物体内累积并对动植物产生毒害作用[1~3]. LAS已成为我国地表水体标志性有机污染物之一, 许多环境工作者一直致力于LAS废水的处理研究[4~13]. 宋扬等[14]在优化的实验条件下采用Fenton氧化-好氧接触工艺将含高浓度硫酸盐的LAS废水中的LAS浓度由490 mg/L降至23 mg/L. 废水中LAS的处理方法较多, 采用吸附法处理LAS废水具有操作简单的特点[15], 但需要进一步开发高效、环境友好、价廉易得的吸附剂[16,17].
我国天然沸石种类多, 资源丰富, 价格低廉, 具有多种特殊理化性能, 在水处理及催化领域已有广泛应用[18~23]. 但天然沸石孔道容易被细碎颗粒堵塞, 造成孔道相互连通的程度较差; 且沸石表面铝氧结构带负电荷且具有极强的亲水性, 导致天然沸石吸附有机物及阴离子污染物的性能极差. 因此, 为了满足沸石对污染物的处理要求, 常常需要对其进行改性处理, 处理方法主要是内部改性[24~26]和外部改性[27,28]. 内部改性是为了改变沸石的内部结构、孔径, 使污染物进入沸石孔道内部从而得以去除, 主要用于小分子污染物的去除; 外部改性是对沸石外表面的改性, 通过离子置换以增大污染物质在不同相的分配系数来使沸石具有去除污染物的能力, 通常是用于有机污染物尤其是大分子有机污染物的去除[29].
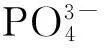
本文对天然斜发沸石进行内部和外部两步改性处理: 先用碱液对沸石进行处理, 制得P型沸石, 降低硅铝比, 增加离子交换能力; 再用CTMAB对P型沸石进行表面有机改性, 在沸石表面形成疏水层; 然后研究两步改性后的沸石对溶液中LAS的吸附性能, 探讨了降低硅铝比对沸石吸附LAS性能的影响.
1实验部分
1.1试剂与仪器
直链烷基苯磺酸钠(天津博迪化工股份有限公司); 十六烷基三甲基溴化铵(成都市科龙化工试剂厂); 浓盐酸(HCl, 质量分数36.46%, 郑州鑫诚化工有限公司); 氢氧化钠(NaOH, 成都市恒亿化工产品有限公司); 浓硝酸(HNO3, 质量分数65%—68%, 成都市科龙化工试剂厂). 以上试剂均为分析纯. 天然斜发沸石(2~4 mm, 北票鑫鑫沸石厂).
美国PE公司LAMDA35型紫外-可见双光束全波段扫描分光光度计; 捷克TESCAN公司VEGA3Easyrobe型扫描电子显微镜及布鲁克X射线电子能谱仪(SEM-EDS); 德国布鲁克AXE公司D2 PHASER型X射线衍射(XRD), CuKα射线源, 管电压30 kV, 管电流10 mA, 扫描角度(2θ)为7°~35°, 步长0.02°, 每步扫描时间0.2 s; 北京彼奥德电子有限责任公司SSA-4300型孔径及比表面测定仪; 美国PE公司Frontier Near/Mid-IR Std型傅里叶变换红外光谱仪(FTIR), 将沸石与溴化钾(质量比为1∶10)混合研磨后压片; 德国Elementar公司Vario EL cube型元素分析仪; 奥豪斯(上海)公司STARTER 2100型酸度计.
1.2有机改性沸石的制备
1.2.1天然沸石的预处理 将天然斜发沸石(Z)用粉碎机粉碎后筛选出60~80目的样品, 用去离子水多次洗涤后在电热鼓风干燥箱(105 ℃)中干燥2 h, 放入干燥器中备用.
1.2.2P型沸石的制备参照文献[32]方法, 将30 g预处理后的沸石放入250 mL圆底烧瓶中, 向烧瓶中加入100 mL 5 mol/L的氢氧化钠溶液, 在(95±5) ℃回流加热70 h, 加少量酸中和后, 用去离子水洗至中性, 于电热鼓风干燥箱(105 ℃)中干燥2 h, 放入干燥器中备用. 所得样品记为PZ.
1.2.3CTMAB改性沸石的制备参照文献[33]方法, 将经过预处理的天然沸石和水热反应后的P型沸石各10 g加入到2个锥形瓶中, 再依次加入150 mL CTMAB(1 g/L)溶液, 混合后放入电热恒温振荡槽振荡24 h, 控制温度为30 ℃, 转速为120 r/min. 用去离子水清洗CTMAB修饰后的沸石2~3次, 放入电热鼓风干燥箱干燥, 即制得样品ZC和PZC.
1.3沸石零净电荷点(PZNC)的测试
沸石的PZNC通过质量滴定(Mass titration)法测定[34,35]: 取25 mL浓度为0.001 mol/L的NaNO3溶液于6个25 mL比色管中, 用HNO3或NaOH溶液调节初始pH值分别为2, 4, 6, 8, 10, 12后, 分别加入一定量的沸石, 使沸石固体浓度(cs)为5 g/L, 在恒温(25±0.2) ℃下振荡24 h, 测定悬浮液的平衡pH值. 再改变沸石固体浓度分别为10, 50, 100, 150和200 g/L, 重复上述操作, 将平衡pH值对cs作图得到质量滴定曲线, 即可得到沸石的PZNC值.
1.4pH值对吸附量的影响
采用HCl和NaOH调节体系pH值, 配制浓度为30 mg/L、pH值分别为2, 4, 6, 8, 10, 12的LAS溶液, 分别取每种pH值溶液各200 mL, 加入0.2 g有机改性后的沸石ZC和PZC, 放入电热恒温振荡水槽中, 调节温度为20 ℃, 转速为120 r/min, 4 h后采用紫外-可见分光光度法测定溶液中LAS的浓度, 得到pH值对吸附量的影响曲线. 按下式计算沸石对LAS的吸附量qt(mg/g).
(1)
式中: c0(mg/L)为LAS的初始浓度; ct(mg/L)为吸附LAS后t时刻的浓度; V(L)为加入LAS溶液的体积; m(g)为沸石质量.
1.5温度对吸附量的影响
称取ZC和PZC各0.2g依次加入到200mL30mg/LLAS(最佳吸附的pH值下)溶液中, 将溶液放入电热恒温振荡槽内, 分别设置温度为20, 30, 40和50 ℃, 转速为120r/min, 吸附4h后采用紫外-可见分光光度法测定溶液中LAS浓度. 按式(1)计算沸石对LAS的吸附量.
1.6时间对吸附量的影响
称取ZC和PZC各0.2g依次加入到200mL30mg/LLAS(最佳吸附的pH值下)的溶液中, 将溶液放入电热恒温振荡槽内, 设置最佳吸附温度, 转速为120r/min, 吸附不同时间后采用紫外-可见分光光度法测定溶液中LAS浓度. 按式(1)计算沸石对LAS的吸附量.
1.7吸附动力学参数的确定
根据1.6节中所得实验数据, 用Langmuir准一级动力学模型和准二级动力学模型进行拟合并求得吸附速率常数:
(2)
(3)
式中: qe(mg/g)为平衡吸附量; k1(min-1)为准一级反应吸附平衡速率常数; k2[g/(mg·min-1)]为准二级反应吸附平衡速率常数.
1.8吸附等温线的确定
配制一系列浓度为10, 20, 30, 40, 50, 60, 70, 80, 90和100mg/L的LAS溶液(最佳吸附的pH值下)各200mL, 分别向每组加入ZC和PZC各0.2g, 将混合后的溶液放入到电热恒温振荡水槽中, 控制转速为120r/min, 调节温度为最佳吸附温度, 振荡至平衡后, 采用紫外-可见分光光度法测定溶液中LAS浓度. 用Langmuir和Freundlich吸附等温式对吸附结果进行处理得到吸附等温线.Langmuir和Freundlich吸附等温式如下:
(4)
(5)
式中:Ce(mg/L)为吸附平衡时LAS的质量浓度;qm(mg/g)为饱和吸附容量;KL(L/mg)表示LAS与吸附剂之间作用力的大小;KF和n为待定系数.
2结果与讨论
2.1沸石的表征
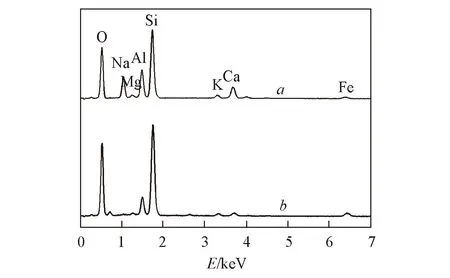
Fig.1 EDS of PZ(a) and Z(b)
对原沸石和在1.2节中制得的P型沸石进行EDS分析(图1), 结果表明, 原沸石中硅与铝的摩尔分数分别为19.70%和4.06%, P型沸石中硅与铝的摩尔分数分别为13.72%和6.84%. 可以看出, 经过碱液处理后, 沸石中的部分硅溶解, 使得硅铝比变为2, 相对于原沸石硅铝比(4.85)降低58.8%. 相关沸石的SEM形貌分析结果见图2. 由图2可见, 原沸石聚结成块, 且细碎颗粒较多; 而P型沸石表面分布着较规则的颗粒. Kazemian等[36]认为是在碱液处理过程中溶解了无定形凝胶杂质和小沸石晶体, 纯化大晶体所致; 经过CTMAB修饰后, 原沸石和P型沸石均可看见覆盖着一层灰色物质, 推测为CTMAB.

Fig.2 SEM images of Z(A), ZC(B), PZ(C) and PZC(D)
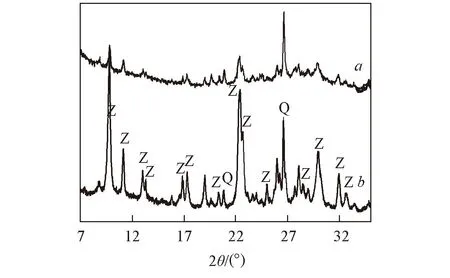
Fig.3 XRD patterns of PZ(a) and Z(b) Z: Zeolite; Q: Quartz.
沸石改性前后的XRD测试结果见图3. 对比沸石经碱液处理后的XRD谱与天然斜发沸石的标准衍射谱(JCPDS39-1383)发现, 经碱液处理后的沸石仍在2θ=9.88°, 11.21°, 13.05°, 17.38°, 19.09°, 22.36°, 22.52°和26.04°处出现了特征衍射峰, 说明沸石的骨架结构并未发生改变. 同时在该沸石样品中可发现有少量共生石英矿物.
沸石的质量滴定曲线见图4. 可以看出, P型沸石的PZNC值比原沸石增大, 可以推测沸石经过碱液处理后硅铝比降低, 铝氧四面体在沸石晶体中所占比例增加, 沸石的结构负电荷增多. 沸石改性前后的比表面积和孔径测试结果见表1. 沸石在内部改性后比表面积、总孔容积和孔径增加; 在进行外表面改性后, 比较面积和总孔容积减小. 这是由于沸石经碱液处理后, 溶解了部分硅和其中的无定形凝胶杂质, 沸石变得疏松; 而在表面改性后CTMAB附着在沸石表面堵塞了一些孔道所致.
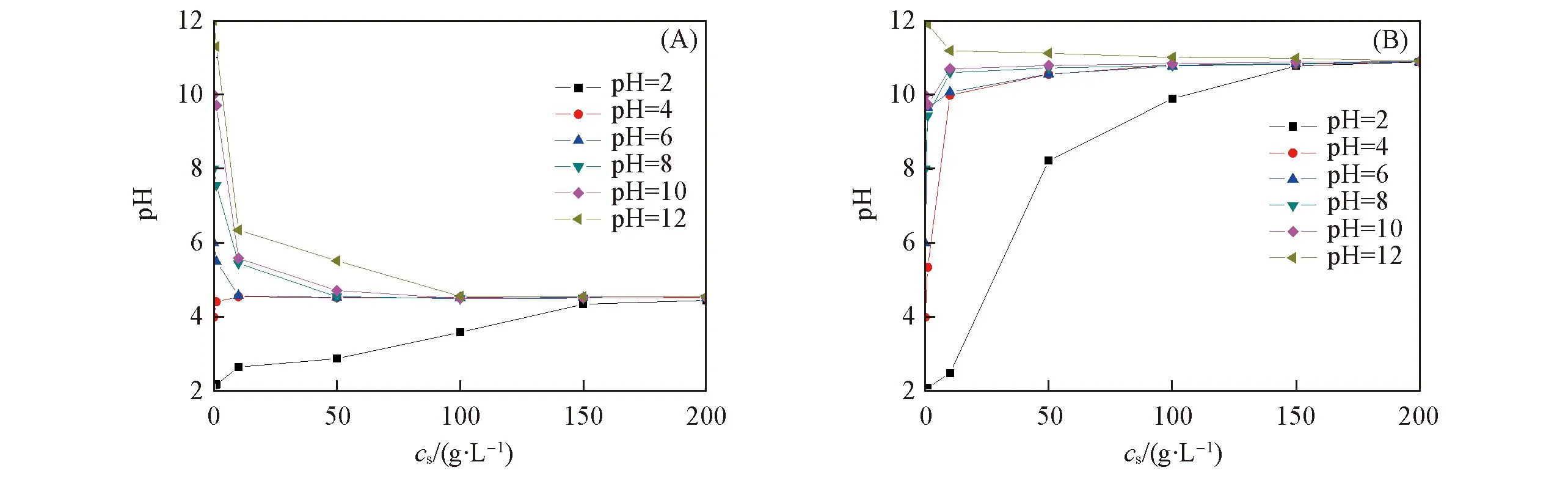
Fig.4 Mass titration curves of Z(A) and PZ(B)

ZeoliteSBET/(m2·g-1)Totalporevolumeofadsorption(BJH)/(cm3·g-1)Mostprobableporesize(BJH)/nmZ12.7940.07041.86ZC9.1810.07001.94PZ42.0530.21473.78PZC30.1350.18271.92

Fig.5 IR spectra of CTMAB(a), ZC(b), PZC(c) and Z(d)
沸石的IR测试结果见图5. 对比有机改性前后样品的红外吸收峰位置可以看出, 有机改性沸石具有与天然沸石相似的骨架, 但在2920及2850 cm-1处出现了CTMAB的—CH2和—CH3对称和反对称伸缩振动强吸收峰, 而天然沸石在相同位置无明显峰出现, 说明沸石经改性处理后表面已经负载了CTMAB.
ZC和PZC沸石表面的C, H, N元素主要来源于CTMAB, 因此测定沸石表面C, H, N元素的含量能够得出沸石表面CTMAB的含量. 表2列出了ZC和PZC两种沸石表面C, H, N的含量及对应CTMAB的含量. PZC表面CTMAB的含量为24.73 mg/g, 是ZC的2倍. 这主要是由于PZ的硅铝比低于Z, 离子交换容量更大[37,38], CTMAB中的R4-N+离子更易与PZ发生离子交换作用.

Table 2 Results of C, H, N measurement and CTMAB loading
2.2pH值、温度和时间对吸附量的影响
图6示出了pH值对吸附效果的影响. 由图6可以看出, 改性沸石的吸附效果随pH值的增高逐渐降低, 低pH值有利于沸石对LAS的吸附. pH=2时, 吸附效果最好, 故选择在pH=2下, 测定不同温度改性沸石吸附LAS的影响. 不同温度下, 改性沸石对LAS吸附影响见图7. 由图7可以看出, 随着温度的升高, 吸附量逐渐减小, 这可能是随着温度升高, 分子运动加剧, 使得LAS难以被吸附; 在pH=2, 温度为20 ℃下, 测定不同时间改性沸石对LAS的吸附情况, 结果见图8. 可以看出在吸附4 h吸附量后趋于平衡.
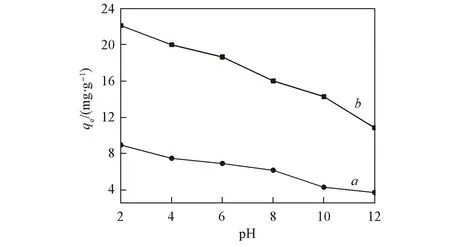
Fig.6 Effect of pH on LAS adsorption onto ZC(a) and PZC(b)
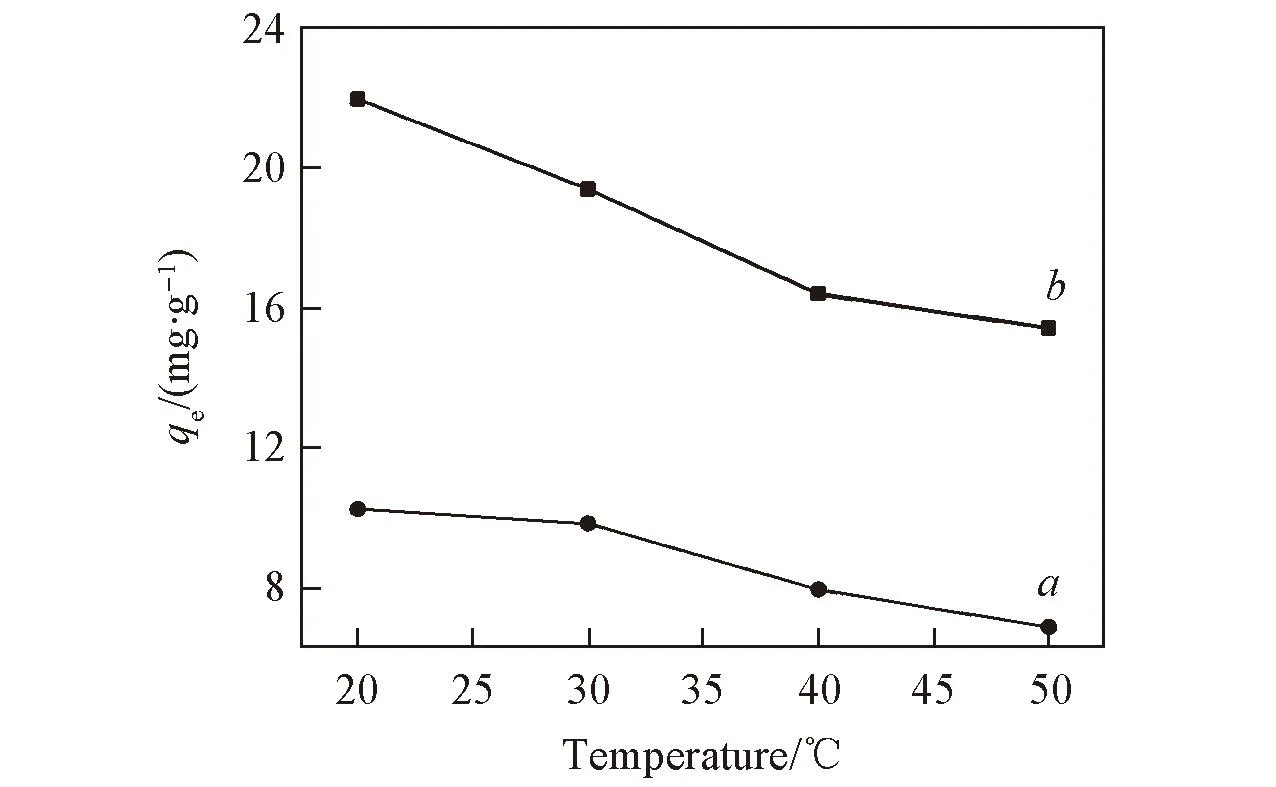
Fig.7 Effect of temperature on LAS adsorption onto ZC(a) and PZC(b)
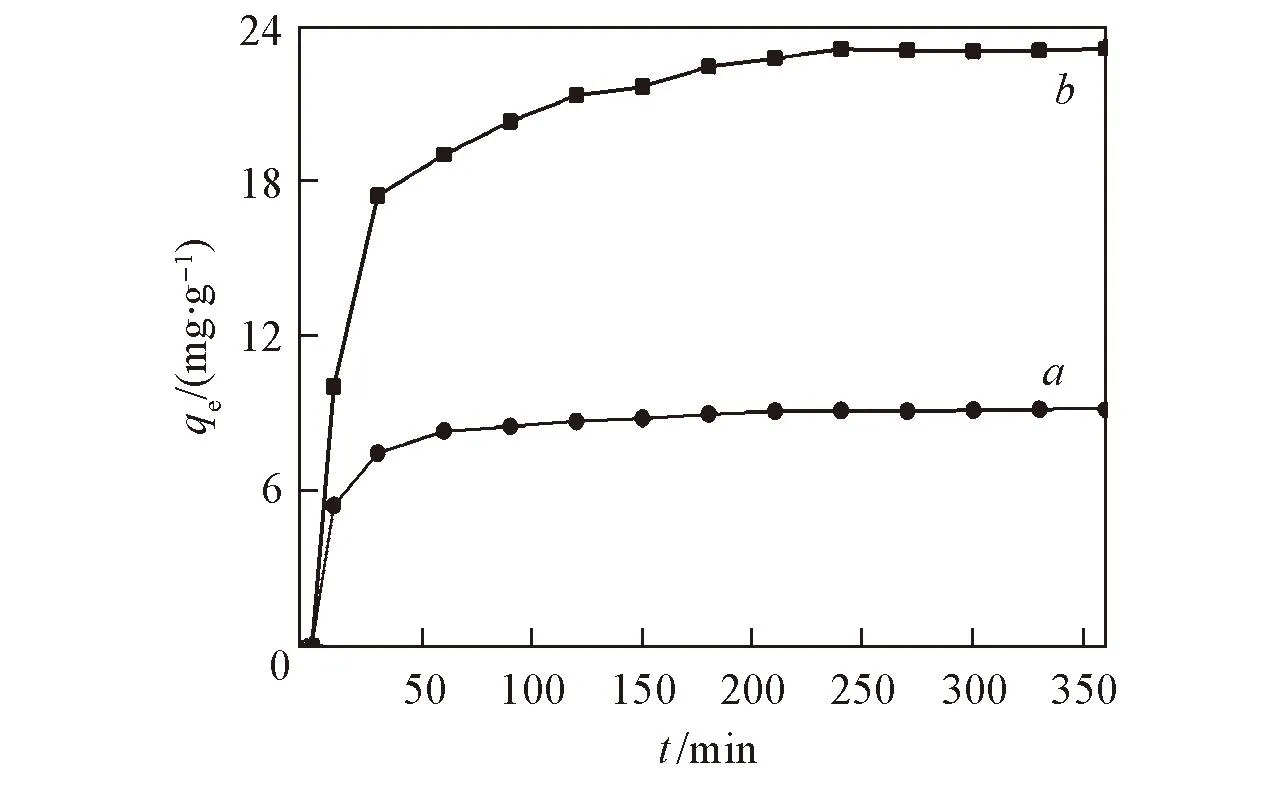
Fig.8 Effect of time on LAS adsorption onto ZC(a) and PZC(b)
2.3吸附动力学参数的确定
将CTMAB修饰改性后沸石吸附LAS的数据分别代入式(2)和式(3)进行拟合, 得到Langmuir准一级和准二级曲线(图9), 速率常数及相关系数见表3. 可以看出, 准二级动力学模型的相关系数(R2)均为0.999, 描述拟合精度的吸附误差Δq均≤0.037, 说明有机改性沸石对LAS的吸附过程更符合Langmuir准二级动力学模型, 以化学吸附为主.
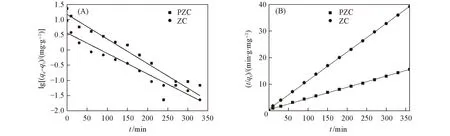
Fig.9 Kinetic model fitting of Langmuir pseudo-first order(A) and pseudo-second order(B)
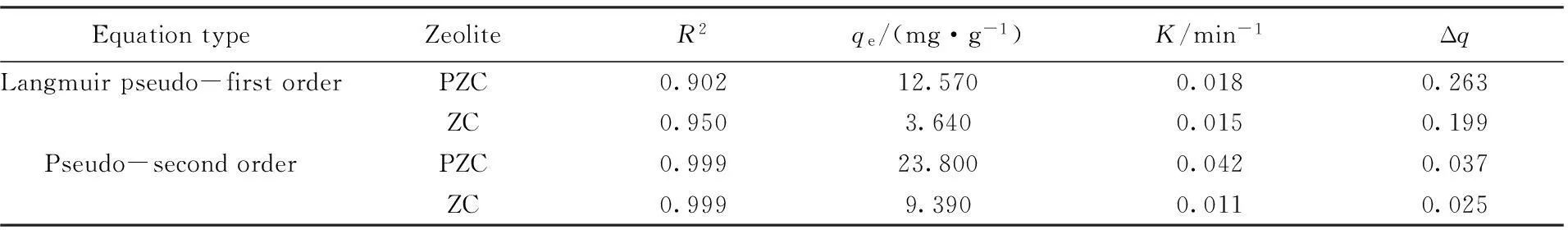
EquationtypeZeoliteR2qe/(mg·g-1)K/min-1ΔqLangmuirpseudo-firstorderPZC0.90212.5700.0180.263ZC0.9503.6400.0150.199Pseudo-secondorderPZC0.99923.8000.0420.037ZC0.9999.3900.0110.025
2.4吸附等温线的确定
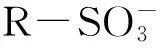
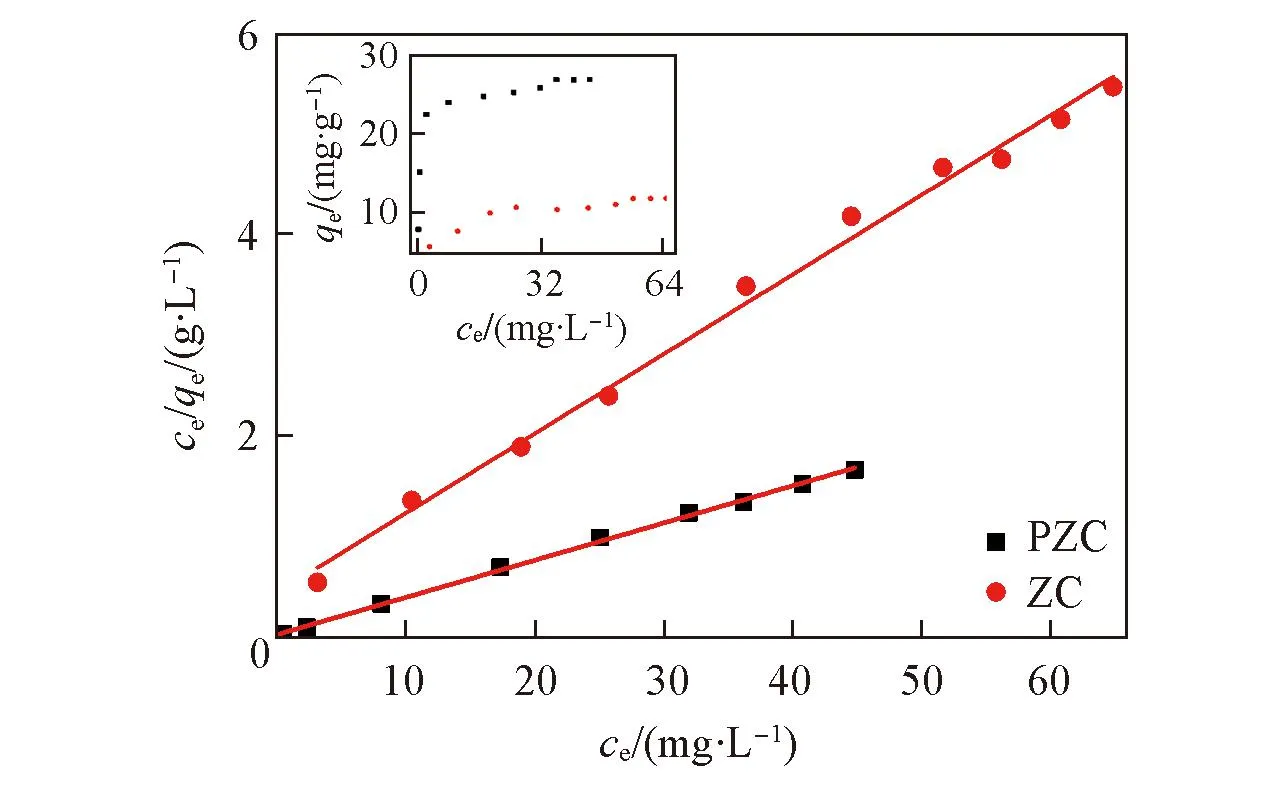
Fig.10 LAS adsorption isotherms of Langmuir equation The inset shows the varies of the adsorption capacity with the concentration at equilibrium.
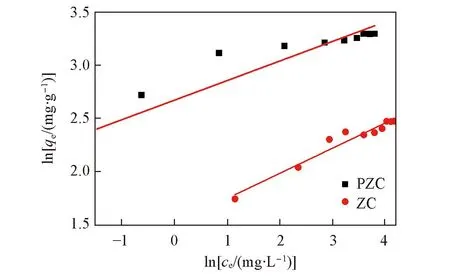
Fig.11 Adsorption isotherms of Freundlich equation

ZeoliteLangmuirequationFreundlichequationqmKLR2KFnrPZC27.1001.1570.98914.4405.4640.950ZC12.6580.1770.9944.5474.2540.818
3结论
以天然斜发沸石为基体, 通过5 mol/L NaOH碱液处理得到P型沸石, 在CTMAB修饰后对其进行了表征, 并研究其对LAS的吸附性能. 实验结果表明, 制得的P型沸石硅铝比为2, 比原沸石(4.85)降低58.8%; P型沸石的零净电荷点、比表面积、孔径和孔容均高于原沸石; 吸附平衡时间为4 h, pH=2时, 达到最佳吸附量; P型沸石和原沸石对LAS吸附均符合Langmuir准二级动力学方程和Langmuir等温吸附方程, 饱和吸附量qm分别为27.100和12.658 mg/g, 说明吸附过程主要为单分子层的化学吸附; P型沸石具有更好的动力学性能, 其吸附速率常数大于原沸石. 该类改性沸石在处理LAS废水中将具有重要的应用前景.
参考文献
[1]Hodges G., Roberts D. W., Marshall S. J., Dearden J. C.,Chemosphere, 2006, 63(9), 1443—1450
[2]Hampel M., Moreno-Garrido I., González-Mazo E., Blasco J.,Ecotoxicol.Environ.Saf., 2009, 72(4), 1303—1308
[3]Rico-Rico A., Temara A., Hermens J. L.,Environ.Pollut., 2009, 157(2), 575—581
[4]Oliver-Rodríguez B., Zafra-Gómez A., Reis M. S., Duarte B. P. M.,Chemosphere, 2015, 131, 1—8
[5]Gong J. S., Wang Y., Zhang D. D., Li H., Zhang X. M., Zhang R. X.,Chem.Res.ChineseUniversities, 2015, 31(1), 91—97
[6]Shah A. A., Nawaz A., Kanwal L.,Int.Biodeterior.Biodegrad., 2015, 98, 35—42
[7]Anachkov S. E., Tcholakova S., Dimitrova D. T., Denkov N. D.,ColloidsSurf.,A:Physicochem.Eng.Asp., 2015, 466, 18—27
[8]García-Luque E., González-Maz E., Forja J. M.,Gómez-ParraA.,CoastalandShelfScience, 2009, 81(3), 353—358
[9]Terechova E. L., Zhang G. Q., Chen J., Sosnina N. A., Yang F. L.,J.Environ.Chem.Eng., 2014, 2(4), 2111—2119
[10]Delforno T. P., Moura A. G. L., Okada D. Y., Sakamoto I. K., Varesche M. B. A.,Bioresour.Technol., 2015, 192, 37—45
[11]Hernández-Soriano M. C., Mingorance M. D., Pea A.,J.Environ.Monit., 2012, 95, S223—S227
[12]García M. T., Campos E., Ribosa I., Latorre A., Sánchez-Leal J.,Chemosphere, 2005, 60(11), 1636—1643
[13]Dehghani M. H., Najafpoor A. A., Azam K.,Desalination, 2010, 250, 82—86
[14]Song Y., Wang X. J., Mai J. S.,ChinaSurfactantDetergent&Cosmeitcs, 2008, 38(1), 12—15(宋扬, 汪晓军, 麦均生. 日用化学工业, 2008, 38(1), 12—15)
[15]Bi Y. J.,PreparationofZn/AlHydrotaicite-likedCompoundandtheResearchonCapabilityofAdsorptionRemovalofAnionicSurfactantsfromAqueousSolution, Shandong University, Jinan, 2007(毕研俊. Zn/Al类水滑石制备及其吸附去除水中阴离子表面活性剂性能研究, 济南: 山东大学, 2007)
[16]Garcia M. T., Compos E., Dalmau M.,Chempsphere, 2002, 49(3), 279—286
[17]Wang L., Zhang C., Zhong M. J., Qian P.,Chem.J.ChineseUniversities, 2015, 36(7), 1358—1366(汪靓, 张超, 钟明静, 钱萍. 高等学校化学学报, 2015, 36(7), 1358—1366)
[18]Hosseinpou M., Charkhi A., Ahmadi S. J.,JournalofSupercriticalFluids, 2015, 102, 40—49
[19]Hou T. Y., Jiang Y. S., Li F. F., Sun S. M.,Chem.J.ChineseUniversities, 2006, 27(1), 100—103(侯天意, 蒋引珊, 李芳菲, 孙申美. 高等学校化学学报, 2006, 27(1), 100—103)
[20]Zhang L. L., Liu S. Y., Li Z. J., Yao J., Wang G. Y.,Chem.J.ChineseUniversities, 2014, 35(4), 812—817(张丽雷, 刘绍英, 李子健, 姚洁, 王公应. 高等学校化学学报, 2014, 35(4), 812—817)
[21]Courtney T. D., Chang C. C., Gorte R. J., Lobo Raul F., Wei F.,MicroporousMesoporousMater., 2015, 210, 69—76
[22]Liao Z. L., Chen H., Zhu B. R., Li H. Z.,Chemosphere, 2015, 134, 127—132
[23]Benaliouche F., Hidous N., Guerza M., Zouad Y., Boucheffa Y.,MicroporousMesoporousMater., 2015, 209, 184—188
[24]Camino G. A., Aida G. A., Elena S., Antonio A. R., Javier G. M., Rafael L.,J.Mol.Catal.A:Chem., 2015, 406, 40—45
[25]Nikolay K., Clement A., Gerard J. B., Venkata G. P., Sripathi, Emiel J . M.,J.Membr.Sci., 2015, 484, 140—145
[26]Thiago F. C., Heloise O. P., Peter H., Dilson C.,MicroporousMesoporousMater., 2015, 202, 198—207
[27]Arezou N., Alireza N. E.,J.Ind.Eng.Chem., 2015, 2567, 1—7
[28]Maedeh B., Alireza N. E.,ColloidsSurf.,A:PhysicochemicalandEngineeringAspects, 2015, 479, 35—45
[29]Li X. H., Zhu K.,WaterPurificationTechnology, 2008, 27(3), 5—8, 24(李效红, 朱琨. 净水技术, 2008, 27(3), 5—8, 24)
[30]Anaraki A. M., Ejhieh A. N.,J.ColloidInterfaceSci., 2015, 440, 272—281
[31]Xiao J. Q., Wei Z. Y.,SP&BMHRelatedEngineering, 2007, 5, 19—22(肖举强, 魏朝燕. 硫磷设计与粉体工程, 2007, 5, 19—22)
[32]Zhang Z. H., Dou T., Zhang Z. Y.,IndustrialCatalysis, 2004, 12(10), 49—53(张志华, 窦涛, 张瑛. 工业催化, 2004, 12(10), 49—53)
[33]Silvio R. T., Rubio J.,Miner.Eng., 2010, 23, 771—779
[34]Xu J., Hou W. G., Zhou W. Z., Tai P. D.,ActaChim.Sinica, 2007, 65(13), 1191—1196(徐洁, 侯万国, 周维芝, 台培东. 化学学报, 2007, 65(13), 1191—1196)
[35]Li L. F., Hou W. G., Dai X. N., Liu C. X.,ActaChim.Sinica, 2004, 62(4), 429—432(李丽芳, 侯万国, 戴肖南, 刘春霞. 化学学报, 2004, 62(4), 429—432)
[36]Kazemian H., Modanls H.,J.Radioanal.Nucl.Chem., 2003, 258, 551—560
[37]Xie J., Wang Z., Wu D. Y.,EnvironmentalScience, 2012, 33(12), 4361—4367(谢杰, 王哲, 吴德意. 环境科学, 2012, 33(12), 4361—4367)
[38]Wan D. J., Yuan H. J., Qu D.,ChineseJournalofEnvironmentalEngineering, 2011, 5(12), 2681—2685(万东锦, 袁海静, 曲丹. 环境工程学报, 2011, 5(12), 2681—2685)
Study on the Adsorption Ability to Linear Alkylbenzene Sulfonate of
Zeolite P Modified by Cetrimonium Bromide in Waste Water†
TAN Wenyuan1,2*, XU Man2, ZENG Ying1
(1.CollegeofMaterialsandChemistry&ChemicalEngineering,ChengduUniversityof
Technology,Chengdu610059,China;
2.AnalysisandTestingCenter,SichuanUniversityofScience&Engineering,Zigong643000,China)
AbstractZeolite P(PZ) was prepared by the natural clinoptilolite(Z) that was treated with lye, and then Z and PZ were modified by cationic surfactant cetrimonium bromide(CTMAB) to prepare ZC and PZC. The adsorption abilities of ZC and PZC to linear alkylbenzene sulfonate(LAS) were studied. The results indicated that the Si/Al ratio of PZ was 2, 58.8% lower than that of Z(4.85); the point of zero net charge(PZNC), specific surface area, pore radius and pore volume of PZ were higher than those of Z; the adsorption equilibrium was reached after 4 h. ZC and PZC had a maximum adsorption capacity for LAS at pH=2. The adsorption process was well fitted with pseudo-second order kinetic equation and Langmuir isothermal adsorption model. The amount of saturated adsorption of ZC and PZC are 12.658 and 27.100 mg/g, respectivey, showing that the adsorption process is described primarily for the monolayer and chemical adsorption, the adsorption of LAS on PZC is better than that on ZC in view of point of capacities and velocities.
KeywordsZeolite P; Cetrimonium bromide(CTMAB); Linear alkylbenzene sulfonate(LAS); Adsorption
(Ed.: F, K, M)
† Supported by the Mineral Resources Chemistry Key Laboratory Foundation of Sichuan Higher Education Institutions, China(No.KCZ201111).
doi:10.7503/cjcu20150579
基金项目:矿产资源化学四川省高校重点实验室项目(批准号: KCZ201111)资助.
收稿日期:2015-08-20. 网络出版日期: 2015-12-20.
中图分类号O647.32
文献标志码A
联系人简介: 谭文渊, 男, 高级实验师, 主要从事污水处理及仪器分析研究. E-mail: tanwenyuan@suse.edu.cn
