聚乙二醇干扰素α-2a联合阿德福韦治疗HBeAg阳性慢性乙型肝炎疗效系统评价
2015-08-12肖作汉王立志
肖作汉,孟 冈,王立志
聚乙二醇干扰素α-2a联合阿德福韦治疗HBeAg阳性慢性乙型肝炎疗效系统评价
肖作汉,孟冈,王立志
【摘要】目的探讨聚乙二醇干扰素α-2a(Peg-IFNα-2a)联合阿德福韦(ADV)治疗HBeAg阳性慢性乙型肝炎(CHB)患者的临床疗效。方法通过检索2004年1月~2014年1月期间Pubmed、万方数据库(CECDB)、中文科技期刊数据库(VIP)、中国学术期刊全文数据库(CNKI)等有关Peg-IFNα-2a联合阿德福韦治疗HBeAg的CHB患者的随机对照试验(RCT),对纳入文献的质量进行严格评价和资料提取,应用Stata/SE version 12.0软件对纳入研究进行系统评价。结果最终纳入7篇RCT,共529例患者,其中实验组261例(接受Peg-IFNα-2a联合ADV治疗),对照组268例(接受Peg-IFNα-2a治疗)。系统评价结果显示,相比单药治疗,经联合治疗48w时CHB患者HBVDNA阴转率显著提高[OR=1.20,95%CI=(1.01,1.43)];48w时CHB患者HBeAg血清转换率显著提高[OR=1.24,95%CI=(1.02,1.52)],但联合治疗对ALT复常率的影响,系统评价显示结果存在显著偏倚[bias_P=0.012、bias_95 CI=(1.442998,6.467852)],不具有推广性。结论Peg-IFNα-2a联合ADV治疗HBeAg阳性CHB患者能显著提高患者HBV DNA阴转率及HBeAg血清转换率。
【关键词】慢性乙型肝炎;聚乙二醇干扰素α-2a;阿德福韦酯;系统评价
据世界卫生组织(WHO)报道,每年近100万人死于HBV感染所致的肝衰竭、肝硬化和肝细胞癌[1]。全世界约有3.5亿人因感染HBV而罹患CHB,其中三分之一在我国[2,3]。由于治疗CHB具有复杂性和长期性,对患者、家属及社会都形成显著的心理和经济压力。HBV感染及持续复制所致免疫功能紊乱是CHB病情进展的主要原因[4],其中HBeAg阳性的CHB患者处于病毒复制的活跃阶段,不仅具有较强的传染性,更是病情恶化的关键时期[5]。据报道[6],该类患者每年约有3.5%进展至乙型肝炎肝硬化,而HBeAg阴性的CHB患者比例不足1%。因此,对于HBeAg阳性CHB患者的治疗目标为持续抑制并有效清除HBV,缓解肝脏炎性损伤,预防肝纤维化、肝功能失代偿和肝细胞癌的发生,从而提升患者的生命质量,改善预后[7]。治疗HBeAg阳性CHB患者主要有干扰素(Interferon-α,IFN-α)和核苷类似物(Nucleoside analogues,NUC)两大类药物[8],以聚乙二醇干扰素α(Peg-IFN-α)为常用[9]。应用阿德福韦(adefovir,ADV) 易产生病毒变异[9]。Wursthorn et al研究证实[10],将Peg-IFN与ADV联合治疗CHB患者48 w,可显著减少肝内病毒共价闭合环状DNA(cccDNA)和血清HBsAg水平。联合用药尚需要更大规模、多中心的随机对照试验以证实其疗效及安全性。本研究参照Cochrane评价体系[11,12],对Peg-IFNα-2a联合ADV治疗HBeAg阳性的CHB患者的临床试验进行了系统评价,以期为本病的进一步治疗提供临床决策依据。
1 资料与方法
1.1文献检索检索以下数据库①外文数据库:英国医学会电子全文期刊数据库(BMA)、荷兰医学文摘数据库(EMbase)、学术期刊集成全文数据库(ASP)、考克兰图书馆(The Cochrane Library)、西文生物医学期刊文献数据库(EMCC)、美国国立医学图书馆生物医学信息检索系统(Pubmed);②中文数据库:万方数据库(CECDB)、维普中文科技期刊全文数据库(CQVIP)、中文科技期刊数据库(VIP)、中国生物医学文献数据库(CBM)、中国学术期刊全文数据库(CNKI)。检索时间为2004年1月至2014年1月。检索关键词:①英文为“HBeAg positive”,“Chronic hepatitis B&CHB”,“Peg-IFNα-2a”,“Adefovir”;②中文为“HBeAg阳性”、“慢性乙型肝炎”、“聚乙二醇干扰素α-2a”、“阿德福韦”。所有关键词以“And”或“和”连接,检索对象设定为“Adult”或“成人”,检索流程见表1。
1.2纳入标准①治疗HBeAg阳性CHB患者的论著;②诊断符合欧洲肝病学会(EASL)于2009年发布的《慢性乙型肝炎临床诊断治疗指南》[13]或中华医学会于2010年发布的《慢性乙型肝炎防治指南》[14,15];③对照组予以Peg-IFNα-2a行常规治疗,试验组在对照组基础上联用ADV治疗。

表1 文献检索步骤(以Pubmed为例)
1.3排除标准①排除“短篇或病例报道”、“综述”、“专家述评”、“临床观察”、“会议纪要”等文章;②排除总体样本量偏少(n≤20)的论文;③排除包含以下患者为研究对象的论文:药物性肝损害、自身免疫性肝病、酒精性肝病、遗传代谢性肝病、严重血液系统疾病、严重肾功能不全、妊娠;④排除合并感染甲、丙、丁、戊型肝炎病毒或人类免疫缺陷病毒(HIV);⑤排除刻意藏匿原始数据,以至不能明确不同治疗方案造成不同结局的论文;⑥排除使用Peg-IFNα-2a单药治疗一段时间后再联用ADV的论文;⑦排除治疗终点≤24 w的论文;⑧排除使用非中英文撰写的论文;⑨排除重复性报道的论文。
1.4质量评价文献质量的高低与纳入研究的偏倚风险,即高估或低估真实效应值的风险密切相关[16]。本文对纳入文献的质量评价依照Cochrane Hand book for Systematic Reviews 5.0.2[17]中推荐的偏倚风险方法(Risk of bias)进行。应用Review manager version 5.0软件,在以下7项中从选择偏倚、实施偏倚、测量偏倚、失访偏倚、报告偏倚5方面总体评价纳入研究的文献质量:①是否交代随机分配序列的产生(random sequence generation);②是否隐蔽分组(allocation concealment);③是否对患者及医生施行盲法(blinding of participants and personel);④是否对结果评价施行盲法 (blindingofoutcome assessment);⑤是否数据完整(without incomplete outcome data);⑥是否存在选择性报告结果(without selective reporting);⑦是否存在其他偏倚(without other bias)。参考CONSORT声明[18],风险偏倚的评价结果以“Yes”表示低度偏倚、“No”表示高度偏倚、“Unclear”表示偏倚情况不确定。对低度偏倚记1分,高度偏倚或偏倚不确定记0分。根据Jadad质量计分法[19]对文献质量进行分级,累计总分0~2分的文献评为C级,3~4分评为B级,≥5分评为A级。
1.5资料提取应用Excel 2010设计专用表格提取随机对照试验 (randomizedcontrolledtrial,RCT),采用双录入法以尽可能规避提取过程中人为操作失误[20]。提取资料包括:①文题、第一作者、发表年份;②样本量及基线情况;③试验组、对照组应用的药物剂量及用法;④随访情况及失访处理;⑤结局变量及相关指标;⑥各种连续性资料的均数、标准差及二分类资料的百分比。
1.6统计学方法应用Stata/SE version 12.0软件进行统计学处理,以α=0.05为检验水准,以P<0.05为具有统计学意义。计量资料采用加权均数差((Weighted mean difference,WMD)、标准均数差(Standardized mean difference,SMD)、95%可信区间(95%CI)表示效应量结果;计数资料采用比值比(Odds ratio,OR)、相对危险度(Relative risk,RR)、95%CI表示效应量结果。统计分析流程符合Preferred Reporting Items for Systemic Reviews and Meta-Analysis(PRISMA)通用标准[21]。
首先直观评判纳入研究的异质性,以合并效应量(b)与其标准误(se_b)为纵轴、以标准误倒数(1/se_b)为横轴,制作Galbraith图[22]。回归线穿过原点代表固定效应模型的合并效应量,再于上下相邻的基本单位处向系统评价中固定效应模型的b斜率相等的95%CI处分别做平行线。当所有点均分布于图中两条平行线内部,说明各研究无异质性。再应用Cochran's Q检验具体计算纳入研究之间的异质性。该检验统计量服从自由度(df)=研究数目(k)-1为中心的卡方(x2)分布,但研究数目相对较少时检验效能偏低,研究数目过多时检验效能过度。为消除研究数目对检验效能的影响,对Q检验行进一步转换,依照公式I2=×100%计算I2及相应的P值[23]。当各研究间不存在显著异质性(P>0.10,I2<50%)时,采用Mantel-Haenszel固定效应模型进行系统评价;当各研究间异质性显著(P≤0.10,I2≥50%)时,则采用Dersimonian-Laird随机效应模型,行亚组分析,去除异质性后进行系统评价,并尽可能探寻异质性来源。当无法判断异质性或无法进行亚组分析时,则放弃本次系统评价。根据整合后的系统评价结果绘制森林图,以显示研究结论。
最后,采用绘制漏斗图、Begg&Egger法、计算失安全系数等三种方法,逐层递进以识别研究结论的发表偏倚(N):①以单项研究的效应量为横坐标、以样本量为纵坐标绘制漏斗图。通过漏斗图验证发表偏倚;②当纳入RCT数量较多时,采用Begg法,以直线相关检验图进一步评价漏斗图的发表偏倚。当纳入RCT数量相对较少时,则采用Egger法,以线性回归检验图进一步评价漏斗图的发表偏倚。当偏倚度对应的P值<0.05或95%CI不涵盖0时,则提示存在发表偏倚;③计算失安全系数,以精确测定发表偏倚的大小。将研究结论的随机效应模型与固定效应模型互换,依照其结果是否能逆转计算结果的稳定性[24]。失安全系数的计算公式为Nfs0.052=(移2-k,其中k表示需合并的研究数目,Z表示合并效应统计检验值。在研究计数资料时,Z=在研究计量资料时,Z=t。
2 结果
2.1纳入研究情况初步检索得到121篇相关临床研究,其中英文文献50篇,中文文献71篇。剔除非论著、质量差、描述性研究、未交待预后、非随机对照、对照组设置不合理的文献[25~31]114篇(94.2%),最终纳入文献7篇,其中中文文献6篇,英文文献1篇。各RCT的基本特征见表2,治疗组用药均为Peg-IFNα-2a180 μg/w联合ADV10 mg/d,对照组均为Peg-IFNα-2a180 μg/w,文献的筛选流程见图1。
2.2纳入研究的质量评价在纳入的7篇RCT中,所有研究均明确描述了随机分配序列的产生流程。2篇[26,28]未对患者施行盲法,2篇[29,31]未对结果实施盲法,1篇[28]数据不完整,2篇[27,31]存在选择性报告结果,5篇[25,27,29~31]存在其他偏倚(测定HBeAg所用化学发光免疫分析仪、测定转氨酶所用生化分析仪为制药公司赞助)。纳入RCT的质量分级:2篇[25,28]为A级、其余5篇[26,27,29~31]均为B级,即本研究所纳入文献的整体可信度尚可。
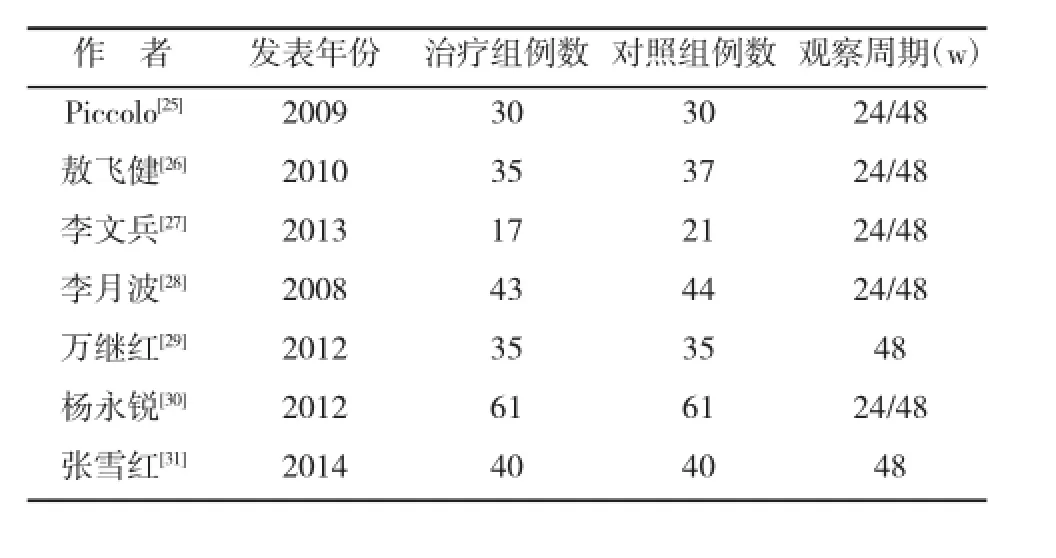
表2 纳入研究的基本特征
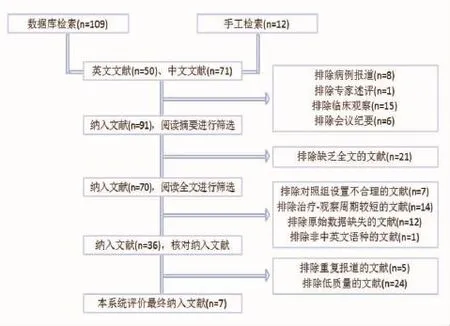
图1 本次系统评价文献筛选流程与结果
2.3Peg-IFNα-2a与ADV联合治疗HBeAg阳性CHB患者血清HBVDNA阴转情况如图2所示,Galbraith图表明部分点分布于两条回归线平行线之外,提示不同观测时限的结果存在异质性。Cochran's Q检验示P=0.685、I2=0.09%,说明各研究间异质性显著,采取随机效应模型进行系统评价。再结合Galbraith图中RCT分布情况,将治疗24w和48 w后患者血清HBV DNA阴转率分别进行亚组分析,以进一步消除异质性。森林图示:①治疗48w亚组Cochran's Q检验P=0.432、I2=0.23%,OR=1. 20,95%CI=(1.01,1.43);②治疗 24 w亚组的Cochran's Q检验P=0.279、I2=21.3%,OR=1.16、95% CI=(0.88,1.54),即Peg-IFNα-2a联用ADV治疗HBeAg阳性CHB患者可提高患者治疗48 w血清HBV DNA阴转率,但对治疗24 w时血清HBV DNA阴转率无明显提高(图3)。根据48 w亚组结果绘制漏斗图,各点基本符合对称倒置分布,提示发表偏倚较低(图4)。本研究纳入的RCT数量相对较少,故采用Egger法评价漏斗图的发表偏倚:治疗48 w,bias_P=0.603,bias_95 CI=(-3.147437,4.877706),提示发表偏倚尚可,其线性回归检验图如图5所示。将合并研究的随机效应模型与固定效应模型互换,未发现不同效应模型的结果发生逆转。进一步计算失安全系数:治疗48 w,Nfs0.05=4.73,表明需纳入近5篇阴性研究才能改变本次系统评价的结果。综上所述,Peg-IFNα-2a联合ADV治疗HBeAg阳性CHB患者可提高48 w血清HBV DNA阴转率,其发表偏倚程度可控,结果可信。

图2 Peg-IFNα-2a联合ADV治疗HBeAg阳性CHB患者血清HBV DNA阴转率的Galbraith图
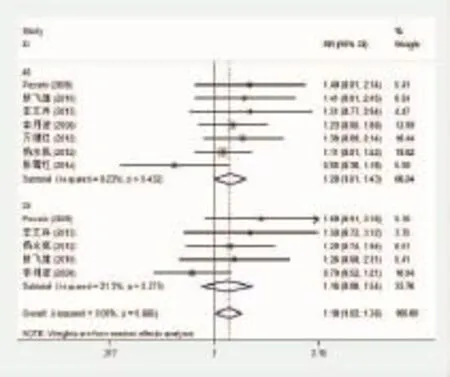
图3 血清HBV DNA阴转率的森林图Peg-IFNα-2a联合DV治疗48 w血清HBV DNA阴转率显著升高
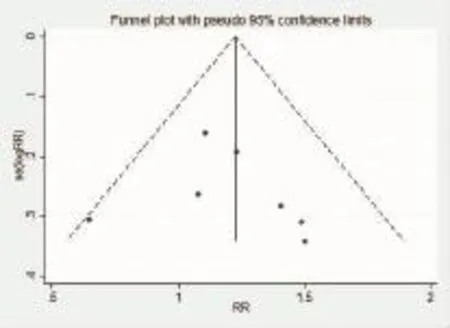
图4 治疗48w血清HBV DNA阴转率的漏斗图Peg-IFNα-2a联合ADV治疗发表偏倚度较低

图5 治疗48w时HBV DNA阴转率的Egger法线性回归检验图 Peg-IFNα-2a联用ADV治疗的结果可信
2.4 Peg-IFNα-2a联合 ADV治疗 HBeAg阳性CHB患者血清HBeAg转换率的变化Cochran's Q检验示P=0.904、I2=0%,说明各研究间异质性显著,采取随机效应模型进行系统评价。将治疗24w和48w患者HBeAg血清转换率分别进行亚组分析,以进一步消除异质性。森林图示:①治疗48w的Cochran'sQ检验示P=0.185、I2=0.26%,OR=1.24、95%CI=(1.02,1.52);②治疗24w的Cochran'sQ检验示P=0.361、I2=6.5%,OR=1.31、95%CI=(0.91,1.88),即Peg-IFNα-2a联合ADV治疗HBeAg阳性CHB患者可提高患者治疗48w时HBeAg血清转换率,但对治疗24 w时HBeAg血清转换率未产生明显的提高。结果还显示亚组结果的发表偏倚较低。采用Egger法评价发表偏倚性:bias_p=0.603、bias_95CI=(-3.147437,4.877706),提示发表偏倚尚可。将合并研究的随机效应模型与固定效应模型互换,并未发现不同效应模型的结果发生逆转,进一步计算失安全系数,结果治疗48w组Nfs0.05=4.73,表明需纳入将近5篇阴性研究才能改变本次系统评价结果。
2.5 Peg-IFNα-2a联合 ADV治疗 HBeAg阳性CHB患者ALT复常率的变化结果表明,Peg-IFNα-2a联用ADV治疗HBeAg阳性CHB患者,对患者治疗48 w和24 w时血清ALT复常率均不产生明显的提高效果。2.6纳入研究的不良事件4篇RCT[25~28]报道了患者治疗周期内所出现的不良反应:①3篇报道在应用Peg-IFNα-2a后出现发热、乏力、头痛等不适;②3篇报道服用ADV后出现食欲减退、恶心等不适;③2篇报道应用Peg-IFNα-2a后出现中性粒细胞减少;④2篇报道应用Peg-IFNα-2a后出现脱发。
3 讨论
联合用药抗病毒治疗,可提高疗效[32]。2008年Takkenberg et al应用Peg-IFNα-2a治疗CHB患者未见显著应答后,加用ADV联合治疗,获得了近20%HBsAg血清学转换率[33]。Peg-IFNα-2a与ADV联用能加强抗病毒效果,可能消除体内残留的HBV[34]。
HBeAg血清学转换是机体建立有效抗HBV免疫应答的重要标志[35],而未能出现HBeAg转阴的患者易在停药后发生HBV DNA反弹[36]。因此,对应于HBeAg阳性CHB患者的治疗终点是HBV DNA低于检测下限、HBeAg血清转阴、ALT恢复正常水平[37]。本研究结果提示Peg-IFNα-2a联合ADV治疗HBeAg阳性CHB患者能显著提高治疗48 w时HBV DNA阴转率和HBeAg血清转换率,但不能进一步提高ALT复常率。
本研究尚存在显著不足之处:①纳入研究的ADV均来源于同一生产公司(葛兰素史克),受试者人种涵盖面不够广,可能会对结果产生一定的影响;②纳入RCT的数量较少,高质量的RCT仅有2篇;③纳入的大部分RCT未对停药后患者的远期预后进行报道;④已证实Peg-IFNα-2a联用拉米夫定在短期内疗效不理想,Peg-IFNα-2a联用替比夫定可诱发患者出现周围神经病变。鉴于本研究部分RCT提示Peg-IFNα-2a联用ADV后出现粒细胞下降现象,下阶段应进一步观察联合药物对造血系统的影响。
通过整合同类研究,系统评价能改善单项研究推广性差、结局指标异质性过大等缺陷,对大量单项研究结果进行合并效应量分析,使结果更为全面、量化、客观。但系统评价并非真正意义的疗效试验性研究,不能取代大规模、多中心的随机分组对照试验,只是对现有研究进行系统整合。随着新的研究证据的出现,其结论必然在不断更新[38]。限于我们自身循证医学水平、文献检索及筛选的精确性尚存在不足,后续研究中应严格遵守循证医学理论,继续追踪国内外相关报道的进展情况,以期进一步完善研究,指导临床。
【参考文献】
[1]Ganem D,Prince AM.Hepatitis B virus infection-natural history and clinicsI conscquence.N Engl J Med,2004,350(2): 1118-1129.
[2] Liaw YF.On-treatment outcome prediction and adjustment duringchronichepatitisBtherapy:nowandfuture.Antivir Ther,2009,14(1):13-22.
[3] Liang X,Bi S,Yang w,et al.Epidemiological serosurvey of hepatitis B in China-declining HBV prevalence due to hepatitis B vaccination.Vaccine,2009,27(3):6550-6557.
[4] Seeger C,Mason WS.Hepatitis B virus biology.Microbiol Mol-Biol Rev,2000,64(4):5l-68.
[5] Liang X,Bi S,Yang W,et aL.Evaluation of the impact of hepatitis B vaccination among children born during 1992-2005 in China.J Infect Dis,2009,200(8):39-47.
[6]Ahn SH,Kweon YO,Paik SW,et al.Telbivudine in combination with Adefovir versus Adefovir mono therapy in HBeAgpositive,lamivudine-resistant chronic hepatitis B.Hepatol Int,2011,12(10):448-451.
[7]樊蓉,侯金林,孙剑.慢性乙型肝炎的个体化治疗策略.中华内科杂志,2012,51(10):746-748.
[8]戎云清.阿德福韦酯和拉米夫定治疗慢性乙型肝炎疗效对比观察.实用肝脏病杂志,2012,15(4):137-138.
[9]Hadziyanllis SJ,Tassopoulos NC,Heathcote EJ,et al.Long-term therapy with adefovir dipivoxil for HBeAg-negative chronic hepatitis B.N Engl J Med,2005,352(8):2673-2680.
[10]Wursthorn K,Lutgehetmann M,Dandri M,et al.Peginterferon alpha-2b plus adefovir induce strong cccDNA decline and HBsAg reduction in patients with chronic hepatitis B.Hepatology,2006,44(9):675-684.
[11]Moher D,Liberati A,Tetzlaff J,et al.Preferred reporting items for systematic reviews and meta-analyses:the PRISMA statement.BMJ,2009,21(7):339-340.
[12]Leandro G.Meta-analysis in Medical Research.Massachusetts: Blackwell Publishing Ltd,2005,74-78.
[13]European Association for the Study of the Liver.EASL clinical practice guidelines:management of chronic hepatitis B.J Hepatol,2009,50(3):227-242.
[14]中华医学会肝病学分会和感染病学分会.慢性乙型肝炎防治指南(2010年版).实用肝脏病杂志,2011,14(2):81-89.
[15]科技部十二五重大专项联合课题组专家.乙型肝炎病毒相关肝硬化的临床诊断、评估和抗病毒治疗的综合管理.实用肝脏病杂志,2014,17(1):1-10.
[16]李静,李幼平.不断完善与发展的Cochrane系统评价.中国循证医学杂志,2008,8(9):742-743.
[17]Higgins JPT,Green S.Cochrane Handbook for Systematic Reviews of Interventions version 5.0.2.The Cochrane Collaboration,2009,201-203.
[18]TURPIN D L.CONSORT and QUOROM guidelines for reporting randomized clinical trials and systematic reviews.American journal of orthodontics and dentofacial orthopedics:official publication of the American Association of Orthodontists,its constituentsocieties,andtheAmericanBoardofOrthodontics,2005,128(6):681-685.
[19]JAdad AR,Moore RA,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary.Control Clin Trials,1996,17(1):1-12.
[20]Walsh C,Walsh S,Tang T,et al.Total abdominal hysterectomy versus total laparoscopic hysterectomy for benign disease:A metaanalysis.Eur J Obstet Gynecol Reprod Biol,2009,144(1):1-2.
[21]Liberati A,Altman D G,Tetzlaff J,et al.The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate healthcare interventions:explanation and elaboration.BMJ,2009,21(6):339-340.
[22]王丹,翟俊霞,牟振云,等.Meta分析中的异质性及其处理方法.中国循证医学杂志,2009,9(10):1115-1118.
[23]Brian S E,Torsten H.A handbook of statistical analyses using R.CRC Press,2006:163-169.
[24]麦劲壮,李河,方积乾,等.Meta分析中失安全系数的估计.循证医学,2006,6(5):297-300.
[25]Piccolo P,Lenci I,Demelia L,et al.A randomized controlled trial of pegylated interferon-alpha2a plus adefovir dipivoxil for hepatitis B e antigen-negative chronic hepatitis B.Antivir Ther,2009,14(8):1165-1174.
[26]敖飞健,马为民,周伯平.聚乙二醇干扰素α-2a、阿德福韦酯酯单用及联合应用治疗HBeAg阳性慢性乙型肝炎患者的疗效及安全性比较.中华传染病杂志,2010,28(4):214-217.
[27]李月波,马桂芹,许蕾,等.PeglFNa-2a联合阿德福韦酯治疗HBeAg阳性慢性乙型肝炎的临床疗效观察.中华临床感染病杂志,2008,l(3):168-170.
[28]万继红,刘凤霞.聚乙二醇干扰素a-2a联合阿德福韦酯治疗HBeAg阳性慢性乙型肝炎患者疗效观察.中国保健营养,2012,22(11):4351-4352.
[29]杨永锐,李晖,贾婷,等.聚乙二醇干扰素α-2a联合阿德福韦酯治疗HBeAg阳性慢性乙肝.昆明医科大学学报,2012,33(10): 106-108.
[30]李文兵,丁继光,孙庆丰,等.聚乙二醇干扰素α-2a与阿德福韦酯联合治疗HBeAg阳性慢性乙型肝炎患者的研究.中华医院感染学杂志,2013,23(6):1250-1252.
[31]张雪红,易长庚.阿德福韦酯联合聚乙二醇干扰素α-2a治疗慢性乙型肝炎的疗效观察.现代医药卫生,2014,11(11):1637-1638.
[32]Wursthom K,Lutgehetmann M,Dandri M,et al.Peginterferon alpha-2b plus adefovir induce strong cccDNA decline and HbsAg reduction in patients with chronic hepatitis B.Hepatology,2006,44(3):675-684.
[33]窦晓光,徐道振,翁心华.当前聚乙二醇干扰素治疗慢性乙型肝炎的热点与难点.中华传染病杂志,2010,28(4):201-203.
[34]Olinger CM,Jutavijittum P,Hubschen JM,et a1.Possible new hepatiffs B virus genotype,southeast Asia.Emerg Infect Dis,2008,14(2):1777-1780.
[35]中华医学会肝病学分会肝癌学组.HBV/HCV相关性肝细胞癌抗病毒治疗专家建议.中华肝脏病杂志,2013,21(2):96-100.
[36]王蜀强,徐开菊,吴家箴,等.不同疗程干扰素联合核苷(酸)类似物治疗HBeAg阳性慢性乙型肝炎的疗效.中华肝脏病杂志,2011,19(10):785-787.
[37]Li C,Ji H,Cai Y,et al.Serum interleukin-37 concentrations and HBeAg seroconversion in chronic HBV patients during telbivudine treatment.J Interferon Cytokine Res,2013,22(5)114-117.
[38]Johnson N,Barlow D,Lethaby A,et al.Methods of hysterectomy:systematic review and meta-analysis of randomised controlled trials.BMJ,2005,330(7506):1478-1480.
(收稿:2014-08-26)(本文编辑:陈从新)
第一作者:肖作汉,男,50岁,大学本科,副主任医师,科室副主任。主要从事感染性疾病的诊治和细菌耐药机制研究。E-mail:162075065@qq.com
DOI:10.3969/j.issn.1672-5069.2015.01.007
作者单位:436099湖北省鄂州市中心医院感染病科
通讯作者:王立志,E-mail:41246751@qq.com
Clinical efficacy of pegylated interferon α-2a combined with adefovir in treatment of patients with HBeAg-positive chronic hepatitis B:A Meta analysis Xiao Zuohan,Meng Gang,Wang Lizhi.Department of Infectious Disease,Central Hospital,Ezhou 436099,Hubei Province,China
【Abstract】Objective To investigate the clinical efficacy of pegylated interferon α-2a(Peg-IFNα-2a)combined with adefovir(ADV)in treatment of patients with HBeAg-positive chronic hepatitis B(CHB).Methods Randomized controlled trials(RCT)involving peg-IFNα-2a combined with adefovir in treatment of patients with HBeAg-positive CHB,were searched from Pubmed,Wanfang Database,Chongqing VIP database,CNKI database,etc,from January,2004 to January,2014,of which the quality were underwent rigorous assessment and data were analyzed by Stata/SE software(version 12).Results 7 allegeable RCT(a total of 529 cases)were included.There were 261 patients receiving peg-IFNα-2a combined with ADV and 268 receiving peg-IFNα-2a alone.Systematic evaluation showed that HBV DNA negative rate in combinational therapy-treated patients with CHB at the end of week 48 was significantly higher as compared to patients receiving interferon alone[OR=1.20,95%CI=(1.01,1.43)];the HBeAg seroconversion rate at 48 w in patients receiving combinational therapy was also significantly higher than that in the controls[OR=1.24,95%CI=(1.02,1.52)];a significant bias of results was found for serum ALT normalization rate[bias_p=0.012,bias_95 CI=(1.442998,6.467852)].Conclusions Peg-IFNα-2a combined with ADV significantly improves HBV DNA negative and HBeAg seroconversion rate in patients with HBeAg-positive CHB.
【Key words】Chronic hepatitis B;Peg-IFNα-2a;Adefovir;Meta analysis
