荷芩止痒搽剂长期毒性实验研究(对家兔生化学的影响)△
2015-07-12赵景云马克坚王振宇宋京风
赵景云 马克坚* 王振宇 宋京风
(1.云南省中医中药研究院,云南 昆明 650223; 2.昆明医科大学,云南 呈贡 650504)
在艾滋病感染者及病人(HIV/AIDS)中皮肤瘙痒症是较为常见的临床症状,国内报道,皮肤瘙痒发生率最高为71.43%[1],居首位,且最易于反复发作。报导可能的发生原因是皮肤感染、丘疹鳞屑改变、光线性皮炎、皮肤干燥和药物反应等,也可能是非特异性淋巴细胞增生或特发性皮肤瘙痒症[2]。其病因及发病机制仍不明确,临床诊疗的循证证据不足,但与AIDS 的发病及进展关系密切[3]。艾滋病皮肤瘙痒症与一般疾病的皮肤瘙痒症有很大区别,HIV/AIDS 患者皮肤瘙痒症状剧烈,常因过度搔抓而出现皮肤局部血迹累累,皮损部位可出现丘疹、丘疱疹、结节等,形状不一、大小不等,并可伴有局部皮肤色素沉着和瘢,瘙痒可发于全身各部皮肤,好发于四肢伸侧,尤以下肢伸侧最为常见,根据其表现类似祖国医学的“粟疮”。随着病情发展,皮损的变化,又与古医文献中记载的“马疥”相似[4]。HIV/AIDS 患者本身因感染HIV 或接受HAART 疗法,皮肤常发生剧烈的瘙痒、泛发皮疹[5],并因过度的搔抓可出现表皮剥脱性丘疹、炎症性色素沉着和瘢痕性结节,给患者造成了极大的痛苦。而在艾滋病患者HAART 疗法过程中,皮肤瘙痒可使患者生活质量明显下降,长期服药依从性难以保证,可能使HIV 对药物产生耐药而导致治疗失败[6,7]。因此,艾滋病皮肤瘙痒症也是临床上一个不容忽视的重要问题,直接影响到患者治疗的依从性以及生活质量。
荷芩止痒搽剂是云南省中医中药研究院经过对HIV/AIDS 患者皮肤瘙痒发病情况的广泛调研,观察患者皮肤发病情况和病情发展过程的基础上,以中医辨证施治的原则,结合各单味药的功效以及相关现代研究而成。主要由红根等经乙醇提取制成,具有解毒、消肿、除湿和止痒作用。为使其安全进入临床观察,进行医院制剂的申报,同时也为临床使用提供可靠的科学依据,对该搽剂进行了安全性评价。
荷芩止痒搽剂家兔皮肤给药4 周,停药恢复2 周血清生化学长期毒性实验研究报导如下。
1 材料与方法
1.1 材料
1.1.1 药物和试剂:荷芩止痒搽剂(原生药1.5g·mL-1、3.0g·mL-1、6.0g·mLI -13 个浓度),批号:120701;50%药用乙醇,批号:120731,由云南省中医中药研究院制剂室提供;氯化钠注射液:250mL:2.25g,批号:1112231,昆明南疆制药有限公司。
1.1.2 实验动物:普通级家兔,年龄(♀/♂,月):3 ~4,体重(♀/♂,kg)2.0 ~2.7/2.0 ~2.7,来源于昆明医科大学实验动物中心,实验动物生产许可证号:SCXK(滇)2005 -0008,实验动物使用许可证号:SYXK(滇)2011 -0004,饲料生产许可证:SCXK(滇)2011 -0004,由昆明医科大学实验动物学部提供。
1.1.3 仪器:采用OLYMPUS AU5400 型全自动生化分析仪。
1.2 方法[8][9][10]
1.2.1 试验分组:60 只合格动物适应性饲养二周并同时进行相关观察后,按性别分别称重,按体重随机分为10 组,即完整皮肤(阴性对照组、溶媒对照组、低剂量组、中剂量组、高剂量组)和破损皮肤(阴性对照组、溶媒对照组、低剂量组、中剂量组、高剂量组),每组6 只,雌雄各3 只,单笼饲养。
1.2.2 剂量设计:荷芩止痒搽剂临床制剂拟为每ml 相当于原生药1.0g,皮肤外用,涂于患处,3 次/d,1 ~3mL/ 次,3 ~9mL/d,5d 为1 个疗程。按成人60 kg-1·bw-1,每天使用9mL 计算:用量为0.15 mL·kg-1·bw-1·d-1,相当于原生药0.15g·kg-1·bw-1·d-1,采用体重与体表面积换算的通用公式“lgS = 0.8762 + 0.698 lgW”换算为体表面积每m2 给药量为:6.87mL·m-2·d-1,相当于原生药6.87g·m-2·d-1,各试验组剂量与临床拟用剂量倍数参比见表1。

表1 各试验组剂量与临床拟用剂量倍数参比表
1.2.3 给药方法及观察时间:与临床给药途径一致,采用皮肤给药,破损皮肤组动物每周人为破损一次皮肤。动物连续给药4wk,每wk 给药7d,每天上午给药1 次,药物保留作用6h 后用温水清洗,每次给药容量为2mL·kg-1·bw-1等容量皮肤给药。末次给药后24h,每组随机抽取4 只动物,雌雄各2 只进行给药末期检查;每组剩余2 只动物,雌雄各1 只,停药恢复观察2wk 进行恢复期检查。
1.2.4 动物采血:禁食不禁水12 ~16h,用3%戊巴比妥钠按40mg·kg-1·bw-1耳缘静脉注射麻醉。将麻醉动物固定,在腹主动脉,用一次性采血针穿刺采血。
1.2.5 生化学检测:主要检测指标:丙氨酸转氨酶(ALT)、血清天冬氨酸转氨酶(AST)、甘油三脂(TG)、总胆固醇TC(CHO)、血糖(GLU)、肌酐(Cre)、肌酸激酶(CK)、尿素氮(Bun)、白蛋白(ALB)、总蛋白(TP)、碱性磷酸酶(ALP)、白/球比值(A/G)、血清钾离子(K +)、血清钠离子(Na+)、血清氯离子(Cl -)。采用OLYMPUS AU5400 型全自动生化分析仪。
1.2.6 统计学方法:计量资料采用SPSSwin12.0 软件进行方差分析,方差齐时两均数比较用LSD,方差不齐用秩和检验;等级资料用秩和检验,进行统计学分析。
2 结果
荷芩止痒搽剂连续给药4wk 停药恢复2wk,给药末期完整皮肤碱性磷酸酶(ALP)中剂量组略低,与溶媒对照组比较有显著性差异(P<0.05);总蛋白(TP)低、中、高剂量组均略升高,以高剂量较明显,与阴性和溶媒对照组比较均有显著性差异(P<0.05/0.01);总胆固醇(T-CHO)略升高,与溶媒对照组和低剂量组比较有显著性差异(P<0.05);肌酸激酶(CK)中剂量组略低,与阴性对照组比较有显著性差异(P<0.05);白/球比(A/G)高剂量组略低,与溶媒对照组比较有显著性差异(P<0.05)。给药末期破损皮肤ALP 高剂量组略低,与溶媒对照组和低剂量组比较有显著性差异(P<0.05);尿素氮(UREA)中、高剂量略低,与阴性和低剂量组比较有显著性差异(P<0.05);CK 溶媒对照、中、高剂量组略低,与阴性对照组比较有显著性差异(P<0.05);氯离子(CL)低剂量组略低,与阴性对照组比较有显著性差异(P<0.05)。给药末期其余各项血清生化学检测指标未见明显异常,组间比较无显著性差异(P>0.05)。恢复期因各组动物数<3,未进行组间比较,但各项检查指标均在正常参考值范围内。(表2、3、4、5)。

指标 阴性对照组 溶媒对照组 低剂量组 中剂量组 高剂量组GLU(mmol/L) 7.61 ±1.87 7.14 ±1.49 7.47 ±1.38 7.39 ±2.04 7.73 ±0.60 AST(IU/L) 60.00 ±8.76 58.25 ±9.98 72.75 ±17.58 60.67 ±18.18 64.67 ±3.51 ALT(IU/L) 46.25 ±13.79 42.00 ±9.76 45.00 ±17.58 47.33 ±28.31 52.00 ±12.17 ALP(IU/L) 216.50 ±58.46 229.30 ±34.35 215.50 ±36.01 153.70 ±23.86▼ 193.50 ±9.19 TP(g/L) 62.53 ±3.15 60.60 ±2.57 66.83 ±3.56▼ 65.60 ±2.44▼ 69.67 ±1.93**/▼ALB(g/L) 39.07 ±3.13 39.28 ±2.88 41.85 ±2.11 39.35 ±3.62 39.50 ±2.75 T-CHO(mmol/L) 1.43 ±0.54 1.13 ±0.42 1.24 ±0.44 1.41 ±0.20 2.19 ±0.76▼/■CR(umol/L) 87.50 ±3.62 104.50 ±15.33 95.75 ±9.36 93.00 ±25.76 82.67 ±7.02 UREA 9.64 ±3.15 10.54 ±1.72 10.34 ±1.54 10.12 ±2.60 9.20 ±2.17 TG(mmol/L) 0.97 ±0.26 0.95 ±0.29 1.05 ±0.35 1.52 ±1.26 0.92 ±0.31 CK(IU/L) 2021 ±228.31 1542 ±473.66 1542 ±899.10 1209 ±174.96* 1910 ±483.07 A/G 1.67 ±0.18 1.88 ±0.36 1.76 ±0.48 1.55 ±0.41 1.34 ±0.28▼
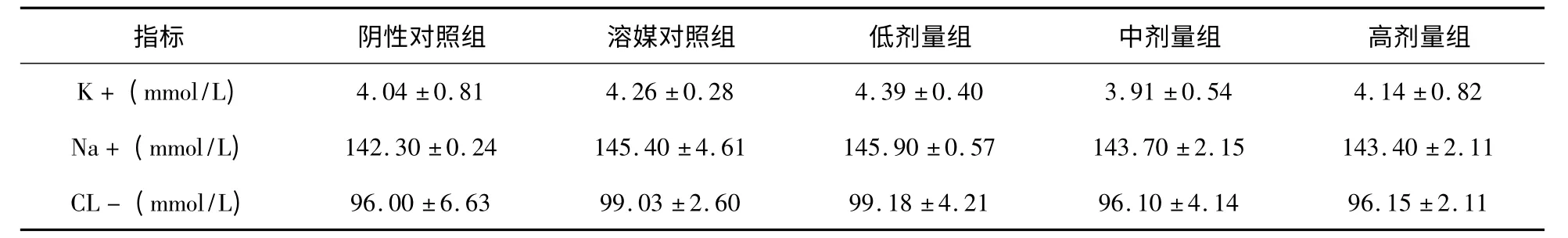
统计学分析:* /**与阴性对照组比较有显著性差异P <0.05/0.01;▼与溶媒对照组比较P <0.05;■与低剂量组比较有显著性差异P <0.05。注:动物数=4
表3 荷芩止痒搽剂破损皮肤给药末期血清生化指标检查结果( ±s)
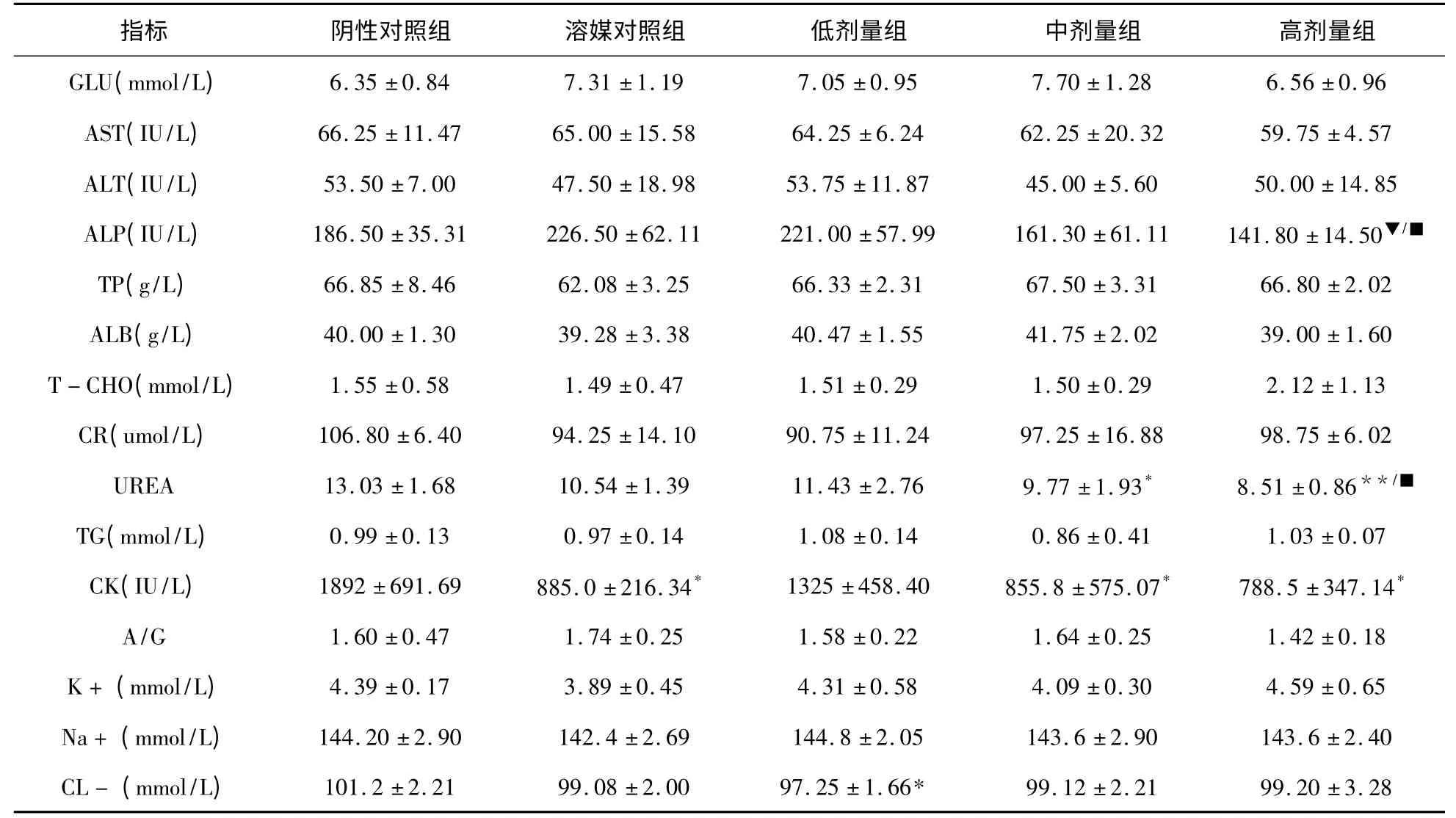
表3 荷芩止痒搽剂破损皮肤给药末期血清生化指标检查结果( ±s)
统计学分析:* /**与阴性对照组比较有显著性差异P <0.05/0.01;▼与溶媒对照组比较P <0.05;■与低剂量组比较有显著性差异P <0.05。注:动物数=4
指标 阴性对照组 溶媒对照组 低剂量组 中剂量组 高剂量组GLU(mmol/L) 6.35 ±0.84 7.31 ±1.19 7.05 ±0.95 7.70 ±1.28 6.56 ±0.96 AST(IU/L) 66.25 ±11.47 65.00 ±15.58 64.25 ±6.24 62.25 ±20.32 59.75 ±4.57 ALT(IU/L) 53.50 ±7.00 47.50 ±18.98 53.75 ±11.87 45.00 ±5.60 50.00 ±14.85 ALP(IU/L) 186.50 ±35.31 226.50 ±62.11 221.00 ±57.99 161.30 ±61.11 141.80 ±14.50▼/■TP(g/L) 66.85 ±8.46 62.08 ±3.25 66.33 ±2.31 67.50 ±3.31 66.80 ±2.02 ALB(g/L) 40.00 ±1.30 39.28 ±3.38 40.47 ±1.55 41.75 ±2.02 39.00 ±1.60 T-CHO(mmol/L) 1.55 ±0.58 1.49 ±0.47 1.51 ±0.29 1.50 ±0.29 2.12 ±1.13 CR(umol/L) 106.80 ±6.40 94.25 ±14.10 90.75 ±11.24 97.25 ±16.88 98.75 ±6.02 UREA 13.03 ±1.68 10.54 ±1.39 11.43 ±2.76 9.77 ±1.93* 8.51 ±0.86**/■TG(mmol/L) 0.99 ±0.13 0.97 ±0.14 1.08 ±0.14 0.86 ±0.41 1.03 ±0.07 CK(IU/L) 1892 ±691.69 885.0 ±216.34* 1325 ±458.40 855.8 ±575.07* 788.5 ±347.14*A/G 1.60 ±0.47 1.74 ±0.25 1.58 ±0.22 1.64 ±0.25 1.42 ±0.18 K+ (mmol/L) 4.39 ±0.17 3.89 ±0.45 4.31 ±0.58 4.09 ±0.30 4.59 ±0.65 Na+ (mmol/L) 144.20 ±2.90 142.4 ±2.69 144.8 ±2.05 143.6 ±2.90 143.6 ±2.40 CL- (mmol/L) 101.2 ±2.21 99.08 ±2.00 97.25 ±1.66*99.12 ±2.21 99.20 ±3.28
表4 荷芩止痒搽剂完整皮肤恢复期血清生化指标检查结果( ±s)

表4 荷芩止痒搽剂完整皮肤恢复期血清生化指标检查结果( ±s)
注:恢复期动物数=2,未进行组间比较。
指标 阴性对照组 溶媒对照组 低剂量组 中剂量组 高剂量组GLU(mmol/L) 8.49 ±1.08 7.69 ±0.56 7.83 ±0.25 7.05 ±0.30 8.29 ±1.63 AST(IU/L) 75.50 ±12.02 64.00 ±7.07 55.50 ±4.95 49.50 ±13.44 52.00 ±1.41 ALT(IU/L) 57.50 ±12.02 55.50 ±9.19 50.00 ±16.97 34.00 ±8.49 37.00 ±8.49 ALP(IU/L) 174.00 ±5.66 214.00 ±69.30 198.00 ±43.84 184.50 ±130.82 194.50 ±40.31 TP(g/L) 66.60 ±2.26 61.55 ±2.19 60.35 ±1.48 57.50 ±2.55 66.60 ±4.38 ALB(g/L) 41.85 ±1.77 40.00 ±2.26 40.05 ±0.92 34.35 ±2.19 40.85 ±0.64 T-CHO(mmol/L) 2.23 ±0.91 1.73 ±1.00 1.49 ±0.29 1.39 ±0.36 1.64 ±0.08 CR(umol/L) 97.50 ±9.19 109.00 ±15.56 101.50 ±4.95 87.00 ±2.83 91.50 ±7.78 UREA 6.90 ±2.06 8.05 ±3.88 7.64 ±0.05 7.26 ±0.73 7.85 ±1.25 TG(mmol/L) 1.79 ±0.01 0.89 ±0.00 1.02 ±0.18 1.18 ±0.28 0.80 ±0.09 CK(IU/L) 1036 ±123.04 894.0 ±100.41 687.50 ±304.76 791.50 ±125.16 724.00 ±25.46 A/G 1.72 ±0.35 1.86 ±0.11 1.99 ±0.28 1.53 ±0.40 1.62 ±0.34 K+ (mmol/L) 4.47 ±0.01 4.31 ±0.69 4.66 ±0.12 4.36 ±0.74 4.61 ±0.08 Na+ (mmol/L) 141.05 ±2.76 141.70 ±1.70 142.45 ±0.35 140.35 ±0.92 140.25 ±0.07 CL- (mmol/L) 92.30 ±1.27 97.70 ±0.57 101.70 ±1.84 98.95 ±3.61 98.90 ±2.12

指标 阴性对照组 溶媒对照组 低剂量组 中剂量组 高剂量组GLU(mmol/L) 8.83 ±0.42 8.81 ±0.98 8.35 ±1.87 8.95 ±1.09 7.09 ±0.83 AST(IU/L) 74.50 ±0.71 83.50 ±21.92 52.50 ±0.71 68.50 ±26.16 84.00 ±24.04 ALT(IU/L) 50.00 ±9.90 65.00 ±35.36 47.50 ±13.44 47.50 ±21.92 68.50 ±9.19 ALP(IU/L) 185.50 ±16.26 135.50 ±9.19 197.00 ±56.57 212.50 ±65.76 158.00 ±55.15 TP(g/L) 62.70 ±5.52 58.20 ±3.96 61.25 ±5.16 60.80 ±0.14 61.35 ±0.07 ALB(g/L) 40.40 ±1.98 37.60 ±3.25 35.50 ±0.85 38.55 ±0.64 41.30 ±0.42 T-CHO(mmol/L) 1.83 ±0.50 1.17 ±0.41 1.26 ±0.62 2.00 ±0.60 2.38 ±0.71 CR(umol/L) 91.00 ±7.07 80.50 ±4.95 96.50 ±7.78 88.00 ±15.56 96.00 ±1.41 UREA 6.53 ±1.26 6.26 ±1.08 7.28 ±0.27 6.24 ±0.82 6.96 ±0.61 TG(mmol/L) 1.45 ±0.45 1.13 ±0.42 0.95 ±0.27 1.13 ±0.35 1.89 ±0.19 CK(IU/L) 1036.0 ±73.54 1528.5 ±128.00 1264.0 ±62.23 1305.0 ±233.35 819.50 ±23.33 A/G 1.85 ±0.18 1.83 ±0.09 1.40 ±0.21 1.74 ±0.09 2.06 ±0.07 K+ (mmol/L) 4.44 ±0.04 4.19 ±0.05 4.36 ±0.03 4.40 ±1.31 4.17 ±0.42 Na+ (mmol/L) 140.50 ±0.71 140.30 ±1.84 140.65 ±0.78 140.90 ±0.14 141.10 ±0.14 CL- (mmol/L) 97.80 ±7.78 98.75 ±0.07 100.65 ±2.19 101.55 ±0.07 96.10 ±2.12
3 讨论
血清生化学及电解质指标检查结果显示,家兔连续给药4 周停药恢复2 周,给药末期完整皮肤总蛋白(TP)低、中、高剂量组均略升高,以高剂量较明显,与阴性和溶媒对照组比较均有显著性差异(P<0.05/0.01),而白蛋白组间比较无显著性差异,提示低、中、高剂量组总蛋白升高以球蛋白升高为主,这是否与该搽剂具有一定的免疫调节功能有关需进一步研究;此外给药末期完整皮肤碱性磷酸酶(ALP)中剂量组略低,与溶媒对照组比较有显著性差异(P<0.05);总胆固醇(T-CHO)略升高,与溶媒对照组和低剂量组比较有显著性差异(P<0.05);肌酸激酶(CK)中剂量组略低,与阴性对照组比较有显著性差异(P<0.05);白/球比(A/G)高剂量组略低,与溶媒对照组比较有显著性差异(P<0.05)。给药末期破损皮肤ALP 高剂量组略低,与溶媒对照组和低剂量组比较有显著性差异(P<0.05);尿素氮(UREA)中、高剂量略低,与阴性和低剂量组比较有显著性差异(P<0.05);CK 溶媒对照、中、高剂量组略低,与阴性对照组比较有显著性差异(P<0.05);氯离子(CL)低剂量组略低,与阴性对照组比较有显著性差异(P<0.05)。但所测数值在文献参考值和本室历史背景资料范围,且无明显剂量反应关系,故无生物学和毒理学意义。给药末期其余各项血清生化学检测指标未见明显异常,组间比较无显著性差异(P>0.05),仅见完整皮肤试验组动物血清总蛋白(TP)略有升高,以球蛋白为主。
以上实验研究结果,家兔皮肤给予荷芩止痒搽剂1.5g·mL-1·kg-1·bw-1,折合原药材3.0g·kg-1·bw-1,相当于成人临床拟用最大药量20 倍以下,对家兔血清生化学及电解质指标无影响。
[1]张毅,杜艾嫒.239 例HIV 感染者并发皮肤损害分析[J].实用皮肤病学杂志,2010,3(3):134 -136.
[2]HOLMES R B,MARTINS C,HORN T.The histopathology of folliculitis in HIV-infected patients[J].J Cutan Patho,2002,(29):93 -95.
[3]潘菊华,王阶,黄世敬.基于专家问卷的艾滋病皮肤瘙痒性病变中医诊疗规程研究[J].中国中西医结合杂志,2013:33(7):890 -895.
[4]闫磊,郭会军.艾滋病皮肤瘙痒症发病机制探析[J].辽宁中医杂志,2012,39(3):562 -563.
[5]赵景云,马克坚,方路,等.HIV/AIDS 皮肤瘙痒症相关性问题简述[J].云南中医中药杂志,2009,30(12):83 -84.
[6]林光惠,陈小英.艾滋病患者抗病毒治疗不良反应的护理[J].护理学杂志,2008,23(11):30 -32.
[7]屈文妍,李春梅,闫会文,等.艾滋病患者抗病毒治疗中药物不良反应的观察与护理[J].中华护理杂志,2007,42(12):1078 -1080.
[8]中药、天然药物长期毒性研究技术指导原则.编号:[Z]GPT3 -1.2004.3.18.
[9]袁伯俊,廖明阳,等.药物毒理学实验方法与技术[M].化学工业出版社,2007.
[10]郝光荣.实验动物学[M].第二军医大学出版社,1991.
