土壤无机磷酸盐中氧同位素分析方法的研究及应用
2015-07-02张晗王佳妮朱永官张娴
张晗 王佳妮 朱永官 张娴
(中国科学院城市环境研究所环境与健康重点实验室分析测试中心,厦门 361021)
土壤无机磷酸盐中氧同位素分析方法的研究及应用
张晗 王佳妮 朱永官 张娴*
(中国科学院城市环境研究所环境与健康重点实验室分析测试中心,厦门 361021)
土壤磷酸盐氧同位素在生物地球化学研究领域中具有重要的应用,土壤成分复杂,氧同位素来源多样,可靠的样品富集和纯化技术是磷酸盐氧同位素研究的前提保障。本研究以土壤无机磷酸盐氧同位素为研究对象,采用多步沉淀法对土壤中无机磷酸盐进行提取,并转化成Ag3PO4沉淀分离,用于磷酸盐氧同位素测试。以氨水重结晶方法对Ag3PO4进行纯化,通过XRD和元素分析验证了产品纯度。结果表明,通过H2O2漂洗去除有机质后,辅助氨水重结晶可有效去除Ag3PO4中夹杂的Ag2O和Ag单质等无机杂质,未产生同位素分馏,采用标准KH2PO4对方法全流程安全性进行验证。对3种不同利用类型的土壤中磷酸盐进行分析,结果表明,方法的平行性良好,不同类型土壤磷酸盐氧同位素差异显著,δ18Op值在15.2‰~19.5‰之间,可用于土壤磷溯源研究。
土壤;无机磷酸盐;磷酸银;氧同位素
1 引 言
磷酸盐氧同位素组成的研究为认识磷源的贡献[1~3],示踪磷酸盐生物化学循环途径[4,5]、反应微生物或酶反应活性[6]、磷酸盐所处周边环境温度变化[7],以及海洋生态系统磷循环研究发挥了重要作用。近年来,土壤中磷酸盐氧同位素在生物地球化学研究中备受关注。在地表自然条件下,单纯无机过程对磷酸盐氧同位素没有影响,而生物或酶作用却可使磷酸盐与周边环境中的氧发生交换,使磷酸盐中δ18Op发生变化。磷酸盐氧同位素组成的变化一定程度反应了土壤生态系统的活动性。由于不同的土壤磷源具有不同的反应活力,其给予植物和土壤微生物的养分的能力不同,磷酸盐氧同位素与微生物的关联使人们有可能阐明有机磷源和无机磷源在土壤中对植物及微生物的作用过程,以及在不同动植物物种之间的差异。因此磷酸盐氧同位素有望成为土壤生态系统磷循环研究的重要途径和手段,以及新型研究土壤磷生物化学反应过程的有力工具。
目前,土壤中δ18Op的报道仍十分有限[8~11],土壤中含有丰富的有机质和其它复杂底质,氧元素的多种来源使得土壤中磷元素的提取过程异常复杂,不仅要避免处理过程中激烈酸碱条件或高温带来焦磷酸盐或有机磷酸盐水解或氧交换产生的氧同位素偏移,更需彻底去除磷酸盐沉淀过程其它氧元素附着的干扰。可靠的样品富集和纯化技术是磷酸盐氧同位素研究的前提保障,也是目前土壤磷酸盐氧同位素研究的重点和难点。文献[8~10]开展了系列土壤磷酸盐的富集、纯化方法的研究。Tamburini等[8]介绍了提取以HCl可溶解的土壤磷酸盐方法,先后采用磷酸钼胺和磷酸铵镁使磷酸盐在相对温和的条件下通过多次沉淀与其它杂质分离,并最终转化为Ag3PO4进行测试;Weiner等[9]介绍了提取土壤表面易被植物吸收的无机磷源的方法,以阳离子交换树脂和土壤在去离子水中振荡吸附磷酸盐,用酸将磷酸盐从膜中洗脱,转为CePO4沉淀,再通过阳离子树脂去除Ce3+,并转为Ag3PO4沉淀;而Zohar等[10]则先后以H2O、弱碱NaHCO3、强碱NaOH和强酸HCl对土壤中磷酸盐逐级进行提取,并将每步提取的磷酸盐分别沉淀为Ag3PO4单独测试,发现不同形态的磷酸盐氧同位素存在差异。
由于土壤中的无机磷一般占土壤全磷的50% ~80%[12],本研究选择土壤无机磷酸盐作为研究对象,选取了不同利用类型的土壤,采用多步沉淀法[8]对土壤中无机磷酸盐进行提取,并探讨了Ag3PO4的纯化方法、纯化效果及方法对同位素分馏影响,为土壤中无机磷酸盐的氧同位素研究奠定基础。
2 实验部分
2.1 仪器、试剂与材料
Sterifil卫生过滤系统(Millipore公司);CR22GII高速离心机、Universal 320R低速离心机(Hettich公司);ZHWY-211B摇床(上海智诚公司);X′Pert PRO X射线衍射仪、AxiosmAX X射线荧光光谱仪(PAN-alytical公司);Delta V advantage元素分析仪-稳定同位素质谱仪(Thermo Fisher公司)。
DAX-8树脂(40~60目,Sigma-Aldrich公司);AG 50W-X8树脂(H+型,100~200目,BioRad公司); Millipore聚碳酸酯滤膜(0.22 μm);钼酸铵、NH4NO3、柠檬酸、氨水、MgCl2(分析纯,上海国药集团); AgNO3(分析纯,上海申博化工),Ag3PO4(99%,Alfa Aesar公司)。
土壤样品自然晾干,过200目分子筛后备用。
2.2 实验方法
(1)提取无机磷酸盐 称取30 g土壤于聚丙烯瓶,向其中加入120 mL新配1 mol/L HCl,室温摇荡过夜。离心,收集褐色滤液A。(2)去除有机质 向溶液A中加入25 mL DAX-8树脂浆,摇床振荡过夜,收集滤液B。(3)第一次沉淀分离(形成磷钼酸铵沉淀) 将B中加入30 mL 4.2 mol/L NH4NO3溶液,50℃水浴搅拌中缓慢加入50 mL 0.5 mol/L钼酸铵溶液,逐渐析出亮黄色磷钼酸铵沉淀,转移至摇床50℃摇荡18 h。冷却,过滤,以0.6 mol/L NH4NO3淋洗。将沉淀转移至锥形瓶中,加入柠檬酸溶液至沉淀全部溶解,得到溶液C。(4)第二次沉淀分离(形成磷酸胺镁沉淀) 室温搅拌,向溶液C中加入镁溶液30 mL(5 g MgCl2和10 g NH4Cl溶解于50 mL H2O,用12 mol/L HCl调至pH 1.0),逐渐有白色沉淀析出,搅拌过夜。过滤,以氨水-去离子水(1∶1,V/V)淋洗,沉淀用0.5 mol/L HNO3溶解,得到溶液D。(5)去除阳离子 将活化后的树脂浆(BioRad AG50WX8)10 mL倒入D中,室温摇荡18 h后取出,过滤,以少量去离子水淋洗,收集滤液E至锥形瓶中。(6)形成Ag3PO4沉淀 滤液E为强酸性,用1.5 mol/L NH4NO3-3 mol/L NH4OH混合液9 mL调至pH中性。向溶液E中加入AgNO3溶液(8 g,16 mL去离子水)2 mL,立即析出黄色沉淀;滴入AgNO3至无黄色沉淀生成即可。用0.2 μm滤膜过滤,去离子水多次洗涤。(7)Ag3PO4纯化 以H2O2漂洗去除Ag3PO4中残余有机质,以氨水重结晶方法去除Ag3PO4中微量无机杂质。(a)H2O2提纯法:以15% H2O2浸泡过夜,其间多次搅拌。过滤,以去离子水洗涤,50℃烘干。(b)氨水提纯法:取100 mg样品溶于5~10 mL氨水,滤掉少量深色杂质,收集无色清亮滤液置于50℃水浴中,让NH3缓慢挥发。每0.5 h添加少量去离子水,保持体积。至溶液pH<7.5,冷确至室温,过滤,去离子水清洗,50℃烘干。
2.2.2 Ag3PO4稳定同位素的测量氧同位素测量采用元素分析仪-稳定同位素质谱仪分析。EA方法:关闭注氧,将Ag3PO4包入银舟压实,在1380℃高温下与裂解炉内石墨反应生成CO。CO在He载气(流速100 mL/min)吹扫下进入色谱柱,在85℃条件下与载气中痕量N2分离,进入稳定同位素质谱分析。IRMS条件:高压3.017 kV,磁场9172 steps,电流1.5 mA,采用纯 Ag3PO4(Strem Chemicals, Ag3PO4,>99%,)作为实验室工作标准,质谱CO参考气校准采用国际原子能机构提供的IAEA601校准(δ18O=23.3‰)。
3 结果与讨论
3.1 提取方法的改进
3.1.1 调节pH值在文献[8]中,Ag3PO4沉淀步骤为直接向溶液E加入银氨混合溶液。实验发现,以该方法得到的Ag3PO4产物中含有少量Ag2O杂质,影响Ag3PO4纯度,本研究对该步骤做了改进:先以NH4NO3和氨水混合溶液调节溶液E(强酸性)pH至中性,然后再滴加Ag3PO4溶液,使Ag3PO4在中性条件下析出,可有效避免Ag2O产生。
3.1.2 氨水重结晶部分样品经过文献[8~12]方法以H2O2处理后,Ag3PO4仍呈现墨绿色。由于Ag3PO4溶于氨水,采用氨水重结晶方法对样品进一步纯化。为验证方法的可靠性,本研究同时采用两家公司Ag3PO4标样(Ag3PO4-1:99%,Alfa Aesar公司;Ag3PO4-2:99%,Strem Chemicals公司)和土壤中提取样品F进行氨水重结晶测试(表1),实验表明,氨水重结晶方法安全可靠,未产生同位素分馏,经过氨水重结晶的磷酸银样品形成良好的晶体形态,可有效排除杂质干扰。

表1 氨水重结晶对标样物质和样品δ18Op结果影响比较Table 1 Comparison of δ18Opin standard Ag3PO4and sample purified by NH4OH method
3.2 纯化结果
3.2.1 XRD检测采用X射线衍射仪对纯化前后的样品进行测定,并与标准做比较。以土壤样品S1为例,图1a为S1的提取产物,通过与数据库比较发现含有AgCl和Ag杂质,该杂质可通过氨水重结晶有效去除(尽管AgCl和Ag亦可形成银氨络合物溶于氨水,由于量少,随着NH3的挥发,其结晶速度低于Ag3PO4,及时过滤出Ag3PO4沉淀即可去除),图1c为标准Ag3PO4样品,样品纯化结果见图1b。
3.2.2 元素分析采用文献[8]的方法,称取不同样品量,通过元素分析,以样品量与裂解产生的CO的量作图,并与标准物质做比较,进一步考察样品的纯度。选取土壤F样品和土壤S3样品与标准Ag3PO4-2作比较,结果见图2。实验表明,本方法提取的土壤磷酸盐所得到的磷酸银样品与标准物质纯度相当,其纯度甚至优于文献[8]。部分样品(如土壤F)尽管颜色偏深,但经过H2O2纯化或氨水重结晶均可有效改善。
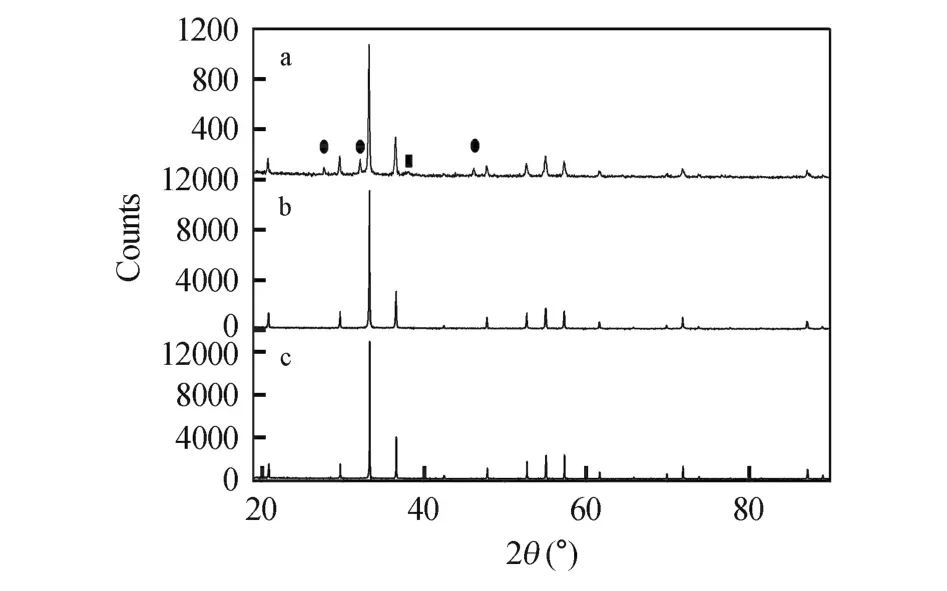
图1 Ag3PO4的XRD谱图Fig.1 XRD spectrum of Ag3PO4
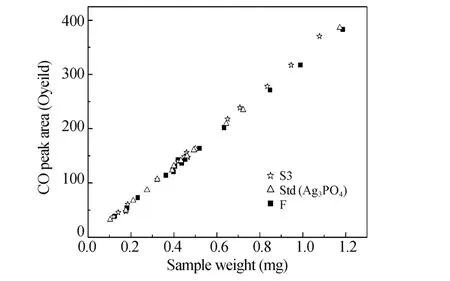
图2 Ag3PO4标准与本方法提取样品的样品量与其裂解产生的CO量线性图Fig.2 Weight of analyte plotted against the area of the CO peak for Ag3PO4satandard and sample treated with this method
3.3 判断全流程氧同位素分馏
Tamburini等[8]通过向样品提取液中添加18O标记的水来全程跟踪是否发生同位素分馏,结果证实方法安全可靠。本实验借鉴海水溶解磷酸盐氧同位素提取方法[13],以KH2PO4在中性条件下与AgNO3反应直接生成Ag3PO4沉淀和KH2PO4以1 mol/L HCl溶解,经过本方法全部流程后形成Ag3PO4沉淀,比较以上两种结果可知,直接反映得到的Ag3PO4沉淀δ18Op值为6.5‰(n=3,σ=0.14‰),经过全部流程后的Ag3PO4沉淀δ18Op值为6.9‰(n=3,σ=0.11‰),在方法可接受范围(σ<0.5‰),表明本方法全程未产生同位素分馏。
3.4 样品量对Ag3PO4稳定同位素测量结果的影响
由于氧同位素测试精度与进入质谱CO的量密切相关,样品量过低,裂解产生的CO不足以使质谱获得稳定的统计信号,影响测量准确度;而样品量过高,裂解不完全则有可能产生同位素分馏,同样无法反映真实值。由于不同类型的样品高温裂解效率存在差异,而Ag3PO4为含金属元素的无机盐,性质稳定,难于裂解,本研究考察了3种不同丰度样品(标准样(Ag3PO4-2)、土壤F和土壤S3)的样品量对测试结果的影响。

图3 不同进样量对测定结果的影响Fig.3 Effect of different weight of sample on δ18Op
由图3可见,当Ag3PO4样品量在0.3 mg以下时,δ18Op值波动较大,标准偏差在0.5‰~1.5‰之间,而当样品量增至1 mg以上时,部分样品δ18Op值出现贫化现象,而0.3~1.0 mg间δ18Op值相对平稳。密集考察了0.4~0.5 mg样品量的δ18Op值稳定情况,3种丰度样品的标准偏差均在0.1‰左右(n=4~8),质谱信号约为8000 mV,结果精准可靠,后续测试样品量均采用此范围。
3.5 方法的回收率
为了研究本提取方法的回收率,以农田土壤为例(每个样品平行测定2次),采用钼锑抗分光光度法对第1步中1 mol/L HCl土壤提取液中磷酸盐进行测定,测得浓度以P计,记为PHCl溶液,每30 g土壤提取实际得到Ag3PO4的质量MAg3PO4和以P计质量PAg3PO4同列于表2。
由表2可见,由于经过多步沉淀和过滤,在样品转移过程中不可避免造成损失,方法的回收率在56.4%~72.2%之间,然而对于经过施肥富含磷酸盐的农田土壤,30 g土壤可得到452~512 mg Ag3PO4,而稳定同位素测试仅需要约0.4 mg,即可满足实验需求。
3.6 不同类型土壤样品测定结果
本实验选取了森林、公园和农田3种不同利用类型的土壤样品进行考察。森林土壤F取自厦门集美后溪坂头水库深处,土层表面林木自然生长,不受人为磷源干扰,通过X射线荧光光谱仪测得其总磷含量为0.21 mg/g。公园土壤G1~G3取自厦门集美杏东公园,土层表面人工栽种观赏植物,总磷含量为0.41~0.59 mg/g,随机取3处表层土壤,平行测试。农田土壤取自厦门集美后溪农田,多年耕种,广泛施肥,总磷含量高达2.38~2.68 mg/g,为了消除采样的误差,进一步验证方法的准确度,对富含磷酸盐的农田3组样品均进行了方法的平行实验,结果如表3所示。
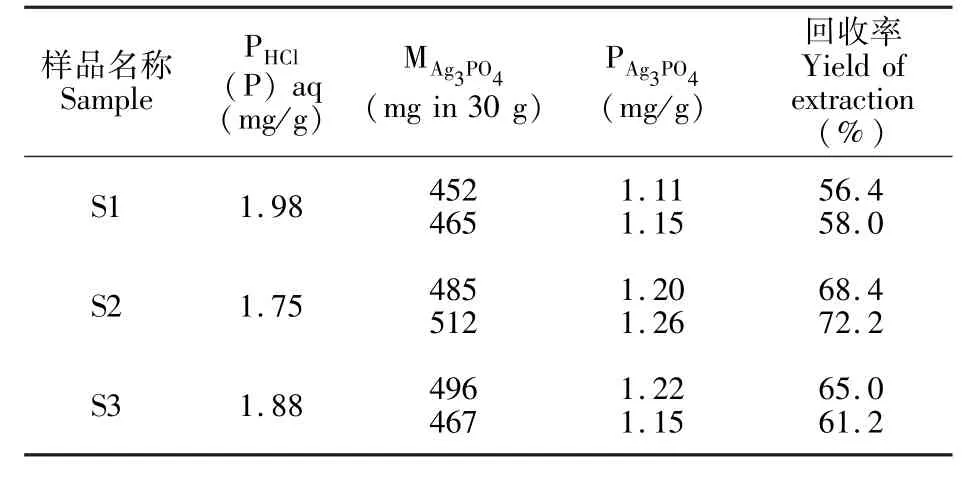
表2 土壤提取无机磷酸盐方法的回收率Table 2 Recovery of inorganic phosphate extracted from soil
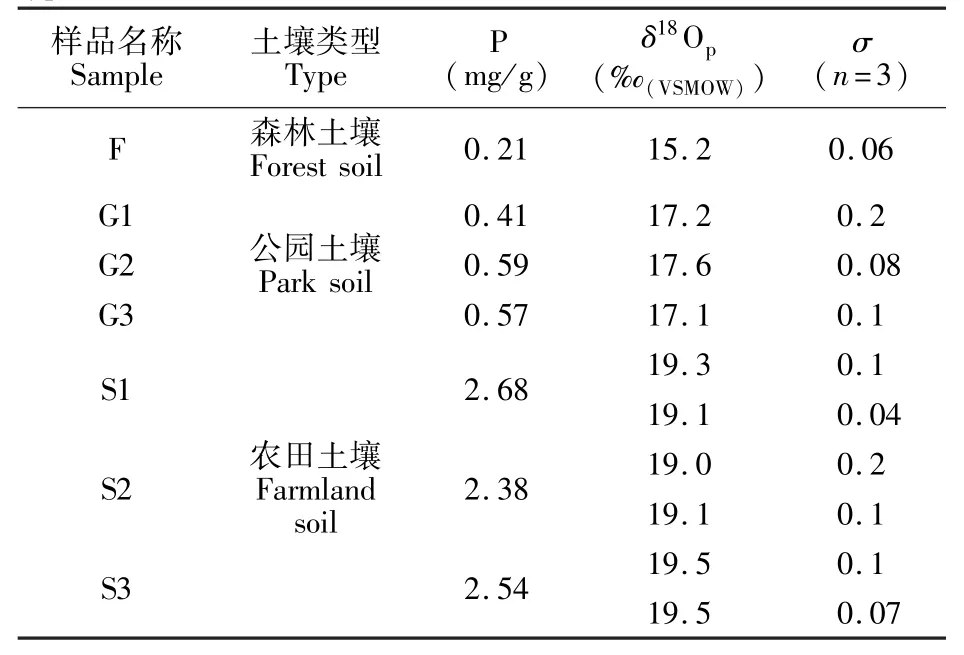
表3 不同类型土壤的磷含量和氧同位素结果Table 3 Total phosphorous and δ18Opof phosphate in different type of soils
由表3可见,本土壤中无机磷酸盐的提取方法的平行性和精度均非常好,高度证实了方法的可靠性,10组样品氧同位素测量标准偏差均在0.2以下。3种不同利用类型的土壤磷酸盐氧同位素表现出较为显著的差异,无人为磷源干扰的森林土壤磷酸盐氧同位素值最为贫化,为15.2‰,在Tamburini等[8]对瑞士和以色列两地未施肥或施以有机肥或矿物磷肥土壤变化无机磷酸盐氧同位素研究范围为13.5‰~17.6‰;而农田土壤的磷酸盐18O同位素最为富集,为19‰左右,与Young等[14]研究的以色列化学肥料中磷酸盐氧同位素比值范围(18.2‰ ~21.3‰),Gruau等[15]研究的法国农用化学肥料(19.6‰~23.1‰)以及Mclaughlin等[16]报道的两种化学肥料(19.4‰和20.5‰)中氧同位素比值变化范围一致,磷酸盐氧同位素比值与总磷含量测定结果均表明该农田土壤经过了充分施肥,磷酸盐供给主要来源于化学肥料。公园土壤磷酸盐氧同位素为17‰左右,磷元素含量亦显示该地土壤磷含量高于天然森林土壤,表明该土地略经施磷肥,土壤磷酸盐氧同位素表现出原始磷源和化学肥料的共同贡献。
4 结 论
建立了土壤中无机磷酸盐氧同位素组成的分析方法,考察了以氨水重结晶方法的纯化效果。通过H2O2漂洗去除有机质后,辅助氨水重结晶可有效去除磷酸银中夹杂的氧化银和银单质等无机杂质,未产生同位素分馏。对3种不同利用类型的土壤中磷酸盐氧同位素进行分析,结果表明,本提取方法的平行性和精度高,证实了方法的可靠性。不同类型土壤的磷酸盐氧同位素存在显著差异,本方法为进一步开展磷酸盐氧同位素的溯源和循环研究提供了参考。
1 Li X,Wang Y,Stern J,Gu B H.Appl.Geochem.,2011,26(5):688-695
2 Elsbury K E,Paytan A,Ostrom N E,Kendall C,Young M B,Mclaughlin K.Environ.Sci.Technol.,2009,43(9): 3108-3114
3 Blake R E,Alt J C.Martini A M.PNAS,2001,98(5):2148-2153
4 Longinelli A,Bartelloni M,Cortecci G.Earth Planet.Sci.Lett.,1976,32(2):389-392
5 Blake R E,O′Neil J R,Surkov A.Am.J.Sci.,2005,305(6/8):596-620
6 Blake R E,Alt J C,Martni A M.PNAS,2001,98(5):2148-2153
7 Colman A S,Blake R E,Karl D M,Fogel M L,Turekian K K.PNAS,2005,102(37):13023-13028
8 Tamburini F,Bernasconi S M,Angert A,Weiner T,Frossard E.Eur.J.Soil Sci.,2010,61(6):1025-1032
9 Weiner T,Mazeh S,Tamburini F,Frossard E,Berbasconi S M,Chiti T.Angert A.Rapid Commun.Mass Spectrom., 2011,25(5):624-628
10 Zohar I,Shaviv A,Klass T,Ronerts K,Paytan A.Environ.Sci.Technol.,2010,44(19):7583-7588
11 Tamburini F,Pfahler V,von Sperber C,Frossard E,Bernasconi S M.Soil.Sci.Soc.Am.J.,2014,78(1):47-53
12 CHEN Ying-Xu.Agriculture Environmetal Protection.Beijing:Chemical Industry Press,2007:176-177
陈英旭.农业环境保护,北京:化学工业出版社,2007:176-177
13 LU Yang-Yang,ZHENG Zhen-Zhen,YIN Xi-Jie,CHEN Zhi-Gang,Cai Yi-Hua,LIU Guang-Shan,HUANG Yi-Pu.Acta Geoscientica Sinica,2012,33(6):961-966
卢阳阳,郑珍珍,尹希杰,陈志刚,蔡毅华,刘广山,黄奕普.地球学报,2012,33(6):961-966
14 Young M B,McLaughlin K,Kendall C,Stringfellow W,Rollog M,Elsbury K,Donald E,Paytan A.Environ.Sci. Technol,2009,43(14):5190-5196
15 Gruau G,Legeas M,Riou C,Gallacier E,Martineau F,Henin O.Water Res.,2005,39:232-238
16 McLaughlin K,Cade-Menun B J,Paytan A.Coastal Shelf Sci.,2006,70:499-506
This work was supported by the National Natural Science Foundation of China(No.21207126)and the Natural Science Foundation of Fujian Province,China(No.2011J0533 )
中国化学会第十一届全国发光分析学术研讨会征文通知(第一轮)
中国化学会主办,西南大学化学化工学院,西南大学发光与实时分析教育部重点实验室和北京化工大学承办的第十一届全国发光分析学术研讨会定于2015年4月24~26日于重庆召开。会议旨在总结和交流近年来在发光材料、发光分析、发光器件及相关应用领域、发光仪器、发光机理研究等方面所取得的研究成果和最新进展,探讨发光研究面临的机遇和挑战,规划未来的发展方向,凝练科学目标,并集中国内优势资源攻克前沿科学问题,促进我国发光领域及其交叉科学领域的发展。大会诚邀相关领域的专家学者参加。
一.征稿内容
1.荧光、磷光、化学发光、生物发光、电化学发光、共振光散射等新的分析方法及相关发光机理研究;2.发光材料、新发光试剂和发光标记物的合成研究;3.色谱、毛细管电泳、生物芯片及微全分析系统的发光检测器研究;4.发光免疫分析、发光成像分析、单细胞与单分子发光检测技术研究;5.光学化学和生物传感器的研究;6.发光分析在食品、环境、临床检测等领域的应用研究;7.化学计量学在发光分析中的应用
二.征稿要求
1.只接收未在国内外学术刊物上公开发表或未在国际、国内学术会议上报告过的原创论文。
2.来稿应是论文详细摘要,每篇1页(包括图表),内容依次为:论文题目、作者姓名、单位、地址、邮编、正文。具体格式要求请参考会议网址(www.syfgfx.com)上的“投稿须知”,下载会议论文模板。
3.会议筹备组将组织专家对应征论文进行评审。录用的论文将在会议上报告或报展,并在会前出版摘要论文集。所有稿件请自留底稿,恕不退还。
4.征文截稿日期2015年3月30日。来稿可在线上传(会议网址www.syfgfx.com)或E-mail电传(faguangfenxi@ 163.com)
三.联系人:
卓颖E-mail:yingzhuo2006@qq.com;yingzhuo@swu.edu.cn
电话:023-68253172;传真:023-68253172 地址:重庆北碚天生路2号西南大学化学化工学院
Research and Application of Analytical Technique on δ18Opof Inorganic Phosphate in Soil
ZHANG Han,WANG Jia-Ni,ZHU Yong-Guan,ZHANG Xian*
(Key Laboratory of Urban Environment and Health,Institute of Urban Environment, Chinese Academy of Sciences,Xiamen 361021,China)
Analytical technique on oxygen isotope composition of phosphate in soil has important applications in biogeochemical research.As the composition of the soil is complex with multiple oxygen sources,a liable phosphate enrichment and purification technology is important for phosphate oxygen isotope research.Here wepresented a protocol on the analysis of the δ18Opof inorganic phosphate in soil,and phosphate was purified with multiple mineral precipitations and finally precipitated as silver phosphate.The efficiency of NH4OH purification method was examined and the purity of the product was verified through XRD and element analysis.The result showed that treatment of the Ag3PO4sample by recrystallizing with ammonia could remove the impurity efficiently without significantly modifying oxygen isotope compositions.The validity of sample processing and reliability of isotope analyses were confirmed by processing a KH2PO4standard in parallel with soil P sample.The analytical result of three soil types indicated that this method provided good precision of 0.2‰.The differences of δ18Opbetween three soils groups are significant(From 15.2‰ to 19.5‰)and can be used to tracing P sources.
Soil;Inorganic phosphate;Silver phosphate;Oxygen isotope composition
26 July 2014;accepted 12 October 2014)
2014-07-26收稿;2014-10-12接受
本文系中国科学院知识创新工程青年人才领域前沿项目(No.IUEQN-2012-02)、国家自然科学基金(No.21207126)、福建省自然科学基金(No.2011J05033)资助
*E-mail:xzhang@iue.ac.cn
10.11895/j.issn.0253-3820.140637
