孤立性浆细胞瘤的临床病理表现及鉴别诊断
2015-06-23杜新全
谢 静,杜新全,杨 朋,杨 超
(四川省第四人民医院 a.病理科,b.检验科,c.放射科,成都,610016)
孤立性浆细胞瘤的临床病理表现及鉴别诊断
谢 静a,杜新全a,杨 朋b,杨 超c
(四川省第四人民医院 a.病理科,b.检验科,c.放射科,成都,610016)
目的 观察孤立性浆细胞瘤的临床特征、影像表现、病理诊断,探讨其诊断和鉴别诊断。方法 对6例孤立性浆细胞瘤作临床、影像和病理观察及随访。结果 6例浆细胞瘤患者年龄36~66岁(平均年龄51岁),男性多见,多发生于鼻腔和椎骨,影像学常表现为患处软组织肿块影并伴有邻近骨质破坏。镜下表现为:肿瘤细胞弥漫性浸润,由不同分化程度的肿瘤性浆细胞构成,分化成熟的瘤细胞形似正常浆细胞,分化不成熟的瘤细胞形似中心母细胞。免疫表型:①6例之瘤细胞均表达CD138,均不表达CD20;②6例均呈lg轻链限制性表达[(Kappa(+)/lambda(-)];③4例表达CD79a、CD56,2例表达MUM-1;④Ki-67阳性率为10%~20%。结论 孤立性浆细胞瘤的临床及影像的表现有一定特点,但并不十分特异,仅靠这两者容易发生漏诊或误诊,必须要做病理活检及相关免疫组化,只有通过三者的结合,才能最终确定其诊断;同时病理诊断浆细胞瘤时应注意与反应性增生、淋巴瘤、低分化癌、恶性黑色素瘤、鼻硬结病等相区别。
孤立性浆细胞瘤;髓外浆细胞瘤;临床病理;免疫表型;鉴别诊断
浆细胞瘤(solitary plasmacytoma,SP)是以浆细胞单克隆增生为特征的恶性肿瘤,临床上少见,国外报道占所有浆细胞疾病的5%~10%[1],易发生漏诊、误诊。最新版WHO将SP分为骨孤立性浆细胞瘤(solitary plasmacytoma of bone,SPB)和骨外(髓外)浆细胞瘤[extraossecus(extramedullary)plasmacytoma,EMP][2]。本研究收集SP 6例,含EMP 2例,SPB 4例,分析该肿瘤的临床及影像学特点,研究其病理表现及免疫组化特点,以提高对该疾病的临床影像、病理表现,及病理的相关鉴别诊断的认识。
1 资料与方法
1.1 一般资料 收集我院病理科2009~2014年6例SP的外检档案资料,包括EMP 2例及SPB 4例。均符合美国国立综合癌症网络(NCCN)SP的最新诊断标准:①组织病理学证实为单发的克隆性浆细胞增殖:②骨髓象正常,浆细胞比例小于5%~10%;③全身X射线、MRI、PET-CT等影像学检查无远处骨受累,无多发病灶,可伴有病灶区邻近骨受侵;④无终末器官受损害如高钙血症、浆细胞瘤导致的肾功能不全、贫血或骨质损害;⑤不出现或仅表现为低水平的血清及尿单克隆蛋白,并保持免疫球蛋白水平大致正常[2]。排除多发性骨髓瘤(MM)及其他疾病。
1.2 方法 采用回顾性分析患者临床病理资料,包括患者一般情况、现病史、主要临床表现、神经受累情况、手术方式与手术进行情况,手术后放、化疗等。以书信、电话形式进行随访,每半年进行一次,随访时间截止2015年2月10日。
2 结果
2.1 临床表现 6例浆细胞瘤患者年龄36~66岁(平均年龄51岁)。2例EMP均为女性,年龄分别为36岁和51岁,均原发于鼻腔,临床表现为鼻腔胀痛伴鼻塞,偶有鼻出血。纤维鼻咽镜示:鼻腔新生物:息肉?肿瘤?鼻中隔偏曲;影像学检查表现为软组织块影,邻近骨质破坏。均采用手术切除术后放化疗(具体方案不详)。随访8~60个月,1例复发,1例目前情况较好。4例SPB均为男性,年龄50~66岁,平均58岁;其中发生于胸椎2例,骶骨1例,肋骨1例,均表现为局部肿胀、疼痛,其中骶骨处病变者出现疼痛麻木不适逐渐向左下肢放射痛。影像学检查为软组织块影,邻近骨质破坏。均采用手术切除加放化疗(具体方案不详)。随访8~60个月,2例死亡,1例转变为MM,1例情况良好。
2.2 影像学资料 2例鼻腔EMP鼻窦CT示:双侧鼻腔软组织密度影填充,骨性组织吸收(图1)。4例SPB X射线均表现为溶骨性破坏;CT显示骨皮质变薄及骨质虫噬状破坏,部分出现骨旁软组织影;MRI则出现信号失均,T1加权像低信号,T2加权像稍高信号,增强扫描有不均匀强化,肿瘤直径2~7 cm;其中1例发生于骶骨者CT及MRI示骶椎巨大软组织占位病变,呈膨胀性生长,临近骶椎、左侧髂骨骨质吸收破坏(图2a、2b);PET-CT未发现其他部位病灶。
2.3 组织学改变
2.3.1 巨检 6例均表现为局部新生物,呈息肉样,灰白或灰红,切面灰白,质脆,呈鱼肉样或胶冻状,可见出血区,其中部分包含少许碎骨组织。

图1 EMP CT表现
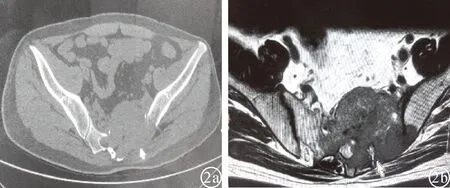
图2 SPB影像学改变 a:CT;b:MRI
2.3.2 镜下表现 肿瘤组织由不同分化程度的肿瘤性浆细胞弥漫分布(图3a)。分化成熟的瘤细胞似成熟浆细胞,细胞中等偏小,呈卵圆形,胞浆丰富,嗜碱性,核偏位,染色质呈轮辐状排列,核周有空晕(图3b);分化不成熟的瘤细胞似中心母细胞或免疫母细胞,细胞中等或较大,呈圆形,胞质中等或稀少,嗜碱性,细胞界限欠清,核大而不规则,核质比例增大,核膜厚,染色质分散,可见一个大而明显的中位核仁或数个嗜碱性小核仁,异型性明显,核分裂象易见(图3c)。肿瘤间质可见富含血管的纤维结缔组织、血湖及淀粉样物质沉积。可见坏死。
2.4 免疫表型检测 6例SP中瘤细胞均呈CD138(+)、Kappa(+)/lambda(-);而CD20、CD3、CK、S-100及HMB-45均呈阴性表达;4例CD79a(+)、CD56(+),2例MUM-1(+);Ki-67阳性率10%~20%,见图4。
3 讨论
3.1 SP的临床及影像特点 SP临床上少见,总结其临床表现主要有:①好发年龄与性别:多为中老年男性,本组研究中SP的平均发病年龄为51岁,男女比2∶1,其中个别发生于较年轻女性,本组SPB发病年龄较EMP稍大;②发病部位:SPB多发于躯干骨,尤以脊柱多见;EMP多发生于中线面部,最常见于鼻腔、鼻窦部。文献报道,90%的EMP发生于头颈部,特别是上呼吸道如鼻腔、鼻窦、口咽部、唾液腺、喉部,其次好发于胃肠道,少见部位有睾丸、膀胱、尿道、乳房、卵巢、甲状、眼眶、大脑和皮肤[4~7]。③临床表现:SPB多出现患处的肿胀、疼痛,骶尾部则易出现神经感觉的异常;EMP以鼻阻、鼻衄最为常见,部分常与鼻息肉表现相似,容易发生漏诊、误诊,延误病情。④影像学检查:一般表现为患处软组织块影,常伴有邻近骨质破坏,因SP临床罕见,影像科医生一般不易考虑到此病,而且单凭影像学检查很难准确诊断,需行病理活检才能进一步明确;⑤部分SP可转化为MM。文献报道[8]很多病例随访后可发展成为MM。⑥SP临床及影像虽具有一定特点,但其表现并不特异,仅靠这两者容易发生漏诊或误诊,因此必须要做病理活检及相关免疫组化检查,只有通过三者的结合,才能最终确定其诊断。3.2 SP的组织学表现及免疫组化特点 SP的组织学表现为:肿瘤组织由单一的肿瘤性浆细胞组成,弥散分布,瘤细胞分化程度不一,分化好者瘤细胞形态似正常浆细胞;而分化差者瘤细胞异型性明显,核分裂像多见。因此应行免疫组化做进一步鉴别诊断。
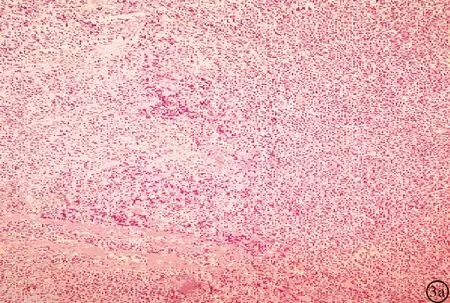


图3 SP镜下表现(HE染色) a:低倍镜下肿瘤性浆细胞弥漫分布(×40);b:分化成熟的瘤细胞似正常浆细胞(×400);c:分化不成熟的瘤细胞异型性明显(×400)



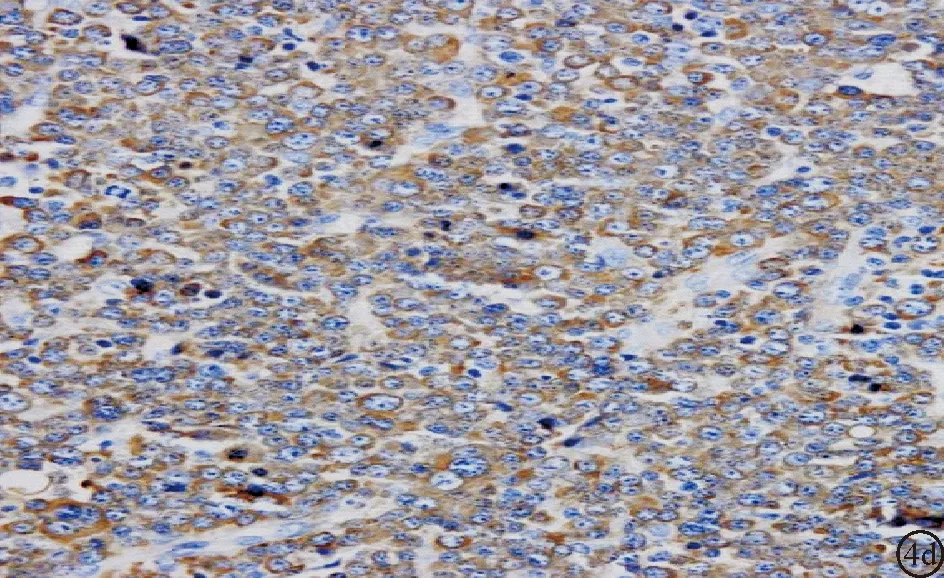

图4 SP瘤细胞的免疫表型(×400) a:CD20(-);b:CD138(+);c:CD79a(+);d:Kappa(+);e:Lambda(-)
SP的免疫组化特点:①主要表达一种轻链蛋白Kappa或lambda,即轻链限制性表达[8];本组研究对象中均为Kappa(+)/lambda(-)的表达模式,未出现Kappa(-)/lambda(+)的情况可能与病例数偏少有关系。②CD138和CD79a具有较高的敏感性;本组100%表达CD138,80%表达CD79a。③SP出现CD56的异常表达,而大部分浆细胞白血病CD56阴性[7,8];本组80%出现CD56阳性。④几乎总是CD20阴性,病变中若出现CD20阳性表达的淋巴细胞或浆细胞样细胞,则诊断更倾向于淋巴瘤[7,8];本组CD20全部为阴性。⑤Ki-67表达水平一般不高[9],本组为10%~20%,与报道一致。
3.3 SP的鉴别诊断 SP与MM:SP的诊断需要与MM的粘膜和骨转移相鉴别,血、尿生化检查,全身骨骼影像学检查和骨髓活检是鉴别诊断的主要手段。
SP与浆细胞反应性增生的鉴别:免疫组化对鉴别高分化SP与浆细胞反应性增生很有帮助。因SP为单克隆性增生,其免疫组化表现为轻链限制性表达;而反应性浆细胞增生为多克隆性增生。本组病例其中1例EMP患者行左侧下鼻甲新生物切除术,术后外院病检结果考虑增生淋巴细胞,但一年半后,患者鼻阻、鼻衄症状明显加重,再次活检才提示浆细胞瘤。因此HE染色下的形态学非常重要,只有想到这个疾病与相关鉴别诊断,再结合免疫组化才能做出正确的诊断。
SP与淋巴瘤的鉴别:两者形态学均表现为弥漫性病变,需依靠免疫组化染色进行鉴别,如CD3、CD20、CD38、CD138等。低分化SP与低分化癌、恶性黑色素瘤的鉴别:部分在形态学上难以鉴别,需借助免疫组化染色,如CK、HMB45、S-100等才能做出正确的诊断。
SP与鼻硬结病的鉴别:鼻硬结病的临床表现与发生于鼻、喉的EMP相似,但前者更常见于年轻人,并有地域性分布趋势。组织学上,病变早期可有大量浆细胞浸润,Mikuliz细胞不明显,易误诊为浆细胞肉芽肿,或慢性炎症伴大量浆细胞浸润,但随着病变的发展,病变内可见到Mikuliz细胞,且通过培养或特殊染色可见硬结病杆菌,此点有助于二者的鉴别[10]。
3.4 SP的治疗与预后 国内的大部分学者认为SP患者在有足够安全缘时,应先手术扩大切除病灶后再加放疗和/或化疗。短时间内孤立瘤灶的数量增加,或放疗后短期内多次复发,提示需要系统性化疗和/或自体造血干细胞移植。参照MM的治疗方法可使SP获得长期的疾病控制[11]。由于MM的不可治愈性及造血干细胞移植后较高的复发率和死亡率,近几年,免疫治疗MM日益成为研究热点[12]。包括T细胞、树突状细胞、NK细胞以及抗CD38单抗等免疫治疗方法的体内、外研究提示,目前已有成功案例的报道[13]。
有文献报道,35%~50%SP可向MM进展,平均进展时间为2~3年,局部复发概率为4.3%[14]。因此,对SP患者应长期随访,并定期进行影像学及实验室检查以排除MM,若显示已进展为MM则应及早给予有效的系统治疗,以达到控制病情、改善患者生存质量的目的。
[1] Dagan R,Morrls CG,Kirwan J,et al.Solitary plasmacytoma[J].Am J Clin Oncol,2009,32(6):612-617.
[2] Sw erdlow SH,Campo E,Harris NL,et al.WHO classification of tumours of haematopoietic and lymphoid tissues[M].IARC:Lyon,2008:200.
[3] Anderson KC,Alsina M,Bensinger W,et al.NCCN clinical practice guidelines in oncology:multiple myeloma[J].J Natl Compr Canc Netw,2009,7(9):908-942.
[4] Belic B,Mitrovic S,Arsenijevic S,et al.Nasal septum extramedullary plasmacytoma[J].Vojnosanit Pregl,2013,70(2):221-224.
[5] Erdogan BA,Sekercan O,Dursun N,et al.Extramedullary plasmacytoma of maxillary sinus[J].J Craniofac Surg,2013,24(1):85-87.
[6] Puliga G,Olla L,Bellisano G,et al.Solitary extramedullary plasmacytoma of the thyroid gland associated with multinodular goiter:case report and review of the literature[J].Pathologica,2011,103(3):61-63.
[7] 刘晋湘,羊娟.鼻腔浆细胞瘤1例报告[J].实用医院临床杂志,2010,7(4):173.
[8] Hawkesford MP,Bowey AJ,Rao J,et al.Synchronous presentation of Gaucher disease and solitary plasmacytoma with progression to multiple myeloma[J].Scott Med J,2011,56(4):236.
[9] 刘彤华.诊断病理学[M].第3版.北京:人民卫生出版社,2012:782.
[10]Valtz NL,Hayes TE,Norregaard T,et al.An embryonic origin for medulloblastoma[J].New Biol,1991,3(4):364-371.
[11]Ashraf MJ,Azarpira N,Khademi B,et al.Extramedullary plasmacytoma of the nasal cavity repon of three cases with review of theliterature[J].Iran Red CrescentMed,2013,15(4):363-366.
[12] Schlude C,Beckhove P.Immunology and immunotherapeutic approaches in multiple myeloma[J].Recent Results Cancer Res,201l,183:97-109.
[13]Yang Bo,Wang Ji,Cai Li-li,et al.Treatment of multiple solitary plasmacytomas with cytokine-induced killer cells[J].Cytotherapy,2014,16(2):278-284.
[14] D'Aguillo C,Soni RS,Gordhan C,et al.Sinonasal extramedullary plasmacytoma:a systematic review of 175 patients[J].Int Forum Allergy Rhinol,2014,4(2):156-163.
The clinicopathologic manifestations and differential diagnosis of solitary plasmacytoma
XIE Jinga,DU Xin-quana,YANG Pengb,YANG Chaoc
R446.8
B
1672-6170(2015)06-0127-04
2015-06-05;
2015-07-24)
