超高效液相色谱法测定半夏不同炮制品中核苷类成分含量*
2015-06-15何丹杨林秦少容张景勍
何丹,杨林,秦少容,张景勍
超高效液相色谱法测定半夏不同炮制品中核苷类成分含量*
何丹1,杨林2,秦少容3,张景勍1
(1.重庆医科大学药学院,重庆 400016;2.重庆医药高等专科学校药学系,重庆 401331;3.太极集团重庆涪陵制药厂有限公司,重庆 408000)
目的 建立以超高效液相色谱(UPLC)法测定不同炮制工艺半夏中尿苷、鸟苷和腺苷含量的方法。 方法 色谱柱为ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm),流动相为水-甲醇,梯度洗脱,柱温30 ℃,流速0.5 mL·min-1,检测波长254 nm。 结果 尿苷在2.214~22.140 μg·mL-1浓度范围内线性关系良好,回归方程为:Y=93 991X-1 653(r=0.999 9),平均回收率为99.18%,RSD=2.40%;鸟苷在1.212~12.120 μg·mL-1浓度范围内线性关系良好,回归方程为:Y=61 542X-806(r=0.999 9),平均回收率为98.88%,RSD=1.16%;腺苷在0.245 2~2.452 0 μg·mL-1浓度范围内线性关系良好,回归方程为:Y=14 994X-145(r=0.999 9);平均回收率为98.66%,RSD=0.97%。结论 该方法准确、快速,能有效地测定不同炮制工艺半夏中尿苷、鸟苷和腺苷的含量。
半夏;炮制工艺;核苷;色谱法,超高效液相
半夏为天南星科植物半夏[Pineliaternate(thumb.)Breit.]的干燥块茎,首载于《神农本草经》,性温,味辛,有小毒,归脾、胃、肺经。具有燥湿化痰,降逆止呕,消痞散结之功效[1]。半夏含有有机酸类、核苷类、生物碱类等化学成分[2]。生半夏有一定的毒性,内服需炮制后使用。根据不同的炮制工艺,炮制品又分为姜半夏、清半夏和法半夏等多种。《中华人民共和国药典》2010年版规定半夏及清半夏药材的质量控制均采用电位滴定法测定其总有机酸的含量[1],以琥珀酸量计算。目前关于半夏含量测定的文献报道有生物碱类成分[3]、有机酸[4]、氨基酸[5]、核苷[6]和多糖[7]成分的测定。其中核苷类成分是半夏药材中较为重要有效成分,含量较高的有尿苷、鸟苷和腺苷[8]。而报道的对半夏药材及饮片中核苷类成分的测定多采用高效液相色谱法(high performance liquid chromatography,HPLC)法和毛细管电泳法。HPLC法测定时间长,毛细管电泳法用内标法,操作繁琐[9-11]。笔者目前未见采用超高效液相色谱(ultra performance liquid chromatography,UPLC)法对不同炮制工艺半夏药材中核苷类成分进行测定比较的报道,故采用UPLC法进行了相关研究。该方法快速、准确,重复性和精密度良好,能够为半夏及不同炮制品的质量控制提供依据。
1 仪器与试药
1.1 仪器 Waters ACQUITY UPLC(美国Waters公司);ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm)色谱柱(美国Waters 公司);AG 135型电子分析天平(瑞士Mettler toledo公司)。
1.2 试药 半夏药材(甘肃天水,经重庆太极集团质检部杨修齐研究员鉴定为天南星科植物半夏Pinelliaternata的干燥块茎);尿苷对照品(中国食品药品检定研究院,批号:110887-200202);鸟苷对照品(上海同田生物有限公司,含量:98%,批号:12111835);腺苷对照品(中国食品药品检定研究院,批号:110879-200202)。甲醇(色谱级,美国默克公司),实验用水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱为ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm);柱温30 ℃;流动相为水-甲醇,按表1梯度洗脱;检测波长254 nm;流速0.5 mL·min-1;进样量5 μL,理论板数按尿苷峰计算不低于4 000。
2.2 对照品储备液的制备 ①精密称取尿苷对照品22.14 mg,置100 mL量瓶中,加水溶解并稀释至刻度,摇匀,得浓度为221.4 μg·mL-1尿苷对照品储备液。②精密称取鸟苷对照品12.12 mg,置100 mL量瓶中,加水溶解并稀释至刻度,摇匀,得浓度为121.2 μg·mL-1鸟苷对照品储备液。③精密称取腺苷对照品24.52 mg,置100 mL量瓶中,加少量甲醇溶解,再加水稀释至刻度,摇匀,得腺苷对照品储备液。精密吸取该储备液1 mL,置10 mL量瓶中,加水稀释至刻度,摇匀,得浓度为24.52 μg·mL-1腺苷对照品溶液。④精密吸取尿苷对照品储备液、鸟苷对照品储备液和腺苷对照品溶液各5 mL,置50 mL量瓶中,加水稀释至刻度,摇匀,得混合对照品溶液。
2.3 供试品溶液的制备 姜半夏:取半夏1 kg,加入饮用水浸泡72 h,8 h换水一次;加入生姜共煎,生姜用量为25%;加入8倍量水,分别90 ℃温浸2次,第1次3 h,第2次2 h,合并减压浓缩至510 mL。取1 mL浓缩液,加水稀释至25 mL,经内径0.22 μm微孔滤膜滤过,收集续滤液即为姜半夏供试品溶液。
清半夏:取净半夏1.5 kg,用8%白矾水溶液浸泡,至内无干心,口尝微有麻舌感,取出,洗净,干燥。筛去碎屑。取清半夏1 kg,加入8倍量水,温浸2次(90 ℃),第1次3 h,第2次2 h,合并减压浓缩至510 mL。取浓缩液1 mL,加水稀释至25 mL,经内径0.22 μm微孔滤膜滤过,收集续滤液,即得清半夏供试品溶液。
法半夏:取净半夏1.5 kg,大小分开,用水浸泡至内无干心。取甘草225 g,加水煎煮2次,合并煎液,倒入用生石灰150 g制成的石灰液中,搅匀,加入上述已浸透的半夏,浸泡,每日搅拌1或2次,并保持浸泡液pH>12,至剖面黄色均匀,口尝微有麻舌感时,取出,洗净,阴干或烘干,即得。取法半夏1 kg,加入8倍量水,分别90 ℃温浸2次,第1次3 h,第2次2 h,合并减压浓缩至510 mL。取浓缩液1 mL,加水稀释至25 mL,经内径0.22 μm微孔滤膜滤过,收集续滤液即为法半夏供试品溶液。
2.4 线性关系考察 精密量取混合对照品溶液1,2,4,6,8,10 mL,置10 mL量瓶中,加水稀释至刻度,摇匀,即得系列混合对照品溶液。按“2.1”项色谱条件测定,以峰面积(Y)对浓度(X,μg·mL-1)进行线性回归。尿苷的回归方程为:Y=93 991X-1 653(r=0.999 9);鸟苷的回归方程为:Y=61 542X-806(r=0.999 9);腺苷的回归方程为:Y=14 994X-145(r=0.999 9)。结果表明,尿苷浓度在2.214~22.140 μg·mL-1范围内与峰面积呈良好的线性关系;鸟苷浓度在1.212~12.120 μg·mL-1范围内与峰面积呈良好的线性关系;腺苷浓度在0.245 2~2.452 0 μg·mL-1范围内与峰面积呈良好的线性关系。
2.5 精密度实验 按样品溶液制备色谱条件制备清半夏样品溶液,按“2.1”项方法连续进样6次,测定峰面积。结果尿苷、鸟苷和腺苷的RSD分别为0.55%,1.28%和1.36%,符合精密度实验要求。
2.6 稳定性实验 按样品溶液制备方法制备清半夏样品溶液,室温下放置0,1,2,4,6,8 h,按“2.1”项下色谱条件分别进样5 μL测定峰面积。结果峰面积基本不变,尿苷、鸟苷和腺苷的RSD分别为0.65%,0.71%和0.88%,表明溶液在8 h内基本稳定。
2.7 重复性实验 按样品溶液制备方法平行配制清半夏样品6份,按“2.1”项下方法进样分析,按外标法以峰面积计算含量,尿苷、鸟苷和腺苷的平均含量分别为55.3,43.0和2.17 μg·g-1,RSD分别为0.88%,1.01%和0.93%。
2.8 加样回收率实验 取已测知含量的清半夏提取物,分别精密量取5 mL,共27份,置10 mL量瓶中,分别精密加入提取物中尿苷、鸟苷和腺苷含量约80%,100%和120%的对照品储备液,加水稀释至刻度,摇匀,滤过,取续滤液,按“2.1”项下色谱条件进样5 μL,按外标法计算回收率。结果尿苷、鸟苷和腺苷的平均回收率分别为99.18%,98.88%和98.66%,RSD分别为2.40%,1.16%和0.97% 。
2.9 不同炮制工艺半夏药材含量测定 取不同炮制工艺半夏供试品溶液,按“2.1”项下的色谱条件测定,以峰面积代入线性方程计算,3种半夏中尿苷、鸟苷和腺苷的含量结果见表2,色谱图见图1。
3 讨论
半夏因其味辛辣、麻舌而刺喉,具有“戟人咽”的刺激性,被列为有毒中药。因此应用时一般要有去毒的炮制过程。采用各种不同的炮制方法,既能降低半夏的毒性,又能扩大半夏的应用范围。临床使用多以炮制品入药,主要有清半夏、姜半夏、法半夏。现代研究认为半夏毒性主要表现为强烈的刺激性,主要由草酸钙针晶引起,由于草酸不溶于水和各种有机溶剂,但能够溶于酸、碱性溶液,而炮制辅料白矾和石灰水则分别呈一定的酸、碱性,因此炮制后草酸钙针晶被不同程度破坏,降低半夏的毒性,使其刺激性降低或消失[12]。

表2 不同炮制工艺半夏核苷含量测定
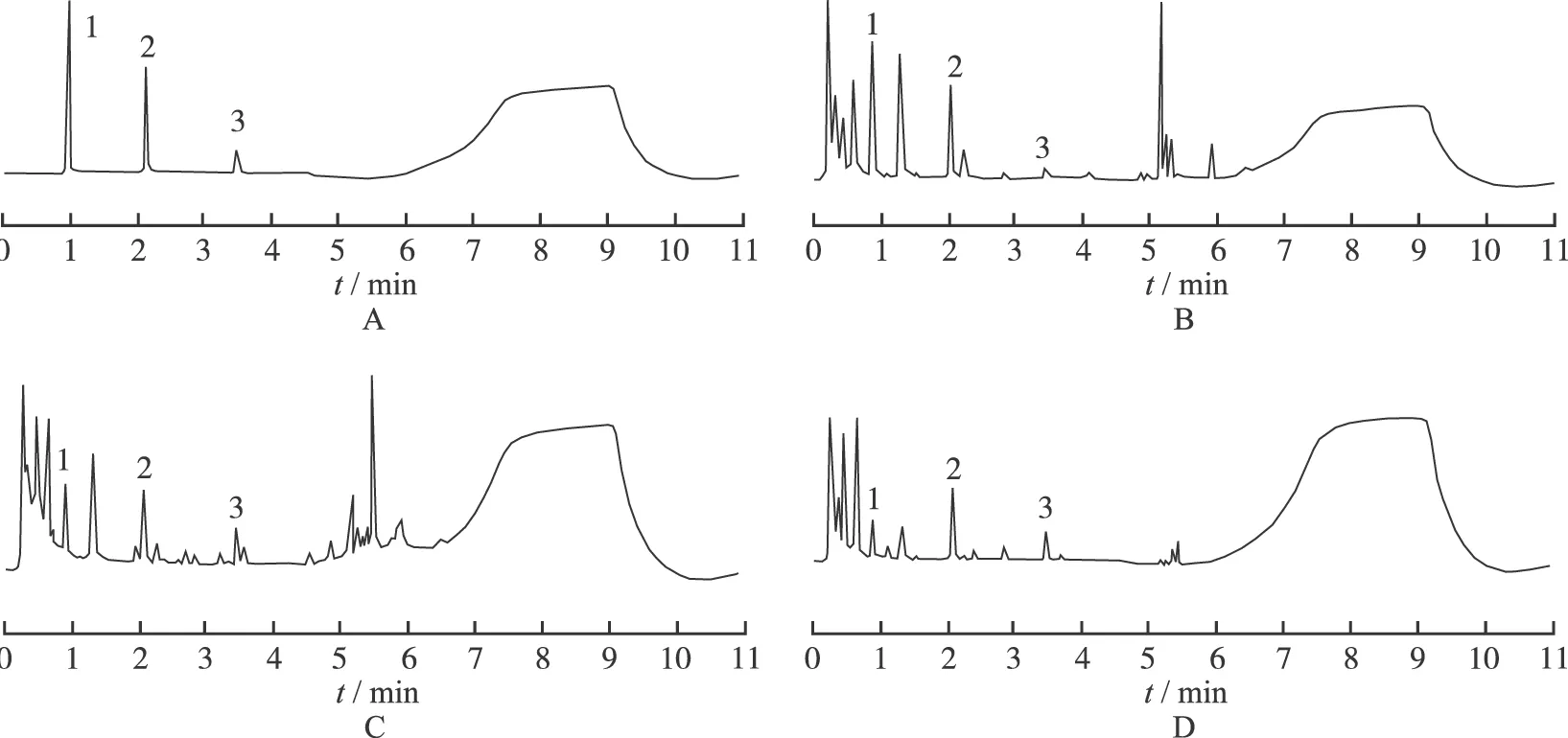
A.混合对照品溶液;B.清半夏;C.法半夏;D.姜半夏;1.尿苷;2.鸟苷;3.腺苷
A.mix standards solution;B.clearPinelliaternate;C.rhizomaPinelliaepraeparatum;D.gingerPinelliaternate;1.uridine;2.guanosine;3.adenosine
Fig.1 UPLC chromatogram of nucleosides inPinelliaternatawith different processing
半夏及清半夏的质量控制方法,《中华人民共和国药典》2010年版中采取电位滴定法对醇提取物中有机酸总量(以琥珀酸含量计算)进行含量测定,姜半夏和法半夏还没有规定含量测定项目[1]。半夏及清半夏药材质量控制指标是有机酸类化合物总量,没有具体的指标成分,且滴定法相对干扰因素较多。对半夏药材及其炮制品中水提取物的质量控制没有明确规定,但核苷的药理活性明确,在半夏药材中含量也较高,从本实验结果看,清半夏中3种核苷的总含量高达100 μg以上,同时不同的半夏炮制品核苷成分含量差异也较大。因此建立核苷类成分的测定方法对于半夏及炮制品的质量控制具有重要参考意义。
[1] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:110.
[2] 张跃进,孟祥海,许玲,等.不同炮制方法对半夏化学成分含量的影响研究[J].中国实验方剂学杂志,2008,14(12):21-23.
[3] 陈华国,汤洪波,周欣,等.半夏中总生物碱及鸟苷含量动态变化研究[J].安徽农业科学,2010,38(3):1242-1244.
[4] 王兵,李敏,卢道会,等.电位滴定法测定不同居群半夏中总酸的含量[J].中药与临床,2010,1(2):15-17.
[5] 陈文琼,余敏灵,陈文秋,等.柱前衍生RP-HPLC法测定法半夏中γ-氨基丁酸的含量[J].中国药房,2008,19(12):929-930.
[6] 张科卫,吴皓.HPLC-PDA测定小半夏汤中的核苷类成分[J].中国药学杂志,2008,43(23):1826-1828.
[7] 吴静芬,张媛媛,吉中强,等.半夏多糖的含量测定[J].中国中医药信息杂志,2006,13(10):54-55.
[8] 陈燕芹,刘红,张俊.反相高效液相色谱法同时测定半夏中尿苷鸟苷和腺苷[J].医药导报,2013,32(12):1634-1636.
[9] 赵杨,靳凤云,伍庆,等.高效液相色谱法测定贵州不同产地半夏药材中鸟苷和腺苷的含量[J].时珍国医国药,2007,18(1):23-24.
[10] 隋利强,吴水生.RP-HPLC法测定不同贮存年限半夏饮片中腺苷和鸟苷的含量[J].黔南民族医专学报,2012,25(3):157-159.
[11] 魏英勤,卢恒,刘鑫欣,等.毛细管区带电泳内标法测定半夏中鸟苷含量[J].中国实验方剂学杂志,2011,18(18):49-51.
[12] 钟凌云,吴皓,张琳,等.半夏毒性成分和炮制机制研究现状[J].上海中医药杂志,2007,41(2):72-74.
Determination of the Content of Nucleosides in Differently ProcessedPinelliaternataby UPLC
HE Dan1, YANG Lin2, QIN Shaorong3, ZHANG Jingqing1
(1.CollegeofPharmacy,ChongqingMedicalUniversity,Chongqing400016,China; 2.DepartmentofPharmacy,ChongqingMedicalandPharmaceuticalCollege,Chongqing401331,China; 3.TaijiChongqingFulingPharmaceuticalGroupCo.LTD,Chongqing, 408000,China)
Objective To establish an ultra-performance liquid chromatography (UPLC) method for detecting content of uridine, guanosine and adenosine inPinelliaternata. Methods Acquity UPLC Ben C18(2.1 mm×50 mm, 1.7 μm) was used.The mobile phase was methanol and water by gradient elution mode, and the column temperature was 30 ℃.The flow rate was 0.5 mL·min-1and the detection wavelength was 254 nm. Results The linear range of uridine was 2.214-22.14 μg·mL-1.The regression equation wasY=93 991X-1 653 (r=0.999 9).The linear range of guanosine was 1.212-12.12 μg·mL-1, and the regression equation wasY=61 542X-806 (r=0.999 9).The linear range of adenosine was 0.245 2-2.452 0 μg·mL-1, and the regression equation wasY=14 994X-145 (r=0.999 9).The average recovery was 99.18% (RSD=2.40%), 98.88% (RSD=1.16%) and 98.66% (RSD=0.97%) for uridine, guanosine and adenosine, respectively. Conclusion The method is rapid, reliable and can be used to determine nucleosides inPinelliaternate.
Pinelliaternate; Processing; Nucleosides; Chromatography, ultra-performance liquid
2014-01-10
2014-03-20
*国家科技支撑计划(2011BAI13B03)
何丹(1977-),女,四川达州人,副教授,在读博士 ,主要从事中药分析研究。电话:(0)15310985850,E-mail:ildoctor@163.com。
张景勍(1973-),女,重庆人,研究员,博士 ,主要从事药物制剂研究。电话:(0)13308300303,E-mail:zjqrae01@163.com。
R282.71;R927.2
B
1004-0781(2015)02-0231-04
DOI 10.3870/yydb.2015.02.025
