类风湿性肺病1例
2015-06-12王正东姚汉清徐兴祥姜正华
王正东 姚汉清 徐兴祥 姜正华
·病例报告·
类风湿性肺病1例
王正东 姚汉清 徐兴祥 姜正华
类风湿性肺病; 类风湿关节炎; 病例报告
类风湿性肺病是指类风湿关节炎引起的呼吸系统的改变,类风湿关节炎患者中约50%发生类风湿性肺病。据文献报道,虽然类风湿关节炎多见于女性,但出现胸膜与肺部病变者男性多于女性,约为2︰1[1]。近期我科收治了一位类风湿性肺病的男性患者,希望通过对典型病例的分析,根据临床-放射-病理诊断,同时对相关文献资料复习提高对该病的认识,避免误诊。
临床资料
患者,男性,66岁,主因“发热20余d”于2014年3月27日入住我院。发热以午后低热为主,最高体温38.0 ℃,无畏寒、寒战,伴两侧膝关节及手指关节肿痛,晨起及发热时明显,活动后缓解。时有咳嗽,咳少许白黏痰,无痰血,无明显胸痛、心慌、胸闷,就诊于当地医院。查全胸片示两肺炎症,血象偏高,C-反应蛋白、类风湿因子升高,予抗感染治疗(具体用药不详),体温未见明显好转,遂至我院拟“肺部感染”收住我科。既往有“两侧膝关节隐痛”病史5年余,一直未诊治。4年前有“胆囊切除”手术史,否认其他疾病史,有“磺胺类”药物过敏史,无烟酒等不良嗜好。入院查体:T 37.6 ℃,神志清楚,精神一般,营养中等,步入病房,全身皮肤黏膜无黄染、淤斑、色素沉着,浅表淋巴结未及肿大,口唇无紫绀,颈软,气管居中,呼吸平稳,两侧呼吸运动对称,触诊语颤正常,叩诊呈清音,听诊双肺呼吸音粗,右下肺可闻及少许湿性啰音,两肺未闻及干啰音。双手指关节活动轻度受限,双手指及双膝关节轻度浮肿。入院后查血常规:白细胞13.5×109/L,中性粒细胞86.41%。生化:白蛋白31.8 g/L,球蛋白31.7 g/L,ALT 64 U/L,C-反应蛋白180.46 mg/L,类风湿因子93 IU/ml。痰找抗酸杆菌及痰、血细菌培养、痰真菌培养均阴性,免疫球蛋白IgG 17.4 g/L。大便常规、凝血常规、肿瘤相关抗原、血沉、降钙素原、CD25、抗O、自身抗体系列、抗中性粒细胞胞浆抗体、感染性标志物、自身免疫肝病系列等指标均正常。3月28日胸部增强CT示两肺见多发斑片影,呈蜂窝样、网格样改变,边界不清,两肺纹理增重、紊乱,右上肺见钙化结节,各支气管开口通畅,纵隔居中,纵隔见小淋巴结,各房室结构大小正常。右侧胸腔少量积液,见图1。诊断为:两肺炎,右侧胸腔少量积液。给予“比阿培南0.3 q 8 h”“替考拉宁0.4 qd”联合抗感染治疗半月,但患者仍有发热,体温高峰达39 ℃。期间进一步完善相关检查,3月28日行骨髓穿刺,骨髓涂片示:骨髓增生明显活跃,粒红比值正常范围。血小板的成簇散在可见;3月30日PET-CT:双侧腋窝淋巴结放射性摄取轻度增高,脂肪肝,痔疮,颈椎胸椎腰椎骨质增生,双膝关节FDG轻度增高、双肺多发斑片影FDG代谢异常增高。抗环瓜氨酸肽抗体331.3 U/ml明显升高。4月3日行纤支镜检查,镜下未见明显异常。结合风湿科会诊意见,诊断为类风湿关节炎、类风湿性肺病。4月3日加用西乐葆 0.2 bid、爱若华10 mg qd、帕夫林0.3 bid治疗,抗风湿治疗后患者关节症状逐渐缓解,体温下降,4月8日降至正常。但4月7日复查胸部CT提示两肺病变,与2014年3月28日比较右肺病变进展,见图2。4月8日行CT引导下肺穿刺活检,病理(右肺)镜下示肺组织部分区被覆柱状上皮,部分区纤维组织增生,间质淋巴细胞等炎细胞浸润,见图3。4月10日加用甲强龙40 mg bid iv×6 d,期间患者一度出现腹泻、痰中带血,给予洛哌丁胺、小蘗碱片、复合乳酸菌胶囊止泻、调节肠道菌群以及氨甲环酸止血等对症治疗后,腹泻、痰血症状好转。体温正常3 d后4月12日将抗生素降级为美洛西林舒巴坦3.75 bid。4月14日复查胸部CT,提示两肺病变与2014年4月7日比较有吸收好转,见图4。后将激素减量为甲强龙40 mg qd iv,3d后改为口服甲泼尼龙片(美卓乐)8 mg bid,之后患者体温一直正常,关节肿痛明显好转,仅个别关节偶有疼痛。4月15日患者顺利出院。出院后患者继续服用抗风湿药物及美卓乐,5月23日患者来院复诊,患者自诉一般情况良好,未再发热,关节疼痛基本消失。胸部CT提示两肺多发性炎症治疗后,较前片(2014年4月14日)相比明显吸收好转,见图5。

图1 3-28日胸部增强CT示两肺见多发斑片影,呈蜂窝样、网格样改变,边界不清,两肺纹理增重、紊乱,右上肺见钙化结节,右侧胸腔少量积液
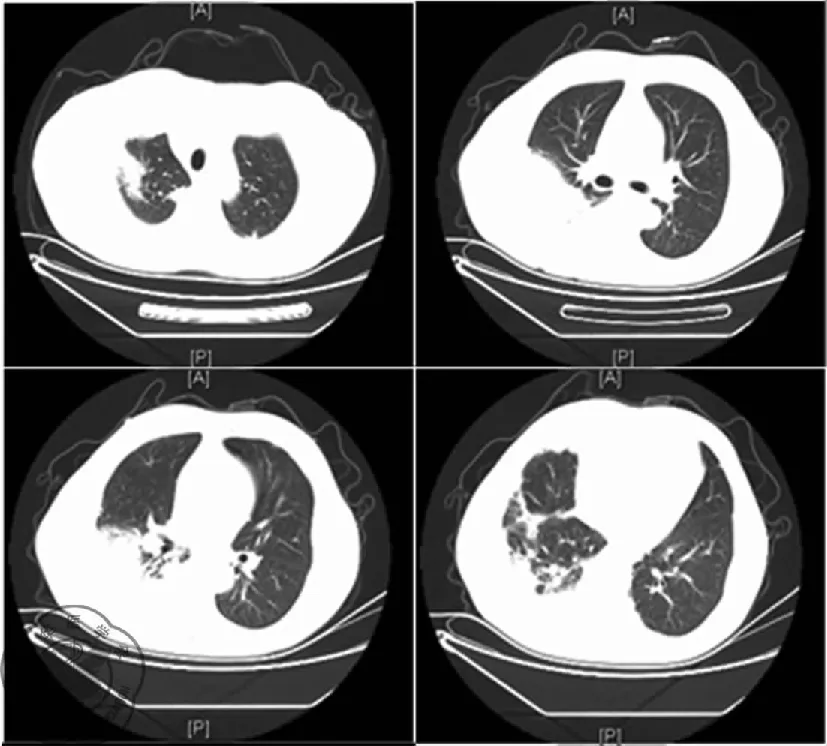
图2 4-7日胸部CT示两肺病变,与14-3-28比较右肺病变进展
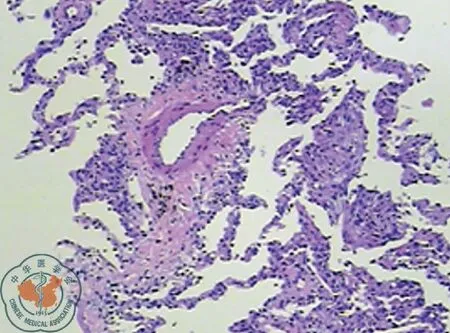
图3 4-8日肺穿刺活检病理:(右肺)镜下示肺组织,部分区被覆柱状上皮,部分区纤维组织增生,间质内见淋巴细胞等炎细胞浸润
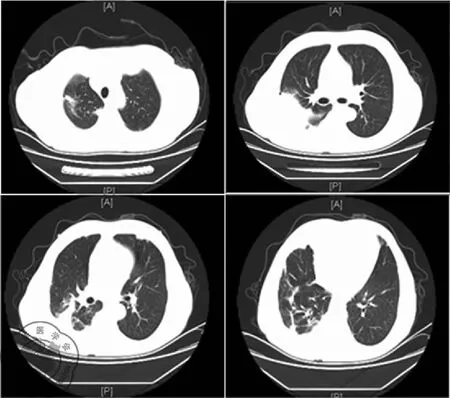
图4 4-14日胸部CT示两肺病变,与2014-4-7比较有吸收好转

图5 5-23日胸部CT示两肺多发性炎症治疗后,较前片(2014-4-14)相比明显吸收好转
讨 论
结缔组织病(connective tissue disease, CTD)是引起间质性肺病(interstitial lung disease, ILD)的常见病因。引起ILD的CTD包括类风湿关节炎(rheumatoid Arthritis, RA)、系统性红斑狼疮(systemic lupus erythematosus, SLE)、干燥综合征(sjogren′s syndrome, SS)、多发性肌炎(polymyositis, PM)、皮肌炎(dermatomyositis, DM)、系统性硬化(systemic sclerosis, SSc)和混合性结缔组织病(mixed connective tissue disease, MCTD)等多种疾病[2-3]。其中RA常常起病隐袭,有时关节肿痛症状不明显,许多患者以不明原因发热和/或ILD为首发表现就诊于呼吸内科并进一步确诊。呼吸内科诊断的CTD引起的ILD原发病以RA为主,而且相当一部分RA在呼吸内科得到确诊。RA是一种慢性全身性自身免疫性疾病。发病原因目前尚不明确,可能与感染、内分泌失调、血运障碍、免疫系统因素、遗传因素及中医学说的风湿寒邪因素有关,其发病机制是机体对抗原刺激免疫反应的结果。类风湿关节炎属于结缔组织病变(即胶原性疾病),其病变集中在身体某些器官的结缔组织的胶原纤维和基质中。由于结缔组织广泛分布于全身各处,因此,类风湿关节炎在不同时期可侵犯体内各系统器官,如肺、胸膜、血管、关节等。据统计,大约50%的类风湿关节炎患者累及到肺,临床上称之为类风湿性肺病[4]。类风湿性肺病的诊断主要从临床表现、影像学及病理学等方面综合考虑。
大多数类风湿性肺病为慢性隐匿性起病,早期一般无特殊表现,往往是在关节炎进展到相当程度之后,才开始出现肺部症状,但部分患者肺部征象发生在关节炎之前。中晚期患者可表现为进行性呼吸困难,可轻咳或阵咳,多为干咳,也可有少数白痰或痰中带有血丝。晚期常继发细菌感染,痰为脓性,量多可伴随发热,75%的患者可有杵状指或紫绀。类风湿性关节炎患者出现肺纤维化时,说明大部分肺组织已受累,易在此基础上继发低氧血症、肺动脉高压,甚至肺心病、呼吸衰竭及肾衰竭等,预后差。本例急性起病,以发热为主要临床表现,呼吸道症状不明显,隐蔽性强,追问病史,患者既往有“两侧膝关节隐痛”病史5年余,但症状轻微,一直未予诊治,入院后查常规血检及自身抗体系列均正常,故诊断不易考虑到类风湿性肺病。
类风湿性肺病在肺和胸膜所引起病变的CT特征性表现可分为以下几种[5]:①广泛性肺间质纤维化病变:A.两肺小片状或小结节阴影,直径1~2 mm,边缘清楚;B.细线或粗网状影,常代表纤维化;C.多发囊性病变,病变以膈上肺底多见,这是本病的特征。早期多呈小结节影、细线影,代表间质性肺炎;而粗网状及蜂窝状影,常是肺明显纤维化、肺实质破坏和肺结构扭曲的表现;②胸膜炎和胸腔积液;③渐进坏死性结节。本例患者胸部CT多种典型表现并存,较为少见。
类风湿性肺病病理类型最常见为普通型间质性肺炎(usual interstitial pneumonia, UIP)和非特异性间质性肺炎(nonspecific interstitial pneumonia, NSIP)[6-7],并可表现为闭塞性细支气管炎伴机化性肺炎(bronchiolitis obliterans with organizing pneumonia, BOOP)、淋巴细胞性间质性肺炎(lymphocytic interstitial pneumonia, LIP)等多种类型。少数患者可表现为急性间质性肺炎(acute interstitial pneumonia, AIP),并可并发弥漫性肺泡损伤(diffuse alveolar damage, DAD),甚至可引起缩窄性细支气管炎(constrictive bronchiolitis, CB),但较少见。UIP影像学表现较特异[8-9],为双肺弥漫分布,以肺底、胸膜下为主,病变时相不均一,蜂窝明显,少量实变和/或磨玻璃阴影。UIP支气管肺泡灌洗液(bronchoalveolar lavage fluid, BALF)以中性粒细胞增高为主,晚期可有嗜酸性粒细胞增高,是间质性肺炎中唯一可根据临床、CT表现、BALF特点诊断的类型,其他类型则必须经肺活检并结合临床、影像特点做出诊断[2]。但由于国内病理科医生对该病认识不足,仍然会报告诸如纤维组织增生,间质淋巴细胞等炎细胞浸润等。从临床、影像学及病理特点分析提示本例患者NSIP可能性大。
类风湿性肺病的治疗包括RA治疗和间质性肺炎治疗两个方面,间质性肺炎的治疗效果往往取决于病理类型,UIP患者预后往往较差,其他类型除AIP进展快、病死率高外,多数对糖皮质激素治疗较敏感,预后较好。糖皮质激素治疗以控制引起肺损伤和纤维化的炎性反应为主,一旦肺部形成纤维化后则不能逆转。激素尤其对于NSIP疗效通常较好。对于糖皮质激素反应不佳的UIP患者可联合应用环磷酰胺(CTX)治疗,能改善患者的肺功能和CT病变进展,使疾病稳定。应用泼尼松的治疗时间一般主张在1~12周。
综上所述,类风湿性肺病由于早期症状不明显,在临床工作中易被忽视或延误诊断,因此有必要提高临床医生和患者对RA所致肺损害的认识。应尽早行胸部CT扫描,特别是肺HRCT检查,可以早期了解RA浸润肺部的程度及估计预后。行肺穿刺活检获取病理可以明确病理类型,有助于进一步确诊、指导治疗并评估预后。
1 甘中亮, 周华清, 楚克付, 等. 类风湿性关节炎累及胸部的CT诊断价值[J]. 实用心脑肺血管病杂志, 2011, 19(9): 1540-1541.
2 Morgenthau AS, Padilla ML. Spectrum of Fibrosing Diffuse Parenchymal Lung Disease[J]. Mt Sinai Med, 2009, 76(1): 2-23.
3 孙耕耘. 关注结缔组织病相关间质性肺疾病[J/CD]. 中华肺部疾病杂志:电子版, 2012, 5(2):95-99.
4 施 毅. 现代呼吸病治疗学[M]. 北京: 人民军医出版社, 2002: 575-576.
5 李 鹏, 张丽波, 赵丽娜. 类风湿性肺病CT特征性表现1例[J]. 中国医学影像技术, 2009, 25(1): 88.
6 Hallowell RW, Horton MR. Interstitial lung disease in patients with rheumatoid arthritis: spontaneous and drug induced[J]. Drugs, 2014, 74(4): 443-450.
7 Kelly CA, Saravanan V, Nisar M, et al. Rheumatoid arthritis-related interstitial lung disease: associations, prognostic factors and physiological and radiological characteristics-a large multicentre UK study[J]. Rheumatology (Oxford), 2014[Epub ahead of print].
8 Assayag D, Elicker BM, Urbania TH, et al. Rheumatoid arthritis-associated interstitial lung disease: radiologic identification of usual interstitial pneumonia pattern[J]. Radiology, 2014, 270(2): 583-588.
9 Kim EJ, Elicker BM, Maldonado F, et al. Usual interstitial pneumonia in rheumatoid arthritis-associated interstitial lung disease[J]. Eur Respir J, 2010, 35(6):1322-1328.
(本文编辑:王亚南)
王正东,姚汉清,徐兴祥,等. 类风湿性肺病1例[J/CD]. 中华肺部疾病杂志: 电子版, 2015, 8(1): 103-105.
10.3877/cma.j.issn.1674-6902.2015.01.028
225001 扬州,江苏省苏北人民医院呼吸内科
姜正华,Email: toeastwang@163.com
R563
B
2014-12-19)
