多肿瘤标志物蛋白芯片检测对乳腺癌新辅助化疗的临床价值
2015-06-01朱宇熹
周 静,朱宇熹
(1.荆楚理工学院形态教研室,湖北荆门 448000;2.重庆医科大学附属第一医院肿瘤科 400016)
论著·临床研究
多肿瘤标志物蛋白芯片检测对乳腺癌新辅助化疗的临床价值
周 静1,朱宇熹2
(1.荆楚理工学院形态教研室,湖北荆门 448000;2.重庆医科大学附属第一医院肿瘤科 400016)
目的 观察多肿瘤标志物蛋白芯片检测在乳腺癌新辅助化疗治疗前后变化,以期发现敏感性较高的肿瘤标志物并评价其临床价值。方法 将40例健康体检者(对照组)与64例乳腺癌患者(试验组)进行多肿瘤标志物蛋白芯片检测,评价出具有诊断意义的指标。试验组术前采取TAC方案化疗4周期,治疗完成后3周再次进行多肿瘤标志物蛋白芯片检测,评价上述指标的临床意义。结果 癌抗原153(CA153)、癌抗原125(CA125)、癌胚抗原(CEA)、铁蛋白(FT)在试验组的阳性率分别为32%、27%、21%、19%,与对照组比较差异有统计学意义(P<0.05)。4项指标联合检测可提高检测灵敏度。化疗后试验组CA153、CA125、CEA呈显著性下降(P<0.05)。结论 CA153、CA125、CEA、FT可作为乳腺癌辅助诊断的肿瘤标志物,其中CA153、CA125、CEA与新辅助化疗疗效具有一致性,具有临床价值。
乳腺肿瘤;蛋白芯片;标志物;化学治疗
乳腺癌是全世界范围内女性常见的恶性肿瘤之一,在我国其发病率亦呈上升趋势,严重威胁女性健康。近年来越来越多的学者关注乳腺癌的早期诊断及早期治疗,因此肿瘤标志物的研究得到临床高度重视。本研究通过对照研究探讨多肿瘤标志物蛋白芯片在乳腺癌新辅助化疗中的变化,以期发现具有临床价值的肿瘤标志物,现报道如下。
1 资料与方法
1.1 一般资料 64例患者(试验组)均在2012年3月至2013年8月在荆楚理工学院第一临床学院肿瘤科治疗,均为初治女性,且经病理学检查证实为乳腺癌。年龄27~68岁,平均(41.3±13.6)岁。根据美国癌症联合委员会制订标准进行临床分期,其中ⅡA期15例,ⅡB期19例,ⅢA期13例,ⅢB期17例。所有患者均为初治患者,KPS≥70分,预计生存时间超过4个月。另 40例健康体检者(对照组)来自体检中心自愿受试者。
1.2 方法
1.2.1 仪器和试剂 多肿瘤标志物蛋白芯片采用上海数康生物公司研制开发的“C-12多肿瘤标志物蛋白芯片诊断系统”。
1.2.2 检测方法 试验组对象均在化疗开始前及治疗完成后3周采集静脉血,分离血清。多肿瘤标志物采用蛋白芯片技术,包括糖链抗原(CA19-9),神经元特异性烯醇化酶(NSE),癌胚抗原(CEA),糖链抗原242(CA242),铁蛋白(FT),β-人绒毛促性腺素(β-HCG),甲胎蛋白(AFP),游离前列腺特异性抗原(Free-PSA),前列腺特异性抗原(PSA),癌抗原125(CA125),生长激素(HGH),癌抗原153(CA153)。对照组进行一次蛋白芯片检测。
1.2.3 治疗方法 采用TAC方案化疗:阿霉素50 mg/m2,d1;多西他赛75 mg/m2,d1;环磷酰胺500 mg/m2,d1,3周使用1次;常规给予托烷司琼静注止吐,多西他赛前给予地塞米松,期间给予G-CSF升白支持。化疗2个周期后,达PR或CR者继续化疗至4个周期后手术;评价未达PR者则终止新辅助化疗行手术。终止治疗者不作为试验组对象。
1.2.4 临床疗效评价 参照WHO评估标准:CR 肿块完全消失;PR 肿块缩小50%以上;SD肿块缩小小于50%,或者增大未超过25%;PD 一个或多个病变增加25%以上,或出现新的病变。
1.2.5 肿瘤标志物的测定 测定标准均按照试剂盒参考标准比较。
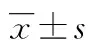
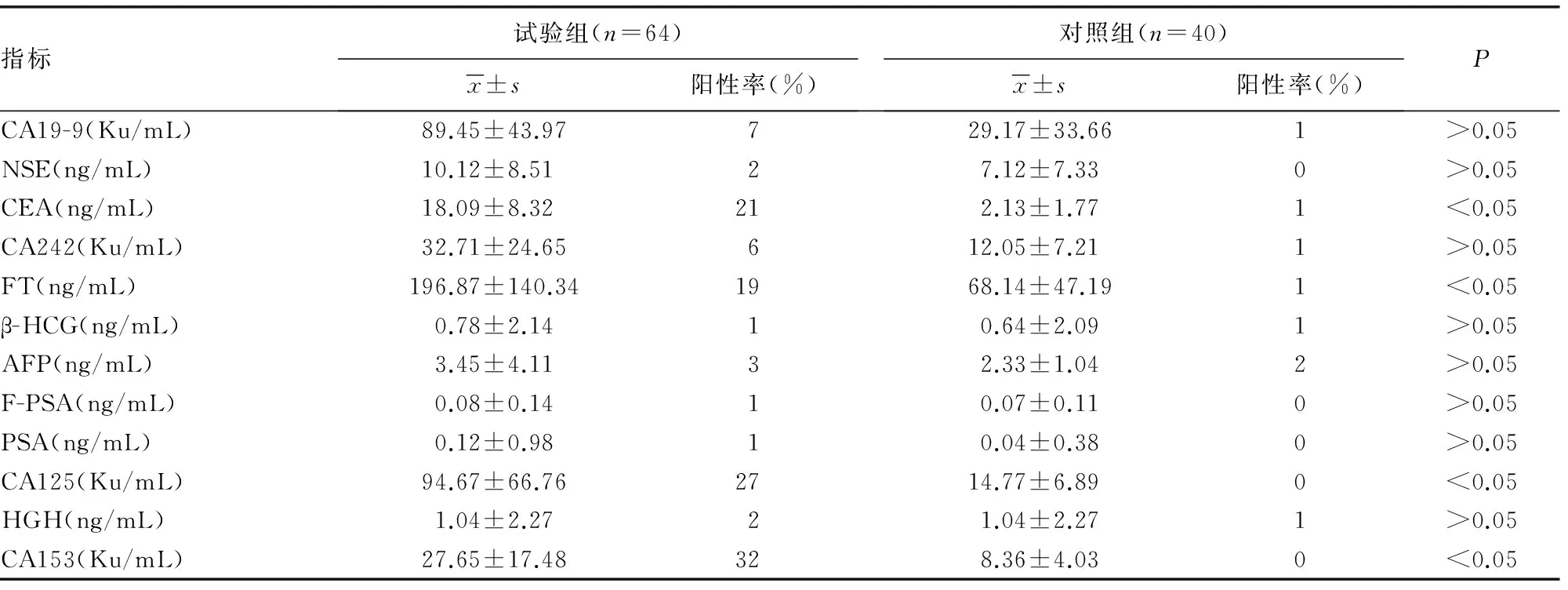
表1 两组多肿瘤标志物各项指标统计结果
2 结果
2.1 试验组与对照组蛋白芯片检测结果 对所有患者及健康体检者进行多肿瘤标志物蛋白芯片检测结果,见表1、图1。

图1 试验组16人份蛋白芯片检测结果
2.2 试验组CA153、CA125、CEA、FT及4项联合检测的价值比较 分别计算上述指标的灵敏度和特异度,与4项指标联合检查相比较,结果见表2。

表2 试验组CA153、CA125、CEA、FT及4项联合检测价值比较(%)
2.3 试验组CA153、CA125、CEA、FT治疗前后水平的变化 试验组64例患者均接受4个周期新辅助化疗,将化疗前后上述指标进行比较,结果见表3。
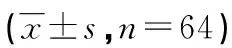
表3 试组CA153、CA125、CEA、FT治疗前后的变化
*:P<0.05,与治疗前比较。
3 讨论
肿瘤标志物由肿瘤组织产生,存在于肿瘤组织本身,或分泌至血液或其他体液中,或因肿瘤组织刺激,由宿主细胞产生而含量明显高于正常参考值的一类物质。近年来,蛋白组学及芯片技术在肿瘤临床研究中已取得引人瞩目的进展。多肿瘤标志物蛋白芯片诊断技术因其具有快速、高效、高通量的特点,已逐渐受到重视,并被广泛应用于临床[1]。
已有文献报道,应用于乳腺癌的血清标志物主要有CA153、CA125、CK19、CEA、AFP和CA19-9等,但目前还未发现可以对乳腺癌进行确诊的单一指标[2]。其中血清CA153是一种在乳腺癌中过度表达的糖蛋白抗原,也是目前公认的诊断乳腺癌比较灵敏的肿瘤标志物。有关CA153在乳腺癌中的阳性表达不同学者报道不一,黄文海等[3]报道乳腺癌患者CA153阳性率可达52.6%。另有报道CA153是监测乳腺癌患者术后复发情况的最佳指标,对乳腺癌的早期诊断和术后疗效监测均有十分重要的临床价值[4]。本研究中,试验组患者CA153阳性率为31%,与对照组比较差异有统计学意义(P<0.05)。另外完成新辅助化疗4个周期后,试验组CA153呈显著性下降趋势。结果表明CA153对乳腺癌的辅助诊断及新辅助化疗疗效判定有一定意义。
CA125是上皮性卵巢癌抗原被单克隆抗体OC125识别的一种糖蛋白,该抗原在细胞内合成和储存,当组织恶变时转出至细胞外。目前主要用于卵巢癌的诊断、术前评估及随访[5]。有文献报道,在乳腺癌患者血清中阳性率占24.0%,尤其是在伴有淋巴结转移的乳腺癌患者中,血清CA125的阳性率可达到44.6%[6]。也有研究表明CA125伴随CEA升高最常见于乳腺癌和结直肠癌[7]。本研究结果表明,乳腺癌患者CA125阳性率为27%,与报道基本一致。试验组治疗后CA125亦呈下降趋势。
CEA是一种具有人类胚胎抗原特异决定簇的酸性糖蛋白,主要存在于胚胎胃肠黏膜上皮与一些恶性组织的细胞表面,是一个广谱性的肿瘤标志物,可在多种肿瘤中表达,主要用于消化道肿瘤的诊断和疗效评定。另外在乳腺癌、肺癌及其他恶性肿瘤患者的血清中也会升高。有报道称CA153、CA125、CEA 3项肿瘤标志物联合检测能提高乳腺癌早期诊断的敏感性且有较好的特异性,具有一定的临床应用价值[8]。本研究试验组CEA阳性率为21%,化疗4个周期后亦呈显著性下降趋势。
FT是体内腺上皮细胞与中性细胞所分泌的一种糖蛋白,具有很强的铁结合能力,广泛分布于具有分泌功能的组织及其分泌物中,是人体体液中重要的蛋白成分之一。由于肿瘤会引发周围组织损伤坏死,或者含铁离子在细胞内皮系统中累积导致血液中FT升高。有报道,FT升高在恶性肿瘤患者中显著高于良性病变患者及健康体检者,肿瘤组阳性率最高,其次为良性组,不过值得注意的是0.5% 的健康体检者FT也有升高[9]。本研究结果显示,试验组FT阳性率为19%,与对照组比较差异有统计学意义(P<0.05),但在治疗前后变化差异无统计学意义(P>0.05)。
综上所述,本研究结果表明CA153、CA125、CEA、FT在乳腺癌患者的阳性率分别为32%、27%、21%、19%,与对照组比较差异有统计学意义(P<0.05)。4项联合检测可进一步提高阳性率水平,联合检测的意义优于单项检测,上述4项指标可辅助乳腺癌的诊断。同时CA153、CA125、CEA 3项指标在患者进行新辅助化疗前后的变化差异有显著性,具有辅助评价临床疗效的价值。
[1]周建光,杨梅.多肿瘤标志物蛋白芯片检测在肿瘤诊断中的临床应用及研究进展[J].中国医学检验杂志,2010,11(3):165-166.
[2]卢晓峰,张俊英,孙淑明,等.CA153、CA125、CEA、AFP联合检测在乳腺癌诊断中的价值[J].中国医药指南,2012,10(30):54-55.
[3]黄文海,陈润浩,俞建平,等.血清肿瘤标志物检测在乳腺癌诊断中的意义[J].中国临床医学,2012,19(3):323-324.
[4]庄浩.乳腺癌患者手术治疗前后血清CA15-3、CA125和VEGF检测的临床意义[J].放射免疫学杂志,2010,23(3):260-261.
[5]Aggarwal P,Kehoe S.Serum tumour markers in gynaecological cancers[J].Maturitas,2010,67(1):46-53.
[6]Dupom WD,Pad FF,Hartmann WH,et al.Breast cancer risk associated with proliferative breast disease and atypical hyperplasia[J].Cancer,1993,71(4):1258-1265.
[7]蒋萱,王东,杨雪琴,等.多肿瘤标志物蛋白诊断价值白芯片检测中CA125对恶性肿瘤的诊断价值[J].中国肿瘤临床,2012,39(9):607-610.
[8]左新华,周斌.CA153、CA125、CEA联合检测在乳腺癌诊断中的应用价值[J].中国医药科学,2011,1(10):135-137.
[9]李毅,许明芳,顾咸庆,等.多肿瘤标志物蛋白芯片检测中铁蛋白在恶性肿瘤中的诊断价值[J].重庆医学,2012,41(19):1920-1924.
The clinic value of multi-tumor marker protein chip in breast cancer with neoadjuvant chemotherapy
ZhouJing1,ZhuYuxi2
(1.MedicalSchoolofJingchuCollegeofTechnology,Jingmen,Hubei448000,China;2.DepartmentofOncology,theFirstAffiliatedHospitalofChongqingMedicalUniversity,Chongqing400016,China)
Objective To observe the evaluation of multi-tumor marker protein chip in breast cancer with neoadjuvant chemotherapy,and to find high saitivity tumor makers,then evaluate the clinical significance.Methods Forty health examination persons(control group) and sixty-four breast cancer patients(experimental group) were accepted with multi-tumor marker protein chip inspection,then we evaluated the markers of diagnosis.The experimental group patients were accepted four cycles preoperative chemotherapy with TAC plan,and tested multi-tumor marker protein chip three weeks after therapy.Then we evaluated the clinical significance of the markers above-mentioned.Results The positive rate of CA153,CA125,CEA and FT was 32%,27%,21% and 19% in the experimental group,it indicated significant change compared with the control group (P<0.05).And it indicated significant reducing change of CA153,CA125 and CEA in the experimental group (P<0.05) after therapy.The sensitivity would be increased when the four markers were tested combined.Conclusion CA153,CA125,CEA and FT could be used as assistance diagnosis index;CA153,CA125and CEA could keep consistence to the curative effect of neoadjuvant chemotherapy and have clinical value.
breast neoplasms;protein chip;tumor marker;chemotherapy
周静(1981-),讲师,硕士,主要从事肿瘤病理研究。
10.3969/j.issn.1671-8348.2015.05.031
R737.9
A
1671-8348(2015)05-0665-02
2014-09-09
2014-11-12)
