HPLC法同时测定强力脑清素片中紫丁香苷与异嗪皮啶含量
2015-03-15董芳
董 芳
(临沂市药品不良反应监测中心,山省临沂276000)
HPLC法同时测定强力脑清素片中紫丁香苷与异嗪皮啶含量
董 芳
(临沂市药品不良反应监测中心,山省临沂276000)
目的应用高效液相色谱法同时测定强力脑清素片中紫丁香苷、异嗪皮啶的含量。方法采用高效液相色谱法,Agilent SB-C18柱(4.6 mm×250 mm,5μm);检测波长265 nm;柱温:40℃;流动相A为1%冰醋酸水溶液,B为乙腈,执行梯度洗脱程序。结果系统适应性试验精密度、重复性、稳定性、回收率均符合规定,紫丁香苷与异嗪皮啶平均回收率分别为101.65%、99.37%,RSD分别为1.27%、0.94%。结论该方法简便、快速、准确、可靠,可用于强力脑清素片的质量控制。
强力脑清素片;高效液相色谱法;紫丁香苷;异嗪皮啶
强力脑清素片载于《卫生部药品标准》中药成方制剂第十七册,系由刺五加浸膏、五味子浸膏、鹿茸精等药材组成的中药复方制剂。功能为补肾健脾、养心安神。临床主要用于脾肾两虚,心神失养引起的心悸失眠,食欲不振,神疲乏力,尿频阳痿,神经衰弱,非器质性性功能衰退及妇女更年期综合症见上述证候者。因原标准中无含量测定项目,刺五加浸膏又是主要有效部位,为保证该复方制剂的临床应用有效,特在原质量标准中,增加了对刺五加流浸膏的主要成分紫丁香苷、异嗪皮啶两种有效成分的含量测定,以期达到对其质量标准提高与完善提供数据支持。本文采用高效液相色谱(HPLC)法同时测定两种有效成分的含量,并对色谱条件进行了方法学验证与考察,结果表明此法简便、准确、重现性好。
1 实验材料
1.1 样品来源 强力脑清素片(广州白云山和记黄埔中药有限公司、哈药集团三精制药四厂有限公司、亚宝药业集团股份有限公司)。
1.2 仪器与试药 Agilent 1260高效液相色谱仪:四元泵,在线脱气机,自动进样器,二极管阵列检测器(DAD);Agilent Chem Station色谱工作站;紫丁香苷(中国食品药品检定研究院,批号:111574-200603);异嗪皮啶(中国食品药品检定研究院,批号:110837-201206)。乙腈、甲醇为色谱纯、冰醋酸为分析纯。
2 方法与结果[1~10]
2.1 色谱条件 色谱柱:Agilent SB-C18柱(4.6 mm×250 mm,5μm);检测波长265 nm;柱温:40℃;流动相:A-1%冰醋酸水溶液,B-乙腈;进样量:10μL;流速:1 mL·min-1;按表1梯度程序进行洗脱,检测时间40 min。
2.2 对照品溶液的制备 精密称取对照品紫丁香苷、异嗪皮啶对照品,7.50 mg,12.32 mg,置200 mL量瓶中,加50%甲醇适量超声溶解,并定容至刻度,摇匀,得混合对照品溶液,结果见图1。

表1 梯度洗脱程序

图1 混合对照品溶液色谱图
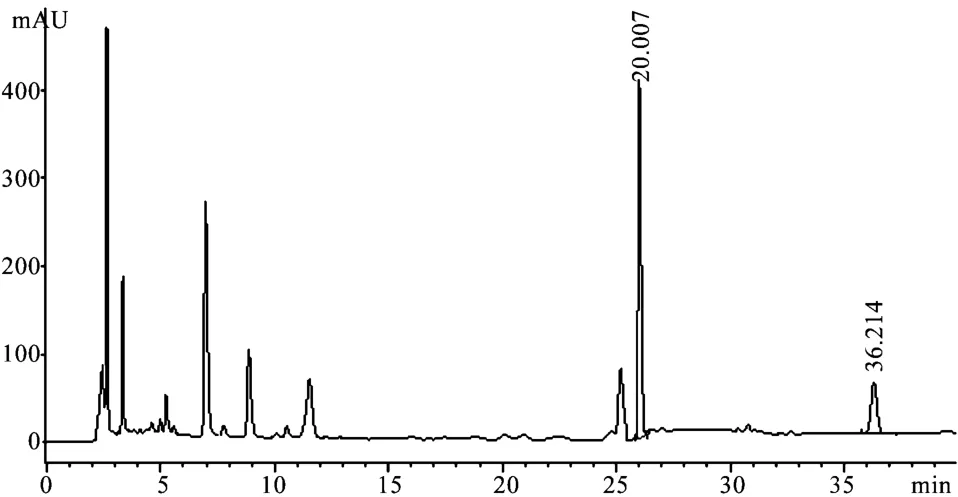
图2 样品溶液色谱图(紫丁香苷、异嗪皮啶)
2.3 供试品溶液制备 称取强力脑清素片粉碎形成的粉末0.5 g,置25 mL量瓶中,加50%甲醇20 mL,浸润,超声30 min,于室温放冷,加50%甲醇定容至刻度,摇匀,以0.45μm微孔滤膜滤过,即得,结果见图2。
2.4 标准曲线的制备 精密吸取“2.2”项下混合对照品溶液适量,分别按2、4、6、8、10、20μL进样,按“2.1”项下色谱条件测定两种组分的峰面积,以峰面积对浓度进行线性回归,绘制标准曲线,求得各自的回归方程,分别为Y=229.23X-2.347 7,r=0.999 9;Y=2 843X+32.18,r=0.999 9。结果表明两个组分在各自浓度范围内呈良好的线性关系,线性范围为0.075~0.75μg、0.123 2~1.232μg。
2.5 精密度试验 按“2.1”项下色谱条件混合对照品溶液重复进样6次,进样量10μL,紫丁香苷、异嗪皮啶的峰面积的RSD分别为0.48%、0.52%(n=6)。结果表明,仪器进样精密度良好。
2.6 重复性试验 精密称取同一批号的供试品6份,按“2.1”项下条件进行测定,计算测得紫丁香苷、异嗪皮啶含量的RSD分别为1.14%、1.17%(n=6)。
2.7 稳定性试验 取于室温放置的供试品溶液,分别于0、2、4、6、8、12、16 h进样测定。紫丁香苷、异嗪皮啶峰面积的RSD分别为1.32%、1.11%(n=6),表明供试品溶液在室温下16 h内稳定。
2.8 加样回收率试验 分别精密称取已知含量的样品粉末6份,每份精密加入混合对照品溶液2 mL,加甲醇适量,超声溶解,并定容至刻度,摇匀,以0.45μm微孔滤膜滤过,按“2.1”项下色谱条件测定各组分的含量,计算回收率。紫丁香苷、异嗪皮啶的平均加样回收率分别为101.65%、99.37%,RSD分别为1.27%、0.94%。
2.9 样品的测定 精密称取样品3批,按“2.3”项下方法制备供试品溶液。按照“2.1”项下色谱条件进行测定。根据峰面积积分值,采用外标法计算出各组分的含量,结果见表2。

表2 样品含量测定
3 讨论
考虑到两个成分要同时检出,结合DAD检测器的特性,开通220、254、265、300、320 nm 5个通道,异嗪皮啶确实最大吸收在344 nm,参照《中国药典》2010年版(一部),在220 nm测定3种成分。用3 d等吸收线,265 nm与344 nm确实吸收度有差异,因顾虑到紫丁香苷是主流质控指标,就偏向使用265 nm,也并未多开通一个344 nm的通道,也可以用可变波长方式来实现。异嗪皮啶的峰是标准品的浓度偏小,在样品中,异嗪皮啶的峰的吸收度不是很小。所以最终选择220 nm作为检测波长,本试验在综合各波长的基础上,选择265 nm作为检测波长,兼顾两种成分的检出,保证试验结果的可靠性与准确性。
目前,随着《中国药典》2010年版(一部)对多种成分控制中药质量的方法收载的频次逐步增多,多种成分同方法同时检测逐步成为质量控制的必然要求,对中药质量监控的全面性与系统性提出了更高的要求。本试验在卫生部药品标准的基础上,建立了紫丁香苷、异嗪皮啶同时测定HPLC方法,为以后该产品标准的升级与完善提供参考数据,相信随着研究的深入,以后会有更多的技术手段与方法将多药味多种成分同时测定进行整合。
[1] 叶文婷,卢绵,欧阳惠芳,等.HPLC法测定强力脑清素片中紫丁香苷含量[J].今日药学,2009,19(12):52-53.
[2] 国家药典委员会.中华人民共和国药典2010年版第三增补本[M].北京:中国医药科技出版社,2014:80.
[3] 丁海昕,韩秋云,苏海波,等.强力脑清素片质量标准研究[J].海峡药学,2008,20(4):16-19.
[4] 郑清瑗,李书渊,仇洁.强力脑清素片中异秦皮啶的含量测定[J].中药材,2003,26(11):814.
[5] 王洪杰,曲艳,邱宇虹.通过HPLC法测定异嗪皮啶含量提高强力脑清素片质量标准[J].黑龙江医药,2011,24(3):351-352.
[6] 周国平,张莉静.刺五加片中总异秦皮啶含量的高效液相色谱法研究[J].中成药,2001,23(2):92-94.
[7] 陈广耀,卢承前,马双成.反相高效液相色谱法测定刺五加片中紫丁香甙的含量[J].中国中药杂志,1999,24(8):472-473.
[8] 王龙云.黄芪刺五加片中紫丁香苷含量测定[J].中医药信息,2010,27(2):95-96.
[9] 杜波,王金杰,荆维荣.高效液相色谱法测定复方刺五加片中紫丁香苷的含量[J].黑龙江医药,2011,24(1):6-7.
[10]张崇禧,张倩,蔡恩博,等.HPLC比较刺五加茎与短梗五加茎中紫丁香苷及异嗪皮啶的含量[J].中成药,2010,32(2):254-256.
Simultaneous determ ination of syringoside and isofraxidin in Qiangli Naoqingsu Tablets by HPLC
DONG Fang
(Linyi Center for Adverse Drug Reaction Monitoring,Linyi276000,China)
ObjectiveTo establish an HPLCmethod for simultaneous determination of syringoside and isofraxidin in Qiangli Naoqingsu Tablets.MethodsHPLC method was adopted with Agilent SB-C18column(4.6 mm×250 mm,5 μm).The detection wavelength was 265 nm,the column temperature was 40℃.The mobile phase A was solution of 1% acetic acid and mobile phase B was acetonitrile by gradient elution.ResultsThe precision,repeatability,stability and recovery of system suitability test were in line with regulations.The average recoveries of syringoside and isofraxidin were 101.65%,99.37%with RSD of1.27%,0.94%,respectively.ConclusionThemethod was simple,rapid,accurate,reliable,and can be used for the quality control of Qiangli Naoqingsu Tablets.
Qiangli Naoqingsu Tablets;HPLC;Syringoside;Isofraxidin
R927.2
A
2095-5375(2015)08-0444-003
董芳,女,副主任药师,研究方向:药品检验,E-mail:271056705@qq.com
