全自动凯氏定氮仪测定干旱区土壤中全氮含量
2014-12-01李艳红
王 磊 李艳红* 袁 婕
(1新疆师范大学 地理科学与旅游学院,乌鲁木齐830054;2新疆维吾尔自治区重点实验室 新疆干旱区湖泊环境与资源实验室,乌鲁木齐830054)
0 引言
土壤肥沃的重要评定指标之一是土壤中氮的含量,氮在土壤中被认为是限制植物生长和最易耗竭的营养元素之一,土壤氮含量的多寡直接影响土壤的肥力[1]。测定土壤中元素的方法很多[2-3],但分析土壤中全氮的报道不多。随着现代仪器的发展,凯氏定氮法在教学、科研和生产实践中有着极为广泛的应用[4-5]。凯氏定氮仪普遍被各类实验室接受,用于土壤全氮,饲料粗蛋白等的测定[6]。现在尽管有很多先进的自动或半自动凯氏定氮仪,可以实现自动蒸馏,自动滴定,但由于干旱区土壤盐渍比较严重、含氮量的匮乏导致操作方法以及各试剂的用量与一般的方法有所不同,基于此,对UDK159凯氏定氮仪测定干旱区土壤全氮含量的方法、实验中的影响因素进行研究,为科研、实验教学和生产实践提供一种经济、环保和省时的氮含量测定方法。
1 实验部分
1.1 主要仪器
UDK159-全自动型凯氏定氮仪(意大利VELP公司);温控消解器:DK8S消解炉(8孔);万分之一电子天平:检定最大允许误差±0.1mg;容量瓶(100mL,1L),移液管(10mL)。
1.2 试剂
实验所用水系二次蒸馏水,试剂均系分析纯。混合催化剂(K2SO4∶CuSO4=10∶1,磨碎混匀)、氢氧化钠溶液(350~400g/L)、硼酸溶液(40g/L)、混合指示剂(甲基红∶溴甲酚绿乙醇溶液=0.7∶1)、盐酸标准溶液(0.100 0和0.100 6mol/L)、硫酸铵(氮含量为21.19%)。
1.3 实验原理
在室温下,土壤样品与催化剂和浓硫酸一同加热消解,使土壤中有机物质的氮分解,分解成氨的形式与硫酸结合成硫酸铵分子。然后在碱性条件下蒸馏使氨游离,用硼酸吸收后再以盐酸或硫酸标准溶液滴定,根据消耗的酸量,计算出氮的含量。
1.4 试样采集与处理
实验所用样品均来自于干旱区艾比湖湿地国家级自然保护区,采集土壤样品(500袋),将土壤样品进行风干、研磨、过筛(0.25mm)、标记和装袋密封处理。
1.5 实验步骤
1.5.1 样品处理
准确称取样品2.000 0g土壤样品倒入消解管中,加入7.0g混合催化剂,用量筒量取20mL硫酸缓慢倒入消解管并混匀。将消解管置于温控消解器上,起初应先设置好温控消解器程序。加热过程:在150℃下加热10min(去除样品水分),350℃下加热10min(接近硫酸沸点),420℃下加热60min(充分消解样品)。最后直至消解溶液呈清亮透明,此为CuSO4溶液的颜色。最后待样品液冷却后(50~60℃),可用全自动凯氏定氮仪进行蒸馏滴定(滴定时间一般为5min)。
1.5.2 标准溶液的标定
称取0.200 0g于270~300℃灼烧至恒重的基准无水碳酸钠,溶于50mL水中,加10滴溴甲酚绿-甲基红混合指示剂,用配好的盐酸溶液滴定至溶液由绿色变为灰红色,煮沸2min,冷却后继续滴定至溶液再呈现灰红色。终点记录盐酸溶液的用量,同时做一空白对照实验。盐酸溶液的浓度计算公式如式(1)所示。

式中:C(HCl)——盐酸标准溶液之物质的量的浓度,mol/L;
m——无水碳酸钠之质量,g;
V1——盐酸溶液之用量,mL;
V2——空白实验盐酸溶液之用量,mL;
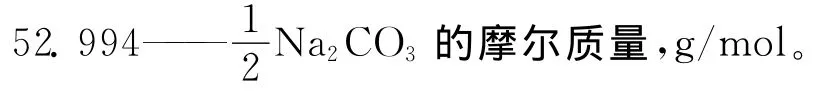
1.5.3 测定土壤样品
首先进行仪器的检查,再进行参数的设定,其次检查各容器中氢氧化钠、硼酸、蒸馏水等表液是否足够,打开冷凝水管,开启电源开关,仪器预热5min后,进行自检,设定空白、硫酸氨溶液及待测样品的参数(重量、方法、组数、编号等),设定好后进行空白溶液及硫酸氨溶液的测定,待硫酸氨校正值氮测定值为(21.19±0.2)%时,进入样品检测。即放入冷却并且消解好的样品,即可自动蒸馏、滴定。根据标准酸消耗量进行自动计算,得出结果,导出数据。土壤中全氮计算公式如式(2)所示。

式中:V—滴定试液时所用的盐酸标准溶液体积,mL;
V0—滴定空白时所用的盐酸标准溶液体积,mL;
C—盐酸标准溶液的质量浓度,mol/L;
14—氮原子的摩尔质量,g/mol;
M—风干试样质量,g。
2 结果与讨论
2.1 消解时间的选择
为考察混合法是否已把土壤中的有机物完全消解,首先对消解时间进行优化,结果见表1。由表1可以看出,消解时间过短(10~20min),则土壤样品未完全消解,致使检测结果偏低;时间过长(40~60min),测定结果也会偏低,梁芳珍等[6]研究表明可能是因为小部分氮随水蒸汽一起逸出引起的。消

表1 消解时间对测定结果的影响Table 1 Effect of digestion time on the determination of TN(n=4) /%
2.2 浓硫酸用量的选择
准确称取2.000 0g的土壤样品,加7.0g混合催化剂,改变浓硫酸的用量,按混合法消解30min,测土壤中全氮含量(表2)。结果表明:浓硫酸用量小于或等于5mL时,无法满足消解过程中所需要的酸用量,硫酸烧干与消解管紧贴,消解管中土壤样品发生碳化,最终造成测定结果偏低;当硫酸用量大于或等于25mL时,由于硫酸过量,仪器自动蒸馏时加入的氢氧化钠溶液会引起剧烈的强酸和强碱中和反应,导致大量放热,瞬间产生大量氨气无法完全冷凝吸收,导致装置漏气,以至于使结果偏低,甚至滴定不准确。因此,对于干旱区凯式定氮仪对全氮测量中硫酸用量应控制在10~15mL。解30min所测平均结果基本一致、平均偏差为0.001 0%、变异系数最为0.008 8,表明土壤中有机物在30min已完全消解,因此实验选择消解时间为30min,所测干旱区土壤中氮含量为(0.260±0.003)%(P=0.95)。
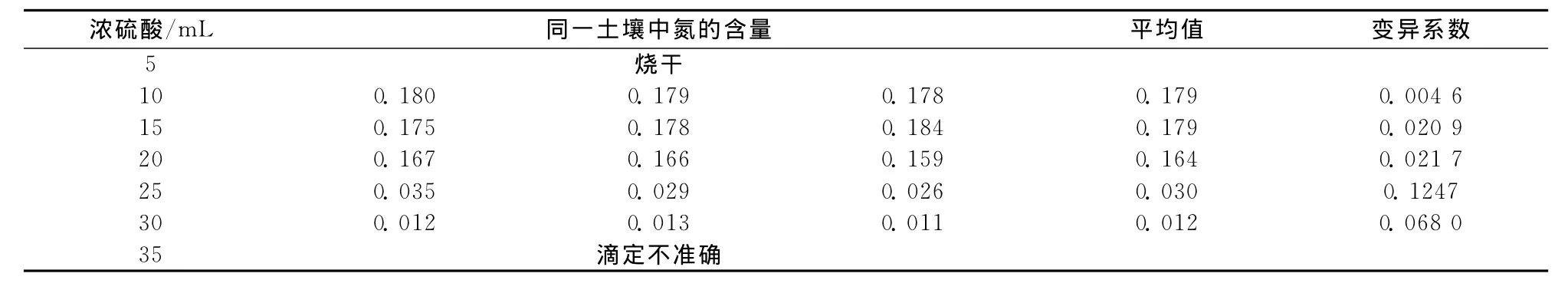
表2 浓硫酸用量不同对总氮测定结果的影响Table 2 Effect of the volume of concentrated sulfuric acid on the determination of TN /%
2.3 精密度实验
精密度实验是以氮含量为21.19%的分析纯硫酸铵为样品,硫酸铵在105℃的烘箱中烘3h,冷却后称样并直接蒸馏,测量其氮含量。分别测定6次,计算测定结果的相对标准偏差(RSD),结果见表3。由表1~6样品可知,测得的结果基本一致,相对标准偏差在0.092%~0.11%,说明仪器正常,并且本方法的准确度符合GB/T 8572—2001中规定的同一实验室测定结果的绝对差值不大于0.30%的要求。

表3 测定干旱区土壤全氮含量的实验结果Table 3Analytical results of TN in soil samples in arid area(n=6) /%
3 结语
通过对混合法测定干旱区土壤中全氮含量条件的优化,硫酸用量在10~15mL时为最佳酸用量,有机物在30min时已完全消解;NaOH标准溶液消耗体积设定在50mL;干旱区土壤中氮一般含量为(0.260±0.003)%。
采用改进凯氏定氮法,消解装置可以缩短消解时间,节约试剂的使用,明显减少了CO2,SO2,SO3等气体的排放量,既经济又环保。
[1]方万东 .氮元素在生物-地球-化学循环过程中的生态环境问题[J].陕西教育学院学报,1999(2):85-87.
[2]徐子优 .固体直接进样石墨炉原子吸收法测定土壤中镉元素[J].中国无机分析化学,2013,3(3):8-12.
[3]赵春燕 .离子色谱法测定东下冯遗址土壤中的无机阴离子[J].中国无机分析化学,2012,2(3):22-23,34.
[4]中华人民共和国卫生部,中国国家标准化管理委员会.GB/T 5009.5—2003食品中蛋白质的测定[S].北京:中国标准出版社,2004.
[5]王雅 .蛋白质测定实验的研究[J].实验室研究与探索,2005,24(4):58-59.
[6]梁芳珍 .无腺体棉仁蛋白粉kjeldahl定氮法的有效消解剂[J].中国油酯,1999,22(5):36.
