BC-6600型全自动血细胞分析仪性能评价*
2014-10-11李春碧四川省广元市中心医院检验科628000
李春碧,伏 攀(四川省广元市中心医院检验科 628000)
血细胞分析仪已广泛应用于各级临床实验室,但如果未对分析仪进行严格的性能评价、不了解仪器性能而盲目操作,将产生明显的检验误差,影响检验结果的准确性和可靠性[1]。对分析仪进行全面性能评价,有助于掌握仪器的性能。本研究以国际血液学标准委员会(ICSH)和美国临床实验室标准化委员会(NCCLS)制定的评价标准对BC-6600型全自动血细胞分析仪(简称 BC-6600型分析仪)进行了性能评价[2-3],现将研究结果报道如下。
1 材料与方法
1.1 标本来源 乙二胺四乙酸二钾抗凝静脉血标本采集自本院门诊患者。
1.2 仪器与试剂 BC-6600型分析仪、BC-5800型全自动血细胞分析仪(简称BC-5800型分析仪)及配套检测试剂、全血细胞质控物(批号BC309AN)、网织红细胞质控物(批号 ME073)均购自迈瑞公司。
1.3 方法 按照ICSH和NCCLS制定的血细胞分析仪性能评价指标,对白细胞计数(WBC)、红细胞计数(RBC)、血红蛋白(Hb)、血小板计数(PLT)、网织红细胞计数(RET)检测精密度、准确度、携带污染率、线性范围和可比性进行性能评价。
1.3.1 精密度 (1)批内精密度测定:取高、中、低值新鲜抗凝静脉血,分别使用手动进样模式和自动进样模式,连续重复测定10次,计算变异系数(CV)。要求CV在厂家标示范围内,未达到要求者,不能进行余下相关试验。厂家标示的BC-6600型分析仪各指标CV要求如下:WBC<2.5%、RBC<1%、Hb<1%、PLT<4%、RET<15%。(2)批间精密度测定:采用高、中、低值质控品,连续测定20d,计算CV。
1.3.2 准确度 选择开放全血模式,完成BC-6600型分析仪校准后,重复10次测定校准品,计算实测值均值、相对偏差(Bias),Bias=(实测值均值-靶值)/靶值×100%。要求Bias小于美国国会颁布的临床实验室修正案(CLIA′88)标准的1/2。
1.3.3 携带污染率 取高值新鲜抗凝静脉血,混合均匀后采用手动进样模式连续测定3次,测定值分别为H1、H2、H3;再取低值新鲜抗凝静脉血,混合均匀后采用手动进样模式连续测定3次,测定值分别为L1、L2、L3。携带污染率(%)=(L1-L3)/(H3-L3)×100%。
1.3.4 可比性 采用校准品对BC-5800型分析仪进行校准,并以其为靶机;随机选择经BC-5800型分析仪检测的新鲜抗凝静脉血50例,采用BC-6600型分析仪进行检测。2台分析仪均采用自动全血模式进行WBC、RBC、Hb、PLT检测。对所得数据进行线性回归分析,计算相关系数的平方值(r2)及线性回归方程。
1.3.5 线性范围 选择 WBC、RBC、Hb、PLT、RET 高值标本,按100%、80%、60%、40%、20%、10%的比例制备稀释标本,计算理论值,理论值=实际值×稀释倍数。开放全血模式下,采用BC-6600型分析仪对所有标本分别连续测定3次,计算实测值。对各指标实测值与理论值进行线性回归分析。
1.3.6 WBC分类计数评价 随机选择20例经BC-6600型分析仪检测的标本(排除采集自血液系统疾病患者的标本),每例标本制作血涂片2张,采用瑞氏-吉姆沙染液进行染色,由高年资、经验丰富的检验医师进行WBC分类计数,Bias=(仪器测定结果均值-手工测定结果均值)/手工测定结果均值×100%。
1.4 统计学处理 采用SPSS11.0软件进行数据处理和统计学分析。计量资料以()表示,组间比较采用t检验。回归分析采用线性回归分析。P<0.05为比较差异或分析参数有统计学意义。
2 结 果
2.1 精密度分析结果 BC-6600型分析仪各指标检测精密度分析结果见表1。手动进样模式及自动进样模式各指标检测精密度均在厂家标示范围内。采用相同进样模式时,批内精密度优于批间精密度,手动进样模式精密度优于自动进样模式精密度。
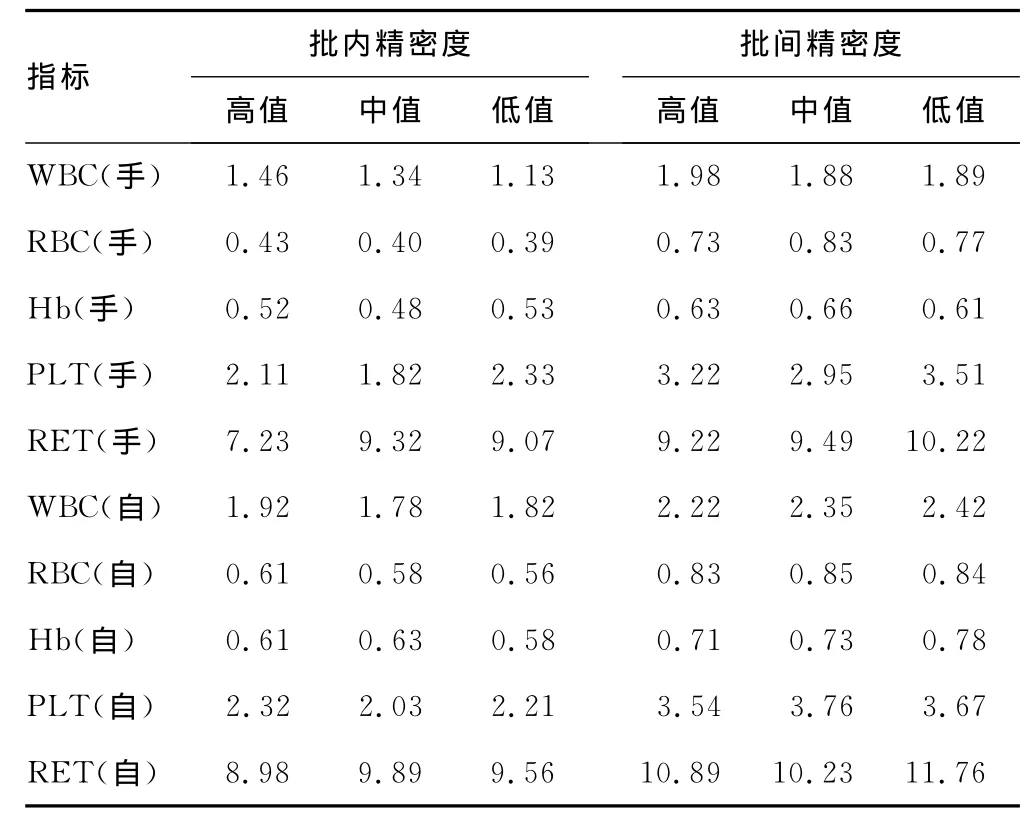
表1 BC-6600型分析仪精密度分析结果(CV,%)
2.2 准确度分析结果 WBC、RBC、Hb、PLT、RET检测Bias均小于CLIA′88要求标准的1/2,见表2。
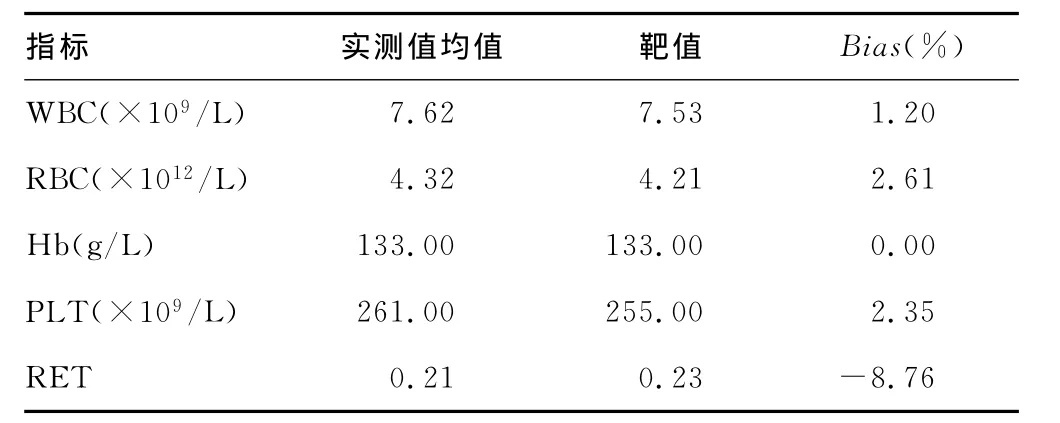
表2 BC-6600型分析仪准确度分析结果
2.3 携带污染率分析结果 WBC、RBC、Hb、PLT、RET检测携带污染率分别为0.38%、0.48%、0.00%、0.98%、0.72%,均小于1%,符合ICSH规定的要求。
2.4 可比性分析结果 线性回归分析结果显示,BC-5800与BC-6600型分析仪 WBC、RBC、Hb、PLT检测结果具有良好的相关性,见表3。t检验结果显示,2台仪器各指标检测结果比较差异无统计学意义(P>0.05)。

表3 BC-5800与BC-6600型分析仪可比性分析结果
2.5 线性范围分析结果 BC-6600型分析仪 WBC、RBC、Hb、RET、PLT检测实测值与理论值的r2均大于或等于0.97,见表4。

表4 BC-6600型分析仪线性范围分析结果
2.6 WBC分类计数评价结果 BC-6600型分析仪中性粒细胞、淋巴细胞、嗜酸性粒细胞计数结果与人工分类计数结果具有较高的相关性,单核细胞计数结果相关性稍差,嗜碱性粒细胞计数结果相关性最差,见表5。

表5 BC-6600型分析仪WBC分类计数评价结果
3 讨 论
BC-6600型分析仪采用鞘流阻抗法、激光散射法以及荧光染色流式细胞技术进行血细胞检测,Hb检测则采用比色法,可进行包括RET、有核红细胞在内的多个外周血指标检测,最高检测速度可达120例标本/小时,能够满足临床血液常规检查的需要。
本研究结果显示,BC-6600型分析仪性能良好,批内、批间精密度较高,符合相关规定。WBC、RBC、Hb、PLT检测Bias均低于行业标准(WBC<5%,RBC<2%,Hb<2%,PLT<9%)[4],也小于 CLIA′88要求标准的1/2,表明检测结果的准确度较好。各项指标检测携带污染率均小于1%,说明高值标本对低值标本的检测影响较小。虽然PLT检测携带污染率为0.98%,但仍符合符合ICSH规定的要求。WBC、RBC、Hb、PLT、RET检测线性范围基本能覆盖临床标本浓度范围,WBC检测高值可达100×109/L,低值则可达0.2×109/L;PLT检测高值可达1 000 109/L。可比性分析结果表明,BC-5800、BC-6600型分析仪各指标检测结果的相关性较好(r2>0.98),说明2台仪器检测结果具有一致性。在排除血液系统疾病患者标本的情况下,BC-6600型分析仪WBC分类计数结果与手工分类计数结果具有较好的一致性,能够足临床诊疗的需要。BC-6600型分析仪淋巴细胞计数结果小于手工计数结果,与类似研究报道一致[5],可能与分析仪无法识别异型淋巴细胞有关。
笔者在日常工作中发现,BC-6600型分析仪无法识别外周血中的幼稚细胞;对于溶血标本,无法进行红细胞各项参数检测;严重溶血时,PLT检测结果需进行手工检测验证;PLT检测结果较易受红细胞平均容积(MCV)的影响,当MCV<65fL时,PLT检测结果假性增高,且 MCV越小,影响程度越大[6]。在出现上述情况时,分析仪可能出现相应的报警信息,因此在临床工作中应注意并善于分析报警信息。手工检测RET仅能提供百分比结果,无法提供绝对计数结果,而BC-6600型分析仪则可提供绝对计数,高荧光强度(HFR)、低荧光强度(LFR)、中荧光强度(MFR)RET百分比,未成熟RET百分比和RET成熟指数检测结果,能够为判断RBC生成情况提供更敏感、准确的数据资料,有利于贫血性疾病的诊断、疗效评价、预后判断,以及骨髓造血功能和器官移植效果评价[7]。手工检测RET极易受操作人员主观因素的影响,且血涂片红细胞分布是否均匀、涂片厚薄、RNA染色效果等因素对检测结果也有很大的影响。血细胞分析仪采用对RNA有很强亲和力的染料对RET进行染色检测,避免了上述因素的影响,但仍然存在其他干扰因素。有研究显示,Howell-Jolly小体、疟原虫、冷凝集素等因素对血细胞分析仪检测RET参数产生直接干扰[8]。
手工检测作为直接观察细胞形态的传统方法,应与血细胞分析仪联合使用,从而弥补手工检测的不足[9]。本研究结果显示,BC-6600型分析仪中性粒细胞、淋巴细胞和嗜酸粒细胞计数结果与手工计数结果相关性良好;单核细胞计数结果相关性一般,嗜碱粒细胞计数结果相关性较差,可能与其在 WBC中所占比例较少有关[10]。目前,WBC分类计数的参考方法仍为人工显微镜分类计数法。因此,对于存在血细胞分析仪检测报警信息的标本,以及血液系统疾病患者和疑似疟原虫感染患者的标本,均需进行涂片检查。
综上所述,BC-6600型分析仪虽然在某些方面存在欠缺,但总体性能良好,能够满足临床诊疗的需要。
[1]郭庆昕,李焕英,张振华,等.某型号五分类血细胞分析仪性能评价[J].国际检验医学杂志,2012,33(5):595-596.
[2]International Council for Standardization in Haematology.Guidelines for the evaluation of blood cell analysers including those used for differential leucocyte and reticulocyte counting and cell marker applications[J].Clin Lab Haematol,1994,16(2):157-174.
[3]National Committee for Clinical Laboratory Standards.EP9-A Method comparison and bias estimation using patient sample;Aproved guidelines[S].Wayne,PA,USA:NCCLS,1986.
[4]丛玉隆,岳家新,袁家颖.实用血细胞分析技术与临床[M].北京:人民军医出版社,2011:14.
[5]李筱梅,杨玉宝,李承文,等.白细胞分类计数方法学比较[J].检验医学,2004,9(2):100-102.
[6]周艺,陈春兰,冯文安,等.血细胞分析仪中 MCV、RDW对PLT计数的影响的调查研究[J].中国卫生检验杂志,2011,7(21):1735-1736.
[7]Bock A,Herkner KR.Reticulocyte maturity pattern analysis as a predictive marker of erythropoiesis in paediarics[J].Clin Lab Haematol,1994,16(3):343-348.
[8]Brown M,Wittwer C.Flow cytometry:principles and clinical applications in hematology [J].Clin Chem,2000,46(8):1221-1229.
[9]陈梅,方伟祯,傅玉如.Sysmex XE-2100全自动血细胞分析仪分析网织红细胞性能评价[J].实用医学杂志,2007,23(2):268-269.
[10]蒋蕾,孙健,顾平.Beckman Coulter LH-750血细胞分析仪的性能评价[J].现代医学,2010,38(5):471-473.
