希罗达联合奥沙利铂治疗转移性结直肠癌的疗效系统评价
2014-09-13江小梅彭杰文萧剑军
江小梅 彭杰文 萧剑军
结直肠癌是常见的消化道恶性肿瘤之一,早期诊断率比较低,就诊时多发生转移,其手术治疗患者中40%~50%出现复发或者转移[1]。转移性结直肠癌往往难以根治切除,化疗成为了其主要的治疗手段。希罗达联合奥沙利铂方案越来越多地应用于临床,为了比较其与氟尿嘧啶联合治疗的标准方案疗效,本次研究收集了2000年1月至2012年12月相关的研究文献,对希罗达联合奥沙利铂治疗转移性结直肠癌的临床疗效进行系统评价,现将结果报告如下。
1 资料与方法
1.1 资料检索
选择2000年至2012年国内外希罗达联合奥沙利铂治疗转移性结直肠癌随机对照试验的相关文献,研究分组已经分为希罗达联合奥沙利铂组与其他方案治疗组,2组患者的性别、年龄和国籍等方面的资料无限制条件。机器检索应用万方数据库、CNKI数据库、Pubmed、Cochrane图书馆。中文检索词主要有乐沙定、奥沙利铂、希罗达、卡培他滨、转移性结肠癌,英文检索词主要有eloxatin,oxaliplatin,capecitabine,capecitabine,metastatic colorectal cancer等。经初步阅读初次筛检的文献摘要,对可能合格的文献下载全文并阅读筛检。同时进行文献索源和手工检索引文。
1.2 方法
1.2.1 文献纳入标准 包括:①试验设计:在中外文期刊上发表的随机对照试验(randomized controlled trial,RCT)。②研究对象:经临床病理学检查为转移性结直肠癌患者。③干预措施:希罗达(卡培他滨)联合奥沙利铂治疗转移性结直肠癌。④重复发表的文献以影响因子最高1篇纳入研究。⑤遵循意向性分析原则。
1.2.2 文献排除标准 包括:①非随机对照试验。②综述文献、病例报道、数据不完整或者缺失的文献。③文献评价Jadad评分低于3的文献。④研究结果不能体现临床疗效。⑤违反意向性分析原则。
1.2.3 文献评价和数据提取 文献质量评价采用改良的Jadad评分量表进行,<3分为低质量文献,≥3分为高质量文献。提取的研究文献的数据包括研究时间、作者、研究对象样本量、平均年龄等基本数据,以及有效率(RR)、中位生存期(OS)、完全缓解(CR)、部分缓解(PR)、中位有效持续时间(DR)、中位治疗失败时间(TTF)等临床疗效数据。文献质量评价和数据提取均由2名研究人员独立完成,存在分歧时讨论解决。
1.3 统计学方法
应用stata 12.0统计软件处理数据。计数资料计算合并相对危险度(RR),连续性变量采用加权均数差(WMD),以点估计及95%可信区间表示。连续资料未提供均数标准差的以中位数表示。本次研究中均为2分类数据,采用优势比(OR)以及95%可行区间(95% CI)表示。文献的异质性分析采用χ2检验,若P>0.05,I2≤50%时,采用固定效应模型进行合并分析;若P≤0.05,I2>50%时,则考虑使用随机效应模型合并分析。发表偏移采用漏斗图表示,发表偏移检验采用Egger检验,P<0.05为差异有统计学意义。
2 结果
2.1 文献检索情况
共检索文献125篇。仔细阅读文献摘要,核对作者和内容,排除重复的以及无关的文献,初步筛选出15篇,按照文献纳入和排除的标准,最终确定纳入meta分析的文献共7篇。其中中文文献2篇,英文文献5篇。7篇纳入研究文献的特征及原始数据见表1。

表1 纳入研究文献的特征及基本资料
注:mCRC: 转移性结直肠癌。CR:完全缓解;PR:部分缓解;TTP:肿瘤进展时间;OS:总生存期;PFS:肿瘤未出现进展生存期;RR:有效率;TTF:中位治疗失败时间;DR:有效持续时间;SD:疾病稳定持续时间。
2.2 Meta分析结果
2.2.1 总有效率 7个研究分析显示,研究组治疗有效率为17.60%(161/915),与对照组有效率18.65%(169/906)比较,2组总有效率差异无统计学意义[RR=0.90,95%CI(0.77,1.05),P=0.174]。见图1。
2.2.2 中位生存期 6个研究组(n=885)的中位生存期与对照组比较,差异无统计学意义[SMD=-0.065,95%CI(-0.158,0.028),P=0.173]。见图2。
2.2.3 中位无疾病生存期 7个研究(n=915)的中位无疾病生存期与对照组比较,差异无统计学意义[SMD=-0.046,95%CI(-0.136,0.045),P=0.323]。见图3。
3 讨论
随着生活水平的提高和生活方式的改变,结直肠癌的发病率呈逐年上升趋势,国外结直肠癌的发病率占恶性肿瘤第2~3位,在我国恶性肿瘤中位居第3~5位,严重危害人群健康[9]。由于结直肠癌早期诊断较为困难,确诊时肿瘤组织常呈晚期病变,手术治疗是结直肠癌的主要治疗手段,而术后进行化疗则是避免病情复发,延长患者生存时间,术后化疗显得尤其重要。氟尿嘧啶联合奥沙利铂治疗转移性结直肠癌,因为治疗有效率高,患者生存期有效延长,生活质量明显提高而被认为是治疗结直肠癌患者的标准方案[10]。近年来,随着医药科学技术的发展,氟尿嘧啶新一代药物希罗达(卡培他滨)的出现,临床上应用希罗达联合奥沙利铂治疗转移性结直肠癌越来越广泛。

图1 2组不同方案治疗转移性结直肠癌总有效率比较
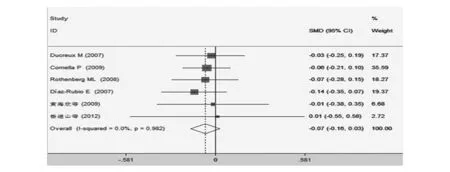
图2 2组不同方案治疗转移性结直肠癌中位生存期的比较

图3 2组不同方案治疗转移性结直肠癌中位无疾病生存期的比较
本次研究结果显示,希罗达联合奥沙利铂治疗转移性结直肠癌总有效率达17.60%(161/915),与对照组(氟尿嘧啶联合组)比较,总有效率、中位生存期、中位无疾病生存期差异均无统计学意义。说明希罗达联合奥沙利铂方案与氟尿嘧啶联合方案中治疗效果上相似,其机理可能由于希罗达是氟尿嘧啶类新一代的口服靶向治疗药物,具有选择性的肿瘤内活化作用,能更有效地作用于病变肿瘤组织。奥沙利铂属于第三代铂类化疗药物,其抗癌活性广泛,无交叉耐药性。希罗达与奥沙利铂联合治疗患者取得了较好的效果[11]。国际大规模的Ⅱ、Ⅲ期临床对照试验,以及希罗达联合奥沙利铂大样本量临床对照试验[12-13]研究结果表明,希罗达联合奥沙利铂与氟尿嘧啶相比具有相同的治疗效果。因此对于转移性或者进展性结直肠癌术后辅助性化学治疗,希罗达联合奥沙利铂治疗可以作为同氟尿嘧啶联合方案的一线治疗方案。
研究显示,希罗达联合奥沙利铂治疗转移性结直肠癌患者白细胞减少、脱发、口腔炎等不良反应均较低[14],可能是因为希罗达,因靶向作用明显,药物的特异性较高,全身的氟尿嘧啶的浓度减低,减轻了药物引起的全身性的不良反应;而奥沙利铂常见的神经毒性常呈可逆性改变,无肾毒性,且骨髓抑制、胃肠道等副反应轻,无需水化减毒,与氟尿嘧啶联合方案相比较轻,口服治疗患者易于接受,治疗依从性较好[15]。
综上所述,希罗达联合奥沙利铂治疗转移性结直肠癌与传统应用氟尿嘧啶联合标准方案相比,在总有效率、中位生存期、中位无疾病生存期等方面相似,具有较好的治疗效果,且治疗不良反应轻,治疗依从性较好,可以作为治疗转移性结直肠癌的一线治疗方案。
[1] Tse VC,Ng WT,Lee V,et al.Cost-analysis of XELOX and FOLFOX4 for treatment of colorectal cancer to assist decision-making on reimbursement〔J〕.BMC Cancer,2011,11:288.
[2] Ducreux M,Bennouna J,Hebbar M,et al.Efficacy and safety findings from a randomized phase Ⅲ study of capecitabine (X) + oxaliplatin (O) (XELOX) vs.infusional 5-FU/LV + O (FOLFOX-6) for metastatic colorectal cancer (MCRC)〔J〕.J Clin Oncol,2007,25(18):4029.
[3] Comella P,Massidda B,Filippelli G,et al.Randomised trial comparing biweekly oxaliplatin plus oral capecitabine versus oxaliplatin plus i.v.bolus fluorouracil/leucovorin in metastatic colorectal cancer patients:results of the Southern Italy Cooperative Oncology study 0401〔J〕.J Cancer Res Clin Oncol,2009,135(2):217-226.
[4] Rothenberg ML,Cox JV,Butts C,et al.Capecitabine plus oxaliplatin(XELOX)versus 5-fluorouracil/folinic acid plus oxaliplatin(FOLFOX-4) as second-line therapy in metastatic colorectal cancer:a randomized phase Ⅲ noninferiority study〔J〕.Ann Oncol,2008,19(10):1720-1726.
[5] Díaz-Rubio E, Tabernero J,Gómez-Espa a A,et al.Phase Ⅲ study of capecitabine plus oxaliplatin compared with continuous-infusion fluorouracilplus oxaliplatin as first-line therapy in metastatic colorectal cancer:final report of the Spanish Cooperative Group for the Treatment of Digestive Tumors Trial〔J〕.J Clin Oncol,2007,25(27):4224-4230.
[6] Martoni AA,Pinto C,Di Fabio F,et al.Capecitabine plus oxaliplatin (xelox) versus protracted 5-fluorouracil venous infusion plus oxaliplatin (pvifox) as first-line treatment in advanced colorectal cancer:a GOAM phase Ⅱ randomised study (FOCA trial) 〔J〕.Eur J Cancer,2006,42(18):3161-3168.
[7] 黄海欣,陈绍俊,李桂生,等.XELOX方案与FOLFOX4方案治疗转移性结直肠癌的临床观察〔J〕.现代肿瘤医学,2009,17(9):1736-1738.
[8] 杨进山,齐保聚.XELOX方案与FOLFOX6方案治疗转移性结直肠癌的临床观察〔J〕.现代中西医结合,2012,21(27):2972-2974.
[9] Conroy T,Hebbar M,Bennouna J,et al.Quality-of-life findings from a randomised phase-Ⅲ study of XELOX vs FOLFOX-6 in metastatic colorectal cancer〔J〕.Br J Cancer,2010,102(1):59-67.
[10] 杨莉萍,靳海峰,王飙落,等.奥沙利铂化学治疗方案在结直肠癌术后辅助治疗的疗效和安全性比较〔J〕.中华消化杂志,2012,32(12):822-824.
[11] 施 兵,张秀兵,徐 健,等.XELOX方案与OLF方案治疗晚期结直肠癌的临床观察〔J〕.实用肿瘤学杂志,2007,21(6):525-526.
[12] Saltz LB,Clarke S,Díaz-Rubio E,et al.Bevacizumab in co-
mbination with oxaliplatin-based chemotherapy as first-line therapy in metastatic colorectal cancer:a randomized phase Ⅲ study 〔J〕.J Clin Oncol,2008,26(12):2013-2019.
[13] Arkenau HT,Arnold D,Cassidy J,et al.Efficacy of oxaliplatin plus capecitabine or infusional fluorouracil/leucovorin in patients with metastatic colorectal cancer:a pooled analysis of randomized trials〔J〕.J Clin Oncol,2008,26(36):5910-5917.
[14] 苏雪清.XELOX与FOLFOX6治疗结直肠癌的临床疗效比较〔J〕.实用癌症杂志,2013,28(4):370-372.
[15] 盛莉莉,朱益平,吉兆宁.FOLFOX4和XELOX一线方案治疗晚期结直肠癌的疗效分析〔J〕.皖南医学院学报,2011,37(6):464.
