氟苯尼考注射液在大鼠体内代谢及生物利用度研究
2014-08-03董宏伟李忠杰吕淑荣刘万卉
董宏伟,李忠杰,吕淑荣,刘万卉
(1.烟台大学药学院,山东 烟台 264005;2.烟台绿叶动物保健品有限公司,山东 烟台 264003)
氟苯尼考(florfenicol,简称F)是一种新型的广谱抗生素.作用机理和抗菌谱与甲砜霉素、氯霉素相似,但抗菌活性要优,且无再生障碍性贫血等不良作用,不易被耐氯霉素和甲砜霉素耐药菌株产生的乙酰转移酶破坏,现已成为兽用抗菌药物之一[1-4].氟苯尼考胺(florfenicol amine,简称FFa)是F的主要代谢产物,我国[5]和欧盟[6]对动物源性食品中的F残留限MRLs值作了规定,并以F与FFa作为检出物.F在畜禽体内药代动力学的研究已有不少[7-10],但对其在大鼠体内吸收代谢产物鲜有报道.本试验研究了氟苯尼考注射液在大鼠体内的药动学行为,为临床制定给药方案提供依据.
1 材料与方法
1.1 实验动物
清洁级SD大鼠18 只,雌雄各半(平均体重200±20 g)随机分为A、B、C 3 组,预饲1周后试验,给药前禁饲12 h,给药后禁饲4 h,自由饮水.
1.2 药品和试剂
试验品:氟苯尼考注射液(F含量30%),批号为120725,由烟台绿叶动物保健品有限公司提供.
对照品:纽弗罗注射液(F含量30%,)批号为RKPB1586,美国先灵葆雅制药有限公司.
标准品:氟苯尼考(含量99.9%),批号为CDCT-C13665000,德国Dr.盐酸氟苯尼考胺(TRC,含量99.9%),批号为CDDM-F405770,多伦多研究院.氯霉素(含量99.6%),中国兽医药品监察所提供.
其他:冰醋酸为分析纯,乙腈为色谱纯.
1.3 主要仪器
Agilent1200 高效液相色谱仪,VWD 检测器,自动进样器,XW-80 A涡旋混合器,HSC-24 A氮吹仪,pH计,十万分之一电子天平,微量移液器,Thermo微量高速离心机等.
1.4 试验方法
1.4.1 给药和血样采集 试验A组尾静脉注射氟苯尼考注射液,B、C两组分别腿部肌肉注射氟苯尼考注射液和纽弗罗注射液,给药剂量均为30 mg/kg,A组于给药前及给药后0.083、0.25、0.5、1.5、2、4、6、8、12、24 h眼眶静脉丛采血0.4 mL;B组、C组于给药前及给药后0.25、0.5、1.5、2、4、6、8、12、24 h眼眶静脉丛采血0.4 mL,置含肝素钠抗凝剂的离心管中,混匀,3 600 r/min离心 10 min,吸取上层血浆,置-20 ℃保存.
1.4.2 血浆样品的处理 取血浆200 μL置10 mL玻璃离心管中,加入300 μg/mL的氯霉素10 μL作为内标物,再加入pH 7.0的磷酸盐缓冲液 1 mL涡旋1 min,加入3 mL乙酸乙酯,涡旋混合3 min,离心分离上层有机相于另一离心管内,重复提取一次,合并乙酸乙酯层提取液, 45 ℃下氮气吹干.用100 μL流动相复溶残渣,以13 000 r/min离心10 min,取上清液进样.
1.4.3 色谱条件 色谱柱:Phenomenex luna-C18(5μm,4.6×250 mm);流动相为乙腈-水-冰醋酸(100:197:3,V/V/V),VWD检测器,检测波长223 nm,流速1.0 mL/min,柱温35 ℃[6].
1.4.4 方法学研究 取空白血浆200 μL置10 mL离心管中,以标准品氟苯尼考与氟苯尼考胺配制浓度均为0.05~16.0 μg/mL的含药血浆,按1.4.2项下操作,以F与内标峰面积比对F浓度做权重系数为1/c2的加权回归,得F、FFa的标准曲线分别为:y=0.176 1x+0.055 4,r=0.991 2;y=0.163 1x+0.051 3,r=0.993 5,结果表明F及FFa在0.05~16 μg/mL范围内线性关系良好,定量下限均为0.05 μg/mL,最低检测限按信噪比S/N=3计算均为0.025 μg/mL.
另取空白血浆200 μL置10 mL离心管中,配制浓度为 0.125、1、8 μg/mL 的含药血浆,按1.4.2项下操作,考察得血浆中F与FFa的日内和日间精密度分别在1.29%~3.12%和3.89%~5.01%范围内;回收率分别为(103.1±5.27)%~(96.15±3.40)%及(105.2±3.76)%~(94.31±2.67)%,符合生物样品分析要求.
2 数据处理
用DAS2.1.1软件计算A、B、C 3组大鼠血浆中F及FFa的药物动力学参数,结果见表1、表2,药时曲线见图1.
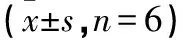
表1 A 组大鼠F的药动参数
注:t1/2α药物分布半衰期;t1/2β药物消除半衰期;AUC药时曲线下总面积;tmax最高血药浓度时间;CLz/F清除率;Cmax最高血药浓度.
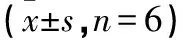
表2 B、C两组大鼠F及FFa的药动参数
注:Ka吸收速率常数;t1/2Ka药物吸收半衰期;其余参数同表1.
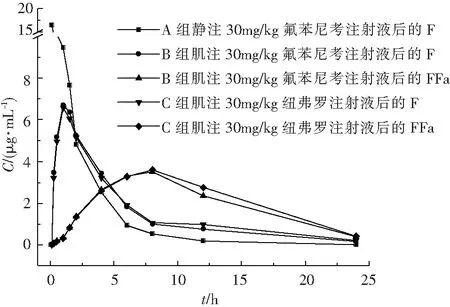
图1 各实验组大鼠的血药浓度-时间曲线
3 讨 论
3.1 静注给药的药动学特征
健康大鼠静注氟苯尼考注射液(30 mg/kg)后,F的药动学行为符合二室开放模型,与F在牛体内的药代动力学研究相符[11-12].大鼠静注后,深室分布较快,分布半衰期为t1/2α为0.84 h, AUC为 51.75 mg/L·h,Cmax为36.51 μg/mL.
据相关报道,F在牛[11-12]、奶山羊[13]、猪[9,14]体内消除半衰期分别为2.3~4.1 h、2.3 h和6.72 h,本试验中F在大鼠体内的消除缓慢,t1/2β为12.85 h;F在牛[11-12]、奶山羊[13]、马[15]和猪[9,14]体内的全身清除率分别为0.15~0.26、0.47、0.40和0.23 L/(h·kg),与试验确定的F在大鼠体内的CLz/F为0.58 L/(h·kg)相近.AfifiNA等认为,F在动物体内清除率低,消除缓慢是由于F化学结构中-OH被-F取代,阻遏葡萄糖醛酸的结合,从而延缓了动物体内F的排泄所致[16].
3.2 肌注给药的药动学特征
大鼠肌注氟苯尼考注射液及对照品纽弗罗注射液(30 mg/kg,按氟苯尼考载药量计算)后,药动学行为均符合一室模型,与文献报道其在牛[11-12]、马[15]、鸡[16]的研究结果一致.吸收较快且完全,吸收半衰期分别为0.72、0.58 h,在1 h均达到最大吸收,分别为6.70、6.57 μg/mL;在大鼠体内消除缓慢,消除半衰期分别为12.63、11.37 h;肌注氟苯尼考注射液与对照品纽弗罗注射液后药动学参数无显著差异,F的相对生物利用度为99.32%,绝对生物利用度为87.38%,比牛[11-12](78.5%)、鸭[17](73.03%)、马[15](81%)和山羊[18](65.72%)高,比鸡[16](96.6%)和猪[9,14](96.86%)低.
3.3 肌注后代谢产物的药动学特征
F的代谢物主要是FFa[19],目前没有报道显示其有抗菌活性,但是F用于可食性动物源时,FFa是残留检测的重要指标之一[5-6].B组大鼠肌注氟苯尼考注射液后代谢产物FFa在给药后0.5 h浓度即达到0.1 μg/mL以上,8 h达到最高峰,与C组大鼠肌注对照品纽弗罗注射液后代谢物FFa药动学参数无显著差异.
4 结 论
本试验研究了静注及肌注氟苯尼考注射液与对照品纽弗罗注射液后F在大鼠体内的药代动力学特征,结果表明F吸收迅速,消除缓慢(12 h仍能维持0.5 μg/mL),据报道F对其敏感菌的MIC均为0.5 μg/mL左右[20],本品(氟苯尼考注射液)能在较长时间内维持药效浓度.
肌注氟苯尼考注射液后代谢物FFa在大鼠体内消除缓慢,分布均匀,氟苯尼考注射液的相对生物利用度为99.32%,绝对生物利用度为87.38%,试验品氟苯尼考注射液与对照品纽弗罗注射液在大鼠体内的药动学参数无显著差异,为氟苯尼考注射液进一步临床试验提供了参考依据.
参考文献:
[1]Cannon M,Harford S,Davies.A comparative study on the inhibitory actions of chloramphenicol,thiamphenicol and some fluorinated derivatives[J].Jantimicrob Chemother, 1990,26(3): 307-317.
[2]Salmon S A,Watts J L.Minimum inhibitory concentration determinations for various antimicrobial agents against 1570 bacteiral isolates from turkey poults[J].Avain Diseases,2000,44(1):85-88.
[3]Graham R,Palmer D,Pratt B C,et al.In vitro activity of florfenico1[J].Eur J Cl in Microbiol Infect Dis, 1988,7(5):691-694.
[4]Ayling R D,Baker S E,Peek M L,et a1. Compairson of in vitro activity of danolfoxacin,florfenicol,oxteracycline,spectinomycin and tilmicosin against recent field isolates of Mycoplasma bovis[J].Veterinary Record,2000,146(26):745-747.
[5]中国兽药典委员会.中华人民共和国兽药典(一部)[S].北京:中国农业出版社,2010:160-161.
[6]EMEA-EU.Committee for veterinary medicinal products:Florfenicol(extension to all food producing species),summary report(6) [Z/OL].London, UK. http://www.emea.eu.int/pdfs/vet/mrls/082202en.pdf.January 2002.
[7]Harrs V D,Lockwood P W,Katz T,et a1.Efficacy of florfenicol in the treatment of bovine respiratory disease—Results of clinical trials in Europe [J].Praktische Tierarzt,1995,76(9):803-807.
[8]Nordmo R,Varma K J,Sutherland I H,et al.Florfenicol in Atlantic Salmon, Salmo Salar:field evaluation of efficacy furunculso is in Norway[J].Journalof Fish Disaeses,1994, 17(3):239-244.
[9]Ueda Y,Ohtsuki S,Narukawa N.Efficacy of florfenicol on experimental Actinobacillus pleuropneumonia in pigs[J].Journal of Veteirnary Medical Science,1995,57(2):261-265.
[10]Byung-Kwon Park, Jong-Hwan Lim, Myoung-Seok Kim, et al. Pharmacokinetics of florfenicol and its metabolite, florfenicol amine, in dogs [J]. Research in Veterinary Science, 2008, 84(1):85-89.
[11]Adams P E,Vanna X I,Powers T E,et al.Tissue concentration and pharmacokinetics of florfenicol in male veal calves given repeateddoses[J].Am J Vet Rese,1987,12:1725-1732.
[12]Vanna K J,Adams P E,Powers T E,et al, Pharmacokinetics of florfenicol in vea1 calvse[J].J Vet Pharmacol Therap,1986,9: 412-425.
[13]Lavy E,Ziv G,Soback S,et al.Clinical pharmacology of florfenicol in lactating goats[J]. Acta Vet Scand,1991,87(Suppl):133-136.
[14]蒋红霞,冯淇辉,曾振灵.氟甲砜霉素在猪体内的药物动力学研究[J].中国兽医学报,2001,1(21),86-89.
[15]Mckeller Q A,Vamra K J.Phamacokinetics and tolerance of florfenicol in Equidae[J]. Equine Vet J,1996,28(3):209-213.
[16]Afifi N A,Aboel-Sooud K A.Tissue concentrations and pharmacokinetics of florfenicol in broiler chickens[J].Birtish Poultry Sciense, 1997,38(4):25-428.
[17]el-Banna H A.Pharmacokinetics of florfenicol in normal and Pasteurella-infected Muscovy ducks[J].British Poultyr Science, 1998,39:492-496.
[18]Atef M,el-Gendi A Y,Aziza M M,et a1.Pharmacokinetics properties of florfenicol in Egyptian goats[J].Deutsche Tierortliche Wochencshrift,2000,107(4):147-150.
[19]Hormazabal V,Steffenak I,Yndestad M.Simultaneous determination of residues of florfenicol and the metabolite florfenicol amine in fish tissues by high-performance liquid chromatography[J].Journal of Chromatography B: Biomedical Sciences and Applications,1993, 616(1):161-165.
[20]江丽,雷淑珍.氟苯尼考与多种抗菌药物联合应用对大肠杆菌的体外抑菌试验 [J]. 广东畜牧兽医科技,2008,3 (8):98-101.
