两亲性聚合物分子自组装的研究进展
2014-07-05李雪梅贺继东
李雪梅,贺继东
(青岛科技大学橡塑材料与工程教育部重点实验室,山东省橡塑材料与工程重点实验室,山东 青岛 266042)
进展与述评
两亲性聚合物分子自组装的研究进展
李雪梅,贺继东
(青岛科技大学橡塑材料与工程教育部重点实验室,山东省橡塑材料与工程重点实验室,山东 青岛 266042)
两亲性聚合物以其同时具有亲水和疏水链段的独特结构,在生物医药、纳米技术等领域有广泛的用途。本文主要介绍了两亲性聚合物通过分子自组装形成聚集体的研究进展,详细论述了几种分子自组装聚集体的制备,包括结构、组成、分子量控制的简单聚集体、半结晶聚集体、交联聚集体以及具有刺激响应性(pH值响应性、温度响应性、pH值/温度双重响应性、氧化还原响应性、溶剂极性响应性等)的智能型聚集体,两亲性聚合物结构的可控性以及如何提高聚集体的稳定性成为国内外专家研究的重点,指出结晶诱导分子自组装及智能型分子自组装是未来研究的热点。
两亲性聚合物;分子自组装;聚集作用;纳米粒子;形态学
两亲性聚合物是指分子链中同时含有亲水和疏水链段的聚合物[1]。两亲性聚合物多为嵌段共聚物,如聚己内酯-b-聚环氧乙烷(PCL-b-PEO)[2]、聚乙二醇单甲醚-b-聚乳酸(mPEG-b-PLA)[3-4]等;此外还有均聚物[5]、接枝共聚物[6-8]以及更加复杂的聚合物[9]。两亲性聚合物因其结构的特殊性,也展现出不同的形态,如线形[2]、牙刷形[10]、梳形[6,10-12]、星形[13-15]、H形[9]、树突状[16]、蝌蚪状[17]等。两亲性聚合物的亲水-疏水的特殊结构使其在选择性溶剂中可以通过自组装,形成以不溶性链段为核、可溶性链段为壳的具有“核-壳”结构的特殊聚集体,包括胶束[2,14]、囊泡[12,18-19]、纳米微球[20-21]、纳米粒子[22]、多舱微囊[13]等,它们具有有趣的形态,比如球形[2,22-23]、圆柱形[2]、棒状[23]、圆盘状[23]、六角形[24]、洋葱头状[6,12]、蠕虫状[25]等。因其在选择性溶剂中的特殊聚集形态以及在生物医药、纳米技术等领域中的潜在应用而引起人们的广泛关注。两亲性聚合物的分子自组装可以是简单的分子自组装形成无定形的聚集体,也可以通过聚合物的结晶诱导分子自组装形成半结晶聚集体,还可以是“智能型”的分子自组装形成具有特殊响应(如pH值响应、温度响应、pH值与温度双重响应、溶剂极性响应)的聚集体。
1 聚合物结构、组成、分子量控制的分子自组装
两亲性聚合物在选择性溶剂中的自组装行为与多种因素有关,其中最基本的是聚合物的结构、组成以及分子量。
Wu等[26]通过直接溶解含有高PEG含量的PLA/PEG嵌段共聚物的方法制备了各向异性的自组装大胶束,发现胶束的形态强烈依赖于PEG的含量。其形态异于传统的球形,而是椭圆形、圆柱形、针状;其长度在150~500nm,宽度在30~100nm。PEG的含量、共聚物的分子量、左旋聚乳酸与右旋聚乳酸链段的立体络合都能影响胶束的聚集数,进而影响胶束的形态。PEG的含量增加,促使形成的胶束的长宽比变大;共聚物的分子量很高时,则观察不到各向异性的胶束;左旋聚乳酸与右旋聚乳酸链段的立体络合不利于各向异性胶束的形成。
1.1 聚合物结构控制的分子自组装
Lonsdale等[19]合成了大环拓扑结构的嵌段共聚物AB、AB2、A2B[其中A表示亲水的PtBA(线性的聚丙烯酸叔丁酯),B表示疏水的环状聚苯乙烯],并通过自组装制备了环状大分子的聚集体,研究了环状结构对自组装行为的影响。聚合物中的PAA(聚丙烯酸,是PtBA去保护后形成的)的重复单元数为22时,聚合物形成囊泡形态;当增加至46时,形成球状的核壳结构。而且相比于线性的类似物,在AB2型杂臂星形聚合物中,由于疏水性环状聚合物PS的流体力学体积较小,导致核堆积得更加密集,使PAA被压缩到壳中,并且延伸到水相中,超出了它正常的高斯链构象。
Wang等[27]合成了线性结构的PCL-b-PTFEA以及星形拓扑结构的POSS[PCL-b-PTFEA]8[PTFEA表示聚(2,2,2-丙烯酸三氟乙酯),POSS表示多面体低聚物倍半硅氧烷,是星形共聚物的核心],并控制两种聚合物的组成和链段长度相同,然后将嵌段共聚物并入到环氧树脂热固性材料中。这两种不同结构的聚合物都能够形成球形的PTFEA纳米结构,环氧树脂的前体作为两亲性嵌段共聚物的选择性溶剂,其中,PCL为亲环氧树脂,PTFEA为疏环氧树脂。但是由于两者的拓扑结构不同,星形嵌段共聚物形成的纳米相尺寸比线性嵌段共聚物形成的纳米相尺寸要小,这是因为两亲性聚合物拓扑结构不同,使胶束表面的亲环氧树脂的PCL链段的构象不同。在线性共聚物中,PCL分层,并有一端自由地沿着PTFEA胶束的法向取向。而在星形共聚物中笼状POSS对PCL的分层有所束缚,PCL的两端都是不自由的,从而导致PTFEA纳米相的尺寸降低。
1.2 聚合物组成控制的分子自组装
两亲性聚合物中疏水性链段不同,会导致其自组装行为的差异。Venkataraman等[23]通过含有硫脲的PEG修饰的两亲性聚合物的自组装形成了不同的纳米结构,纳米结构不同的原因在于疏水性链段的不同。疏水性链段分别为硬脂酰、油烯基、十二烷醇聚合物分别自组装形成的细长棒状胶束(其直径为15nm,长度为100nm~1μm)、球状胶束(直径约为15nm)、圆盘状胶束(直径12~20nm)。而棒状胶束与球形胶束形成差异的原因在于后者疏水性链段中含有一个双键,双键的引入导致了聚集形态的改变,说明分子中疏水性链段的饱和性能够支配胶束的形态。改变疏水性链段的局部,即疏水性链段缩短并引入端羟基,聚合物会形成圆盘状的胶束,而圆盘状胶束中的薄核很可能是由于十二烷醇中的羟基端基与硫脲形成了氢键,导致疏水性部分的交错。
类似地,Hao等[28]合成了含有亲水性的聚{γ-2-[2-(2-甲氧基乙氧基)乙氧基]乙氧基-ε-己内脂}以及疏水性的聚(γ-烷氧基-ε-己内脂)的二嵌段共聚物,其中五种γ-烷氧基分别为辛氧基、乙基己氧基、乙氧基、苄氧基、环己基甲氧基,所形成的聚合物分别标记为P1、P2、P3、P4、P5。五种聚合物都表现出低临界溶解温度(LCST,36~39℃)。由于γ-取代基的不同,聚合物自组装形成的球形胶束性能也有所不同。P1、P5由于取代基比较大,形成的胶束尺寸最大,且胶束的尺寸分布也最宽;P3由于取代基较小,形成的胶束尺寸最小。而P2、P4由于取代基的支化结构, 形成的胶束尺寸则处于中间水平。另外,五种聚合物的载药(DOX阿霉素)性能也有所差异,P1、P4载药量相比于P2、P3、P5更高。
改变亲水性链段与疏水性链段的长度比例也能够影响聚合物的分子自组装过程。Sun等[29]合成了二嵌段共聚物左旋聚乳酸-b-聚四氢呋喃丙烯酸酯(PLLA-b-PTHPA),在65℃的混合溶剂四氢呋喃/水(THF/H2O)中,共聚物中的嵌段PTHPA水解,同时在结晶诱导分子组装作用下,聚合物形成两亲性左旋聚乳酸-b-聚丙烯酸酯(PLLA-b-PAA)圆柱形的胶束。调节亲水链段PAA与疏水链段PLLA的长度比例,发现PLLA链段的长度可以控制圆柱形胶束的长度,PAA链段的长度可以控制圆柱形胶束的宽度。在PLLA质量分数不变的前提下,增加其链段长度,圆柱形胶束的长度逐渐降低,这是PLLA的结晶性所致,一方面PLLA链段越长,越容易结晶,无定形的球心形成的结晶种就越多;另一方面,含有PLLA链段越长的聚合物,结晶时链段折叠的时间就越长,容易结合到结晶种的两个活性端。而在PLLA链段长度不变的前提下,增加PAA的链段长度,即疏水性链段的长度比例降低(从36.6%降为14.9%),可以形成尺寸分布较窄的平滑的圆柱形胶束;而疏水链段比例为63.4%时,可形成圆柱形和薄片状粒子的混合相;当疏水性链段比例仅为12.8%时,可形成球形与圆柱形胶束共存的状态。
类似地,Yuan等[30]合成了两亲性的三嵌段共聚物聚乙二醇-b-聚丙烯酸叔丁酯-b-聚(2-甲基丙烯酸羟乙酯)(PEG-b-PtBA-b-PHEMA),其中PEG和PHEMA是亲水性的,PtBA是疏水性的。该共聚物能够在水介质中自组装形成胶束,随着亲水性PHEMA链段长度的增加,其临界胶束浓度(CMC)逐渐增大,胶束的尺寸从53.8nm增加至151.0nm。这是因为随着亲水性链段长度的增加,亲水性链段形成的壳增厚,导致胶束的尺寸增加。
Gou等[31]制备了药物共轭的两亲性的A14B7杂臂星形聚合物,它采用β-环糊精作为核心,有14个PCL臂和7个PEG臂,并研究了其在水溶液中多形态的自组装行为,结果发现随着聚合物中PEG质量分数的增加(由19.4%增至46.2%),CMC增加(由1.35mg/L增至6.46mg/L);当PEG质量分数为19.4%时,聚合物形成带状的聚集体;当PEG质量分数为29.2%时,聚合物形成蠕虫状聚集体;当PEG质量分数为32.8%和46.2%时,聚合物形成球形胶束(平均直径为10~20nm)。这说明亲水性的PEG链段的组成对共聚物的自组装行为具有很大的影响。
另外,聚合物功能化也能够引起其自组装行为的变化,功能化基团的含量不同,形成的纳米结构也有所变化。Venkataraman等[32]合成了二嵌段共聚物mPEG113-b-P(MTC-Chol)n(n=4或11),其中MTC-Chol表示胆固醇功能化的脂肪族环状碳酸酯单体。当n为4和11时,聚合物形成的纳米结构分别为圆盘状胶束[平均直径为(19.2±3.1)nm]和堆叠圆盘状的复杂胶束[平均直径为(18.7±2.7)nm,堆叠宽度为(18.6±4.7)nm],且临界聚集浓度(CAC)值分别为4.0mg/L和2.1mg/L。堆叠的复杂聚集形态可能是因为胆固醇功能化的疏水性链段能给堆叠的圆盘状复杂胶束提供一个中心轴,而CAC值的降低很可能是由于胆固醇链段之间的相互作用造成的。
此外,聚合物混合物中的某一组分的含量对聚合物的自组装行为也有很大的影响。Chen等[33]研究了均聚物PBLG的含量对聚丙烯酸-g-聚(γ-苄基-左旋谷氨酸)(PAA-g-PBLG)和PBLG混合体系的自组装行为的影响。结果发现单纯的接枝共聚物在水中自组装聚集形成了短棒状胶束(平均直径150nm,平均长度230nm);随着fhomo(混合物中均聚物PBLG的质量分数)的增加,棒状胶束的长度和直径增加;当fhomo达到0.08时,棒状胶束略有弯曲,且平均直径在100nm左右;继续增加fhomo至0.12,发现环形线圈状胶束与弯曲的棒状胶束共存;当fhomo达到0.22时,只能观察到环形线圈状胶束;当fhomo≥0.54时,只有沉淀生成。
1.3 聚合物分子量控制的分子自组装
Pang等[34]制备了以β-环糊精(β-CD)为中心的、亲水性的PAA为核、疏水性的PS为壳的多臂星形PAA-b-PS嵌段共聚物,并研究了其在无水二甲基甲酰胺(DMF)中的单分子胶束化行为,发现胶束结构是静态且单分散的稳定的球状。随着PAA-b-PS分子量的增加,单分子胶束的尺寸也从19nm增至65nm,且PAA核的尺寸大约是单分子胶束尺寸的一半。
对于接枝共聚物来说,骨架聚合物的分子量对聚合物的自组装行为也有一定的影响。Piyapakorn等[35]合成了两亲性无规共聚物聚(γ-谷氨酸)-g-左旋苯丙氨酸(γ-PGA-Phe),它可以形成具有药物载体潜在应用的球形胶束,并发现主链γ-PGA的分子量(70kDa、140kDa、220kDa)和疏水性部分的接枝度可以影响其自组装形成的胶束的性能。当接枝度在27%~42%时,通过直接分散聚合物(主链γ-PGA分子量大于140kDa)的方法,其可以自组装形成具有核壳结构的9~13nm的纳米粒子,随着γ-PGA分子量的降低,形成纳米粒子的尺寸多分散性指数增加。而当接枝度大于42%时,用透析的方法通过改变氯化钠溶液的浓度可以制备聚合物的纳米粒子。当接枝度为42%时,随着氯化钠溶液浓度的增加,主链分子量低的聚合物的纳米粒子的尺寸以及Nagg(聚集数量)相应增加。
He等[36]在选择性溶剂(H2O/THF)中制备了由AuNPs(金纳米粒子)和PEO-b-PS组成的APMNs(两亲性的等离子体胶束状纳米粒子),发现APMNs能够自组装形成多种超结构,其自组装行为强烈依赖于聚合物链的分子量和纳米粒子核的尺寸。当采用相同尺寸的金纳米粒子时,随着嵌段聚合物链中PS链段分子量的增加(由7000到49000),共聚物自组装形态由单分子胶束到胶束的群簇再到囊泡转变。在这一转变过程中,亲水的PEO链段的活动性起着至关重要的作用,疏水的PS链段的分子量越高,PEO链段的活动性就越高,从而导致囊泡结构的形成。
2 结晶诱导的分子自组装
当两亲性聚合物中含有结晶性的链段时,结晶对于分子的自组装过程也起着重要的作用。调整聚合物链段的结晶性,可以调整自组装形成聚集体的性能,从而使其具有特殊的用途,比如药物载体等。
Schacher等[37]首次报道了星形嵌段共聚物的结晶诱导分子自组装行为,他们制备了[PEO50-b-PFDMS35]4星形嵌段共聚物,其外层嵌段为半结晶的聚二茂铁基硅烷(PFDMS,疏水性物质),内层嵌段为PEO。共聚物在四氢呋喃与醇类的混合溶剂中能够形成直径在100~200nm的球形囊泡,且在其中发现厚度在2~3nm的颜色较深的胶囊状支撑物,这是不溶性的半结晶PFDMS段形成的,而PEO则作为冠状物稳定囊泡。PFDMS的结晶性使得这些聚集体保持囊泡状,并且没有塌陷的痕迹,从而保证了囊泡的稳定性。
Gwyther等[38]制备了两亲性不对称的结晶-线团的P3HT-b-P2VP,其中P3HT是聚(3-己基噻吩),是结晶性的;P2VP是聚(2-乙烯基吡啶),是无定形的。并研究了共聚物在四氢呋喃与乙醇的混合溶液中的结晶诱导溶液自组装行为,发现其可以形成以P3HT为核,P2VP为壳的纤维状的半结晶胶束。在明场TEM照片中发现紧密堆积的P3HT核呈现明显的黑色,通过UV/Vis、PL和WAXD证实了P3HT核的结晶性和π-共轭性。同时,共溶剂的存在以及共溶剂通过蒸发或者透析缓慢的移除可以导致几个微米长的长度一致的胶束形成,这是因为P3HT核结构重排成热力学上更稳定的排列以及自成核的抑制。纤维状胶束的宽度依赖于P3HT的长度,P3HT与P2VP的链段长度之比为1∶5时明显比1∶3时形成的核结构更规整,这很可能是因为前者的P3HT缓慢可控结晶,从而形成了规整结构。
类似地,Zhai等[39]通过两亲性的结晶-线团嵌段共聚物的各向异性的胶束制备了具有核壳结构的纳米纤维,聚乙烯醇(PVA)和两亲性的聚乙二醇-b-聚对二氧环己酮(PEG-b-PPDO)分别作为纳米纤维的壳层和结晶性的核层。PEG-b-PPDO在PPDO的结晶诱导作用下可以在水溶液中自组装先形成薄片状的粒子,然后形成各向异性的八角形的纳米聚集体;当混入PVA后,由于疏水性的PPDO链段的结晶性,八角形的纳米聚集体离解成各向异性的薄片状粒子,薄片的表面有助于PPDO的片晶的复杂堆砌,也有助于无定形的PPDO混合到纳米纤维的核中,从而使PPDO片晶的有序度增加,核壳相分离,使其具有明显的核壳结构。而对于具有八角结构的PEG-b-PPDO粒子,由于没有足够的时间以及灵活性再组装成平衡的形态,会发生微相分离的形态。具有核壳结构的纳米纤维的PPDO的有序度比具有微相分离结构的纳米纤维的PPDO有序度要高。
Glavas等[40]合成了一系列以PEG作为亲水链段、以聚酯均聚物[PCL(聚ε-己内酯)、PLA(聚乳酸)、PεDL(聚ε-癸内酯)]或聚酯的无规共聚物作为疏水链段的两亲性聚合物,其中PCL、PLA是半结晶的,PεDL是无定形的。形成胶束核的疏水性链段的结晶性对聚合物的自组装形成胶束的性能有非常显著地影响。有无定形核的胶束的CMC比结晶性核的胶束的CMC要高很多;且随着形成核的链段的分子量增加,有无定形核的胶束尺寸增加,有半结晶性核的胶束尺寸减小,即前者载药能力提高,而后者降低。因此通过调整核的结晶性可以调整形成胶束的CMC以及尺寸,从而可以更好地应用于药物载体方面。
两亲性嵌段共聚物的结晶诱导的分子自组装是形成圆柱形胶束或蠕虫状胶束的有效途径[29]。He等[2]研究了半结晶的圆柱形PCL-b-PEO胶束的两种生长模式,并研究了形成核的PCL的结晶性与胶束生长的关系。他们首先在不同的混合溶剂中制备了不同形态胶束的半结晶种子溶液,然后再将种子溶液置于4℃下,在形成核的PCL段的外延结晶的诱导下进行胶束的生长,随着时间的延长,圆柱形胶束的长度也随之增加。而且发现了胶束生长的两种模式:一种是单聚体在半结晶的种子溶液的活性末端直接生长;另一种是圆柱形的半结晶种子胶束通过尾尾耦合生长。
3 交联控制的分子自组装
Wang等[41]首次制备了三甲氧基硅烷(TMS)终止的、—S—S—(二硫键)连接的嵌段共聚物TMS-PCL—S—S—PEO,并制备了核交联的混合胶束。发现烯丙基终止的PCL—S—S—PEO可以自组装形成以疏水性的PCL为核、亲水性的PEO为壳的未交联的球形胶束;而经TMS终止的TMSPCL—S—S—PEO则可以自组装形成核交联的、尺寸更大的球形胶束,这是PCL核之间的溶胶-凝胶转变与自组装过程同时发生的结果,内层的二氧化硅很可能吸收水分使外层的PCL核膨胀,从而导致聚集体的尺寸增加。
Li等[42]制备了两亲性嵌段共聚物PMA82-b-P(NAS0.29-co-NAM0.71)155{聚丙烯酸甲酯-b-聚[N-(丙烯酰氧基)琥珀酰亚胺-co-(N-丙烯酰吗啉)]},并在水中制备了未交联的胶束,通过二氨基终止的交联剂与壳层部分的丙烯酸之间的化学交联制备了壳交联的纳米粒子。通过测试发现壳交联的纳米粒子所具有的流体力学直径相对较小,而且电子密度也发生了再分配。
4 智能型分子自组装
除了上述所介绍的分子自组装以外,如今,智能型的分子自组装越来越引起人们广泛的关注,所形成的组装体具有特殊的响应性(pH值、温度、pH值/温度双重响应、氧化还原响应、溶剂极性响应等),可以适应不同的应用环境。尤其是在药物载体方面,对于药物的可控释放、疾病的治疗具有靶向针对性。
4.1 pH值响应性分子自组装
Surnar等[43]首次制备了pH值响应性的可用于双重药物载体方面的羧酸功能化的PCL基聚合物囊泡,如图1所示,他们首先制备了两亲性共聚物聚乙二醇-b-γ-羧酸功能化的聚己内酯,然后经过自组装形成了具有pH值响应性的尺寸在100~250nm的囊泡,囊泡可以包封亲水性药物(Rh-B,即若丹明B)、疏水性药物(IBU,即布洛芬;CPT,即喜树碱),以及同时包封亲水与疏水药物。由于PCL的羧酸功能化使得囊泡在类似于胃的酸性环境(pH<2.0)中保持稳定,而在类似于肠的弱碱性环境(pH=7.4)下,囊泡破裂,药物得到释放。这使得该共聚物囊泡可以通过口服作用于肠道,在药物载体等生物医药领域有潜在的应用。
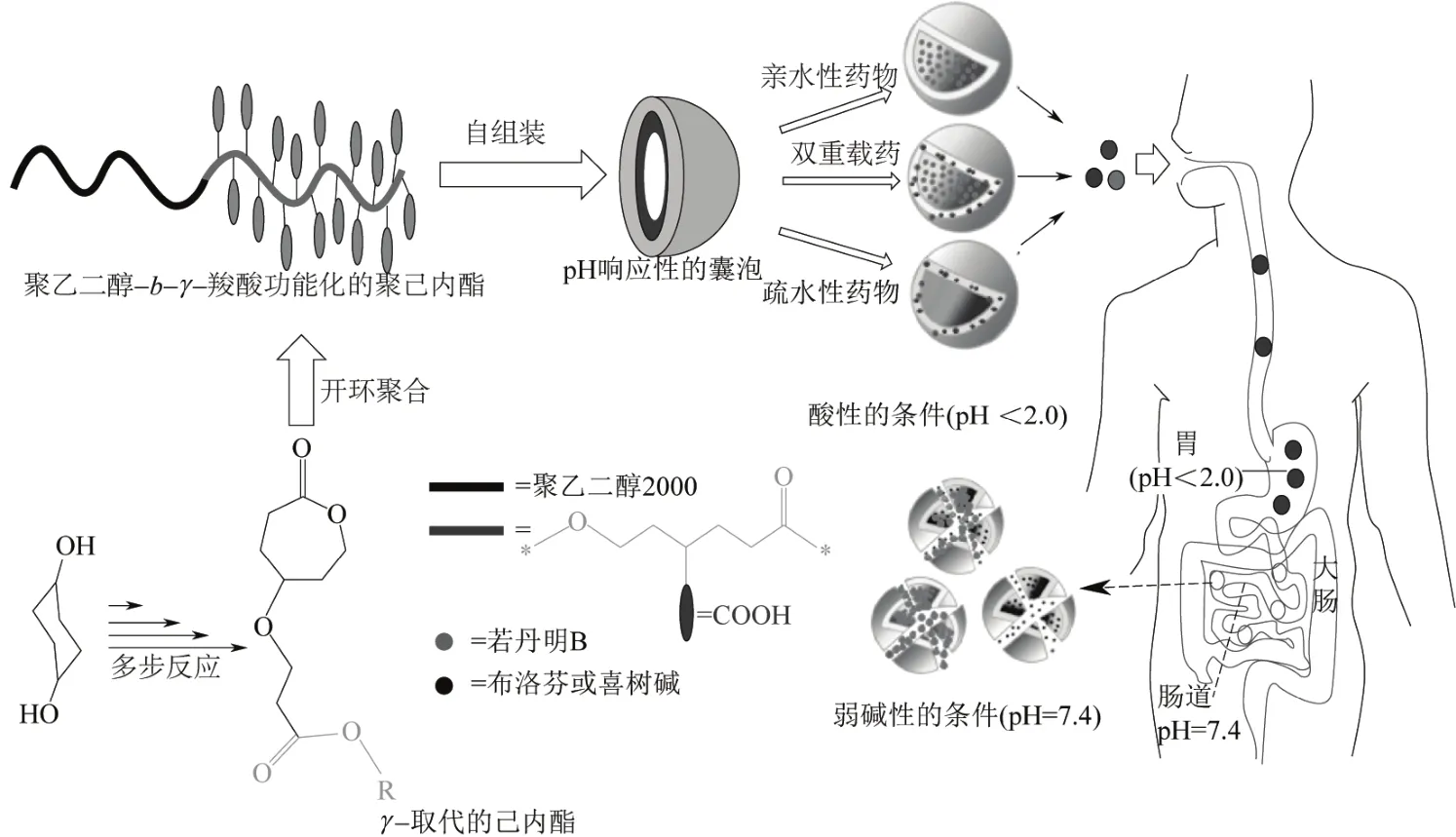
图1 pH值响应性双重药物载体的制备以及药物的可控释放示意图[43]
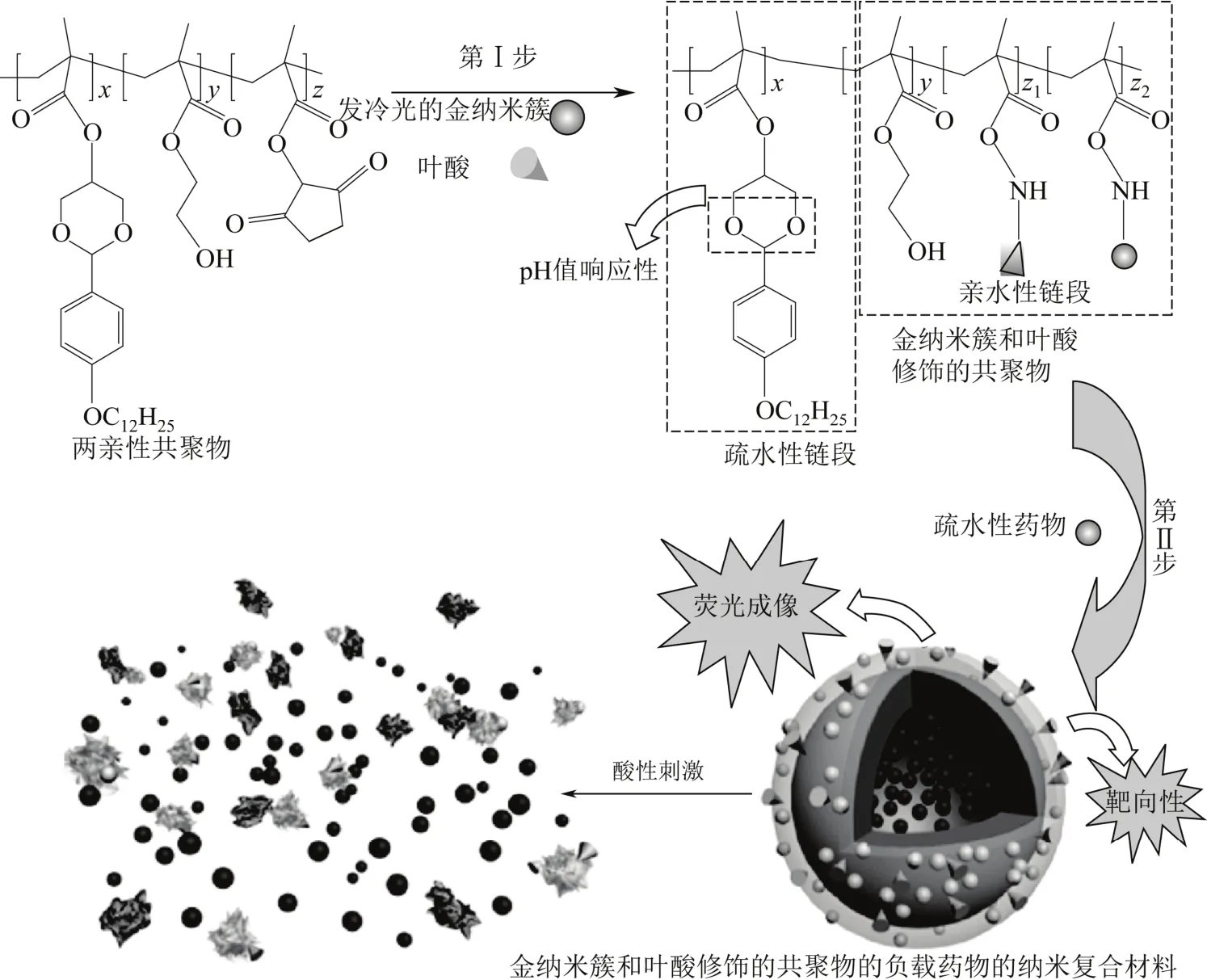
图2 L-AuNCs/FA-PDNH纳米复合材料的合成示意图[44]
Chen等[44]合成了可用于药物可控释放的含有发冷光的金纳米簇(L-AuNC)的两亲性的聚合物基纳米载体,如图2所示。他们首先合成了具有pH值响应性的两亲性聚合物PDNH[Poly(DBAM-co-NAS-co-HEMA)],即4-正十二烷氧基苯亚甲基丙酮、丙烯酸琥珀酰亚胺酯和甲基丙烯酸羟乙酯的共聚物,经过具有靶向性的叶酸(FA)修饰后,将可用于诊断探针且具有光稳定性的L-AuNC结合到上述修饰过的聚合物上形成L-AuNCs/FA-PDNH。通过两亲性聚合物的分子自组装将疏水性的药物PTX(紫杉醇)包封到具有核壳结构的核中,在叶酸的靶向作用下,胶束到达叶酸过表达的癌细胞中,在弱酸性环境的刺激下,包封在纳米复合材料中的药物释放,达到癌症治疗的目的。他们发现药物的释放很大程度上依赖于环境的pH值,在接近人体正常组织pH=7.4的情况下,纳米材料很稳定;而在酸性(pH=5.0)环境下12h后,包封在纳米复合材料中的药物即可释放90%。
Ray等[18]制备了左旋聚赖氨酸-b-聚氧化丙烯-b-左旋聚赖氨酸(KPK)三嵌段共聚物,其中聚赖氨酸是亲水性的,其含量大于75%。并研究了随着pH值的变化,嵌段共聚物自组装的特殊形态转变。发现在较低的pH值条件下,聚合物中的赖氨酸的二次结构采取无规线团构象;随着pH值的升高,逐渐变为α-螺旋形构象。赖氨酸链构象的不同导致聚合物在不同的pH值条件下呈现出不同的形态 ,在较低pH值条件下,聚合物形成高表面曲率的球形胶束;而在高pH值条件下,因赖氨酸链长短的不同,聚合物则形成低表面曲率的囊泡或者圆盘状胶束。
Chang等[6]研究了含有疏水性骨架、侧链具有pH值响应性以及亲水性的两亲性梳形接枝共聚物的自组装行为。依赖于pH值,两亲性聚合物的聚集形态是多样的。在较低的pH值下,共聚物形成胶束状聚集体;随着pH值的增加,共聚物能够形成单层的囊泡;当pH值增加至中性时,共聚物则会形成具有层层自组装结构、类似于洋葱头形状的多层囊泡。聚合物囊泡能够融合,而且在中性条件下,融合过程最快,融合之后,囊泡的层数比融合之前要多。
Kellum等[45]制备了具有pH值响应性的两亲性P(AMPS-b-AAL)的胶束,其中AMPS表示2-丙烯酰胺基-2-甲基-1-丙磺酸钠,AAL表示N-丙烯酰基-左旋丙氨酸。在低pH值下,AAL被质子化,表现出疏水性,AMPS保持负电性,聚合物自组装形成以AAL为核、AMPS为壳的具有核壳结构的胶束。在较低pH值下,含有负电性壳层的胶束与含有阳离子的均聚物聚(N-[3-(二甲氨基)丙基]丙烯酰胺)(PDMAPA)能够形成层层自组装的薄膜,胶束形态能够得到保持。而将薄膜浸没在中性的水中,则能够引发胶束的破裂。
4.2 温度响应性分子自组装
Shen等[46]研究了两亲性的聚乙二醇-b-聚[γ-(2-甲氧基乙氧基)酯-左旋-谷氨酸](PEG-b-poly-LEG2Glu)的构象特殊的自组装过程,其中poly-L-EG2Glu是温度敏感性的。在初始的水溶液中,共聚物中的poly-L-EG2Glu呈现螺旋形的构象,随着温度的升高,聚合物的构象保持不变,由于可逆的疏水相互作用,共聚物形成了以poly-L-EG2Glu为核的蠕虫状的胶束;随着热处理时间的延长,poly-L-EG2Glu的构象转变为β-薄片构象,特殊构象的氢键作用使共聚物的形态由蠕虫状胶束转变为纳米带。
Korchagina等[47]合成了温敏性的二嵌段共聚物,即聚(2-异丙基-2-恶唑啉)-b-聚(3-丙烯酰胺)三甲基氯化铵(PIPOZ-b-PAMPTMA),其中PIPOZ具有温敏性以及疏水性,PAMPTMA具有亲水性。实验发现加热速率对聚合物的自组装行为有显著影响。当升温速率为0.2℃/min,聚合物水溶液被加热到40℃时,其自组装形成小的球形聚集体,随着温度缓慢升高至60℃,亲水性带电的PAMPTMA嵌段扩散到中心,最终形成囊泡。而升温速率为0.7℃/ min,聚合物水溶液被加热到40℃时,形成棒状或者蠕虫状的胶束,随着温度快速升高至60℃,最终形成囊泡。
Zhao等[48]研究了两亲性的三萜烯-聚环氧乙烷共轭体的温度响应性的聚集行为,发现PEO质量分数小于70%的CE(胆固醇-PEO)溶液和BE(桦木醇-PEO)溶液在加热过程中,共聚物会沉淀下来;在室温下,CE溶液中有纳米级的聚集体存在。含有短PEO链段的质量分数为5%的聚合物溶液有双重温度响应行为,其在高温下会形成沉淀,在低温下会形成凝胶。
Xiang等[49]制备了可用于药物载体方面的两亲性超支化的聚脲胶束,他们首先合成了羰基双己内酰胺(B)与双(六亚甲基)三胺(A)的反应物AB2(具有疏水性),再与PEG反应形成超支化聚合物,其在水中能够形成半径为6~14nm的球形胶束,随着聚合物浓度的增加,可形成半径为80nm的球形胶束。这些胶束具有接近人体体温的低临界溶解温度(LCST),且转变是可逆的。由于聚合物分子中含有仲氨基基团,使得LCST对酸是敏感的。添加酸后,所形成的粒子尺寸降低,且加入柠檬酸(三官能度)后粒子尺寸最低。
4.3 pH值/温度双重响应性分子自组装
Savoji等[50]制备了具有pH值和温度双重响应性的Poly(nPA0.8-co-DEAEMA0.2)-block-poly (nPA0.8-co-EA0.2)二嵌段无规共聚物的囊泡[其中,nPA表示N-正丙基丙烯酰胺,DEAEMA表示2-(二乙胺基)甲基丙烯酸乙酯,EA表示乙基丙烯酰胺],Poly(nPA0.8-co-DEAEMA0.2)具有温度和pH值双重响应性,poly(nPA0.8-co-EA0.2)具有温度响应性;在水溶液中,其核、壳在不同的pH值与温度条件下可以反转。在pH值为7、温度为25℃时,共聚物溶解在水中;随着温度升高至37℃,聚合物形成poly(nPA0.8-co-EA0.2)为核、Poly(nPA0.8-co-DEAEMA0.2)为外壳的囊泡膜;当温度为25℃、pH值为10时,聚合物形成核壳反转的囊泡膜,而且这些转变过程是可逆的。上述两种聚集体在加热的情况下,会聚集形成大尺寸的群簇。
Mao等[51]用水添加法(WA)和直接溶解法(DD)两种方法制备了具有不同结构的PLLA-b-PDMAEMA共聚物的胶束,其中PLLA是疏水性的,PDMAEMA具有亲水性以及pH值和温度双重响应性,并研究了胶束的pH值/温度响应性行为。在pH=6.2时,随着温度从24.2℃升至46.3℃,WA法制备的胶束的Rh(流体力学半径)都是93.0nm;DD法制备的胶束的Rh从128.3nm升至134.7nm。在pH=7.4时,随着温度从24.2℃升至46.3℃,WA法胶束的Rh从97.8nm变为88.3nm;而DD法胶束的Rh从132.1nm变为118.1nm。在pH=8.3时,从24.2℃升至低于46.3℃的温度,两种胶束的尺寸都增加至几百个纳米的大结构。在pH=8.6时出现了与pH=8.3时类似的现象。但在pH值为8.6时,两种胶束尺寸急剧转变的温度比在pH值为8.3时的转变温度要低。在pH≤7.4时,胶束的Rh比在pH>7.4时要大。同样的,在降温过程中也会呈现出pH值/温度响应性行为。
Johnson等[52]制备了负载DOX的可用于药物载体的刺激响应性的胶束,如图3所示,首先制备两亲性的二嵌段共聚物聚异丙基丙烯酰胺-b-聚左旋组氨酸[p(NIPAM)55-b-p(His)n],通过聚合物的自组装胶束化将疏水性的抗癌药物DOX包覆于疏水性的核中,由于p(NIPAM)具有可逆的温度响应性,使得共聚物有接近人体体温(37.2℃)的LCST。负载于胶束核中的DOX在类似于人体肝癌细胞的环境(37℃,pH=7.4~6)中,药物得到释放;在pH=7.4的环境中,随着温度的升高,聚合物的溶解性降低,p(NIPAM)的疏水性能提高,胶束不稳定,药物释放。
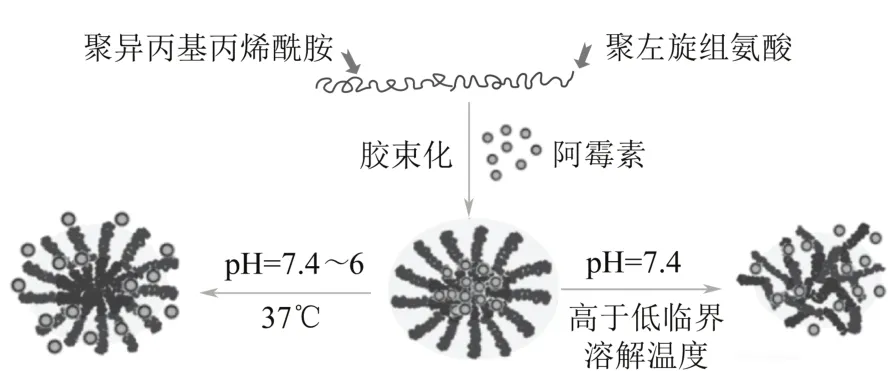
图3 负载DOX的pH值/温度双重响应性胶束进行可控药物释放的示意图[52]
4.4 氧化还原响应性分子自组装
Kim等[53]制备了由苯胺四聚体(疏水性的)和聚乙二醇组成的两亲性刚柔嵌段共聚物,并研究了其氧化还原响应的自组装行为。发现囊泡膜在氧化电压下,棒状的苯胺四聚体平行堆砌的密度发生改变,导致囊泡膜收缩,囊泡破裂转变成更小尺寸的球状胶束;而球状胶束在还原电压下则会再次形成囊泡,而且这一转变过程是可逆的。
Wang等[54]制备了氧化还原响应的两亲共聚物,即聚[6-氧-甲基丙烯酰-右旋吡喃半乳糖-co-2-(N,N-二甲氨基乙基)甲基丙烯酸]-b-吡啶基二硫化甲基丙烯酸乙酯[P(MAGP-co-DMAEMA)-b-PPDSMA],其在水溶液中能够自组装,在胶束化作用下,DOX被包封到胶束内部,向胶束溶液中添加谷胱甘肽(其广泛存在于动物组织中)后,由于谷胱甘肽的硫醇与PPDSMA中的二硫键的交换反应,使形成胶束核的疏水性链段PPDSMA变成亲水性的链段,DOX可以得到释放。同时由于聚合物中半乳糖功能化的基团与肝癌细胞有靶向相互作用,这使得该聚合物可以作为癌症靶向药物以及基因的运输载体,在生物医药领域有潜在应用。
类似地,Khorsand等[55]制备了具有谷胱甘肽响应性的两亲性共聚物,即聚环氧乙 烷-b-二硫键标记的聚甲基丙烯酸酯(PEO-b-PHMssEt),其中PEO是亲水性的。如图4所示,共聚物可以自组装形成用于药物载体的包封疏水性药物DOX的胶束,通过细胞内吞作用(endocytosis),载药的胶束可以进入到细胞质(cytoplasm)中,聚合物链段中的二硫键对细胞质中的谷胱甘肽的硫醇基团具有响应性,二硫键裂解,胶束不稳定,胶束尺寸增大,从而导致抗癌药物的释放,实现癌症治疗的目的。
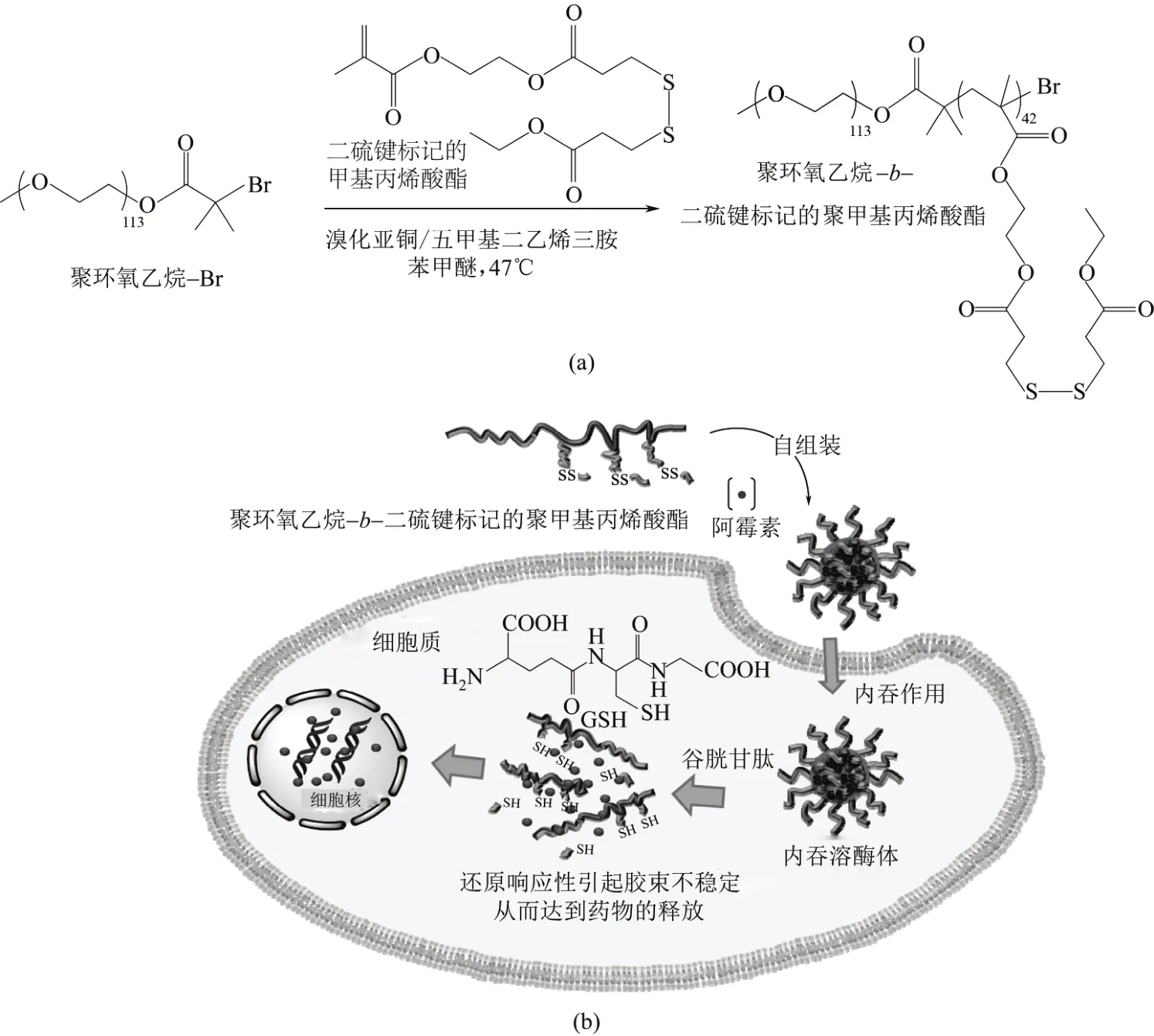
图4 聚环氧乙烷-b-二硫键标记的聚甲基丙烯酸酯(PEO-b-PHMssEt)的制备(a)及其载药性能和DOX对癌症细胞中的谷胱甘肽的响应性释放(b)[55]
同样地,Li等[11]制备了含有交替的PEG和PCL接枝的单裂解的两亲性梳形聚合物,并研究了其还原响应性(即硫醇响应性)。发现在没有还原剂存在的水溶液中,共聚物的聚集体尺寸及其分布是非常稳定的,其聚集体可能是囊泡和胶束的混合物,尺寸在56~226nm;而在还原剂二硫代苏糖醇(DTT)存在的情况下,聚集体是不稳定的,从而诱导聚集体重排和再聚集,其尺寸及分布都受到影响,形成聚集体的尺寸更大。
4.5 溶剂极性响应性分子自组装
Das等[56]制备了发蓝光的萘二亚胺(NDI)功能化的两亲性聚合物的囊泡,并研究了其在不同极性的溶剂(水和非极性的苯)中的可逆囊泡的自组装体。发现在两种不同的溶剂中,聚合物都能够聚集形成具有相同发光性和稳定性的囊泡,但是两者的核壳组成是反转的。在水中,形成了直径大约为200nm的具有较薄外壳的球形中空的囊泡;在苯中,形成了直径大约为350nm的球形的核壳反转的可逆囊泡。而且两种囊泡可在苯-水表界面上稳定存在。
Lee等[57]制备了两亲性可逆的共聚物聚乙烯亚胺-g-聚甲基丙烯酸甲酯(PEI-g- PMMA),其中PEI是亲水性的,PMMA是疏水性的),共聚物在水中可形成PMMA为核、PEI为壳的胶束;而在非极性二氯甲烷(DCM)中则形成核壳反转的胶束组装体。通过移除核中的均聚物可形成中空粒子,在DCM中其Rh为110nm,而在水中其Rh为150nm,这种中空粒子可以在DCM和水中稳定存在,且在可逆反转过程中保持稳定性及完整性。
Hevus等[58]研究了由PEG与PTHF(聚四氢呋喃)、PEG与癸二酸、PEG与十二烷二酸组成的两亲性可逆聚合物(AIPs)的可逆胶束组装体(IMAs)的溶剂极性响应行为。发现在水(极性)中和在正辛醇(非极性)中,聚合物由于构象的可逆性,形成的胶束也是可逆的。这种胶束的可逆组装体可以作为水溶性较差的药物的载体,在水中,聚合物形成胶束,亲脂性的药物包覆在胶束的疏水性的核中;在水-正辛醇的界面处,聚合物构象发生改变;在正辛醇中,聚合物形成了核壳反转的胶束,同时亲脂性的药物溶解在正辛醇中,药物达到释放。
4.6 光响应性分子自组装
Wang等[59]制备了具有光响应性的树枝状的苯乙烯与顺丁烯二酸酐的交替共聚物(PSt-alt-PMAh),聚酰胺胺树突作为共聚物的侧基。聚合物自组装形成的聚集体被紫外光照射后,其聚集体结构发生改变,初始的聚集体变得疏松,尺寸显著增加(15nm变为70nm)。将具有荧光性和光稳定性的尼罗红作为模药包封到聚合物胶束中,经紫外光照射后,尼罗红的荧光强度降低,说明聚合物降解,模药得到释放。聚集体对光的响应性使其在药物载体方面有潜在的应用。
4.7 pH值/酶双重响应性分子自组装
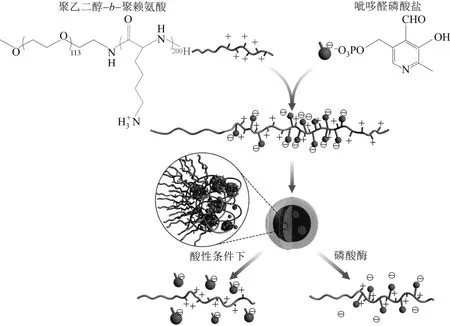
图5 由PEG-b-PLKC及PLP组成的超两性聚合物制备多舱胶束的过程[60]
Wang等[60]提出了基于非共价键或者动态共价键的超两性聚合物的概念,以此概念作为基础,他们制备了双亲水性的聚乙二醇-b-聚赖氨酸(PEG-b-PLKC),PEG是中性的,PLKC含有带正电的胺基,该共聚物中的胺基与水溶性的吡哆醛磷酸盐(PLP),含有醛基和带负电荷的磷酸盐基团)上的醛基形成亚胺基团,导致反应位点表面电荷发生反转,这使得赖氨酸分子链上部分呈现电中性,使赖氨酸具有疏水性,从而形成超两亲性的聚合物,其在水中自组装形成多舱胶束,如图5所示。所形成的胶束在酸性环境下,亚胺键被破坏,聚合物失去两亲性,胶束聚集体解离;而在磷酸酶环境下,带负电荷的磷酸盐基团被破坏,胶束聚集体同样被解离,聚合物的pH值和酶响应性使其在靶向药物载体方面有潜在的应用。
5 结 语
两亲性聚合物因其同时具有亲水链段和疏水链段而具有独特的性能,在生物医药等领域具有广泛的应用。两亲性聚合物的分子自组装从简单的形成无定形聚集体、结晶诱导形成半结晶聚集体到交联聚集体、再到复杂的刺激响应性(pH值响应、温度响应、pH值/温度双重响应等)的智能型聚集体,已取得了巨大的进步。如今,智能型的分子自组装已成为研究热点,其具有针对性、靶向性、智慧性的特点,使其在医药领域方面的应用具有尤为广阔的前景。结晶诱导分子自组装以及智能型分子自组装应是未来的研究热点。
[1]Ji X F,Dong S Y,Wei P F,et al. A novel diblock copolymer with a supramolecular polymer block and a traditional polymer block:Preparation,controllable self-assembly in water,and application in controlled release[J].Advanced Materials,2013,25:5725-5729.
[2]He W N,Zhou B,Xu J T,et al. Two growth modes of semicrystalline cylindrical poly(ε-caprolactone)-b-poly(ethylene oxide) micelles[J].Macromolecules,2012,45:9768-9778.
[3]Garofalo C,Capuano G,Sottile R,et al. Different insight into amphiphilic PEG-PLA copolymers:Influence of macromolecular architecture on the micelle formation and cellular uptake[J].Biomacromolecules,2014,15(1):403-415.
[4]Bensaid F,Thillaye du Boullay O,Amgoune A,et al. Y-shaped mPEG-PLA cabazitaxel conjugates:Well-controlled synthesis by organocatalytic approach and self-assembly into interface drug-loaded core-corona nanoparticles[J].Biomacromolecules,2013,14(4):1189-1198.
[5]Feng C,Lu G L,Li Y J,et al. Self-assembly of amphiphilic homopolymers bearing ferrocene and carboxyl functionalities:Effect of polymer concentration,β-cyclodextrin,and length of alkyl linker[J].Langmuir,2013,29:10922-10931.
[6]Chang H Y,Lin Y L,Sheng Y J. Structural characteristics and fusion pathways of onion-like multilayered polymersome formed by amphiphilic comb-like graft copolymers[J].Macromolecules,2013,46(14):5644-5656.
[7]Huang W,Wang Y J,Zhang S,et al. A facile approach for controlled modification of chitosan under γ-ray irradiation for drug delivery[J].Macromolecules,2013,46:814-818.
[8]Chen W,Zou Y,Jia J N,et al. Functional poly(ε-caprolactone)sviacopolymerization ofε-caprolactone and pyridyl disulfide-containing cyclic carbonate:Controlled synthesis and facile access to reduction-sensitive biodegradable graft copolymer micelles[J].Macromolecules,2013,46:699-707.
[9]Liu H H,Li S X,Zhang M J,et al. Facile synthesis of ABCDE-type H-shaped quintopolymers by combination of ATRP,ROP,and click chemistry and their potential applications as drug carriers[J].Journal of Polymer Science Part A:Polymer Chemistry,2012,50:4705-4716.
[10]Zhang M J,Liu H H,Shao W,et al. Synthesis and properties of multicleavable amphiphilic dendritic comblike and toothbrushlike copolymers comprising alternating PEG and PCL grafts[J].Macromolecules,2013,46:1325-1336.
[11]Li S X,Ye C N,Zhao G D,et al. Synthesis and properties of monocleavable amphiphilic comblike copolymers with alternating PEG and PCL grafts[J].Journal of Polymer Science Part A:Polymer Chemistry,2012,50:3135-3148.
[12]Ozdemir F,Keul H,Mourran A,et al. Polyglycidol based amphiphilic double-comb copolymers and their self-association in aqueous solution[J].Macromolecular Rapid Communications,2011,32:1007-1013.
[13]Choi I,Malak S T,Xu W N,et al. Multicompartmental microcapsules from star copolymer micelles[J].Macromolecules,2013,46:1425-1436.
[14]Gao C,Wang Y,Gou P F,et al. Synthesis and characterization of resorcinarene-centered amphiphilic A8B4miktoarm star copolymers based on poly(ε-caprolactone) and poly(ethylene glycol) by combination of CROP and “click” chemistry[J].Journal of Polymer Science Part A:Polymer Chemistry,2013,51:2824-2833.
[15]Yuan W Z,Zhang J C,Wei J R,et al. Synthesis,characterization,and properties of tunable thermosensitive amphiphilic dendrimer-star copolymers with Y-shaped arms[J].Journal of Polymer Science Part A:Polymer Chemistry,2011,49:4071-4080.
[16]Xu Y C,Dong C M. Dendron-like poly(ε-benzyloxycarbonyl-llysine)/linear PEO block copolymers:Synthesis,physical characterization,self-assembly,and drug-release behavior[J].Journal of Polymer Science Part A:Polymer Chemistry,2012,50:1216-1225.
[17]Wang G W,Hu B,Fan X S,et al. Synthesis of amphiphilic tadpole-shaped copolymers by combination of glaser coupling with living anionic polymerization and ring-opening polymerization[J].Journal of Polymer Science Part A:Polymer Chemistry,2012,50:2227-2235.
[18]Ray J G,Naik S S,Hoff E A,et al. Stimuli-responsive peptide-based ABA-triblock copolymers:Unique morphology transitions with pH[J].Macromolecular Rapid Communications,2012,33:819-826.
[19]Lonsdale D E,Monteiro M J. Synthesis and self-assembly of amphiphilic macrocyclic block copolymer topologies[J].Journal of Polymer Science Part A:Polymer Chemistry,2011,49:4603-4612.
[20]Zhang L,Feng Y K,Tian H,et al. Amphiphilic depsipeptide-based block copolymers as nanocarriers for controlled release of ibuprofen with doxorubicin[J].Journal of Polymer Science Part A:Polymer Chemistry,2013,51:3213-3226.
[21]Mckenzie B E,Nudelman F,Bomans P H H,et al. Temperature-responsive nanospheres with bicontinuous internal structures from a semicrystalline amphiphilic block copolymer[J].Journal of the American Chemical Society,2010,132:10256-10259.
[22]Shah M,Ullah N,Choi M H,et al. Amorphous amphiphilic P(3HV-co-4HB)-b-mPEG block copolymer synthesized from bacterial copolyesterviamelt transesterification:Nanoparticle preparation,cisplatin-loading for cancer therapy andin vitroevaluation[J].European Journal of Pharmaceutics and Biopharmaceutics,2012,80:518-527.
[23]Venkataraman S,Chowdhury Z A,Lee A L,et al. Access to different nanostructuresviaself-assembly of thiourea-containing PEGylated amphiphiles[J].Macromolecular Rapid Communications,2013,34:652-658.
[24]Tsai H C,Chang C H,Chiu Y C,et al.In vitroevaluation of hexagonal polymeric micelles in macrophage phagocytosis[J].Macromolecular Rapid Communications,2011,32:1442-1446.
[25]Jain S,Bates F S. On the origins of morphological complexity in block copolymer surfactants[J].Science,2003,300(5618):460-464.
[26]Wu X H,El Ghzaoui A,Li S M. Anisotropic self-assembling micelles prepared by the direct dissolution of PLA/PEG block copolymers with a high PEG fraction[J].Langmuir,2011,27:8000-8008.
[27]Wang L,Zhang C Y,Cong H L,et al. Formation of nanophases in epoxy thermosets containing amphiphilic block copolymers with linear and star-like topologies[J].The Journal of Physical Chemistry B,2013,117:8256-8268.
[28]Hao J,Cheng Y X,Ranatunga R J K U,et al. A combined experimental and computational study of the substituent effect on micellar behavior ofγ-substituted thermoresponsive amphiphilic poly(ε-caprolactone)s[J].Macromolecules,2013,46:4829-4838.
[29]Sun L,Petzetakis N,Pitto-Barry A,et al. Tuning the size of cylindrical micelles from poly(L-lactide)-b-poly(acrylic acid) diblock copolymers based on crystallization-driven self-assembly[J].Macromolecules,2013,46:9074-9082.
[30]Yuan L,Chen W L,Li J,et al. PEG-b-PtBA-b-PHEMA well-defined amphiphilic triblock copolymer:Synthesis,self-assembly,and application in drug delivery[J].Journal of Polymer Science Part A:Polymer Chemistry,2012,50:4579-4588.
[31]Gou P F,Zhu W P,Shen Z Q. Synthesis,self-assembly,and drug-loading capacity of well-defined cyclodextrin-centered drug-conjugated amphiphilic A14B7miktoarm star copolymers based on poly(ε-caprolactone) and poly(ethylene glycol)[J].Biomacromolecules,2010,11:934-943.
[32]Venkataraman S,Lee A L,Maune H T,et al. Formation of disk- and stacked-disk-like self-assembled morphologies from cholesterolfunctionalized amphiphilic polycarbonate diblock copolymers[J].Macromolecules,2013,46:4839-4846.
[33]Chen L L,Jiang T,Lin J P,et al. Toroid formation through self-assembly of graft copolymer and homopolymer mixtures:Experimental studies and dissipative particle dynamics simulations[J].Langmuir,2013,29:8417-8426.
[34]Pang X C,Zhao L,Akinc M,et al. Novel amphiphilic multi-arm,star-like block copolymers as unimolecular micelles[J].Macromolecules,2011,44(10):3746-3752.
[35]Piyapakorn P,Akagi T,Hachisuka M,et al. Structural analysis of unimer nanoparticles composed of hydrophobized poly(amino acid)s[J].Macromolecules,2013,46:6187-6194.
[36]He J,Huang X L,Li Y C,et al. Self- assembly of amphiphilic plasmonic micelle-like nanoparticles in selective solvents[J].Journal of the American Chemical Society,2013,135:7974-7984.
[37]Schacher F H,Elbert J,Patra S K,et al. Responsive vesicles from the self-assembly of crystalline-coil polyferrocenylsilane-block-poly (ethylene oxide) star-block copolymers[J].Chemistry-A European Journal,2012,18:517-525.
[38]Gwyther J,Gilroy J B,Rupar P A,et al. Dimensional control of block copolymer nanofibers with a π-conjugated core:Crystallization-driven solution self-assembly of amphiphilic poly(3-hexylthiophene)-b-poly(2-vinylpyridine)[J].Chemistry-A European Journal,2013,19:9186-9197.
[39]Zhai F Y,Huang W,Wu G,et al. Nanofibers with very fine core-shell morphology from anisotropic micelle of amphiphilic crystalline-coil block copolymer[J].ACS Nano,2013,7(6):4892-4901.
[40]Glavas L,Olsén P,Odelius K,et al. Achieving micelle control through core crystallinity[J].Biomacromolecules,2013,14:4150-4156.
[41]Wang Y J,Dong C M. Bioreducible and core-crosslinked hybrid micelles from trimethoxysilyl-ended poly(ε-caprolactone)-S-S-poly (ethylene oxide) block copolymers:Thiolene click synthesis and properties[J].Journal of Polymer Science Part A:Polymer Chemistry,2012,50:1645-1656.
[42]Li Y,Akiba I,Harrisson S,et al. Facile formation of uniform shell-crosslinked nanoparticles with built-in functionalities fromN-hydroxysuccinimide-activated amphiphilic block copolymers[J].Advanced Functional Materials,2008,18:551-559.
[43]Surnar B,Jayakannan M. Stimuli-responsive poly(caprolactone) vesicles for dual drug delivery under the gastrointestinal tract[J].Biomacromolecules,2013,14:4377-4387.
[44]Chen D Y,Luo Z T,Li N J,et al. Amphiphilic polymeric nanocarriers with luminescent gold nanoclusters for concurrent bioimaging and controlled drug release[J].Advanced Functional Materials,2013,23:4324-4331.
[45]Kellum M G,Harris C A,McCormick C L,et al. Stimuli-responsive micelles of amphiphilic AMPS-b-AAL copolymers in layer-by-layer films[J].Journal of Polymer Science Part A:Polymer Chemistry,2011,49:1104-1111.
[46]Shen J Y,Chen C Y,Fu W X,et al. Conformation-specific self-assembly of thermo-responsive poly(ethylene glycol)-bpolypeptide diblock copolymer[J].Langmuir,2013,29:6271-6278.
[47]Korchagina E V,Qiu X P,Winnik F M. Effect of heating rate on the pathway for vesicle formation in salt-free aqueous solutions ofthermosensitive cationic diblock copolymers[J].Macromolecules,2013,46:2341-2351.
[48]Zhao J P,Jeromenok J,Weber J,et al. Thermoresponsive aggregation behavior of triterpene-poly(ethylene oxide) conjugates in water[J].Macromolecular Bioscience,2012,12:1272-1278.
[49]Xiang F,Stuart M,Vorenkamp J,et al. One-pot synthesis for biocompatible amphiphilic hyperbranched polyurea micelles[J].Macromolecules,2013,46:4418-4425.
[50]Savoji M T,Strandman S,Zhu X X. Switchable vesicles formed by diblock random copolymers with tunable pH- and thermoresponsiveness[J].Langmuir,2013,29:6823-6832.
[51]Mao J,Bo S Q,Ji X L. pH/temperature-responsive behavior of amphiphilic block copolymer micelles prepared using two different methods[J].Langmuir,2011,27:7385-7391.
[52]Johnson R P,Jeong Y I,John J V,et al. Dual stimuli-responsive poly(n-isopropylacrylamide)-b-poly(l-histidine) chimeric materials for the controlled delivery of doxorubicin into liver carcinoma[J].Biomacromolecules,2013,14:1434-1443.
[53]Kim H,Jeong S M,Park J W. Electrical switching between vesicles and micellesviaredox-responsive self-assembly of amphiphilic rod-coils[J].Journal of the American Chemical Society,2011,133:5206-5209.
[54]Wang Y,Hong C Y,Pan C Y. Galactose-based amphiphilic block copolymers:Synthesis,micellization,and bioapplication[J].Biomacromolecules,2013,14:1444-1451.
[55]Khorsand B,Lapointe G,Brett C,et al. Intracellular drug delivery nanocarriers of glutathione-responsive degradable block copolymers having pendant disulfide linkages[J].Biomacromolecules,2013,14:2103-2111.
[56]Das A,Ghosh S. Luminescent invertible polymersome by remarkably stable supramolecular assembly of naphthalene diimide (NDI) π-system[J].Macromolecules,2013,46:3939-3949.
[57]Lee C H,Wong C H,Ouhab D,et al. Synthesis and characterization of solvent-invertible amphiphilic hollow particles[J].Langmuir,2013,29:7583-7590.
[58]Hevus I,Modgil A,Daniels J,et al. Invertible micellar polymer assemblies for delivery of poorly water-soluble drugs[J].Biomacromolecules,2012,13:2537-2545.
[59]Wang Z J,Gao M,Sun J B,et al. Photoresponsive dendronized copolymers of styrene and maleic anhydride pendant with poly(amidoamine) dendrons as side groups[J].Macromolecules,2013,46:1723-1731.
[60]Wang C,Kang Y T,Liu K,et al. pH and enzymatic double-stimuli responsive multi-compartment micelles from supra-amphiphilic polymers[J].Polymer Chemistry,2012,3:3056-3059.
Research progress of molecular self-assembly of amphiphilic polymers
LI Xuemei,HE Jidong
(Key Laboratory of Rubber-plastics of Ministry of Education,Shandong Provincial Key Laboratory of Rubber-plastics,Qingdao University of Science & Technology,Qingdao 266042,Shandong,China)
Amphiphilic polymers have a wide range of applications in biomedicine and nanotechnology because of their unique structures with both hydrophilic chains and hydrophobic chains. Research progress of aggregates formed by molecular self-assembly of amphiphilic polymers is introduced. Some molecular self-assembled aggregates,such as aggregates controlled by structure,composition and molecular weight,semi-crystalline aggregates,crosslinked aggregates,smart aggregates with stimuli-responsiveness (such as pH,temperature,pH/temperature,redox,solvent polarity) are discussed. Research efforts have been focused on controllability of amphiphilic polymers structure and enhancement of stability of aggregates. Crystallization induced molecular self-assembly and smart molecular self-assembly are future research trends.
amphiphilic polymers;molecular self-assembly;aggregation;nanoparticles;morphology
O 631.1
A
1000-6613(2014)10-2665-12
10.3969/j.issn.1000-6613.2014.10.024
2014-04-01;修改稿日期:2014-06-13。
李雪梅(1989—),女,硕士,主要研究生物医用高分子材料。联系人:贺继东,教授,主要研究功能与特种高分子材料的设计合成、结构与性能。E-mail hejidong@chemist.com。
