镍、锌盐对纳米碳酸钙结晶的影响
2014-06-11薛瑞
薛 瑞
(1.陕西核工业集团综合分析测试中心,陕西西安710024;2.陕西核工业集团211大队)
纳米碳酸钙是一种重要的超细粉体材料。因为其粒径小,比表面积大,已处于原子簇和宏观物体的交界区域,具有体积效应、表面效应、量子尺寸效应和宏观量子隧道效应[1]等纳米材料特有的效应,已在塑料、橡胶、涂料、造纸、油墨、医药和日用品化学等行业得到广泛应用[2]。
碳酸钙存在方解石型、文石型、球霰石等多种晶型,通常以最稳定的方解石型存在。在某些晶型控制剂的影响下,碳酸钙往往会呈现其他几种晶型,或以几种晶型的混合形式出现[3-4]。在普通碳化过程中,由于立方形碳酸钙表面能最低,在自然界中最稳定,所以最后通常会得到立方形碳酸钙超细方解石型颗粒。不同行业对碳酸钙颗粒的形态需求不同:生产油墨需立方形或球形;橡胶行业则需要针形或链状;电子、陶瓷行业要求高纯的球形纳米碳酸钙。因此,针对不同晶型和形态碳酸钙制备技术的研究和开发成为许多国家和科研组织竞相开发的热点[3]。纳米碳酸钙可通过物理方法和化学方法合成,其中化学方法主要包括气相法、液相法和固相法。目前液相法根据反应机理的区别,可以分为Ca2+─H2O─、Ca(OH)2─H2O─CO2、Ca2+─R─(R 为有机介质)等反应系统[5-7]。笔者采用复分解法,设计了适当的反应装置和实验条件,分别使用硝酸镍和硫酸锌作为合成纳米碳酸钙过程中的晶型控制剂,考察了其对纳米碳酸钙结晶的影响,并使用傅里叶变换红外拉曼光谱仪、扫描电子显微镜、X射线衍射分析仪对产物进行表征。
1 实验部分
1.1 试剂及仪器
试剂:无水氯化钙(莱阳化工实验厂)、无水碳酸钠(广东光华化学厂有限公司)、硝酸镍(烟台市双双化工有限公司)、硫酸锌(烟台市双双化工有限公司)、溴化钾(西安化学试剂厂),以上均为分析纯;蒸馏水(自制)。
仪器:SM-6701F型冷场发射型扫描电镜、XRD-7000LX型X射线衍射仪、VERTEX70型傅里叶变换红外拉曼光谱仪、FA1004N型电子分析天平、SHB-ⅢS型循环水式多用真空泵、101-1型电热鼓风干燥箱。
1.2 碳酸钙的制备
将CaCl2和Na2CO3的水溶液分别在60℃水浴中加热至60℃,在水浴和搅拌条件下将Na2CO3溶液以中速倾入CaCl2溶液中,保持水浴温度为60℃,使用磁力搅拌器搅拌使之充分反应3 h。反应结束后,陈化24 h,将样品取出,抽滤,用蒸馏水洗涤3次,烘干后研磨,装入样品袋以备进一步测试。
按照上述步骤和实验条件制备样品,在实验过程中分别加入ZnSO4和Ni(NO3)3的水溶液作晶型控制剂,并按相同步骤处理样品。
分别用傅里叶变换红外拉曼光谱仪(FT-IR)、扫描电子显微镜(SEM)、X射线粉末衍射仪(XRD)对以上3种碳酸钙产物进行表征。
1.3 产物的表征
取少量的碳酸钙样品粉末与一定量的溴化钾混合,干燥后研磨,再用粉末压片机压片制样,进行FT-IR测试。
将碳酸钙样品使用无水乙醇分散,均匀涂在样品台上,喷金处理后进行SEM分析。SEM二次电子图像分辨率:1.0 nm(15 kV),2.2 nm(1 kV);放大倍数:25~650 000 倍;加速电压:0.5~30 kV。
取一定量的碳酸钙粉末压片制样进行XRD的分析与测试,测试条件:Cu靶,Kα辐射,电压为40 kV,电流为 30 mA,λ=0.154 06 nm,2θ=20~80°,扫描速率为 20 (°)/min,步宽为 0.05°。
2 结果与讨论
2.1 FT-IR分析
图1、图 2 为分别添加 Ni(NO3)3和 ZnSO4前后的产物的FT-IR谱图。

图1 无添加剂和添加Ni(NO3)3后样品的 FT-IR谱图
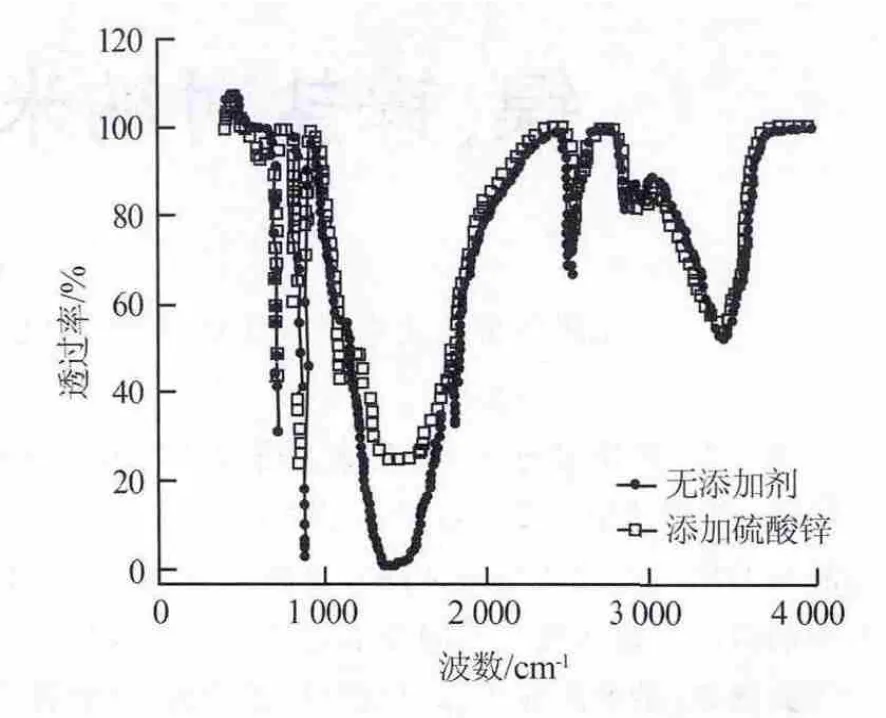
图2 无添加剂和添加ZnSO4后样品的FT-IR谱图
由图1、2中无添加剂的碳酸钙FT-IR谱图可以发现,在 712、875、1 415、3 450 cm-1附近出现了较强的特征吸收峰,在1 799、2 513 cm-1附近出现的是碳酸钙比较弱的特征吸收峰。说明在无添加剂时,使用上述实验方法和条件,生成的碳酸钙颗粒主要为方解石型。
由图 1 可见,添加 Ni(NO3)3后的样品在712、875、1 415、3 450 cm-1附近有明显的振动吸收峰,这些都是方解石型碳酸钙的特征吸收峰。而碳酸钙在1 799、2 513 cm-1附近的另外两个特征吸收峰只有2 513 cm-1处出现,这可能与C=O振动的减弱有一定关系。此外,在745、1 083 cm-1附近可以观察到明显的球霰石特征峰,说明产物中可能混有少量的球霰石型碳酸钙颗粒。
由图 2可见,添加 ZnSO4后的样品在 712、875 cm-1附近出现方解石的特征吸收峰,1 415、3 450 cm-1附近出现了碳酸钙的特征吸收峰,在745、1 083 cm-1附近可以观察到碳酸钙较弱的2个吸收峰。1 415 cm-1附近碳酸钙的吸收峰相比有一定的减弱,可能是Zn2+及SO42-的影响,使碳酸钙的微晶结构发生了变化,晶格结构存在许多缺陷,有较大的畸变应力,导致使吸收峰宽化的晶体场效应变弱,多重峰叠加减弱甚至消失,弱化了吸收峰。
2.2 SEM分析
图3 为添加 Ni(NO3)3和 ZnSO4前后的碳酸钙颗粒的SEM形貌照片。
从图3a、3b可见,在没有添加剂的情况下,碳酸钙颗粒呈椭球状或者不规则的方形及其他不规则形状,团聚非常严重,大小分布很不均匀,颗粒表面也比较粗糙,颗粒不够饱满。
从图 3c、3d 可见,添加 Ni(NO3)3会对碳酸钙产物产生明显影响。产物有柱状、棱柱状、球状以及一些不规则的形状。产物分散度不好,有一定程度的团聚,且大小分布不很均匀,颗粒的表面也不够光滑。

图3 无添加剂和添加 Ni(NO3)3和ZnSO4的碳酸钙样品的SEM照片
从图3e、3f可见,添加ZnSO4对碳酸钙产物的影响比较显著。产品颗粒呈现特征明显的棒状或者棱柱状,且这种棒状或者棱柱状的碳酸钙直径比较均匀,表面也比较平滑,由中心向四周伸展开来,但有时会显得比较杂乱,并且伴有其他不规则的颗粒,存在团聚现象。
2.3 XRD分析
图4、5 为添加 Ni(NO3)3和 ZnSO4前后的碳酸钙产物的XRD谱图。由图4、5可见,无添加剂的碳酸钙产品在衍射角 2θ位于 23.04、29.28、35.98、39.58、43.34、47.52、48.76°附近存在方解石型碳酸钙的特征衍射峰, 分别对应 (102)、(104)、(110)、(113)、(202)、(018)和(116)晶面,没有发现明显的球霰石型或者文石型碳酸钙的特征衍射峰,表明使用复分解法在无添加剂时生成方解石型碳酸钙颗粒。
由图 4可见,添加 Ni(NO3)3后的碳酸钙产品在衍射角 2θ位于 21.08、25.1、27.24、32.96、44.08、50.34、55.92°附近存在球霰石型碳酸钙的特征衍射峰,分别对应 (002)、(100)、(101)、(102)、(110)、(104)、(202)晶面。 在 23.04、29.48、36.16、39.58、47.5、48.82、57.66°附近的衍射峰分别对应方解石的(012)、(104)、(110)、(113)、(018)、(116)、(122)晶面,样品的衍射峰与标准谱图相对应,说明产物主要以方解石和球霰石型为主。通过比较可以发现,Ni3+会使方解石型碳酸钙的衍射峰有明显的减弱,说明Ni3+可能有利于球霰石型碳酸钙的生成。

图4 无添加剂和添加Ni(NO3)3后样品的XRD谱图

图5 无添加剂和添加ZnSO4后样品的XRD谱图
由图5可见,添加ZnSO4后的碳酸钙产品在衍射 角 2θ位 于 23.24、29.5、36.2、39.56、43.18、47.68、48.82、55.9、57.38°附 近的衍射峰 分 别 对 应 (012)、(104)、(110)、(113)、 (202)、 (018)、(116)、 (211)、(122)晶面,对照标准谱图后可确定产物中存在方解石型碳酸钙。此外,衍射角2θ位于26.24、27.26、33.1、37.3、37.9、38.46、39.56、50.16°附近的衍射峰分别对应 (111)、(021)、(121)、(031)、(112)、(130)、(211)、(221)晶面,可以确定为文石型碳酸钙的特征衍射峰。同时,对比图5中的谱线a可以发现,方解石的特征衍射峰有一定程度的减弱,说明在ZnSO4的作用下,使用上述实验方法和条件,反应会生成文石型和方解石型的碳酸钙晶体。
3 结论
利用CaCl2与Na2CO3的复分解反应合成碳酸钙微晶颗粒。在反应过程中分别使用Ni(NO3)3和ZnSO4作为晶型控制剂,考察了这2种过渡金属盐类的添加对碳酸钙微晶的影响,并采用傅里叶变换红外光谱仪、扫描电子显微镜、X射线衍射仪对产物样品进行表征。结果表明,Ni(NO3)3和 ZnSO4的加入对碳酸钙的结晶有比较明显的影响。在无添加剂的条件下,碳酸钙微晶颗粒呈椭球状或者不规则的方形及其他不规则形状,团聚非常严重,大小分布很不均匀,颗粒表面也比较粗糙且不够饱满,产物主要为方解石型碳酸钙微晶。Ni(NO3)3的加入使产物变成柱状、棱柱状、球状等形状的微晶颗粒,主要以方解石和球霰石型的碳酸钙颗粒为主。而ZnSO4的添加,使颗粒呈现特征明显的棒状或者棱柱状,生成文石型和方解石型的碳酸钙晶体。
本研究可以为不同添加剂的使用及其效果提供实验数据,确定了较合理的实验方法和条件,为这类反应提供了可行的实验经验和思路。
致谢:西北师范大学/中石油兰州化工研究中心杜晓辉博士在实验准备阶段给予了帮助,在此致以衷心的感谢。
[1]宋根宗,张多.纳米碳酸钙红外光学性质的研究[C]∥2011中国功能材料科技与产业高层论坛论文集(第一卷).重庆:重庆材料研究院学会,2011:322-324.
[2]吉捷,蒋惠亮,殷福珊.纳米级超细碳酸钙的制备研究[J].海湖盐与化工,2003,32(4):8-10.
[3]王勇,赵风云,胡永琪,等.晶型控制剂对沉淀碳酸钙晶型、形态的影响[J].无机盐工业,2006,28(3):5-8.
[4]Helmut Cölfen.Precipitation of carbonates: recent progress in controlled production of complex shapes[J].Current Opinion in Colloid&Interface Science,2003,8(11):23-31.
[5]薛瑞.纳米碳酸钙的结晶控制与表面包覆[D].兰州:兰州交通大学,2012.
[6]张士成,韩跃新,蒋军华,等.纳米碳酸钙的合成方法[J].矿产保护与利用,1998(3):12-15.
[7]杨宇平.纳米碳酸钙的晶形控制与包覆机理[D].兰州:兰州交通大学,2011.
