维生素B12注射液细菌内毒素检查方法的建立*
2014-05-02武海萍卜莹张心悦周国华
武海萍,卜莹,张心悦,周国华
1南京军区联勤部药品仪器检验所,南京 210002;2南京大学医学院附属金陵医院药理科,南京 210002
维生素B12注射液细菌内毒素检查方法的建立*
武海萍1,卜莹1,张心悦1,周国华2**
1南京军区联勤部药品仪器检验所,南京 210002;2南京大学医学院附属金陵医院药理科,南京 210002
目的:建立维生素B12注射液的细菌内毒素检查方法。方法:按《中国药典》2010年版二部(附录ⅪE)的细菌内毒素检查方法及指导原则进行实验。结果:维生素B12注射液的最大不干扰浓度为0.25 mg·mL-1。在内毒素限值确定为400 EU·mg-1情况下,用灵敏度为0.25 EU·mL-1的鲎试剂按凝胶限度检查法对6批次供试品进行细菌内毒素检查,结果均符合规定。结论:建议药典增加维生素B12注射液的细菌内毒素检查项,规定每1mg维生素B12中含内毒素的量应小于400EU。
维生素B12注射液;细菌内毒素;凝胶限度检查法
维生素B12注射液临床上主要用于治疗原发性或继发性内因子缺乏所致的巨幼细胞贫血,还可用于神经炎的辅助治疗等。《中国药典》2010年版二部中维生素B12注射液未收载细菌内毒素检查项[1],而《美国药典》(USP35-NF30)中已收载[2]。为了进一步加强对注射液的质量控制,依据《中国药典》2010年版二部中有关细菌内毒素的检查方法[1]及相关文献[3-6],进行维生素B12注射液干扰试验,建立了维生素B12注射液的细菌内毒素检查方法。
1 材料
1.1 仪器
HG202-2型电热干燥箱;ET-96型细菌内毒素凝胶检测仪;WH-3型旋涡混合器;Eppendorf微量移液器;无热原吸头。
1.2 试剂
细菌内毒素工作标准品(效价160 EU/支,批号150601-201174,中国食品药品检定研究院);鲎试剂(灵敏度0.25 EU·mL-1,批号1206152,湛江安度斯生物有限公司);鲎试剂(灵敏度0.25 EU·mL-1,批号1206190,湛江博康海洋生物有限公司);细菌内毒素检查用水(BET水,批号1110170,湛江安度斯生物有限公司)。
1.3 试药
维生素B12注射液(规格1 mL∶0.5 mg,批号1108182、1103251、1108192,天津药业集团新郑股份有限公司);维生素B12注射液(规格1 mL∶0.5 mg,批号20101210、21109021、21110071,湖北天药药业股份有限公司)。
2 方法与结果
2.1 内毒素限值的确定
根据《中国药典》2010年版二部(附录ⅪE)的有关要求[1],内毒素限值(L)按以下公式计算:L=K/ M。式中K为人每千克体重每小时最大可接受的内毒素剂量,注射剂K=5 EU/(kg·h);M为人用每千克体重每小时的最大供试品剂量。《临床用药须知》2010年版中规定维生素B12注射液的每日最大用量为500 μg[7]。因此代入公式计算,得到L值为600 EU·mg-1。而《美国药典》中规定每1 μg维生素B12中含内毒素的量应小于0.4 EU,其限值较公式计算出的数值更加严格。为保障安全用药,故将维生素B12注射液的内毒素限值确定为400 EU·mg-1。
2.2 鲎试剂灵敏度的复核
为了考察鲎试剂灵敏度的标示值(λ)是否准确、人员操作方法是否正确及实验条件是否符合规定,按《中国药典》2010年版二部(附录ⅪE)中细菌内毒素规定λc应在0.5 λ~2 λ(包括0.5 λ和2 λ)。本实验结果显示,批号1206152的鲎试剂λc值等于0.5 λ,批号1206190的鲎试剂λc值等于λ,均符合药典规定,可以其标示灵敏度0.25 EU·mL-1用于细菌内毒素检查。
2.3 干扰试验的预实验
为确定维生素B12注射液在多大浓度下对内毒素和鲎试剂的反应不存在干扰作用,首先进行干扰试验的预实验。按照公式最大稀释倍数Dλ0.03=CL/ λ0.03,计算得到维生素B12注射液Dλ0.03=6666.7,即最大的稀释倍数不得超过6666.7倍。因此将维生素B12注射液供试品用BET水分别稀释2、20、200、800、1600、3200、6400倍,将此系列溶液记为供试品阴性对照(NPC);制备同样系列浓度的供试液,并使每个稀释倍数的供试液中均含有2 λ浓度的内毒素标准溶液,记此系列溶液为供试品阳性对照(PPC)。取灵敏度为0.25 EU·mL-1的鲎试剂,分别对上述NPC和PPC溶液进行检验,每一个平行做2支;另取2支鲎试剂加入2 λ浓度的内毒素标准溶液作为阳性对照(PC);2支加入BET水作为阴性对照(NC)。37℃保温60 min后,观察记录结果。
使用两个厂家鲎试剂的检验结果见表1。阴性对照均为阴性,阳性对照均为阳性,表明实验有效;两个厂家的鲎试剂检验结果相同,2个供试品对鲎试剂的反应结果也相同,表明该品种适于建立内毒素检查法;在系列浓度中出现供试品阳性对照为阳性且供试品稀释液为阴性的最小稀释倍数为2,即维生素B12注射液的最大不干扰浓度为0.25 mg· mL-1。

表1 维生素B12注射液干扰试验预实验结果
2.4 正式干扰试验
根据预实验结果,在进行正式干扰试验时选择供试品的不干扰浓度为0.0625 mg·mL-1。取两个不同厂家的共6个供试品,用BET水稀释8倍至终浓度为0.0625 mg·mL-1,分别用0.0625 mg·mL-1的供试品稀释液和BET水稀释细菌内毒素标准品,制备成含0.5、0.25、0.125、0.0625EU·mL-14种浓度内毒素的系列溶液。按照《中国药典》2010年版中的凝胶法进行干扰试验,测定结果如表2所示。
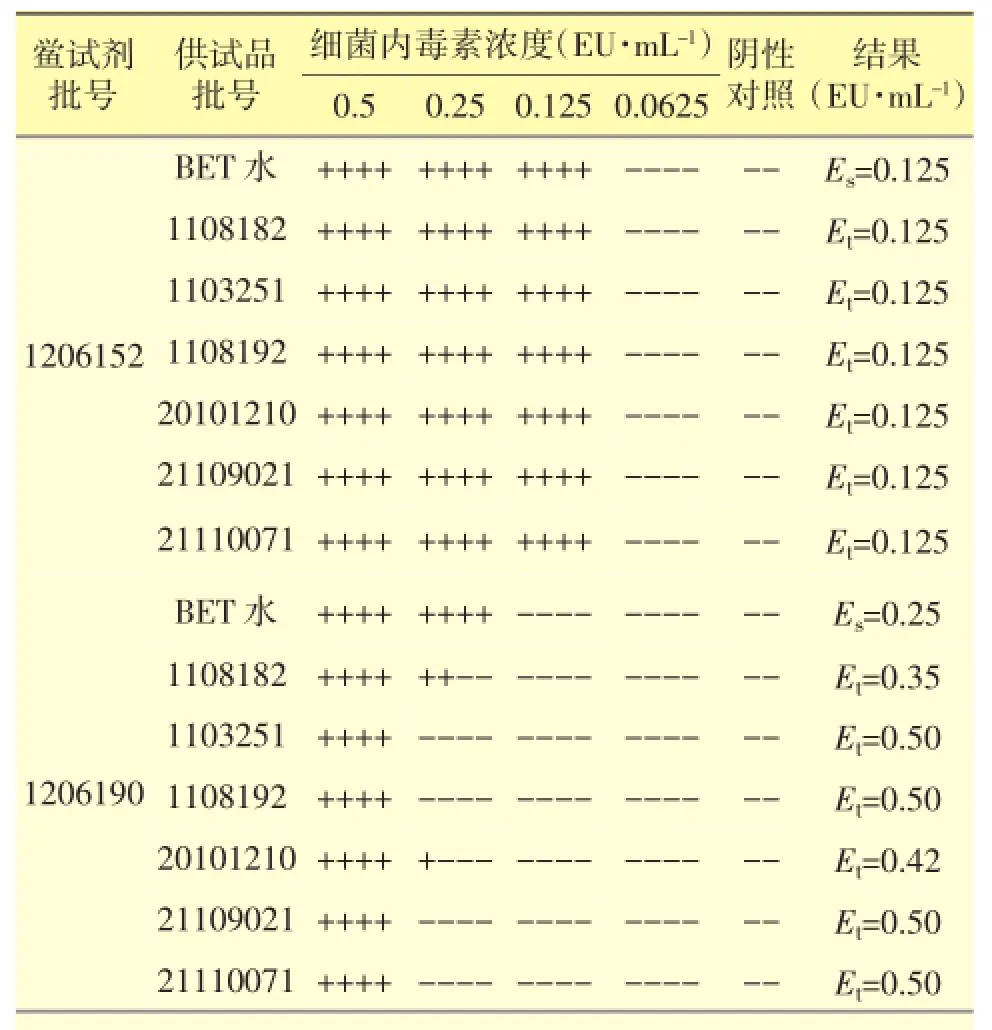
表2 维生素B12注射液干扰试验结果
使用湛江安度斯生物有限公司生产的鲎试剂(批号1206152)的检验结果显示,Es等于0.5 λ(0.125 EU·mL-1),且6批供试品的Et值均等于Es。使用湛江博康海洋生物有限公司生产的鲎试剂(批号1206190)的检验结果显示,Es等于λ(0.25 EU· mL-1),且6批供试品的Et值均在0.5~2 Es(0.125~0.5 EU·mL-1)。《中国药典》2010年版中规定Es在0.5~2 λ(包括0.5 λ和2 λ)及Et在0.5~2 Es(包括0.5 Es和2 Es)时,认为供试品在该浓度下无干扰作用。因此,本干扰试验的结果表明,用两个厂家的鲎试剂(灵敏度均为0.25 EU·mL-1)进行检验,该6批供试品在8倍稀释条件下均无干扰作用。
2.5 供试品细菌内毒素检查
用灵敏度为0.25 EU·mL-1的鲎试剂,按《中国药典》2010年版二部(附录ⅪE)中的凝胶限度试验检查法,对6批次供试品进行细菌内毒素检查。计算最大有效稀释倍数MVD=800。将供试品稀释800倍制备成供试品溶液(NPC),制备供试品溶液中含2 λ浓度的内毒素标准品(PPC),同时设立阳性对照即2 λ浓度的内毒素标准品,阴性对照即BET水。检验结果显示6批次供试品的检验结果均符合内毒素限值为400 EU·mg-1的规定。
3 讨论
供试品对不同厂家的鲎试剂的干扰程度可能存在不同,因此在干扰试验的预实验中使用了两个不同厂家的鲎试剂,分别对两个生产厂家各2个批次的维生素B12注射液进行凝胶法内毒素检查,结果显示两个厂家的鲎试剂检验结果相同,不同生产厂家以及同一厂家不同批次的供试品对鲎试剂的反应结果也无差异,因此确定维生素B12注射液的最大不干扰浓度为0.25 mg·mL-1。在正式干扰实验中,将供试品稀释至0.0625 mg·mL-1,用两个厂家的鲎试剂进行干扰验证,结果显示Es均在0.5~2 λ范围,6个供试品的Et均在0.5~2Es范围,确认在该浓度下供试品无干扰作用。
在内毒素限值确定为400 EU·mg-1情况下,用灵敏度为0.25 EU·mL-1的鲎试剂按凝胶限度检查法对6批次供试品进行细菌内毒素检查,结果均符合规定,表明维生素B12注射液可适用凝胶法进行细菌内毒素检查。因此,建议《中国药典》增加维生素B12注射液的细菌内毒素检查项,规定每1 mg维生素B12中含内毒素的量应小于400 EU。
[1] 国家药典委员会.中华人民共和国药典:二部[S].北京:中国医药科技出版社,2010:901,附录99-101.
[2] The United States Pharmacopeial Convention.United States Pharmacopoeia(USP35-NF30)[S].United Book Press,Inc.,Baltimore,MD,2012:2784.
[3] 中国药品生物制品检定所.中国药品检验标准操作规范[S].北京:中国医药科技出版社,2010:310-25.
[4] 樊华,林鹏,焉媛媛,等.9个生产企业清开灵注射液细菌内毒素检查方法学研究[J].辽宁中医药大学学报,2014,16(4):48-50.
[5] 时荣同,谢冬梅,郭道华,等.地佐辛注射液细菌内毒素检查法研究[J].中国实用医药,2013,8(31):3-4.
[6] 代秀梅,于风平.氟马西尼注射液细菌内毒素检查方法的建立[J].中国药房,2014,25(21):2003-4.
[7] 国家药典委员会.中华人民共和国药典临床用药须知:化学药和生物制品卷[S].北京:中国医药科技出版社,2010:1052-4.
Development of Bacterial Endotoxin Test Method for Vitamin B12Injection
WU Hai-ping1,BU Ying1,ZHANG Xin-yue1,ZHOU Guo-hua2*
1The Institute of Quality Control of Medical Material and Equipment under the Joint Logistic Department of Nanjing Command,Nanjing 210002;2Department of Pharmacology,Jinling Hospital,Medical School of Nanjing University,Nanjing,210002,China
Objective:To establish a detection method of the bacterial endotoxin in Vitamin B12injection.Methods:The experiments were done according to the bacterial endotoxin detection method and guiding principles in Chinese Pharmacopoeia 2010 edition(appendixⅪE).Results:The maximum undisturbed concentration of vitamin B12injection was 0.25 mg·mL-1in the bacterial endotoxin test.Six batches of samples were detected by using limulus reagents wit sensitivity at 0.25 EU·mL-1,and the results were all qualified to the standards under the threshold of bacterial endotoxin within 400 EU·mg-1.Conclusion:The bacterial endotoxin inspection items should be supplied in Chinese Pharmacopoeia,and the amount of bacterial endotoxin in Vitamin B12should be under 400 EU per mg.
Vitamin B12injection;Bacterial endotoxin;Gel limit test
R927.12
A
1673-7806(2014)06-521-03

第54批中国博士后科学基金面上资助项目(2013M542575);国家自然科学基金项目(31300706)
武海萍,女,博士,主管药师,研究方向:药物分析 E-mail:fenger19800512@126.com
**通讯作者 周国华,男,主任药师 E-mail:ghzhou@nju.edu.cn
2014-06-29
2014-07-18
