高效液相色谱法测定米非司酮血药浓度
2014-04-26邓洁雄肖洋娟颜惠芳
邓洁雄,肖洋娟,颜惠芳
(1.广州市药品检验所 四分所,广东 广州 510405;2.广州市荔湾区骨伤科医院,广东 广州510140)
高效液相色谱法测定米非司酮血药浓度
邓洁雄1,肖洋娟1,颜惠芳2
(1.广州市药品检验所 四分所,广东 广州 510405;2.广州市荔湾区骨伤科医院,广东 广州510140)
目的:建立高效液相色谱法测定血浆中米非司酮的浓度。方法:采用固相萃取技术处理血浆样品,以炔诺酮为内标,Phenomenex Synergi 4u Fusion-RP 80A C18柱(4.6mm×250mm,4μm)为分析柱,流动相为甲醇-水(75∶25),流速1.0mL·min-1,柱温:25℃。采用双波长法检测,炔诺酮的检测波长为240nm,米非司酮检测波长为302nm。结果:米非司酮的线性范围为0.01~2.0μg·mL-1,最低定量限为0.01μg·mL-1,回归方程为Y=1.6439X-0.0297,r=0.9998。结论:该方法简便、准确、灵敏,适用于米非司酮药代动力学研究。
米非司酮;血药浓度;固相萃取;内标法;高效液相色谱法
米非司酮(mifepristone)是一种甾体类抗孕激素药物,临床广泛应用于终止早孕、引产等[1]。目前报道的有关血浆中米非司酮浓度测定的方法有放射性免疫测定法(RIA)[2]、放射性受体测定法(RRA)[3]、高效液相色谱法(HPLC)[4]。RIA和RRA方法无法区分米非司酮母体和代谢物,且实验过程复杂、危险、成本高,因此这两种方法的使用受到限制。在报道的HPLC方法中,国内有研究[4-5]采用乙醚萃取方法处理样本,由于乙醚提取的样品中血浆内源性杂质太多,干扰米非司酮测定;国外有研究报道,Stith等[6]采用固相萃取技术测定米非司酮血药浓度,但该方法所用内标物RTI-3021-003难以获得,另有国外文献[7]以炔诺酮为内标,采用固相萃取技术测定血浆中米非司酮浓度,其炔诺酮与血浆内源性物质分离效果差,影响测定结果的准确性。本研究通过优化固相萃取方法中清洗步骤,消除了血浆内源性物质对米非司酮及炔诺酮测定的干扰,建立了一种专属性强、灵敏度高的HPLC方法测定血浆中米非司酮浓度,为药代动力学研究和生物等效性评价提供了可靠的保证。
1 材料和对象
1.1 仪器
日本Shimadzu公司LC-20AT泵,SIL-20A全自动进样器,SPD-M20A二极管阵列检测器,LC-Solution工作站;德国IKA MS2涡旋混合器;TCL-16G高速台式离心机(上海安亭科学仪器厂);固相萃取仪(天津奥特赛恩斯仪器有限公司);Oasis HLB固相萃取小柱(1cc/30mg)由Waters公司提供。
1.2 药品和试剂
炔诺酮对照品(100053-200705)由中国食品药品检定研究院提供;米非司酮原料药由浙江仙琚制药股份有限公司提供,批号:100131;米非司酮普通片剂(规格:10mg)由北京紫竹药业有限公司提供,批号:43090105;甲醇为色谱纯(SK Chemicals),磷酸为分析纯(天津富宇精细化工有限公司),水为重蒸馏水。
1.3 实验动物
雌性Spague-Dawley大鼠,体重(200±20)g,由广州中医药大学实验动物中心提供。
2 色谱条件
色谱柱:Phenomenex Synergi 4u Fusion-RP 80A C18柱(4.6mm×250mm,4μm);流动相:甲醇-水(75∶25);流速:1.0mL·min-1;检测波长:炔诺酮采用240nm,米非司酮采用310nm,柱温:25℃,进样量:30μL。
3 样品处理
3.1 对照品溶液和内标溶液的制备
对照品溶液的配制:精密称取10mg米非司酮置于100mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,得到米非司酮对照品储备液。分别精密量取储备液0.025、0.125、0.25、0.5、1.25、2.5、5.0mL置于50mL量瓶中,用0.025%磷酸稀释至刻度,得浓度分别为0.05、0.25、0.5、1.0、2.5、5.0、10.0μg·mL-1的系列对照品溶液。
内标溶液的配制:精密称取10mg炔诺酮置于100mL量瓶中,甲醇溶解并稀释至刻度,摇匀,得炔诺酮对照品储备液。精密量取储备液1.25mL置于50mL量瓶中,用0.025%磷酸稀释至刻度,配成2.5μg·mL-1的内标溶液。
3.2 血浆样品处理
HLB小柱用1mL甲醇进行活化,1mL重蒸馏水平衡,备用。取血浆样品150μL加入内标溶液30μL,涡旋2min,加入1mol·L-1磷酸30μL,涡旋2min,静置5min后上样。用3mL重蒸馏水清洗小柱,再用1mL 0.5%甲醇清洗小柱1次,弃去清洗液。最后用1mL甲醇洗脱样品,洗脱液置于50℃真空干燥箱中挥干。洗脱液挥干后用100μL 50%甲醇溶解,涡旋2min, 16 000rpm离心4min,取上清液进样。
4 方法与结果
4.1 方法专属性
在上述色谱条件下测得空白血浆及空白血浆加样色谱,见图1。内标炔诺酮、米非司酮的保留时间分别为7.2、13.6 min,结果表明血浆中无内源性物质干扰炔诺酮及米非司酮。
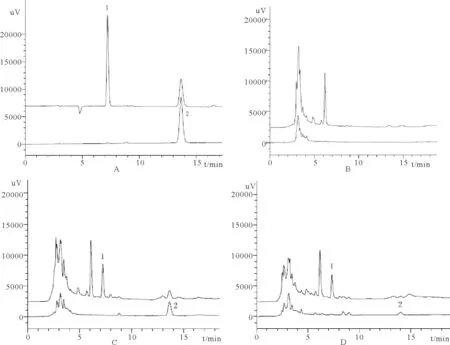
图1 米非司酮+炔诺酮溶液(A)、空白血浆(B)、空白血浆+米非司酮+炔诺酮(C)、大鼠给药后血浆样品(D)色谱
4.2 线性关系及灵敏度
取大鼠空白血浆150μL,加入不同浓度的米非司酮系列对照品溶液30μL及内标溶液30μL,使血浆中米非司酮的浓度分别为0.01,0.05,0.1,0.2,0.5,1.0,2.0μg·mL-1,内标炔诺酮浓度为0.5μg·mL-1。自“加入1mol·L-1磷酸30μL”,按“3.2”项下方法操作,以血浆中米非司酮的浓度为横坐标,米非司酮与内标的峰面积之比为纵坐标绘制标准曲线,回归方程为:Y=1.6439X-0.0297,r=0.9998,定量下限为0.01μg/mL-1,结果表明米非司酮在0.01~2.0μg·mL-1浓度范围内线性关系良好。
4.3 绝对回收率
按“4.2”项下方法制备米非司酮低、中、高(0.05、0.5、2.0μg·mL-1)三个浓度的对照品血浆质控样本(QC),每个浓度平行制备5份样品,自“加入1mol·L-1磷酸30μL”,按“3.2”项下操作处理后进样,记录米非司酮的峰面积为As。另取对照品储备液适量,用0.025%磷酸稀释成相应浓度的米非司酮溶液,不经处理直接进样,记录米非司酮的峰面积为Asd。血浆中米非司酮的绝对回收率=As/Asd×100%。按公式计算低、中、高三个浓度下血浆中米非司酮的绝对回收率,结果见表1。
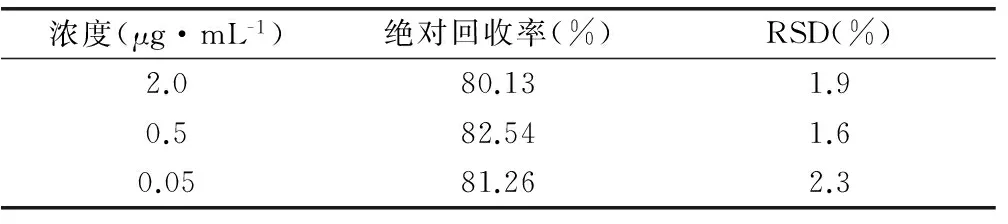
表1 血浆中米非司绝对回收率 (n=5)
4.4 精密度和准确度
按“4.2”项下方法制备米非司酮低、中、高三个浓度(0.05、0.5、2.0μg·mL-1)质控样本,每个浓度平行制备6份样品,自“加入1mol·μL-1磷酸30μL”,按“3.2”项下操作处理后进样,连续测定3天并与标准曲线同时进行,以当日的标准曲线计算质控样本的浓度,精密度以实际测得量的相对标准偏差(RSD)表示,计算日内RSD和日间RSD。准确度以质控样品实测浓度值与理论浓度值之比计算,结果见表2。
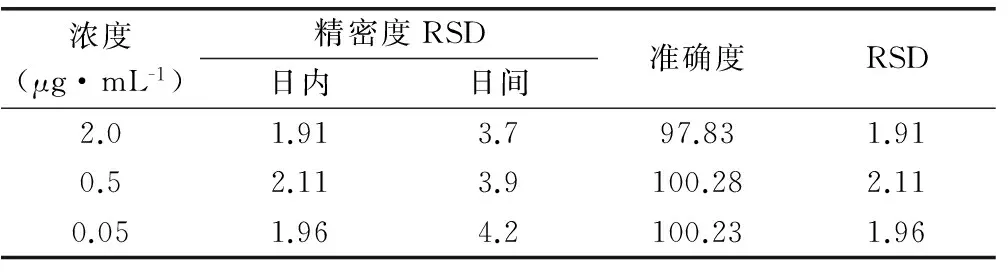
表2 米非司酮的日内、日间精密度和准确度 (%)
4.5 稳定性试验
4.5.1 室温稳定性 按“4.2”项下方法制备米非司酮低、中、高三个浓度(0.05、0.5、2.0μg·mL-1)质控样本,每个浓度平行制备3份样品,于室温分别放置不同时间后,自“加入1mol·L-1磷酸30μL”,按“3.2”项下操作处理后进样,与0h相比求得血浆样本的RSD为3%。结果表明,对照品血浆质控样本在8h内可保持稳定。
4.5.2 冻融稳定性 按“4.2”项下方法制备米非司酮低、中、高三个浓度(0.05、0.5、2.0μg·mL-1)质控样本,每个浓度平行制备3份样品,于-20℃冷冻24h,取出解冻,反复冻融3次后,自“加入1mol·L-1磷酸30μL”,按“3.2”项下操作处理后进样,与未冻融前相比求得标准血浆样本的RSD为3.6%。结果表明,对照品血浆质控样本在冻融条件下可保持稳定。
4.5.3 长期稳定性 按“4.2”项下方法制备米非司酮低、中、高三个浓度(0.05、0.5、2.0μg·mL-1)质控样本,每个浓度平行制备3份样品,于-20℃分别冷冻7、14、21天后取出待完全解冻后,自“加入1mol·L-1磷酸30μL”,按“3.2”项下操作处理后进样,与0h相比求得对照品血浆质控样本的RSD为4.8%。结果表明,对照品血浆质控样本在-20℃条件下可保持21天稳定。
4.6 样品血药浓度测定
取米非司酮片剂10片,碎成细颗粒,备用。取禁食12h的SD大鼠6只,按照5.2mg/kg剂量经特制灌胃针灌胃,试验期间自由饮水,给药后4h给予食物。分别于0.25、0.5、1、2、4、6、8、24h眼眶后静脉丛取血0.5mL,置肝素化离心管中,4 000rpm离心10min,分离血浆,于-20℃下保存,直至分析。按“3.2”项下方法处理后进样分析,各取样时间点的平均血药浓度为240.14、292.77、155.03、83.28、52.73、47.44、43.29、38.41ng·mL-1,其SD分别为7.76%、9.38%、4.14%、2.61%、1.31%、0.41%、0.43%、0.41%,以取样时间点为横坐标,血药浓度为纵坐标作图,结果见图2。
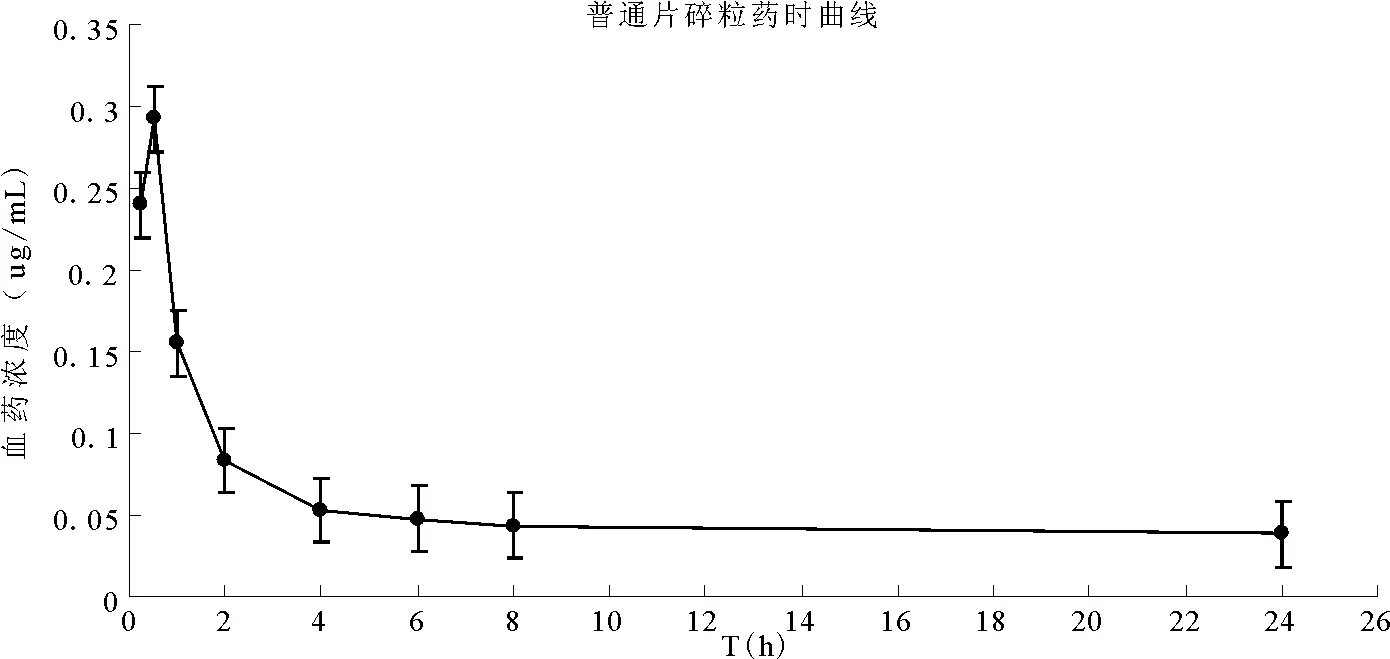
图2 大鼠灌胃米非司酮后的平均血药浓度-时间曲线
5 讨论
5.1 固相萃取条件的选择
加入血浆中的米非司酮对照品溶液及炔诺酮内标溶液若采用甲醇稀释定容,会产生蛋白沉淀,使样品通过固相萃取小柱变得极为困难,故不采用甲醇稀释工作液。由于米非司酮难溶于水,在酸性条件下易溶解,因而采用0.025%的磷酸水溶液(pH值约为2.4)来稀释定容对照品及内标溶液。
为保证被分析物的高回收率并尽可能除去血浆内源性物质,试验过程中考察了几种清洗液:水、5%的甲醇溶液、30%的甲醇溶液、5%甲醇-2%乙酸溶液、5%甲醇-2%氨水溶液对萃取结果的影响。结果表明加大清洗液中有机相的比例,并不能减少待测物质出峰位置的杂质干扰,反而导致部分待测物质在洗脱前已经被清洗出来,降低样品回收率。此外,在5%甲醇中添加一定比例的乙酸或氨水,其清洗效果也未有明显提高。本研究还对水的清洗量进行了比较,发现通过增加水的清洗量,能更好地降低杂质干扰。最后采用以3mL水、1mL0.5%甲醇依次清洗,1mL甲醇洗脱的方法。结果表明,血浆内源性物质与炔诺酮及米非司酮分离度良好,对炔诺酮及米非司酮的测定无干扰,萃取物的绝对回收率高,结果稳定可靠。
5.2 内标物的选择
本研究采用双波长检测方法,以内标法定量分析,提高了分析结果的准确性和可靠性。试验过程中,还对使用左炔诺孕酮和炔诺酮作为内标物质进行了对比。结果显示,左炔诺孕酮主峰位置与血浆内源性物质分离度较差,而采用炔诺酮为内标,与血浆内源性物质分离度好,故选用炔诺酮作为内标物质。
5.3 色谱条件的选择
本试验对比了甲醇-0.2%甲酸溶液(75∶25)、甲醇-0.1%甲酸溶液(75∶25)、和甲醇-水(75∶25)三种流动相的分离效果。发现在酸性条件下,炔诺酮与米非司酮的保留时间大大缩短,与血浆中的内源性物质分离度差,而采用甲醇-水(75∶25)为流动相在保证分析时间不是太长的同时能实现炔诺酮、米非司酮与血浆内源性物质的良好分离。
5.4 方法适用性
本研究建立的米非司酮血浆浓度测定方法,具有操作简便、专属性强、灵敏度高等特点,可满足体内药物浓度测定,适用于米非司酮药代动力学的研究。
[1] BAULIEU EE,SEGAL SJ.The antiprogestin steroid RU 486 and human fertility control[M].New York: Plenum Press,1985:1.
[2] WANG JD, SHI WL, ZHANG GQ, et al.Tissue and serum levels of steroid hormones and RU 486 after administration of mifepristone[J]. Contraception,1994,49( 3) :245.
[3] KAWAI S,NIEMAN L,BRANDON D,et al.Pharmacokinetic properties of the antiglucocorticoid and antiprogesterone steroid RU 486 in man[J].Pharmacol ExpTher,1987,241( 2):401.
[4] GUO ZHIYONG,WEI DANYI,CHU CHENGDING,et al.Determination of mifepristone in human plasma by high performance liquid chromatography[J].PTCA ( PART B:CHEM.ANAL),2007,43(1):15.
[5] WU LIHUA,SHENTU JIANZHONG,ZHANG XIA,et al.Determination of mifepristone in plasma by high performance liquid chromatograph[J].Chinese Journal of Modern Applied Pharmacy,2003,20(1):65.
[6] STITH C,HUSSAIN MD.Determination of mifepristone levels in wild canid serum using liquid chromatography[J].Journal of Chromatography B,2003,794(1):9.
[7] GUO ZY,WANG S,WEI DY,et al.Development of a high-performance liquid chromatographic method for the determination of mifepristone in human plasma using norethisterone as an internal standard: application to pharmacokinetic study[J].Contraception,2007,76(1):228.
(责任编辑:姜付平)
Determination of mifepristone in plasma using HPLC method
Deng Jiexiong, Xiao Yangjuan,Yan Huifang
(1.Guangzhou Fourth Substation Institute For Drug Control, Guangzhou 510405,China;2.Liwan District Orthopedics Hospital of Guangzhou,Guangzhou 510140 China)
Objective:A convenient HPLC method was developd to determine the concentration of mifepristone in plasma.Methods:Solid-phase extration cartridges were used to extract plasma samples .Separation was carried out on a Phenomenex Synergi 4u Fusion-RP 80A C18(4.6mm×250mm,4μm)column maintained at 25℃ with methanol-water(75∶25) as mobile phase at a flow rate of 1.0mL·min-1.Norethisterone was employed as the internal standard. Dual wavelength was used, with norethisterone monitored at 240 nm and mifepristone at 302 nm.Results:The linearity range of mifepristone was 0.01~2.0μg·mL-1and the lowest limit of quantification was 0.01μg·mL-1, the regressive equation was Y = 1.6439X-0.0297,r=0.9998.Conclusion:The method was simple, accurate and sensitive. And it could be applied to study on the pharmacokinetics of mifepristone.
Mifepristone; Plasma Drug Concentration;Solid-Phase Extraction; Internal Standard; HPLC
2014-03-19
邓洁雄(1962-),女,广州市药品检验所四分所主管药师,研究方向为药物分析。
R284
A
1673-2197(2014)11-0019-03
