结核分枝杆菌NrdF1、PE_PGRS35、Rv1985c和Rv1986的原核表达及检测牛结核病抗体之应用
2014-04-02闵晨雨胡亚辰焦新安
孙 林,刘 艳,2,闵晨雨,胡亚辰,陈 祥,焦新安
牛结核病是主要由牛分枝杆菌(Mycobacteriumbovis,M.bovis,M.bhuo或Mb)感染引起的一种慢性消耗性人兽共患传染病,被世界动物卫生组织列为需通报的动物疫病[1],我国将其列为二类动物疫病,该病不仅严重危害畜牧业的健康发展,同样也会引起人结核病的发生,对人类健康造成重大威胁。国际上普遍采用“检疫-扑杀”的手段来对牛结核病进行防控,目前法定的牛结核检疫方法是结核菌素皮内变态反应(tuberculin skin test,TST),但是结核菌素是粗提物,含有200多种组分,与环境分枝杆菌等存在交叉反应,导致假阳性产生,因此迫切需要研制特异的牛结核病诊断方法。
差异区2(region of difference 2,RD2)是BCG在1927-1931年传代过程中丢失的基因片段[2-3],RD2的丢失将有利于BCG进一步的减毒,RD2共包含11个基因,这些基因在所有结核分枝杆菌毒株中保守存在。研究表明,RD2区域中的MPT64和CFP21具有较强的免疫原性[4],现已被用于结核病疫苗和诊断试剂的开发,但是对该区域中的其它组分还知之甚少,特应用大肠杆菌表达系统表达RD2区域的NrdF1、PE_PGRS35、Rv1985c和Rv1986,并分别以此4种融合蛋白纯化产物作为包被抗原进行牛结核病血清学检测,探讨牛结核病新型诊断试剂研制。
1 材料与方法
1.1菌株和载体 大肠杆菌E.coliDH5α、E.coliBL21(DE3)由本实验室保存;灭活的结核分枝杆菌标准株H37Rv由中国疾病预防控制中心传染病预防控制所万康林研究员馈赠;原核表达载体pET-32a(+)由本实验室保存,pEASY-E1购自北京全式金生物技术有限公司。
1.2试剂 限制性内切酶NdeⅠ、XhoⅠ、Hind Ⅲ、PyrobestTMDNA聚合酶、DL2000 DNA Marker、T4 DNA连接酶等购自宝生物工程(大连)有限公司,基因组提取试剂盒购自天根生化科技(北京)有限公司;DNA胶回收试剂盒购自北京百泰克公司;羊抗兔IgG-HRP购自Invitrogen公司;抗His单抗、羊抗鼠IgG-HRP购自Sigma公司;Ni-NTA His Bind®purification Kit购自Novagen公司,BOVIGAMTM牛结核病IFN-γ检测试剂盒购自Prionics公司。
1.3牛血清来源 137份牛血清来源于中国东部某牛场,经牛γ干扰素试验检测,68份样本为阳性,69份样本为阴性。
1.4目的基因的扩增 使用基因组提取试剂盒提取H37Rv基因组DNA,根据http://genolist.pasteur.fr/TubercuList/index.html公布的nrdF1、pe_pgrs35、rv1985c和rv1986序列,设计引物,引物由华大基因有限公司合成,详细序列信息见表1。以所提取的基因组DNA为模板,用高保真DNA聚合酶进行PCR扩增,反应条件为94 ℃预变性5 min;94 ℃ 30 s,Tm 40 s,72 ℃ 30 s,30次循环,72 ℃延伸5 min。
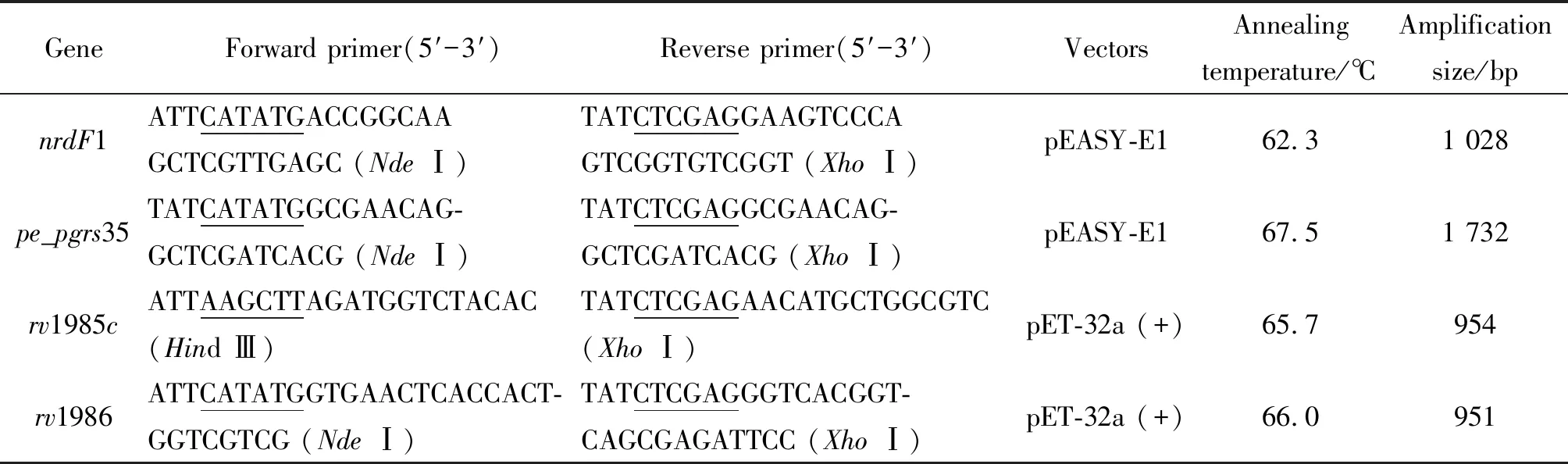
表1 目的基因引物和表达载体
1.5重组表达质粒的构建 目的基因和表达载体分别进行双酶切,基因对应的表达载体及酶切位点信息见表1,酶切产物进行琼脂糖凝胶电泳后分别切胶回收目的片段,将nrdF1和pe_pgrs35基因分别与pEASY-E1载体片段连接,rv1985c和rv1986基因分别与pET-32a (+)载体片段连接,连接产物转化DH5α 感受态细菌,通过Amp+抗性筛选、经NdeⅠ/XhoⅠ或者Hind Ⅲ/XhoⅠ双酶切鉴定,阳性克隆送南京金斯瑞生物科技有限公司测序,测序正确的质粒命名为pEASY-E1-nrdF1、pEASY-E1-nrdF1、pET32a-rv1985c和pET32a-rv1986。
1.6重组蛋白的诱导表达与纯化 将鉴定正确的重组表达质粒转化表达菌E.coliBL21(DE3),重组菌命名为BL21(DE3)(pEASY-E1-nrdF1)、BL21(DE3) ( pEASY-E1-pe_pgrs35)、BL21(DE3)(pET32a-rv1985c)和BL21(DE3)(pET32a-rv1986)。将重组菌小量接种,过夜培养,过夜培养物1∶100扩大培养,37 ℃摇床培养至OD600 nm为0.4~0.5,加入IPTG使其终浓度为0.5 mmol/L,30 ℃诱导5~6 h。4 ℃、8 000 r/min离心收集细菌,PBS充分洗涤2次后进行超声波裂解菌体,分别收集裂解上清和沉淀进行SDS-PAGE,分析蛋白表达情况。融合蛋白的纯化按照Novagen公司的Ni-NTA His Bind®purification Kit说明书进行。
1.7Western-blotting分析 将纯化的NrdF1、PE_PGRS35、Rv1985c和Rv1986融合蛋白进行SDS-PAGE,然后转移至硝酸纤维素膜,含1% BSA的PBST封闭过夜,加入抗HIS单抗,37℃孵育2 h,PBST洗涤3次,与HRP标记的羊抗鼠IgG 37 ℃ 作用1h,PBST洗涤3次,DAB显色并观察结果。
1.8融合蛋白在牛结核病ELISA检测中的初步应用 按照文献[5]方法,利用牛γ干扰素试验进行牛结核病检测,对于检测阳性的样品,分别以NrdF1、PE_PGRS35、Rv1985c和Rv19864种融合蛋白纯化产物作为包被抗原,应用间接ELISA方法对血清中的特异抗体进行检测。
2 结 果
2.1目的基因的PCR 扩增及表达载体的构建 以结核分枝杆菌H37Rv基因组DNA 为模板,PCR 扩增nrdF1、pe_pgrs35、rv1985c和rv1986基因,产物进行10 g/ L 琼脂糖凝胶电泳,结果显示,扩增片段与预期大小相符,分别为1 028 bp、1 732 bp、954 bp和951 bp(图1)。将PCR产物与表达载体连接,转化E.coliDH5α感受态细胞,Amp+抗性筛选阳性克隆,经NdeⅠ/XhoⅠ或者Hind Ⅲ/XhoⅠ双酶切,目的片段符合预期大小,同时测序结果表明插入基因序列与发表的序列100 %一致,说明结核分枝杆菌nrdF1和pe_pgrs35基因成功克隆入pEASY-E1表达载体、rv1985c和rv1986基因成功克隆入pET-32a (+)表达载体。
2.2重组菌的诱导表达及纯化 挑取重组菌BL21(DE3)(pEASY-E1-nrdF1) 、BL21(DE3)(pEASY-E1-pe_pgrs35)、BL21(DE3)(pET32a-rv1985c)、BL21(DE3) ( pET32a-rv1986)单个克隆,经IPTG诱导,超声波裂解离心后的上清和沉淀进行SDS-PAGE 分析,结果表明nrdF1、pe_pgrs35、rv1985c和rv1986基因在大肠杆菌中都获得了表达,对应分子量分别为42 ku、63 ku、46 ku和41 ku,其中NrdF1、PE_PGRS35以及Rv1986以包涵体形式存在,Rv1985c以可溶和包涵体两种方式表达(图2)。经过镍柱亲和纯化后,均获得了纯化蛋白(图2),其中Rv1985c是从上清纯化获得,其余的蛋白均是由包涵体纯化获得。
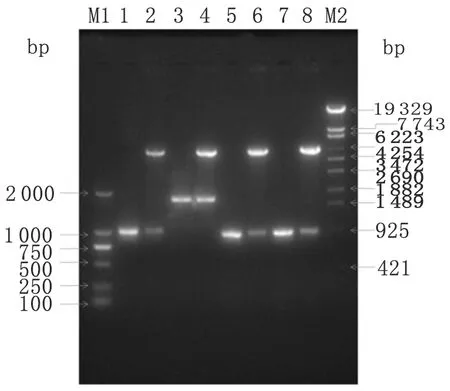
图1nrdF1和pe_pgrs35基因PCR扩增及表达载体酶切鉴定
Fig.1PCRamplificationofnrdF1,pe_pgrs35,rv1985c,andrv1986DNAfragmentsfromMycobacteriumtuberculosisH37Rvgenomeandenzymedigestion
M1: DL2000 DNA Marker;
1:nrdF1 PCR amplification;
2: pCR2.1-nrdF1 digested byNdeⅠ andXhoⅠ;
3:pe_pgrs35 PCR amplification;
4: pCR2.1-pe_pgrs35 digested byNdeⅠ andXhoⅠ;
5:rv1985cPCR amplification;
6: pCR2.1-rv1985cdigested byHind Ⅲ andXhoⅠ;
7:rv1986 PCR amplification;
8: pCR2.1-rv1986 digested byNdeⅠ andXhoⅠ;
M2: λ-EcoT14 Ⅰdigest DNA Marker.
2.3Western-blot分析 抗HIS单抗能够识别纯化的重组蛋白NrdF1、PE_PGRS35、Rv1985c和Rv1986,说明表达的重组蛋白具有良好的免疫反应性。
2.4融合蛋白在牛结核病ELISA检测中的初步应用 通过牛γ干扰素试验共检出68头阳性牛,以纯化的重组蛋白作为包被抗原进行牛结核病血清学检测,结果NrdF1的阳性检出率为7.35% (5/68),阴性检出率为85.51%(59/69);PE_PGRS35的阳性检出率为22.06%(15/68),阴性检出率为86.96%(60/69);Rv1985c的阳性检出率为16.18%(11/68),阴性检出率为79.71.0%(55/69);Rv1986的阳性检出率为16.18%(11/68),阴性检出率为84.06%(58/69)。

图2重组菌诱导表达产物的SDS-PAGE分析
Fig.2SDS-PAGEanalysisoftheexpressedproductsoftherecombinantBL21(DE3)
M:Low molecular protein marker;
1: Sediments of lysate of BL21 (DE3) (pEASY-nrdF1) induced by IPTG;
2: BL21 (DE3) (pEASY) induced by IPTG;
3: sediments of lysate of BL21 (DE3) (pEASY-pe_pgrs35) induced by IPTG;
4: supernatant of lysate of BL21 (DE3) (pET32a-rv1985c) induced by IPTG;
5: BL21 (DE3) (pET32a) induced by IPTG;
6: sediments of lysate of BL21 (DE3) (pET32a-rv1986) induced by IPTG;
7: purified NrdF1; 8: purified PE_PGRS35;
9: purified Rv1985c; 10: purified Rv1986.
3 讨 论
至今为止“检疫→扑杀”是控制牛结核的有效方法,因此准确而及时的诊断对该病的控制极为重要。细菌学检查方法仍被认为是结核病确诊的金标准,但是牛分枝杆菌生长缓慢,分离率低(20%左右),需要生物安全措施,同时对于病理部分样品的采集需要屠宰奶牛,不适用于活畜的检疫,严重影响了该方法的推广[5]。目前皮试变态反应在牛结核病的诊断中被广泛使用,但是特异性较差,诊断结果假阳性率较高,因此迫切需要研究开发出特异性好、便于临床应用的鉴定方法。
特异性的不足主要是由于使用的抗原和环境分枝杆菌存在交叉反应,因此鉴定特异的牛分枝杆菌抗原对研发特异性诊断试剂显得尤为必要,比较基因组学的研究提供了大量特异性抗原信息,常用于新型抗结核病候选疫苗和诊断试剂研发。Mahairas等[2]利用差减杂交技术比较了结核分枝杆菌、牛分枝杆菌毒力株与BCG基因组发现3个差异区,命名为RD1、RD2及RD3;后来Behr等[3]利用细菌人工染色体文库、细菌人工染色体阵列及DNA微阵列,又鉴别出13个差异区:分别命名为RD4—RD16。

图3融合蛋白的Westernblotting分析
Fig.3Western-blottingassayofpurifiedfusionproteins
M: Low molecular protein marker;
1: Purified NrdF1; 2: Purified Rv1985c;
3: Purified Rv1986; 4: Purified PE_PGRS35.
由RD区基因编码的蛋白质构成潜在免疫诊断特异性抗原的来源[2-3,6],尤其是对RD1区蛋白已研究得较为清楚,ESAT-6、CFP10、Rv3872和Rv3873(TB37.6)已被确定为诊断抗原[7-9]。本研究选取RD2区域中的NrdF1、PE_PGRS35,Rv1985c和Rv1986等四种蛋白进行原核融合表达与纯化,并分别以NrdF1、PE_PGRS35、Rv1985c和Rv1986四种融合蛋白纯化产物作为包被抗原,应用间接ELISA方法对血清中的特异抗体进行检测,结果显示4种蛋白的阳性检出率分别为7.35%、22.06%、16.18%和16.18%,显示出一定的诊断价值,在接下来的研究中,我们将结合实验室前期工作中表达纯化的其他结核分枝杆菌特异的抗原,采用组合多种抗原的方法来进一步提高特异性和灵敏度。
参考文献:
[1]World Organization for Animal Health. Manual of diagnostic test and vaccines for terrestrial animals[M]. Paris: Office international des epizooties. 2009: 16-22.
[2]Mahairas GG,Sabo PJ,Hickey MJ,et al. Molecular analysis of genetic differences betweenMycobacteriumbovisBCG and virulentM.Bovis[J]. J Bacteriol,1996,178(5): 1274-1282.
[3]Behr MA,Wilson MA,Gill WP, et al. Comparative genomics of BCG vaccines by whole-genome DNA microarray[J]. Science,1999,284(5419): 1520-1523. DOI: 10.1126/science.284.5419.1520
[4]Sable SB,Goyal D,Verma I,et al. Lung and blood mononuclear cell responses of tuberculosis patients to mycobacterial proteins[J]. Eur Respir J,2007,29(2): 337-346. DOI: 10.1183/09031936.00111205
[5]Chen X,Xu ZH,Shi ZH,et al. Comparision of gamma-interferon assay and tuberculin skin test for detection of bovine tuberculosis[J]. Chin J Zoonoses,2011,27(2): 97-100. (in Chinese)
陈祥,徐正中,时振华,等. γ-干扰素试验和皮试变态反应对检测奶牛结核病的比较[J]中国人兽共患病学报,2011,27(2): 97-100.
[6]Brosch R,Gordon SV,Billault A, et al. Use of aMycobacteriumtuberculosisH37Rv bacterial artificial chromosome library for genome mapping,sequencing,and comparative genomics[J]. Infect Immun,1998,66(5): 2221-2229.
[7]Brusasca PN,Colangeli R,Lyashchenko KP,et al. Immunological characterization of antigens encoded by the RD1 region of theMycobacteriumtuberculosisgenome[J]. Scand J Immunol. 2001,54(5): 448-452. DOI: 10.1046/j.1365-3083.2001.00975.x
[8]van Pinxteren LA,Ravn P,Agger EM,et al. Diagnosis of tuberculosis based on the two specific antigens ESAT-6 and CFP10[J]. Clin Diagn Lab Immunol,2000,7(2): 155-160.
[9]Lyashchenko K,Colangeli R,Houde M,et al. Heterogeneous antibody responses in tuberculosis patients[J]. Infect Immun,1998,66(8): 3936-3940.
