气相中乙醇对水吸收CO2过程界面对流的影响
2014-02-06胡伟超贾学五袁希钢
胡伟超,贾学五,袁希钢
(天津大学化工学院,化学工程联合国家重点实验室,天津 300072)
界面对流现象对相际传质及多相流动过程会产生显著影响。Marangoni效应是在传质过程中由表面张力差引发的一种界面流动现象,会导致近界面流体的流动,即界面对流,进而对传质过程产生影响[1-3]。如何通过界面张力变化引发 Marangoni现象,进而强化传质过程则成为了重要的研究课题。Okhotsimskii[4]利用纹影技术对静态池中不同气液体系产生的对流形态和界面扰动结构进行了光学观察。Sun和 Yu[5]通过有机溶剂吸收和解吸CO2的实验观测了气液传质系统中Marangoni对流产生的有序结构。陈炜[6]采用微观粒子成像测速仪(Micro PIV)对液滴组成变化引起的Marangoni效应进行了观察,分析了液滴形状和组成的改变对其内部对流的影响。然而,上述研究主要是通过传质过程本身导致的界面张力变化来考虑界面对流对传质过程的强化,因而会受到物系的限制。本研究提出在水吸收二氧化碳过程中通过主动向气相中加入低表面张力的第三组分,以改变液体表面局部界面张力,通过调节第三组分的浓度实现引发界面对流。本研究采用乙醇作为第三组分,利用粒子成像测速仪(PIV)测得垂直于界面的液相流场速度矢量信息,并定量分析了气相中乙醇的加入对气液传质过程界面对流的影响。
1 实验部分
1.1 实验试剂和仪器
试剂:无水乙醇(质量分数为99.7%,天津光复科技有限公司);高纯水(电导率小于0.3μS/cm,天津绿源水厂);气体 CO2和 N2(体积分数均为99.99%)。
仪器:PIV测量系统(德国LaVision公司生产);气相色谱仪(型号为 7890A,美国安捷伦公司生产);WZ-50C6微量注射泵。
1.2 气液传质过程中界面对流测量系统
测量水-CO2体系吸收过程中气液界面对流的实验装置如图1所示,主要由PIV测量系统[7-8]和气液传质系统组成。PIV测量系统主要由北京镭宝光电公司生产的双脉冲 Nd-YAG激光系统,LaVision公司生产的CCD相机和图像处理软件组成。Nd-YAG激光系统的输出波长为532nm,激光脉冲宽度10~15 ns,最大脉冲能量200 m J,双脉冲时间间隔1~98000μs,激光脉冲频率 0~10 Hz。CCD相机用于采集流场中粒子图像,其分辨率为1376×1040,并配有波长为532nm的滤光片以消除杂光的影响。实验中采用直径为8~10μm的中空玻璃微球作为示踪粒子,其密度约为1000 kg/m3,在水中具有很好的跟随性。
图1所示的气液传质系统中的透明光学传质实验盒由有机玻璃制作,其内部尺寸为100mm×50mm×5mm(长×高×宽),实验时加入的液体高度大约为40mm,气体在静止的液体上方水平通过并与液体接触。实验中传质盒内的液体采用微量注射泵加入,流量控制在40~60 mL/h,以避免加液过程造成液体的流动。由于传质实验盒在z方向上的厚度仅为5mm,可认为对流被限制为二维,故可通过二维测量很好地获得对流的基本结构。
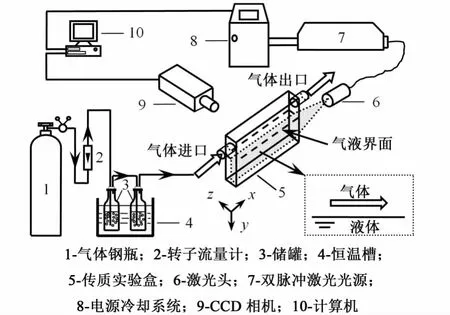
图1 PIV测量实验装置图Fig.1 Schematic diagram of the experimental apparatus for PIV measurement
所有的实验均在温度25℃、常压下进行。在气液传质过程界面对流测量实验开始之前,需要做空白实验,即使用N2作为气相,在不同的流量下通过液体表面。若液层没有大的波动,也没有对流漩涡结构出现,并且整个流场的速度都很小,便可以认为排除了气体吹扫对液体流场的影响,相应的气体流量可以作为实验中采用的适宜流量。
1.3 气相中乙醇的加入及定量方法
乙醇为易挥发物质,若将图1中储罐内的纯水换为乙醇或乙醇水溶液,气体二氧化碳通过储罐后就会携带部分乙醇蒸汽出来,这样就达到了向气相中加入乙醇的目的,并且还可以通过改变乙醇溶液的浓度控制气相中乙醇加入量的多少。由于实验条件下水的饱和蒸汽压要比乙醇小得多,所以CO2通过乙醇溶液时混入到气相中水蒸气的量很小,并且吸收剂同样为水,因此水蒸气的影响相对于乙醇带来的影响是可以忽略的。
采用气相色谱对从储罐出来的CO2和乙醇的混合物进行分析,并使用外标法计算得到气相中乙醇的浓度。
2 结果与讨论
实验过程中所用的水-CO2体系及乙醇的物性参数在表1中列出。

表1 水-CO 2体系和乙醇在T=298.2 K、p=1.013×105 Pa下的物性参数Table 1 Physical properties of water-CO 2 system and ethanol at T=298.2 K and p=1.013×105 Pa
其中,ρw与 ρeth分别为纯水和乙醇的密度;σw与σeth分别为纯水与乙醇的表面张力;DL为CO2在水中的扩散系数;μw为水的动力学黏度。为了进行对比,分别采用如表2给出的4种气体条件进行实验。其中1为空白实验,即仅有气体的流动,不发生气液传质;2为 CO2在水中吸收实验,气相不加入乙醇;3和4分别是气体中具有不同浓度CO2的吸收实验。为了消除气体流速的影响,实验中气体流量均为80 mL/min。
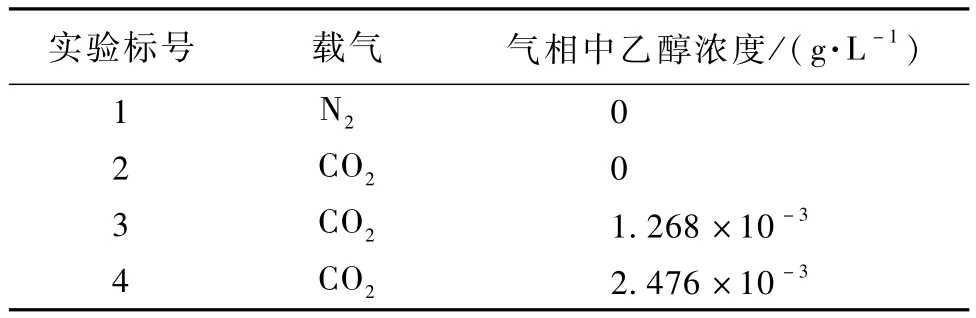
表2 不同条件下的实验对比Table 2 Comparison of experimen ts under different conditions
2.1 流场平均速度的分析
为了测量实验盒内传质过程中的界面对流,首先测量了全流场的平均速度随时间的变化以及瞬时平均速度分布。
由于PIV系统测量分辨力的限制,全流场的平均速度会出现一定的随机波动。为了方便地观察和比较平均速度随时间变化的趋势,本研究采用20点移动平均方法将原始数据平滑处理。平滑后的曲线可正确地反映实验测量的全流场平均速度随时间的变化趋势[13]。图2所示即为通过 PIV测量系统得到的全流场平均速度随时间变化的趋势图。
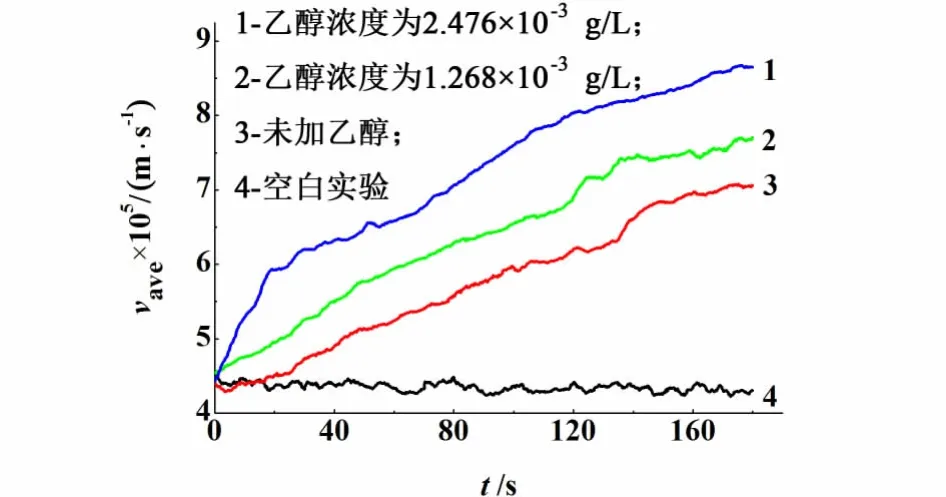
图2 全流场平均速度随时间变化图Fig.2 Evolution of spatially averaged velocity versus time
首先在空白实验中,液体平均流速较小,且不随时间变化。在 CO2吸收实验中,由于传质的作用,液体产生对流,且平均流速随时间增加,这主要是CO2在液体中扩散所导致的。当气相中加入乙醇后,气体和液体接触后 CO2与乙醇均会被水吸收,乙醇在水中的溶解度比 CO2要大,所以乙醇更容易被水吸收。被吸收的乙醇在气液界面处分布不均匀,使得乙醇存在处的表面张力下降,进而在液体表面形成了界面张力差,这种界面张力的不均匀破坏了界面力的平衡,界面张力高的区域液体趋于收缩,这一区域液体受到挤压而转向液相主体,从而引发局部的对流,即局部的 Marangoni现象。随着乙醇扩散和张力梯度的持续存在,这种对流还会向液相主体发展,从而表现出整个流场速度都会增大的效果。随着气相中乙醇浓度的增大,表面张力梯度产生的效果会更明显,流场平均速度也会相应地增加。
从图2中还可以发现,在气液传质过程的初始阶段,气相中加入乙醇后速度要比不加乙醇时增加得快,这是由于不加乙醇时CO2在开始阶段主要以扩散的形式向液相传递。而乙醇的存在则会引发Marangoni对流,增大液相表面更新速率,继而增强气液传质推动力,增加了 CO2在液相中的对流传递。
图3为120 s时4种实验中液体流场的速度矢量分布图与对应的流线图。
从图3可以看出,气相中加入乙醇后会有更多的对流漩涡出现,流场速度也会增大,且乙醇浓度越大这种现象也就更明显。
通过对液相流场不同高度的水平截面内速度取算术平均值,可以得到流场瞬时平均速度沿垂直于界面方向的分布,如图4所示,坐标原点表示界面所在位置。
由图4可发现,气相中不加乙醇时较大的流场速度出现在液相主体内,而气相中加入乙醇后,液相流场中距离界面大约10mm范围内不同位置的流场平均速度要明显大于液相主体中的速度,说明表面张力梯度引起的局部Marangoni效应导致的对流漩涡主要分布在界面附近的区域。这是实验中观测到的加入第3组分引发局部Marangoni效应的速度分布主要特征。

图3 120 s时流场的速度矢量分布图和流线图Fig.3 Vectorial velocity distributions and streamline of flow field at 120 s
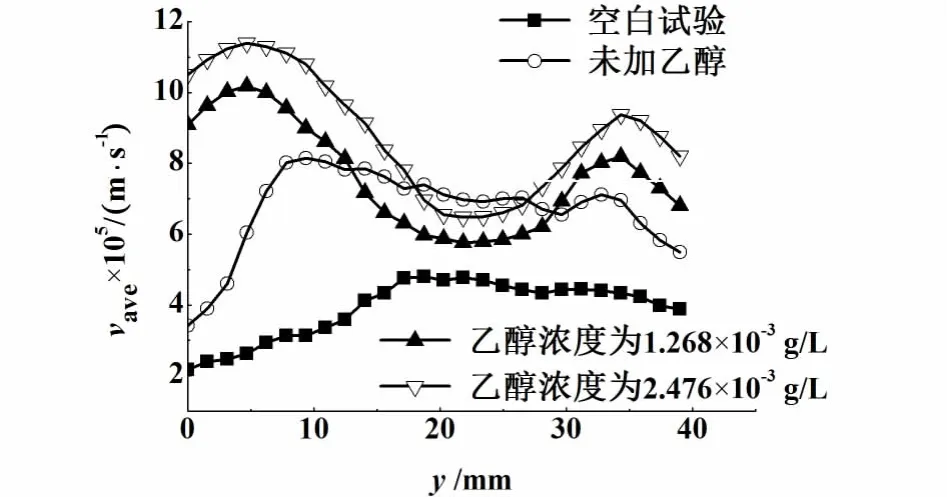
图4 120 s时平均速度沿垂直于界面方向的分布Fig.4 Distributions of average velocity along the vertical direction of the interface at 120 s
2.2 流场湍动能的分析
为了全面地反映气液传质过程中局部Marangoni对流的特征,本研究借用湍动能理论来说明流场速度变化的剧烈程度和对流现象的特征[14]。本研究以平均瞬时速度相对于时均速度的标准差作为一种拟脉动速度,以类比湍流中的脉动速度,进而对液体由于局部Marangoni效应引发的对流对应的动能进行估算。这一标准差表示为:


其中ui和vi分别为某一个高度水平截面上x和y方向在时刻i的平均速度,¯u和¯v分别为该截面在两个方向上从第40 s开始10 s内的时均流速。与对流相对应的湍动能则可以表示为

通过对实验数据进行处理,得到了流场内湍动能在垂直于气液界面方向上的分布,如图5所示。
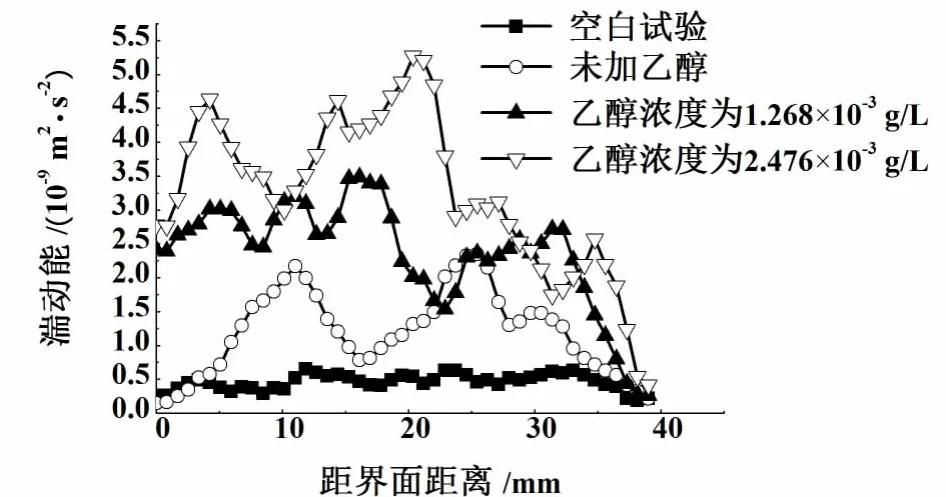
图5 湍动能沿垂直于界面方向的分布Fig.5 Distributions of turbulent kinetic energy along the vertical direction of the interface
从图5可以看出气相中加入乙醇后流场内各处的湍动能比气相中不加乙醇时的湍动能要大,且湍动能随乙醇添加量增加而有所增大。气相中不加乙醇时较大的湍动能分布在远离界面的区域,说明液相主体处流动变化比界面处剧烈。而气相中加入乙醇后的气液传质过程中,近界面处的湍动能明显增大,界面附近Marangoni对流形成的漩涡较多。同时,Marangoni效应还会向液相主体渗透,加剧流体流动,湍流特性增强。
3 结论
气相中乙醇的加入对水-CO2体系气液传质过程液相流场产生了重要影响,乙醇加入后测得的液相流场平均速度和湍动能整体上比不加乙醇时要大。同时,由于气相中乙醇的存在,引发了界面对流,使得近界面处的速度和湍动能明显大于不加乙醇时的速度和湍动能,界面湍动剧烈程度增大,促进了气液传质。
[1]Farajzadeh R,Salimi H,Zitha P L J,et al.Numerical simulation of density-driven natural convection in porous media with application for CO2injection projects[J].International Journal of Heat and Mass Transfer,2007,50(25/26):5054-5064
[2]Sun Z,Yu K.Rayleigh-Bénard-Marangoni cellular convection expressions for heat and mass transfer rates[J].Chemical Engineering Research and Design,2006,84(3):185-191
[3]Arendt B,Dittmar D,Eggers R.Interaction of interfacial convection and mass transfer effects in the system CO2-water[J].International Journal of Heat and Mass Transfer,2004,47(17/18):3649-3657
[4]Okhotsimskii A,Hozawa M.Schlieren visualization of natural convection in binary gas-liquid systems[J].Chemical Engineering Science,1998,53(14):2547-2573
[5]Sun Z,Yu K,Wang S,et al.Absorption and desorption of carbon dioxide into and from organic solvents:Effects of Rayleigh and Marangoni instability[J].Ind Eng Chem Res,2002,41(7):1905-1913
[6]陈炜.气液界面 Rayleigh-Bénard-Marangoni对流现象实验测量及传质研究 [D].天津:天津大学,2010 Chen Wei.Experimental measurement of gas-liquid interfacial Rayleigh-Bénard-Marangoni convection and mass transfer[D].Tianjin:Tianjin University,2010(in Chinese)
[7]Westerweel J.Fundamentals of digital particle image velocimetry[J].Meas Sci Technol,1997,8:1379-1392
[8]Adrian R J.Twenty years of particle image velocimetry[J].Experiments in Fluids,2005,39(2):159-169
[9]Arce A,Rodil E,Soto A,et al.Density,refractive index,and speed of sound for 2-ethoxy-2-methylbutane+ethanol+water at 298.15 K[J].J Chem Eng Data,2000,45(4),536-539
[10]Vázquez G,Alvarez E,Navaza JM.Surface tension of alcohol+water from 20 to 50℃ [J].JChem Eng Data,1995,40(3),611-614
[11]Dittmar D,Fredenhagen A,Eggers R,et al.Interfacial tensions of ethanol-carbon dioxide and ethanol-nitrogen.Dependence of the interfacial tension on the fluid density:Prerequisites and physical reasoning[J].Chemical Engineering Science,2003,58:1223-1233
[12]Takahashi M,Kobayashi Y,Takeuchi H.Diffusion coefficients and solubilities of carbon dioxide in binary mixed solvents[J].JChem Eng Data,1982,27(3):328-331
[13]Chen S,Fu B,Yuan X,et al.Lattice Boltzmann method for simulation of solutal interfacial convection in gasliquid system[J].Ind Eng Chem Res,2012,51(33):10955-10967
[14]Cui Z,Fan L.Turbulence energy distributions in bubbling gas-liquid and gas-liquid-solid flow systems[J].Chemical Engineering Science,2004,59(8/9):1755-1766
