超滤-混凝-酸析法回收涤纶碱减量废水中对苯二甲酸
2014-01-18李永贵贺永林陈东生35008
李永贵,贺永林,陈东生[. , 35008;. (), 4]
涤纶碱减量是将涤纶织物放在碱液中处理,利用碱对涤纶的水解剥蚀作用,赋予其丝绸般的风格、手感、吸湿透气性能,同时又保持涤纶挺爽和弹性好的优点[1]。碱减量工艺的广泛应用产生了大量的废水。目前,该废水的处理主要采用物理法、化学法和生物法相结合的方法直接处理排放。该方法适合于印染企业集中处理废水,但废水中的对苯二甲酸(TPA)有效成分随水排放,造成很大的资源浪费。关于碱减量废水中TPA回收方法主要有:向废水中投加酸中和得到TPA[2-4];通过离子交换膜[5]或用超滤[6]先过滤除杂,再酸中和得到TPA。近年来,国内学者也开始关注这方面的研究,如贺永林等采用有机溶剂盐析结晶[7]比较有效地回收了碱减量废水中的TPA。这些方法优点在于能够实现废弃的TPA回收利用,但回收的TPA纯度不高。
为了有效回收碱减量废水中的TPA,本研究用超滤、混凝、酸析相结合的方法从碱减量废水中回收TPA,并对回收工艺及回收产物进行分析,以期为碱减量废水中的TPA资源化利用提供技术支持[8-9]。
1 试验部分
1.1 试验材料
原料为江苏盛泽某工厂对碱减量废水初级过滤处理后的废水。实验试剂有TPA(标准试剂)、10%硫酸、混凝剂硫酸铝[Al2(SO4)3·18H2O]、吡啶、酚酞、氢氧化钾、氢氧化钠及陶瓷超滤膜,均由国药集团化学试剂公司提供。
1.2 试验仪器
FT-IR傅里叶红外光谱仪(赛默飞世尔科技有限公司),Uvmini-1240型紫外分光光度计(Shimadzu Corporation Kyoto Japan),SU-1510型超发射扫描电子显微镜(Hitachi公司),DELTA 320型pH计(梅特勒-托利多仪器有限公司),DGG-9140A型电热恒温鼓风干燥箱,RH basic 1型电磁搅拌器(IKA)及常规玻璃仪器。
1.3 实验原理
超滤是在一定的压力下,根据不同分子量和形状将水中分子质量相对较高的物质进行分离,而像水等一些低分子物质和一些较小的溶质颗粒则能够透过膜的分离过程[10-11]。碱减量废水中含有少量聚酯水解下来的低聚物、碱减量处理过程中添加的溶胀剂以及涤纶油剂等较高分子物质,这些物质不易分离除去。同时碱减量加工过程中还会带来一些金属离子,因此,需将废水经超滤之后再结合混凝剂将这些杂质去除。
酸析则是一个化学反应结晶过程,其反应式如下式所示:

本研究采用超滤膜首先对经粗滤后的碱减量废水进行过滤,除去微细杂质,气压为0.1 Mpa;然后对滤液以硫酸铝[Al2(SO4)3·18H2O]作为混凝剂,对其进行处理,除去一些较小的溶质颗粒杂质,最后经酸析得到回收产物TPA。实验工艺流程如下:
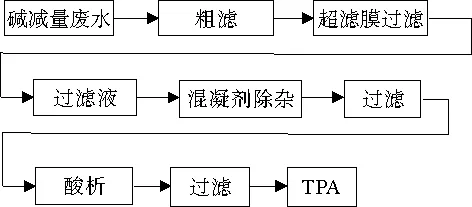
1.4 测试方法
1.4.1定性分析
将1~2 mg样品粉末与100~200 mg磨细干燥的KBr混合均匀后,放入压片模具内抽真空加压,制成厚1 mm、直径约10 mm左右的透明压片[12],进行测试,并记录IR谱图。
1.4.2TPA相对纯度的测定
由于TPA的绝对纯度测试比较困难,本研究采用TPA标准试剂做参照物,测试方法如下。
(1)绘制标准曲线:将0.1 gTPA标准试剂溶于0.1 mol/L NaOH溶液中,移至100 mL容量瓶中,加水稀释配置成浓度为1 g/L的TPA标准溶液。在波长240 nm处,取不同浓度TPA溶液测定吸光度,绘制标准曲线。
(2)样品测试:将0.1 g样品溶于0.1 mol/L NaOH溶液,移至1 000 mL容量瓶中,加水稀释至刻度线。取溶液于50 mL比色管中,在波长240 nm处测定吸光度,根据标准曲线求得浓度C1(g/L)。
(3)TPA相对纯度(P)计算公式为:
1.4.3TPA酸值
按GB SH/T 1612.2 —1995(2004)《工业用精对苯二甲酸酸值的测定》进行TPA酸值测定。
1.4.4TPA回收率
TPA的回收率计算方法如下:
式中:m1为回收的TPA质量(mg);C为废水含固量(g/L),每升废水直接酸析所得固体的质量;V为所取废水的体积(L)。
1.4.5表面形态分析
在SU-1510扫描电镜下观察样品的外观形态及晶型。
2 结果与讨论
2.1 酸析pH值
在室温下,用10% H2SO4溶液对碱减量废水进行酸析,搅拌速度为150 rpm。当pH=5.0±0.1时,白色固体(TPA)开始从废水中析出,说明此时的pH值为TPA的析出点;当pH=4.5±0.1时,TPA大量析出,但是晶粒较小,溶液静置不分层,TPA从溶液中分离困难;TPA晶粒小的主要原因是加酸量小,在溶液中只能够形成TPA的晶核,溶液并未达到饱和状态,没有足够的TPA生成使晶核继续成长,同时由于晶核细小,不易团聚,因而悬浮于溶液中不能分层且不易分离;当pH=3.0±0.1时,TPA晶粒成形良好,晶粒较大,静置溶液出现分层,TPA较易分离;当pH=2.4±0.1时,TPA结晶成形良好,溶液静置分层明显,上层澄清,下层为TPA凝聚体。将TPA颗粒过滤后,继续滴加H2SO4溶液不再有TPA析出。当pH低于3.0后,加酸的量使溶液能够产生足够的TPA,使溶液达到溶质饱和的状态,饱和的TPA溶质能够在其生成的晶核上沉积下来,促进TPA晶核的成长,使晶粒粒径逐渐增大,因而易于分层且易于分离。结合以上实验可知,为减少硫酸的添加量,酸析时比较合适的pH值为2.6,在以下实验中均采用该值。
2.2 混凝剂用量对回收产物的影响
对经超滤后的废水添加混凝剂除杂时,先添加H2SO4调节溶液pH为7.0,在该条件下,TPA不会因加酸析出,然后加入混凝剂Al2(SO4)3·18H2O,同时进行搅拌,反应时间为5 min。然后,静置沉淀,时间为15 min。混凝剂用量(c)选取0 g/L 、0.4 g/L、0.6 g/L 、0.8 g/L、1.0 g/L及1.2 g/L五个浓度。当c= 0.4 g/L时,废水过滤后,溶液稍显浑浊;当c= 0.6 g/L时,滤液已变得澄清,此时混凝剂反应结束,溶液中杂质基本除去。c与回收产物纯度(P)、酸值及回收率(η)的关系如图1所示。
由图1 (a)可知,随着c的增加,P逐渐提高,说明混凝剂用量的增加能提高废水中杂质去除效果,从而有效提高P;而当c≥ 0.6 g/L时,其对P的影响已开始逐渐减弱,继续增加c,对P提高作用很小。由于回收产物的纯度是相对于标准试剂进行比较的,因此,在c=1.2 g/L时出现超过100%的现象,有可能是回收产物的纯度确实已超过标准试剂的纯度。
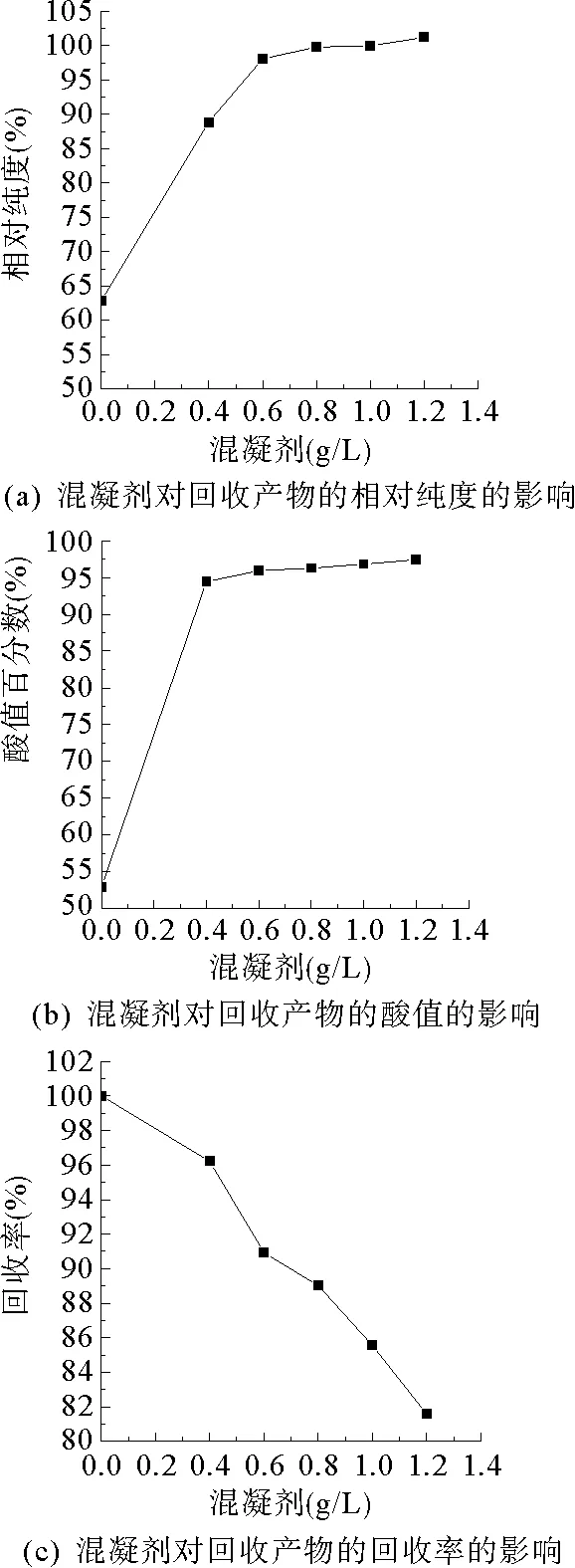
图1 混凝剂用量与回收产物关系图
酸值作为TPA的一项重要指标,可以间接表示其纯度。采用不同c回收的TPA产物酸值百分数如图1 (b)所示。图中,酸值百分数为回收TPA与标准试剂TPA的酸值比值。随着c的增加,回收产物的酸值也在逐步提高,也说明回收产物纯度的逐渐提高。
如图1 (c)所示,随着c的增加,呈现逐渐下降的趋势。造成这种现象的主要原因是在一定的范围内,随着c的增加,通过混凝剂与杂质之间的吸附架桥作用,悬浮颗粒之间充分凝聚,形成絮状沉淀,从而有效除去废水中的杂质;而当c超过该范围时,由于混凝剂在废水中能够迅速形成沉淀,这些沉淀具有较大的比表面,其粘附颗粒的作用也极大增强,在一定程度上能够进一步提升除杂的效果,但由于部分TPA颗粒将被这些沉淀网捕进而被去除,造成部分TPA的缺失,反而使η降低。因此,在保证P的同时又兼顾η的情况下,选取c=0.8 g/L比较合理。
2.3 回收产物定性分析
为探知回收产物成分,我们测试了回收产物与TPA标准试剂的IR谱图,如图2所示。由图2(a)可知,1685 cm-1处的强峰为羧基中的羰基与苯环发生共轭,C=O伸缩振动产生的;1429 cm-1处和1302 cm-1处的两强峰是由于羧酸C-O-H面内弯曲震动与C-OH的伸缩振动发生耦合作用产生的,这些峰的出现表明回收物质中含有-COOH。3105 cm-1处和3072 cm-1处的两个弱吸收峰为苯环上的C-H伸缩振动峰。1580 cm-1处和1510 cm-1处为苯环骨架上C=C伸缩振动所产生的峰,指纹区787 cm-1与732 cm-1两处吸收峰为对位取代时苯环上C-H面外弯曲振动产生的,说明此物质为对位取代苯环。上述分析表明回收产物可能是TPA。回收产物IR谱图与TPA标准试剂的IR谱图(图2(b))基本一致,因此可以判断,回收产物的主要成分为TPA。

图2 回收产物与TPA标准试剂红外谱图
2.4 回收产物表面形态分析
如图3所示,标准试剂晶粒较大且表面比较整洁,而回收产物晶粒相对较小,且分布不均匀,表面明显不规则。造成这种现象的原因可能是因为两种产品的结晶方式不同。同时通过对粒径大小的统计发现,超滤酸析得到的TPA粒径分布极不均匀。
这主要是由于对加酸速度控制不够,由于酸析过程中,晶体成核速度远大于晶体成长速度,加酸速度过快,导致部分TPA晶体成长时间不充分,使得其粒径较小;而加酸速度较慢,使部分TPA晶体有充分的成长时间,因而晶体粒径较大。此方面的原因及对策有待进一步深入研究。

图3 回收产物与标准试剂SEM照片
3 结论
采用超滤膜过滤—混凝—酸析相结合的工艺回收并纯化碱减量废水中的TPA,合理的酸析pH值为2.6、混凝剂用量为0.8 g/L、废水中TPA回收率可达89.03%;回收的TPA的纯度及酸值均接近于TPA标准试剂,但晶粒形态较粗糙且粒径不均匀。该工艺切实可行,但超滤效率较低。
[1] 范雪荣.纺织品染整工艺学(2版)[M].北京:中国纺织出版社, 2006.
[2] 杨期勇,杨涛,陈季华.碱减量废水对苯二甲酸回收工艺的影响因素[J].印染, 2010,36(2):30—33.
[3] 刘超男,陈季华.碱减量废水中回收对苯二甲酸技术[J].印染,2006,(15):7—10.
[4] PARK S F,CHANG T S,LEE Y K,et al.Process for preparing polymer grade terephthalic acid: USA,5210292 [P].1993-5-11.
[5] SHIBA M,ONO T.Method for recovering available component from waste liquid generated in processing polyester fiber with alkali: Japan,60216884 [P].1985-10-30.
[6] YOSHIDA T,SHIMANO Y,MATSUMOTO M,et al.Recovery of terephthalic acid: Japan,60019748 [P].1985-01-31.
[7] 贺永林,李永贵,葛明桥.有机溶剂对回收涤纶碱减量废水中苯二甲酸的影响[J].纺织学报,2013,34(12):18—21.
[8] 李永贵,佴友兵,李准准等.聚酯纤维乙二醇醇解法(Ⅱ): 醇解产物表征[J].纺织学报,2007,28(12):12—15.
[9] 李永贵,李准准,佴友兵,等.聚酯纤维乙二醇醇解法(Ⅰ): 醇解工艺[J].纺织学报,2007,28(11):21-24.
[10] 孙爱华,张春华.膜技术处理印染废水回用工程实例剖析[J].印染,2013,39(12): 25—26,55.
[11] 刘劲松,张健君,杨淑芳,等.印染废水的超滤/反渗透法深度处理及回用[J].印染,2013,39(10):32—34.
[12] 翁诗甫.傅里叶变换红外光谱仪[M].北京: 化学工业出版社,2005.
