辛伐他汀在年轻健康受试者中的群体药动学研究
2013-12-03朱立勤章袁季双敏庄艳楠陈敬国天津市第一中心医院天津0019天津医科大学天津00070北京大学医学部北京100191天津中医药大学天津0019
朱立勤,章袁,季双敏,庄艳楠,陈敬国(1.天津市第一中心医院,天津0019;.天津医科大学,天津00070;.北京大学医学部,北京 100191;.天津中医药大学,天津 0019)
辛伐他汀(Simvastatin)为3-羟基3-甲基戊二酰辅酶A(HMG-CoA)还原酶抑制剂[1-2],目前广泛应用于高脂血症、冠心病等的治疗。辛伐他汀为前体药物,在人体内的血药浓度较低,口服生物利用度为仅5%,口服吸收后对肝脏有高度选择性,通过细胞色素P450(CYP)3 A4代谢,大部分在肝脏进行首关吸收。其主要作用在肝脏,随后经胆汁排泄。目前,辛伐他汀在年轻受试者中的经典药动学研究国内、外已有报道[3-7],本研究采用非线性混合效应模型(NONMEN)法,建立年轻受试群体中辛伐他汀药动学模型,为个体化给药提供临床参考。
1 资料与方法
1.1 研究对象
从中国知网(CNKI)、万方数据库、维普数据库、PubMed电子检索系统、Medline收集和筛选出符合要求的29篇文献中共474例年龄在18~35岁之间的年轻健康受试者作为受试群体药动学研究对象。
1.2 软件
运用NONMEM软件VersionⅥ,Level 1.1(Globomax Corp MD,USA);中文Win 2007操作系统。
1.3 研究方法
1.3.1 文献数据获取方法。(1)文献检索方法。以辛伐他汀、药动学、生物利用度、生物等效性等为检索词,检索1990年1月至2012年1月CNKI、万方数据库、维普数据库;以Simvastatin、pharmacokinetics、population、bioavailability等为检索词,检索PubMed电子检索系统和Medline数据库。文献检索语种限制为中文或英文。(2)文献纳入及排除标准。符合下列条件的文献纳入研究:①研究对象为服用辛伐他汀片,剂量为20 mg、qd的年轻健康受试者;②文献包含辛伐他汀的血药浓度或药-时曲线数据;③文献包含用药人群的人口统计学资料等。符合下列条件的文献从研究中排除:①非人体临床研究试验;②药动学数据或人口统计学资料严重缺失;③重复发表的文献和普通综述性文献。(3)文献数据提取方法。将文献中药-时曲线图以高精度(600 dpi)扫描入计算机,用Photoshop软件读出相关的矢量坐标点。
1.3.2 群体药动学模型的建立方法。以NONMEM对年轻受试群体辛伐他汀血药浓度数据进行处理,拟合模型。采用逐步回归法考察年龄(Age)、性别(Gend)、体质量(WT)、身高(HT)、肌酐清除率(Ccr)等固定效应对药动学参数的影响。若将某一个相关因素引入模型后目标函数(Objective function value,OFV)的下降值>3.8,表示该因素的加入使模型拟合优度显著改善(χ2,df=1,P<0.05),模型中保留该因素;再在此基础上引入下一因素。将有显著性影响者保留在模型中,建立全量回归模型。从全量回归模型中每次剔除一个固定效应因素,以考察因素存在的必要性。此时用更严格的统计学标准进行检验(χ2,df=1,P<0.01),若OFV增加值>7.88,那么该因素的存在具有极显著意义,应该留在模型中,否则应从模型中剔除,得到最终回归模型。个体间变异模型和残差模型分别用加法模型、乘法模型和指数模型进行拟合,取OFV和变异值最小的模型为最终统计学模型。残差指个体间变异以外的变异,包括取样、分析方法、模型等造成的误差[7]。Bootstrap是一种数据重采样技术[8],1999年被美国FDA推荐作为群体药动学模型的验证方法。一次Bootstrap的基本过程是从n个观察值中有放回的随机抽样n个观察值,组成一个新样本,然后求算模型的参数值[9]。本研究采用500次Bootstrap对最终模型进行验证,对验证成功所得的参数进行统计学计算,得到的最终模型参数平均值(Mean)和95%置信区间(Confidence interval,CI)与最终模型的群体参数进行比较。
2 结果
2.1 基本资料
按照筛选标准从文献中筛选出文献29篇。其中中文22篇,这些文献来自2000-2011年发表的18种杂志,涉及《中国临床药理学杂志》、《中国药房》、《中国药师》、《中国新药杂志》、《中国医院药学杂志》等;外文7篇,来自2003-2009年发表的杂志,涉及《美国心脏病学杂志》(The American Journal of Cardiology)、《英国临床药理学杂志》(British Journal of Clinical Pharmacology)、《生物药剂药物处置杂志》(Biopharm.Drug Dispos.)、《英国癌症杂志》(British Journal of Cancer)、《抗生素与化疗杂志》(AntimicrobialAgent and Chemotherapy)。
474例年轻受试群体的Age、WT、HT、Gend等人口学资料见表1;年轻受试群体辛伐他汀药-时曲线见图1。
表1 年轻受试群体人口学资料(±s,n=474)Tab 1 Demographic information of young population( ±s ,n=474)

表1 年轻受试群体人口学资料(±s,n=474)Tab 1 Demographic information of young population( ±s ,n=474)
项目A g e,岁W T,k g H T,c m G e n d(男性/女性)数据25.15±6.3466.97±4.803172.2456/18

图1 年轻受试群体辛伐他汀药-时曲线(n=474)Fig 1 Blood concentration-time curves of simvastatin in young population(n=474)
2.2 群体药动学模型的建立
2.2.1 基础模型。由于年轻人的数据比较富集,在基础模型建立过程中同时考察一房室和二房室对数据的拟合状况,获得各种模型的目标函数量小值(OFVmin),比较其差值,判断增加房室是否有显著意义。通过OFV和总体拟合优度比较,确定基础药动学模型。本研究最终选用一房室模型进行拟合。年轻受试群体群体药动学基础模型和残差模型分别为指数型(见式1)和混合型(见式2)。

θj是第j个个体的药动学参数,θ是该参数的群体典型值。ŋj是该参数个体值与群体值之间的差异,即参数的个体间变异,符合以0为中心,方差为ε2的正态分布。cobs为观测值,cpred为模型预测值,ε1、ε2分别表示残留随机效应中的比例误差和加和型误差,符合均值为0,方差分别为的正态分布。
2.2.2 固定效应模型。由于年轻人的数据中的Age、WT、HT 3个协变量引入基础模型后,各效应因素对清除率(CL)及表观分布容积(V)均无影响(P>0.05),模型无明显改善,因此将基础模型作为最终模型。
2.2.3 模型评价。绘制年轻受试群体个体血药浓度cpred与cobs间的散点图(图2)以及加权残数(WRES)对个体的散点图(图3)。由图2可知,年轻受试群体个体cpred对cobs有较好的相关性,趋势线同对角线接近,cpred在cobs的上下分布均匀,因此模型能很好地拟合cobs。由图3可知,WRES值分布于横轴上下,且绝大部分分布于±2之间,并且WRES的分布无明显趋势,未见特别异常的点,模型拟合效果较好。

图2 年轻受试群体个体cpred对cobs值散点图Fig 2 Scatter plots of individual predicted concentration vs.observed concentration in young population

图3 WRES对个体cpred散点图Fig 3 Scatter plots of WRES vs.individual predicted concentration
2.2.4 模型验证。对年轻受试群体模型进行Bootstrap验证,500 Bootstrap验证中,成功406次,成功率为81.2%,最终群体参数值和Bootstrap验证结果见表2(表中,ω示个体间变异,δ示个体内变异)。由表2可知,年轻受试群体最终模型得到的主要药动学参数的估计值在Bootstrap所得到5%~95%分位数之间,与最终模型参数比较差异无显著性,证明模型稳定、可靠,所得参数稳定、可信度较好。最终药动学模型各项药动学参数符合实际意义,个体间变异、个体内变异均在允许的误差范围之内,模型的最终拟合优度良好。
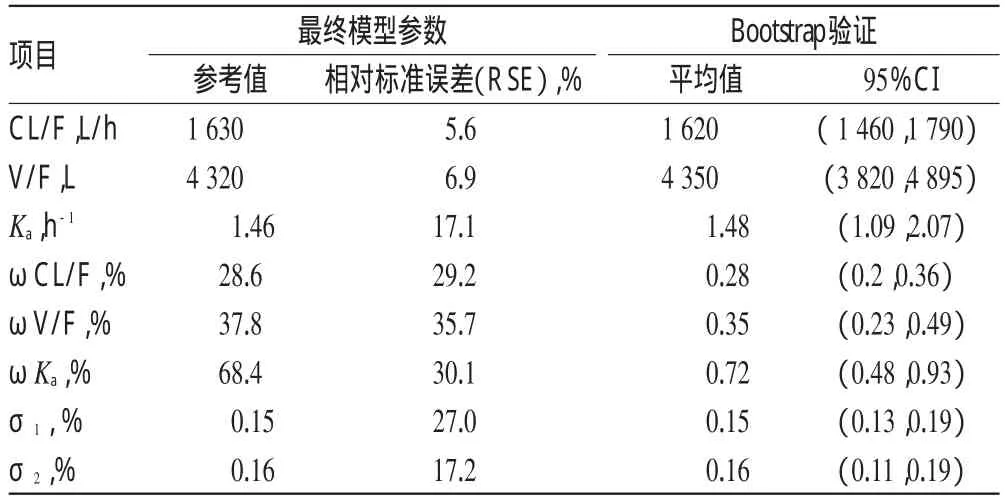
表2 年轻受试群体辛伐他汀最终模型与Bootstrap验证结果Tab 2 Final model of simvastatin in young population and results of Bootstrap validation
3 讨论
临床药动学研究表明,不同人群对于药物的体内处置过程存在很大差异,临床用药过程中需要全面了解这些特征才能保证药物的安全、有效。目前,辛伐他汀在高血脂患者中广泛应用,本研究首先针对年轻受试者人群探讨药物体内处置规律,为临床合理、安全用药提供参考。
本研究结果显示,辛伐他汀在年轻受试者体内的CL/F群体典型值为1630 L/h,与欧阳冬生等[10]报道的经典法测定辛伐他汀在10名健康男性受试者体内的CL/F为2080 L/h相比较为接近。而本课题组进行的老年人群群体值为1230 L/h,年轻受试群体CL高于老年人群。结果提示老年患者的药物清除能力低于年轻人。本研究中,年轻受试者V/F群体典型值为4320 L,与本课题组进行的老年人群V/F群体典型值2350 L相比,也有明显的差别,年轻受试者明显高于老年患者,与文献[5-6]报道的在年轻健康受试者和老年患者的研究结果一致。
研究显示,老年人代谢能力减弱与其肝质量和肾血流量有密切关系,老年人的肝质量与年轻时相比减轻约15%;肝血流量也随着年龄的增长而下降,每年减少约1.5%,65岁比25岁时减少40%~50%[10];同时老年人肝药酶的活性降低,也是其代谢速度变慢的又一原因。
需要说明的是,由于本研究中年轻受试者的血药浓度数据来自于文献中的药-时曲线图,曲线图采用相应软件读取矢量坐标点的方法,可准确得出血药浓度数据。
[1]张光银,张军平.辛伐他汀联合用药研究进展[J].世界科技研究与发展,2010,32(3):393.
[2]何笑荣,邹定.降血脂新药匹伐他汀[J].中国新药杂志,2005,14(4):483.
[3]石萍,陈相潘.辛伐他汀口腔崩解片的人体生物等效性研究[J].中国药房,2007,18(35):2757.
[4]李大平,崔凤云,郑家润,等.国产辛伐他汀片的生物等效性[J].药物与临床,2009,29(8):105.
[5]O’Brien SG,Meinhardt P,Bond E,et al.Effects of imatini mesylate(ST1571,Glivec)on the pharmacokinetics of simvastin,a cytochrome P4503 A4 substrate,in patients with chronic myeloid leukaemia[J].British Journal of Cancer,2003,89(10):1855.
[6]任秀华,刘宇,陈倩,等.高效液相色谱串联质谱法测定人血浆中辛伐他汀浓度及药动学研究[J].中国药师,2011,14(8):1126.
[7]焦正,钟明康,施孝金,等.非线性混合效应模型考察丙戊酸、苯妥英和苯巴比妥西平及其环氧化代谢产物相对清除率的影响[J].中国临床药理学杂志,2003,19(5):360.
[8]Sun H.Population pharmacokinetics.Aregulatory perspective[J].Chin Pharmacokinet,1999,37(1):41.
[9]焦正,张明,梁惠琪,等.肾移植患者麦考酚酸的群体药动学研究[J].中国药学杂志,2007,42(1):57.
[10]欧阳冬生,黄松林,谭志荣,等.理舒达人体药动学和相对生物利用度研究[J].中国新药杂志,2004,13(4):39.
