D231强碱性环氧系阴离子交换树脂吸附铀性能研究
2013-11-21平爱东罗明标刘建亮蒋小辉
平爱东, 罗明标, 刘建亮, 蒋小辉
(东华理工大学核资源与环境国家重点实验室培育基地,江西抚州 344000)
铀作为核燃料,在核反应堆中可释放巨大的能量,广泛用于交通运输工具的推进动力方面。核动力堆可装于潜艇、远洋货轮,其燃料负荷量和续航能力,都是一般燃料无法比拟的。铀作为核炸药,能用作核武器的装料。鉴于其多种高尖端用途,分离提取铀元素也成为国内外学者研究的重要内容,在许多国家甚至把此项研究列为国防重点项目,可见其应用价值的重要性。
铀在环境中的含量很低,在准确测定复杂组分样品中的痕量铀时,往往需要采取合适的分离富集手段,以满足分离干扰元素、降低检出限和提高测定结果准确度的需要(Prasada et al.,2006)。近些年来,由于测定对象越来越复杂、要求的检测限越来越低,铀分析中的分离富集技术得到了迅速发展。依据分离富集原理的不同,国内外近10年发展的新分离富集技术有浮选(Hosseini et al.,2006)、毛细管电泳(Collins et al.,2001)、吸附分离(唐国梁,2001;Starvin,2004)和萃取4 类方法。铀的分析方法较多,常用的有分光光度法、容量法、荧光法、放射性分析方法、缓发中子法等等。D231树脂是一种大孔型强碱性环氧系阴离子交换树脂,本文研究了该树脂吸附铀的动力学性能,为D231树脂用于铀的分离、富集、回收工艺提供理论依据。
1 实验部分
1.1 主要试剂和材料
铀标准溶液:移取基准U3O80.117 g,用王水溶解转入100 mL 容量瓶中用水定容,此液为1 g/L 铀溶液,取一定量溶液稀释,配制所需浓度的工作液;D231强碱性环氧系阴离子交换树脂,粒度40 ~60目;硝酸:0.3 mol/L,4 mol/L;氨水(1 +1):1 份氨水与1 份水混合;盐酸:3 mol/L,4 mol/L;氯乙酸-NaOH 缓冲溶液:pH 2.5;偶氮胂III 溶液:0.05%;pH 0.5,1.0,2.0,3.0,4.0 溶液:用稀硫酸和稀氢氧化钠在酸度计上调得;2,4-二硝基酚溶液(1 g/L):称取0.1 g 2,4-二硝基酚溶于100 mL 乙醇中;抗坏血酸:50 g/L;混合掩蔽剂:10 g/L TTHA(三乙四胺六乙酸)-5 g/L EDTA(乙二胺四乙酸二钠)。
1.2 仪器设备
酸度计:pHS -3C 型;721 - E 型分光光度计(上海光谱仪器有限公司制造);玻璃交换柱:上部带有贮液杯的U 型玻璃交换柱Ф10 ×75 mm。树脂床层高约为32 mm(树脂床层体积2.5 mL)。
1.3 实验方法
1.3.1 静态法
称取一定量干树脂于带盖聚碳酸酯瓶中,加入一定量铀标准溶液,配成一定组成和酸度的溶液(控制总体积),在室温下振荡直至吸附平衡状态,取部分滤液,偶氮砷III 光度法测定铀含量,用下式计算铀的分配比和吸附量:

式中:C0为水相中铀的起始浓度(mg/L);Ce为水相中铀的平衡浓度(mg/L);V 为反应液体积(mL);W为干树脂重量(g);Q 为平衡状态下每克干树脂吸附铀的量(mg/g)。
1.3.2 动态法
取一定量树脂湿法装柱,柱底加少许玻璃纤维压紧,用与吸附液相同酸度的溶液平衡交换柱,然后以一定流速使预定组成的吸附液通过柱床,分批接收流出液,测定铀的含量。吸附达到平衡的柱床,用少量与吸附液同酸度的溶液淋洗1 ~2 次。再用解吸剂洗脱树脂所吸附的铀,分批接收洗脱液,测定其中铀的浓度。按下式计算吸附率:

式中:C0为水相中铀的起始浓度(mg/L);Ce为水相中铀的平衡浓度(mg/L);E 为吸附率。
1.3.3 标准曲线的绘制
分别移取10 μg/mL 铀标准溶液0.5,1,2,3,4,5 mL 于25 mL 容量瓶中,加1 ~2 滴2,4-二硝基酚指示剂,用(1 +1)氨水调至黄色,用3 mol/L HCl调至黄色褪去,再过量2 滴,加pH 2.5 氯乙酸-NaOH 缓冲溶液2 ml,0.05%偶氮胂III 2 mL,用水定容,摇匀,放置5 min,在721-E 光度计660 nm处,用1 cm 比色皿,以试剂空白为参比,测定吸光度,绘制标准曲线。
1.3.4 最佳吸附酸度
取D231树脂湿法装入U 型交换柱,用水淋洗交换柱至pH 为7,分别用pH 0.5、pH 1.0、pH 2.0、pH 3.0、pH 4.0 溶液平衡,移取5 ml 100 μg/mL 铀标溶液通过交换柱,流出液接于25 mL 容量瓶中,再用pH 0.5、pH 1.0、pH 2.0、pH 3.0、pH 4.0 各5 mL淋洗柱子两次,淋洗液接于同一容量瓶中。按照上述中铀标准曲线绘制方法,测定铀量,计算吸附率,确定最佳吸附酸度。
1.3.5 最佳解吸剂的选择
逐次移取100 μg/mL 铀溶液2 mL,以2 mL/min 流速,通过U 型交换柱。分别用不同解吸剂洗脱,每次2.5 mL,接于25 mL 容量瓶,测定铀含量,绘制解吸曲线,选择最佳解吸剂。
2 结果与讨论
2.1 吸附酸度
称取0.015 g 树脂6 份,分别置于200 mL 聚碳酸酯瓶中,加入含500 μg 不同pH 值溶液10 mL,振荡30 min,分取液相,测定铀含量,计算吸附量,以溶液酸度对吸附量作图(图1)。

图1 吸附酸度曲线Fig.1 The curve of adsorption acidity
由图1 可见,随溶液pH 增大,吸附量逐渐增大。当溶液pH 为3.0 ~4.0 时,吸附量稳定在31 mg/g 左右,较pH 2.0 吸附量稍大。但溶液中如有磷酸盐或砷酸盐杂质,会产生沉淀,影响树脂吸附铀,故吸附酸度选择pH 2.0 为佳。
2.2 吸附速率
称取0.03 g 树脂7 份分别于200 mL 聚碳酸酯瓶中,加入5 mL pH 2.0 溶液和5 mL 100 g/L 铀溶液,总体积为10 mL,置振荡器上振荡相同时间,取液相测定的残余量,计算吸附量,绘制曲线(图2)。
由图2 和图3 可见,振荡时间30 min 之前吸附量变化较大,30 min 后吸附量增加缓慢,表明振荡30 min 已接近平衡,实验选择振荡30 min。

图2 吸附量与振荡时间关系曲线Fig.2 Adsorption capacity in diferent adsorption time

图3 吸附速率曲线Fig.3 The curve of adsorption rate
按Boya 液膜公式-ln(1 -F)=kt,以-ln(1 -F)对振荡时间t 作图,见图3。根据图中所得直线可知,此吸附反应符合Boya 液膜公式,树脂吸附铀的历程主要以液膜扩散为主要步骤(Boyd et al.,1947;Bhattacharyya et al.,2006;Shu et al.,2007a,2007b;Huang et al.,2007),由直线斜率求出吸附速率常数K 为2.3 ×10-3s-1。
2.3 吸附温度对分配比的影响
称取0.015 g 树脂5 份分别置于聚碳酸酯瓶中,加入500 μg 铀,pH 2.0 溶液10 mL,在20 ~60℃不同温度下,振荡30 min,测定液相中铀含量,计算树脂对铀分配比,以lgD 对吸附温度作图4。

图4 lgD-1/T×103 关系曲线Fig.4 Effect of temperature on distribution coefficient
由图4 可见,lgD-1/T ×103关系曲线为一直线,随温度升高分配比略有增加,线性回归方程式为y= -0.97x+7.27。
根据热力学公式:

由lgD-1/T ×103直线斜率求出ΔH = 18. 57 KJ/moL。ΔH 为正值,表明D231树脂吸附铀为吸热反应,升高温度对吸附有利,但实验结果表明随温度升高,铀分配比略有增加。因此,可在常温下进行吸附反应。
2.4 等温吸附曲线与饱和吸附量
称取0.015 g 树脂数份,分别置于聚碳酸酯瓶中,改变500 μg/mL 铀溶液加入量,溶液总体积为10 mL,室温下振荡30 min,测定液相中铀残余量,计算吸附量,以平衡时溶液中铀浓度与吸附量关系绘制吸附曲线(图5)。
由图5 和图6 可知,随铀平衡浓度增加,树脂吸附量也增加,铀平衡浓度Ce 在196 ~247.5μg/mL 吸附量稳定。饱和吸附量为131 mg/g。
根据Freundlich 等温吸附式Q =KC1/n 或lgQ=1/nlgC+lgK。以lgQ 对lgCe 作图,得一直线,见图6。在铀浓度范围内,该吸附平衡服从Freundlich等温式(北川浩等,1983;舒增年等,2008;Xu et al.,2008),从直线斜率求得n =2.19,n 值在2 ~10 之间表明此吸附反应容易进行(Shu et al.,2006;Chen et al.,2006;Bhatnagar et al.,2007)。

图5 等温吸附曲线Fig.5 The curve of adsorption isotherm
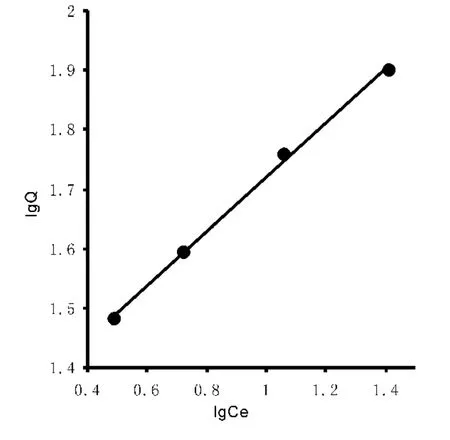
图6 lgQ-lgCe 关系曲线Fig.6 The relation curve of the logQ and logCe
2.5 吸附流速对吸附率的影响
逐次移取25 mL 铀含量浓度为20 μg/mL 的pH 2.0 溶液,分别以不同流速通过直管式交换柱(Ф1 cm 树脂层高3.2 cm 柱床体积2.5 mL),接流出液测定铀含量,计算吸附率(表1)。

表1 吸附流速对吸附率的影响Table.1 The effect of current velocity on adsorption rate
由表1 可知,吸附流速20 mL/min,吸附率尚有98%,可见D231树脂对铀的吸附能力很强,吸附流速对吸附率影响不大。
2.6 洗脱液的选择
逐次移取含200 μg 铀的pH 2.0 溶液(100 μg/mL 铀2 mL),以2 mL/min 流速通过交换柱(Ф1 cm树脂层高3.2 cm),接流出液,再分别用不同洗脱液,每次2.5 mL 淋洗,连续淋洗10 次,分别置于25 mL 容量瓶中,测定铀含量,绘制洗脱曲线(图7)。

图7 不同解吸剂的洗脱曲线Fig.7 The eluting curve of different eluant
实验结果表明,D231树脂吸附200 μg 铀,分别用4 种解吸剂洗脱,洗脱效率最好的是硝酸盐,峰值铀浓度高,洗脱率99%以上,氯化物解吸效果稍差,富液铀浓度低,但氯化铵比氯化钠解吸效果要好。NH4Cl 洗脱液峰值铀浓度为8.1 μg/mL,NaCl洗脱峰值铀浓度只有4.9 μg/mL。
2.7 解吸流速对洗脱率的影响
逐次移取2 mL 100 μg/mL 铀标准溶液(即200 μg),以2 mL/min 流速通过已用pH 2.0 溶液平衡的交换柱(Ф1 cm 树脂层高3.2 cm 柱床体积2.5 mL),用5 mL pH 2.0 溶液淋洗2 次,淋洗液弃去,再用25 mL 0.9 mol/L NaCl-0.05 mol/L H2SO4以不同流速洗脱树脂上吸附的铀,测定洗脱液中铀含量,计算洗脱率(表3)。
由表3 可知,用25 mL 0. 9 mol/L NaCl-0. 05 mol/L H2SO4为解吸剂,解吸流速为1 mL/min,洗脱率为97.64%,解吸流速增大,洗脱率减小,6 mL/min 流速,洗脱率降至86.3%,可见洗脱流速不能快,控制2 mL/min 以下,能获得90%以上洗脱率。
2.8 动态吸附曲线
称取0.2 g 树脂湿法装入Ф3 mm,L80 mm 微型交换柱,安装于加压蠕动泵上,移取1 g/L 铀溶液上柱,接流出液测定铀含量,连续上柱直至流出液中铀浓度与上柱液铀浓度相等,停止操作,以流出液体积与流出液中铀浓度或C/C0绘制吸附曲线(图8),计算铀饱和吸附量。

表2 解吸剂洗脱效果Table 2 The elution effectivity of eluant

表3 解吸流速对洗脱率的影响Table 3 Effect of eluting velocity on desorption efficiency

图8 流出液体积与C/C0 关系曲线Fig.8 The relation curve of the outflow liquid product and C/C0
实验结果表明,当流出液体积为44 mL 时,C/C0为0.74,不再增大。表明吸附铀饱和,取C/C0为0.37,所对应的流出液铀含量为32.4 mg,铀饱和吸附量为162 mg/g。
2.9 主要共存离子对吸附铀的影响
2.9.1 不同酸度溶液中钼的分配比
称取0.015 g D231树脂2 份,分别置于200 mL聚碳酸酯瓶中,加入pH 1.0 和pH 2.0 含400 μg 钼溶液10 mL,置振荡器上振荡30 min,分取液相测定钼吸附量和分配比(表4)。

表4 不同pH 溶液中钼分配比Tab.4 The distribution ratio of Mo on different pH solution
由表4 和表5 可见,在pH 1.0 ~2.0 溶液中D231树脂对U 和Mo 有较大的分配比,铀和钼的分离系数为1 左右,表明在此酸度下,铀与钼不易分离。
2.9.2 不同酸度溶液中铁的分配比
称取0.015 g D231树脂3 份分别置于聚碳酸酯瓶中,依次加入pH 1.0,pH 1.5,pH 2.0 含1000 μg铁溶液10 mL,振荡30 min,分取液相于50 mL 容量瓶中,用磺基水杨酸光度法测定铁含量,计算吸附量和分配比(表6)。
由表6 和表7 可知,在pH 1.0 ~2.0 酸性溶液中,铀与铁分离系数随pH 增大而增大,pH >1.5 分离系数>102。可见选择pH 2.0 条件下吸附铀与铁易于分离。
3 结论
(1)本方法使用的D231强碱性环氧系阴离子交换树脂吸附铀,吸附酸度范围为pH 1.0 ~4.0,且吸附率较高。树脂上吸附的铀又易被硝酸盐溶液如NH4NO3洗脱,洗脱效果好,回收率高。
(2)离子交换分离-偶氮胂III 光度法测定铀,测定范围为0.000n% ~0.n%,不适于分析铜、铅、钼、铋等含量较高的矿样。
(3)本实验研究D231强碱性环氧系阴离子交换树脂吸附铀的性能,通过实验选择了吸附铀的最佳条件,得到了较满意的结果。
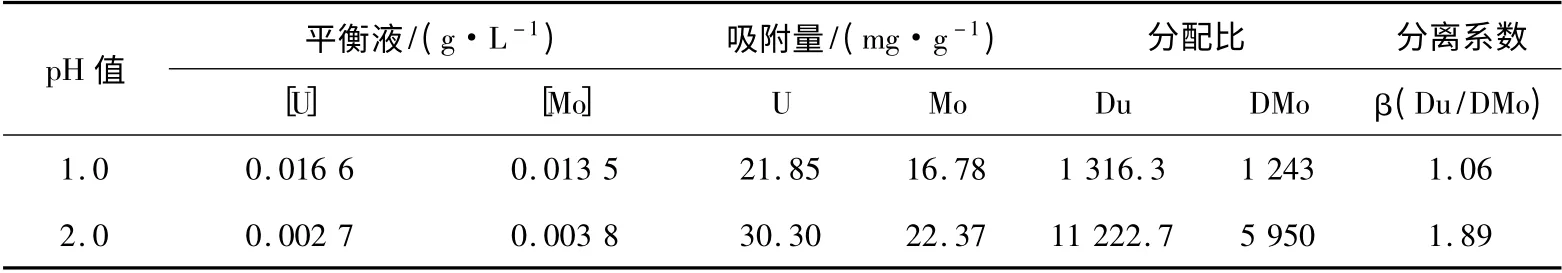
表5 不同pH 值溶液中铀,钼分离系数Table 5 The separation coefficient of U/Mo on different pH solution

表6 不同pH 溶液中铁分配比Table 6 The distribution ratio of Fe on different pH solution

表7 不同pH 溶液中铀铁分离系数Table 7 The separation coefficient of U/Fe on different pH solution
(4)树脂颗粒最佳目数为40 ~60 目,颗粒太大测定结果不稳定,颗粒太小影响流速。
(5)当用王水分解样品时要将溶液蒸干,除去硝酸根离子,否则硝酸根离子与铀形成硝酸铀酰不被树脂吸附,使结果偏低。
北川浩,铃木廉一郎.1983. 吸附的基础与设计[M]. 鹿政理译. 北京:化学工业出版社,33-36.
舒增年,莫建军.2008. C-800 氨基羧酸树脂对铬(III)的吸附性能研究[J]. 矿物学报,28(4):483-487.
唐国梁.2001. 净水活性炭吸附偶氮胂(III)光度法监测废水中铀[J].理化检验-化学分册,37(6):261-265.
Bhatnagar A,Minocha A K,Jeon B H,et al. 2007. Adsorptive removal of cobalt from aqueous solutions by utilizing industrial waste and its cement fixation[J]. Sep Sci Technol,42(6):1255-1266.
Bhattacharyya K G,Gupta S S. 2006. Adsorption of chromium(VI)from water by clays[J]. Ind Eng Chem Res.,45(21):7232-7240.
Boyd G E,Adamson A W,Myers L S. 1947. The exchange adsorption of ions from aqueous solutions by organic zeolites II kinetics[J]. J Am Chem Soc.,69:2836-2848.
Chen Y G,Zhang K N,Zou Y S,et al. 2006. Removal of Pb2+and Cd2+by adsorption on clay-solidified grouting curtain for waste landfills[J]. J Cent South Univ Technol,13(2):166-169.Collins G E,Qin Lu. 2001. Microfabricated capillary electrophoresis sensor for uranium(VI)[J].Anal. Chim. Acta,436 (2):181-189.
Hosseini M S,Raissi H,Yavari H R.2006. Synergistic flotation of U(VI)-alizarin complex with some diamines followed by spectrophotometric determination of U(VI)using 4,4c-diamino-phenylmet hane[J]. Ana l. Chim. Acta,559 (2):181-185.
Huang S K,Qin W,Dai Y Y. 2007. Sorption of pyruvic acid with weakly basic polymer sorbents[J]. Chin J Chem Eng.,15 (6):868-871.
Prasada Rao T,Metilda P,Mary Gladis J. 2006. Preconcentrat ion techniques for uranium (VI)and thorium(IV)prior to analytical determination-an overview[J].Talanta,68:1047-1064.
Shu Z N,Du R J,Wang X,et al. 2007a. Adsorption of XSD-296 resin for Cr(VI)[J]. Trans Nonferrous Met Soc China,17 (4):869-873.
Shu Z N,Xiong C H,Shen Q X,et al. 2007b. Adsorption behavior and mechanism of D113 resin for lanthanum[J]. Rare Metals,26(6):601-606.
Shu Z N,Xiong C H,Wang X. 2006. Adsorption behavior and mechanism of amino methylene phosphonic acid resin for Ag(I)[J]. Trans Nonferrous Met Soc China,16(3):700-704.
Starvin T P R A M. 2004. Solid phase extractive preconcentration of uranium(VI)onto diarylazo -bisphenol modified activated carbon[J].Talan-ta,63(2):225-232.
Xiong C H,Wu X M. 2003. Study on the adsorption of iminodiacetic acid resin for yttrium(III)[J]. Chin J Inorg Chem,19(12):1356-1360.
Xu T,Liu X Q. 2008. Peanut shell activated carbon,Characterization,surface modification and adsorption of Pb2+from aqueous solution[J]. Chin J Chem Eng,16(3):401-406.
