以卵磷脂为手性添加剂制备手性介孔二氧化硅
2013-10-17国永敏李宝宗
王 晴 国永敏 李 艺 李宝宗
(苏州大学材料与化学化工学部,苏州 215123)
自20世纪90年代Mobile公司首次报道了介孔二氧化硅材料MCM-41[1]的合成以来,有序介孔二氧化硅材料由于具有可调孔径、可控形貌、有序孔道、比表面积大、易于修饰等优点,因此在吸附、分离、催化、药物释放等方面有广阔的应用前景[2-4]。目前合成介孔二氧化硅材料的方法很多,总体来说分为“硬”模板法和“软”模板法。“硬”模板法主要是指使用模板剂的结构相对较 “硬”,即结构刚性的材料,如碳材料或无机离子等固体材料[5]。“软”模板主要包括双亲分子形成的各种有序聚合物,如液晶、微乳状液、囊泡[6-7]、自组装膜等。相对于硬模板法,软模板法具有如下特点:软模板法是双亲分子形成的有序聚集体,软模板的形状具有多样性;软模板一般都很容易控制构筑,不需要复杂的设备[8-9]。虽然软模板法不能总是严格控制产物的尺寸和形状,但由于该模板法具有方法简单、操作方便、成本较低等优点引起了人们的广泛重视。
在介孔二氧化硅的形貌控制上,螺旋结构得到了广泛关注,这类固体材料如二氧化硅等具有合适的孔径,因此可以作为催化剂应用于特定的反应;与有机非均相催化剂相比,这类材料具有较高的热稳定性;与DNA、蛋白质相比,这类材料的螺旋结构形貌更易于控制[10],同时其水溶性较差易于从反应体系中分离。这类材料可能在分子尺度上表现出手性,则有希望应用于对映体拆分和不对称催化[11-12]。其合成可以使用手性小分子自组装体为模板[13-14],虽然使用手性小分子自组装体为模板可以成功得到单手螺旋的结构,而且在分子尺度上也表现出手性[15]。但是由于手性小分子的使用,使得所得到手性二氧化硅存在成本较高的问题。以非手性的表面活性剂为模板,也可以制备出螺旋的介孔二氧化硅材料。其形成的驱动力一般为:熵增加[16],表面自由能的降低[17],螺位错[18]等,但很难控制其形成单手螺旋。尽管,有报道通过加入手性添加剂可以改变左右手螺旋的比例,但还是难于得到单手螺旋的结构,而且,其在分子尺度上的手性也没有进行表征[19]。为了将这类材料应用于对映体拆分和不对称催化,不但需要表征其在纳米尺度下的螺旋孔结构,而且必须检测其在分子尺度上的手性。
本文以十六烷基三甲基溴化铵(CTAB)为模板剂,卵磷脂(PC)为手性添加剂,四乙氧基硅烷(TEOS)作为硅源,制备螺旋介孔二氧化硅纳米棒。圆二色谱表征证明该纳米棒在埃尺度下倾向于形成单一手性。所得到的材料有希望应用于对映体拆分和不对称催化。
1 实验部分
1.1 试剂与仪器
36.0wt%~38.0wt%浓盐酸购于国药集团化学试剂有限公司;无水乙醇购于天津市巴斯夫化工有限公司;正硅酸乙酯(TEOS)购于Aldrich;磷脂酰胆碱(PC)购于上海迈瑞尔化学技术有限公司;4,4′-二(三乙氧基硅)-1,1′-联苯(BTSB)由苏凯路化学科技有限公司赠送;圆二色谱仪(CD):AVIV-410,美国AVIV Biomedical,Inc; 冷 场 发 射 扫 描 电 镜 (FESEM):S-4800,日本日立公司;高分辨透射电镜(TEM):TecnaiG220,美国FEI公司;多孔道物理吸附与孔径分布仪(BET):TristarII3020,美国麦克公司;X-射线多晶衍射仪(SAXRD):X Pert-Pro MPD,荷兰帕纳科公司。
1.2 实验过程
(1)称取 100 mg(0.27 mmol)的 CTAB,加热溶解在装有35 mL去离子水的茄形瓶中,将质量为10 mg(0.013 mmol)的两亲性小分子PC超声分散在装有15 mL的去离子水试管中,1.0 h后将其加入到CTAB溶液中,在80℃搅拌速度为1 500 r·min-1下混合均匀,30 min 后加入 0.35 mL NaOH(2.0 mol·L-1)溶液,10 min 后逐滴加入 2.0 mmol TEOS,反应2.0 h后停止,抽滤,将所得滤饼用40 mL乙醇和5.0 mL 浓盐酸(8∶1,V/V)混合溶液煮沸 10 min 除去模板,抽滤,所得样品真空干燥1.0 h,然后在550℃煅烧5.0 h彻底除去模板,得到了白色粉末状产物。
(2)重复上述步骤,其硅源中加入5.0wt%的BTSB。模板剂利用索式提取器回流24 h去除,溶剂为体积比为8∶1(V/V)的乙醇和浓盐酸混合液,室温下干燥得到样品,所得样品用于圆二色谱的表征。
2 结果与讨论
由扫描电镜照片图1a可知,样品为螺旋纳米棒,其左右手螺旋的比例约为1∶1,且长约50~200 nm,直径为30~50 nm,表明手性添加剂PC的加入具有延长胶束的作用。先前的结果亦表明:脂肪醇或阴离子表面活性剂的引入都有利于胶束的延长[20-21]。PC的长碳链与CTAB的长碳链的相互作用可能是导致其胶束延长的主要原因。另外,纳米棒的表面还可以看到层状孔道(图1a)。这可能是由于CTAB和二氧化硅齐聚物所形成的混合胶束由六角柱相向层状相转变形成的[20]。透射电镜照片图1b和1c表明纳米棒的内部存在沿着纳米棒长轴方向的螺旋孔道[22],其螺距约为180~240 nm,螺距随着纳米棒的直径增加而增加。纳米棒的末端透射电镜照片表明其孔道呈二维六方排列(图1b)。透射电镜照片图1b和1c表明螺旋棒的两端是半圆形,即有比表面减少的趋势,说明该螺旋结构的形成的驱动力是表面能降低[17]。由透射电镜照片还可以看到其孔径和壁厚均为2.0 nm。

图1 介孔二氧化硅纳米棒的扫描电镜照片(a)和透射电镜照片(b,c)Fig.1 FESEM(a)and TEM(b and c)images of the mesoporous silica nanorods
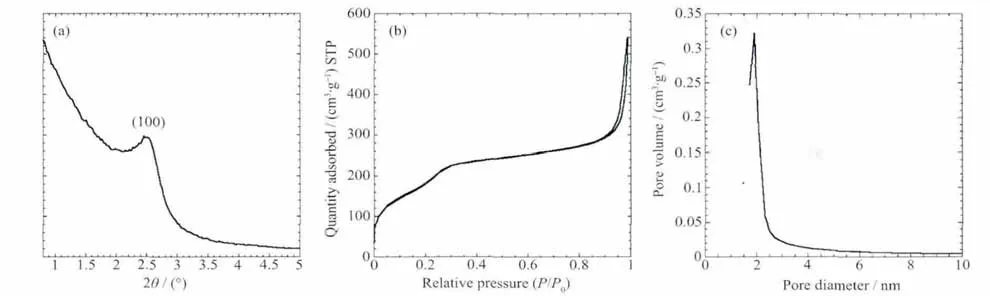
图2 介孔氧化硅纳米棒的SAXRD(a)和N2吸附-脱附等温曲线(b)及孔径分布图(c)Fig.2 (a)SAXRD pattern of the mesoporous silica nanorods(b)N2adsorption-desorption sorption isotherms and(c)BJH pore size distribution plots calculated from the desorption branch
样品在 2θ=2.54°时只出现一个较宽的衍射峰(图2a),为(100)的布拉格衍射峰,然而并没有出现其它的2个二维六方特征衍射峰,可能是由于纳米颗粒太小并且孔道扭曲导致的。其d=3.5 nm,相邻两孔道中心距离约为4.0 nm,这与透射电镜表征的结果相一致。图2b是介孔氧化硅纳米材料的N2等温吸附-脱附等温线,属于典型的Ⅳ型曲线。相对压力P/P0在0.2和0.3之间出现毛细冷凝现象,但没有出现滞后环,这可能与氮气分子的单层吸附有关。在相对压力P/P0>0.9时出现一滞后环,表明存在二级构造孔,应该是由纳米棒堆积而成的空腔。以BJH方法对吸附分支曲线计算得到孔径为2.0 nm,且孔径分布很窄,这也与透射电镜表征的结果相符,该样品比表面积为 663 m2·g-1。
由于二氧化硅没有紫外-可见活性,不能利用圆二色谱直接检测其手性。这里,采用BTSB为手性指示剂对所得到的二氧化硅手性进行检测。联苯通常以扭曲构象存在,扭曲角度为30°~45°。其构象手性可以随着外界手性环境变化而变化,这种构象手性可以通过圆二色谱表征。由于联苯基可以通过共价键与二氧化硅的骨架相连,所以二氧化硅的手性可以通过来源于芳环的扭转产生的圆二色谱信号进行表征。最近,利用该方法已经成功检测了二氧化硅纳米管的手性[15]。为了避免破坏螺旋介孔二氧化硅纳米棒的形貌,本实验通过加入5.0wt%的BTSB用来检测螺旋介孔二氧化硅纳米棒的手性。图3a,图3b分别是所得到样品的扫描电镜和透射电镜照片,结果表明BTSB的加入并没有剧烈地改变螺旋介孔二氧化硅纳米棒的形貌及孔结构。
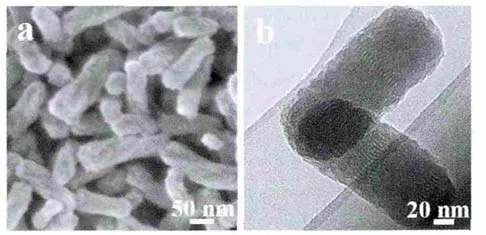
图3 有机无机杂化的介孔二氧化硅纳米棒的扫描电镜照片(a)和透射电镜照片(b)Fig.3 FESEM(a)and TEM(b)images of the mesoporous hybrid silica nanorods
图4 为在25℃的条件下将1.5 mg的样品分散在25 mL的色谱醇中的圆二色谱表征。在300 nm左右的负信号来源于联苯基团在骨架当中的左手堆积,在250 nm的正信号来源于联苯基团的左手扭转。该结果证明,前面所得到的二氧化硅虽然在纳米尺度上左右手混合比例约为1∶1,但在分子尺度上更倾向于形成单一手性。先前的结果亦表明:对于手性纳米材料,其在纳米和分子尺度上的手性既可能相同也可能相反[23]。换句话说,即使该纳米棒在纳米尺度上表现为右手螺旋,其在分子尺度上的硅氧链亦可为左手螺旋结构。这种在分子尺度或埃尺度上形成的手性与PC的手性可能会有着密切的关系。PC的手性通过分子印迹的方式传递到介孔二氧化硅纳米棒的骨架中。因为该材料在分子尺度上具有手性,其很有希望应用于映体拆分和不对称催化。

图4 有机无机杂化的介孔二氧化硅纳米棒的圆二色谱图Fig.4 CD image of the mesoporous hybrid silica nanorods
3 结 论
以CTAB的超分子自组装体为模板和手性两性小分子PC为手性添加剂,通过溶胶-凝胶的方法,制备出螺旋介孔二氧化硅纳米棒。PC的加入不仅有利于胶束的延长从而形成纳米棒,而且还使得该介孔二氧化硅纳米棒在分子尺度上倾向于形成单一手性,使得该材料有可能应用于对映体拆分和不对称催化。
[1]Kresge C T,Leonowicz M E,Beck J S,et al.Nature,1992,359:710-712
[2]Corma A.Chem.Rev.,1997,97(6):2373-2419
[3]Wan Y,Zhao D.Chem.Rev.,2007,107:2821-2860
[4]Yoshina I C,Asefa T,Coombs N,et al.Chem.Commun.,1999,24:2539-2540
[5]Wang H N,Wang Y H,Zhou X,et al.Adv.Funct.Mater.,2007,17(4):613-617
[6]Ding J X,Xi C S,Zhou X L,et al.Mater.Lett.,2012,73:17-20
[7]DONG Xiu-Fang(董秀芳),CAO Rui-Lin(曹瑞林),LI Yu(李裕),et al.Chem.Engineer(Huaxue Gongchengshi),2010,5:43-45
[8]WU Hong-Yu(伍宏玉),LI Hai-Tao(李海涛),ZHANG You-Yu(张友玉),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2012,28(2):257-262
[9]Chen J F,Ding H M,Wang J X,et al.Biomaterials,2004,25(4):723-727
[10]Kawasaki T,Ishikawa K,Sekibata H,et al.Tetrahedron Lett.,2004,45(42):7939-7941
[11]Moreau J,Vellutini L,Bied C,et al.J.Am.Chem.Soc.,2001,123:1509-1510
[12]Yang Y G,Nakazawa M,Suzuki M,et al.Chem.Mater.,2004,16(20):3791-3793
[13]Yang Y,Suzuki M,Hanabusa K,et al.J.Am.Chem.Soc.,2007,129(17):581-587
[14]Wan X,Pei X,Yang Y,et al.Nanotechnology,2008,19:315603
[15]Li B,Xu Z,Yang Y,et al.Chem.Commun.,2011,47:11495-11497
[16]Zhou L,Hong G,Lu Y,et al.Langmuir,2009,25:6040-6044[17]Yang S,Zhao L,Zhao D,et al.J.Am.Chem.Soc.,2006,128:10460
[18]Yang H,Ozin G A,Kresge C T.Adv.Mater.,1998,10(11):883-887
[19]Hu Y,Yuan P,Yu C,et al.Chem.Lett.,2008,37:1160-1161
[20]Li Y,Bi L,Yang Y,et al.Chem.Commun.,2010,46:2680
[21]Zhuang W,Bi L,Yang Y,et al.Chin.J.Chem.,2011,29:883-887
[22]Che S,Liu Z,Tatsumi T.Nature,2004,429:281-284
[23]Li Y,Wang S,Yang Y,et al.Nanotachnology,2013,24:035603
