Dawson 型磷钨酸盐与混合配体桥连的四核Cu-Phen 配合物构筑的杂化物
2013-08-20张先徽那延祥李昌立冯克成
孙 岳 张先徽 那延祥 李昌立*, 冯克成*,
(1 长春理工大学理学院,长春 130022)
(2 厦门大学物理与机电工程学院,厦门 361005)
0 引 言
由于过渡金属配合物的引入使基于多金属氧酸盐的无机-有机杂化材料具有迷人的拓扑结构和广泛的应用,并成为设计新型材料的主要研究对象[1-6]。通过选择不同的配体能够形成具有新颖的结构和不同核性的过渡金属配合物,在特定的反应条件下与多金属氧酸盐作用得到能够应用于光学、磁学、电化学等研究领域的新型化合物[7-11]。
近几年来,Cu-phen 配合物由于其可变的核性而受到了广泛的关注[12-15]。一些由多金属氧酸盐阴离子和不同Cu-phen 配合物组成的杂化化合物已经被报道,并且这些Cu-phen 配合物的核性从一到四,桥连的配体通常为羧酸类配体(例如醋酸和草酸)[16-19]。当前我们致力于研究含有多核Cu 簇的配合物与多金属氧酸盐的反应,期望获得新颖的能够应用于不同研究领域的无机-有机杂化化合物。在合成的过程中1,10-邻菲罗啉(phen)和Cl 被引入到反应体系中。另外,由于对苯二甲酸(1,4-H2bdc)具有可变的配位形式,并且它作为刚性的桥连配体连接Cu(Ⅱ)离子能形成具有不同维度的扩展结构(0D 到3D)[20-22]也被引入到该反应体系。由于反应物的混合通常导致大量的沉淀使化合物在常温条件下很难结晶,我们采用水热合成的方法成功的合成了一个新颖的化合物[CuCl(H2O)4)][CuCl(H2O)(Phen)][{(CuPhen)2Cl2}2(bdc)]2[P2W18O62]·5H2O (1)。这里我们研究了它们的合成、结构、热稳定性和电化学性质。
1 实验部分
1.1 试剂和仪器
前驱体Na12[α-P2W15O56]·18H2O 根据文献方法制备[23],并通过红外光谱和核磁证明其纯度。其它的试剂都是商业购买(分析纯),使用时没有进一步纯化。晶体学数据用德国Bruker 公司生产的Bruker Smart CCD Apex(Ⅱ)单晶衍射仪进行收集;红外光谱在Alpha Centraurt FT/IR 红外光谱仪上测量,采用KBr 压片,测量的范围400~4 000 cm-1;元素分析在Perkin-Elmer 240 CHN 元素分析仪和PLASMASPECガICP 仪器上测量; 热重分析采用Perkin Elmer Pyris Ⅱ热分析仪,氮气环境中,升温速率为10 ℃·min-1; 电化学分析使用CHI660B CHI660 电化学工作站连接一台电脑用于电化学测试和数据收集。所用体系为常规三电极体系:工作电极为空白碳糊电极(CPE)、杂化材料本体修饰的碳糊电极,参比电极为Ag/AgCl 电极,铂丝做对电极。
1.2 化合物的合成
化合物[CuCl(H2O)4)][CuCl(H2O)(Phen)][{(CuPhen)2Cl2}2(bdc)]2[P2W18O62]·5H2O (1)的 合 成:称 取0.5 g(1.350 mmol)Cu(ClO4)2·6H2O,0.1 g(0.549 mmol)Phen,0.06 g (0.361 mmol) 1,4-H2bdc 溶 于5 mL (277 mmol) H2O 中,在室温下继续搅拌30 min,得到混合物A。将0.6 g (0.139 mmol) Na12[α-P2W15O56]·18H2O溶于5 mL(277 mmol) H2O 中,得到溶液B,将B 缓慢的滴加到混合物A 中,室温下搅拌20 min 得到混合物C,将混合物C 装入30 mL 聚四氟乙烯衬里的高压釜中,在170 ℃下加热4 d 后以10 ℃·h-1的速度降到室温,得到绿色块状的晶体1。经去离子水充分洗涤后过滤收集。产率约为63%(按照Cu 计算)。化合物1 在空气中稳定并且不溶于水和一般的有机溶剂。元素分析(C124H100Cl10Cu10N18O80P2W18)计算 值(%):C,19.90;H,1.35;N,3.37;P,0.83;Cl,4.74;Cu,8.49;W,44.22;实 验 值(%):C,20.11;H,1.27;N,3.45;P,0.79;Cl,4.89;Cu,8.37;W,43.98。IR(KBr 压片,cm-1):3 339 (w),1 609 (m),1 559 (m),1 516(m),1 427(m),1 384(m),1 339(m),1 225(m),1 143(m),1 091(m),953(m),906(m),786(s),721(s),524(m)。
1.3 X-射线晶体学测定
选取尺寸为0.25 mm×0.23 mm×0.22 mm 的化合物1 的单晶,在293 K 下,在Bruker Smart CCD Apex(Ⅱ)单晶衍射仪上用石墨单色化的Mo Kα (λ=0.071 037 nm)射线扫描,收集单晶衍射数据。化合物的晶体结构使用SHELXLTL 程序采用直接法解出,对所有的非氢原子坐标及其各向异性热参数进行了全矩阵最小二乘法精修。氢原子位置坐标通过理论加氢计算法给出。化合物1 的晶体学数据见Table1,化合物1 的选择性键长和键角见Table2。
CCDC:952036。
2 结果与讨论
2.1 化合物的合成
虽然在合成过程中使用缺位的前驱体Na12[α-P2W15O56]·18H2O 作为初始原料,但是在化合物1 中生成了饱和的多阴离子[P2W18O62]6-。在反应的过程中多氧阴离子[α-P2W15O56]12-经历了从缺位到饱和Dawson 型多氧阴离子的转化。一些已经报道的实验结果也表明在酸性的条件下缺位的Dawson 型多氧阴离子能够转化成饱和的多氧阴离子[24-26]。值得注意的是在水热条件下,我们也尝试用[P2W18O62]6-代替缺位的反应前躯体,可是并不能得到化合物1。
2.2 化合物的晶体结构
化合物1 结晶在单斜的C2/c 空间群,图1 与图2 分别为化合物1 的非对称单元结构图和分子结构示意图。如图2 所示,化合物1 包含1 个[Cu(H2O)4Cl)]+配阳离子,1 个[CuCl(H2O)(Phen)]+配阳离子,1 个[P2W18O62]6-阴离子,2 个与多金属氧酸盐阴离子共价相连的四核铜阳离子配合物[{(CuPhen)2Cl2}2(bdc)]2+和5 个结晶水分子。化合物1 包含6 个晶体学独立的Cu 中心,四核铜阳离子配合物[{(CuPhen)2Cl2}2(bdc)]2+中包含Cu1、Cu2、Cu3 和Cu4,其中Cu1、Cu2和Cu3 分别与2 个Cl 原子,2 个phen 配体上的N原子和1 个来自于bdc 的氧原子配位,形成了五配位的“4+1”型几何构型,而Cu4 原子与2 个来自于phen 配体的N 原子、1 个[P2W18O62]6-上的氧原子、1个Cl 原子则和1 个来自于bdc 的氧原子配位,形成
了六配位“4+2”八面体配位几何构型,[(CuPhenH2O)Cl]+配阳离子中的Cu5 分别与2 个来自于phen 配体的N 原子、1 个水分子和1 个Cl 原子配位形成4配位的平面四方形几何构型,而[CuCl(H2O)4)]+配阳离子中的Cu6 别与1 个Cl 原子,4 个水分子配位,形成了五配位的“4+1”型几何构型。Cu-N、Cu-O、Cu-Cl 的键长范围分别为0.190~0.211、0.191~0.275 和0.228 ~0.269 nm,N-Cu-N、N-Cu-O、Cl-Cu-Cl、N-Cu-Cl、O-Cu-Cl 键角的范围分别是81.0°~83.9°、86.5°~170.6°、91.2°~96.5°、90.1°~174.4°、90.6°~93.9°。多金属氧酸盐阴离子[P2W18O62]6-的所有的键长和键角都

表1 化合物1 的晶体数据Table 1 Crystal data and structural refinement for compound 1

表2 化合物1 的主要键长和键角Table 2 Selected bond lengths (nm) and bond angles (°) in compound 1
在化合物1 的铜配合物阳离子[{(CuPhen)2Cl2}2(bdc)]2+中bdc 配体连接2 个二核的[(CuPhen)2Cl2]2+阳离子,Cl 和phen 分别作为这2 个二核铜配合物片段的桥连配体和外围配体。配合物阳离子[{(CuPhen)2Cl2}2(bdc)]2+通过[P2W18O62]6-的末端氧原子与多金属氧酸盐连接,铜氧的键长为0.275 nm。每1 个[CuCl(H2O)4)][CuCl(H2O)(Phen)][{(CuPhen)2Cl2}2(bdc)]2[P2W18O62]分子通过bdc 和Phen 的π-π 作用(0.352~0.373 nm) 及阴阳离子间的静电作用沿c 轴在正常的范围内,与文献报道的相一致[27-29]。方向堆积成拉链状的一维链。相邻的链通过POMs的端氧原子与Phen 环上的C 原子间的氢键作用在bc 平面上形成二维层(Fig.3)。二维的层又通过phen之间的π-π 作用堆积成三维的超分子框架[30]。在化合物1 中[CuCl(H2O)4)]+阳离子[CuCl(H2O)(Phen)]+阳离子分别在2 个位置上无序,无序占有率为50%(Fig.4)。价键计算表明所有的W 原子都是+6 价氧化态,Cu 原子都是+2 价氧化态。

图1 化合物1的不对称单元椭球图Fig.1 Ortep view of the asymmetric unit of 1 with 30% probability of ellipsoid

图2 化合物1 的分子结构示意图Fig.2 Molecular structural unit of 1

图3 化合物1的空间排列Fig.3 Packing arrangement of 1

图4 化合物1 的[(CuPhenH2O)Cl]+阳离子结构示意图(a);无序的[(CuPhenH2O)Cl]+阳离子结构示意图(b)Fig.4 View of [CuCl(H2O)(Phen)]+of 1 (a) and the view of the disordered [CuCl(H2O)(Phen)]+of 1 (b)
2.3 化合物的红外光谱
化合物1 在3 339 cm-1处的峰归属为水分子的振动,在1 091 cm-1处的峰归属为ν(P-O),而在953、906、786、721 和524 cm-1处的峰则归属为Dawson多金属氧酸盐阴离子中的νas(W-Ob-W),νas(W-Oc-W)和νas(W-Od)的振动。在1 609、1 516、1 427、1 339、1 225 和1 143 cm-1处显示了phen 配体的伸缩振动,而在桥连配体bdc 中的两种不同配位模式的振动峰νs(COO-)和νas(COO-)分别在1 559 和1 384 cm-1处被观察到[31-32]。
2.4 化合物热重分析
我们对化合物1 的稳定性进行了初步研究。它的晶体在室温下的空气中放置几个月后仍然保持完整,没有观察到风化现象,并且不溶于水和常见的有机溶剂(包括甲醇、甲酸、乙醇、乙酸、乙腈、丙酮、DMF、氯仿)。
此外我们还研究了化合物1 的热稳定性,同时也进一步证明了它们的化学结构组成,如Fig.5 所示。化合物1 的热重曲线表明在22~631 ℃范围内有三步连续的失重约为33.41%,与计算值33.20%相接近。在125 ℃前的第一步失重约1.29%对应于所有的结晶水分子的失去(计算值为1.20%)。在125~631 ℃间的二步失重大约为32.12%归属为配位水分子、bdc、phen 和Cl2配体的分解(计算值为32.00%)。在631~800 ℃范围内样品没有进一步的重量失去。

图5 化合物1 的热重曲线Fig.5 TG curve of compound 1
2.5 电化学性质及分析
由于化合物1 不溶于水及常见的有机溶剂,我们研究了以化合物1 为修饰剂的本体修饰碳糊电极(1-CPE)的电化学行为和电催化活性。记录了1-CPE 在1 mol·L-1H2SO4水溶液中,-600~400 mV 电势范围内不同扫速的电化学行为(Fig.6)。当扫速为60 mV·s-1时,2 对可逆的氧化还原峰Ⅱ-Ⅱ′、Ⅲ-Ⅲ′归属为W 中心的2 个连续的两电子过程,它们的半波电位(Emid)分别为-146(Ⅱ-Ⅱ′)和-343 (Ⅲ-Ⅲ′)mV Emid=(Epc+Epa)/2,Epc和Epa分别为阴极和阳极峰电势)[33-34]。在+118 mV 处不可逆的峰Ⅰ′归属为铜中心的氧化。

图6 1-CPE 的循环伏安图Fig.6 Cyclic voltammograms of the 1-CPE
NOx的催化还原,尤其是用多金属氧酸盐催化还原亚硝酸盐已经成为检测其电催化活性的经典的检验。但是只有一些多金属氧酸盐对于亚硝酸盐的还原具有电催化活性。并且在NOx体系中亚硝酸盐的电催化还原过程需要几个电子,以至于这一过程的实现仍然具有一定的困难。因此我们用1-CPE电催化还原NO2-来进一步研究化合物1 的电催化活性。实验证明1-CPE 对于亚硝酸盐还原具有很好的电催化活性。如Fig.7 所示,随着亚硝酸盐的增加,所有的还原峰电流增加,而对应的氧化峰电流降低,这表明化合物1 的还原种类对于亚硝酸的还原具有催化活性。值得注意的是,1-CPE 是十分稳定的,当扫描速率为100 mV·s-1时,经过几百圈的扫描峰电流几乎保持不变。1-CPE 在室温下储存一个月后,峰电流只有微小的改变,并且从管中挤出少量的碳糊后其电化学性质能够得到复原。1-CPE可能成为研究多金属氧酸盐杂化化合物电催化性质的一个理想的电极材料。
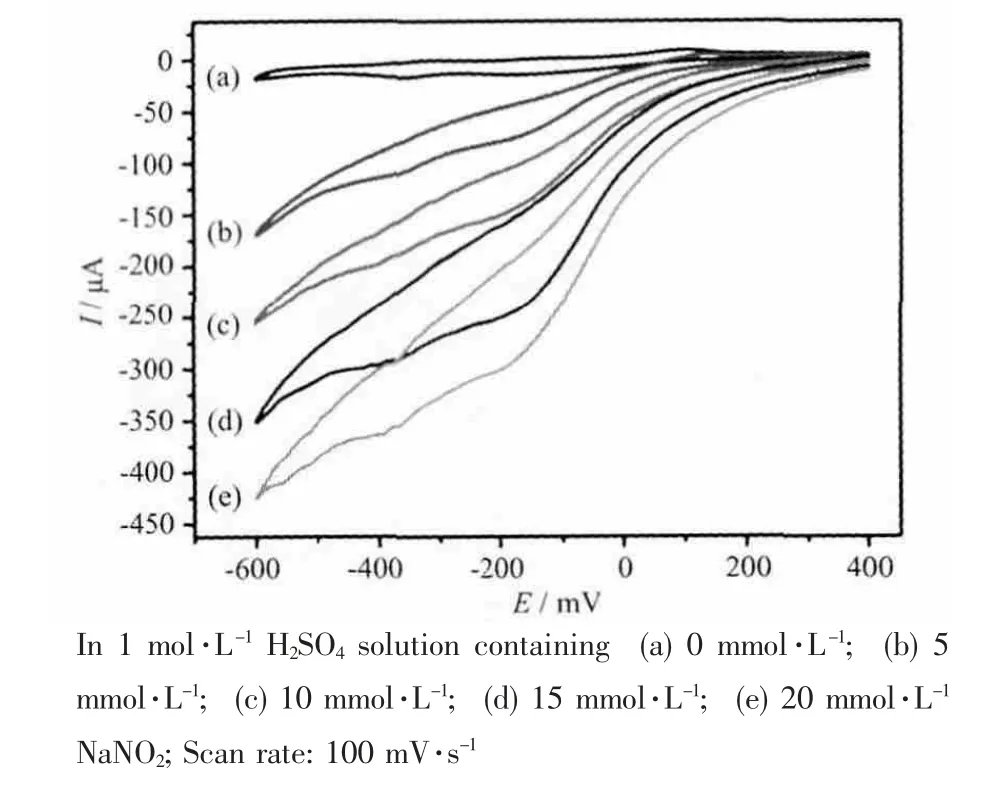
图7 1-CPE 的循环伏安图Fig.7 Cyclic voltammograms of 1-CPE
3 结 论
在水热条件下使用Cu-phen 配合物与多金属氧酸盐前驱体反应合成出一个基于多金属氧酸盐簇[P2W18O62]6-的无机-有机杂化化合物。在化合物1中不同的Cu-phen 配合物片段通过Cl 和bdc 桥的连接组合成了新的四核Cu-phen 配合物。化合物1的高热稳定性、在不同溶剂中的低溶解性及富含多金属氧酸盐的特性使1-CPE 对于亚硝酸盐的还原具有很好的电催化活性,有可能成为理想的电催化材料。化合物1 的成功合成表明反应原料、反应物的比例和阴阳离子的尺寸的适当结合在水热条件下能够形成具有新颖结构和功能的新型材料。
[1] Pope M T, Müller A. Angew. Chem. Int. Ed., 1991,30:34-48
[2] Hill C L, Prosser-McCartha C M. Coord. Chem. Rev., 1995,143:407-455
[3] Müller A, Peters F, Pope M T, et al. Chem. Rev., 1998,98:239-271
[4] Rhule J T, Hill C L, Judd D A, et al. Chem. Rev., 1998,98:327-357
[5] Gouzerh P, Proust A. Chem. Rev., 1998,98:77-111
[6] Clemente-Juan J M, Coronado R. Coord. Chem. Rev., 1999,193-195:361-394
[7] Hagraman P J, Hagraman K, Zubieta J. Angew. Chem. Int.Ed, 1999,38:2638-2684
[8] Chesnut D J, Hagrman D, Zapf P J, et al. J. Coord. Chem.Rev., 1999,190-192:737-769
[9] Hagrman P J, Finn R C, Zubieta J. Solid State Sci., 2001,3:745-774
[10]Kozhevnikov I V. Catalsis by Polyoxometalates. Chichester(UK): Wiley, 2002.
[11]Contant R, Hervé G. Rev. Inorg. Chem., 2002,22:63-111
[12]Ushak S, Spodine E, Fur E L, et al. Inorg. Chem., 2006,45:5393-5399
[13]Burrows A D, Chan C W, Chowdhry M M. Chem. Soc. Rev.,1995,24:329-339
[14]Wang S T, Wang E B, Hou Y, et al. Inorg. Chim. Acta,2003,349:123-127
[15]Ghosh A K, Ghoshal D, Ribas J, et al. Cryst. Growth Des.,2006,6:36-39
[16]Reinoso S, Vitoria P, Felices L S, et al. Chem. Eur. J.,2005,11:1538-1548
[17]Reinoso S, Vitoria P, Felices L S, et al. Inorg. Chem., 2006,45:108-118
[18]Shivaiah V, Chatterijee T, Srinivasu K, et al. Eur. J. Inorg.Chem., 2007:231-234
[19]Reinoso S, Vitoria P, Gutiérrez-Zorrilla J M, et al. Inorg.Chem., 2007,46:4010-4021
[20]Bian H, Xu J, Gu W, et al. Inorg. Chem. Commun., 2003,6:573-576
[21]Mukherjee P A, Hoshal D, Zangrando E, et al. Eur. J. Inorg.Chem., 2004:4675-4680
[22]Paul B,Zimmermann B,Fromm K M,et al. Z.Anorg.Allgem.Chem., 2004,630:1650-1654
[23]Contant R. Inorg. Synth., 1990,27:104-109
[24]WANG En-Bo(王恩波), HU Chang-Wen(胡长文), XU Lin(许 琳). Introduction of Polyacid Chemistry(多 酸 化 学 导 论).Beijing: Chemical Industry Press, 1998.
[25]Zhang C D, Liu S X, Ma F J, et al. Dalton Trans., 2010,39:8033-8037
[26]Zhao J W, Zheng S T, Liu W, et al. J. Solid State Chem.,2008,181:637-645
[27]Niu J, Guo D, Zhao J, et al. New J. Chem., 2004,28:980-987
[28]Lu Y, Xu Y, Li Y, et al. Inorg. Chem., 2006,45:2055-2060
[29]Tian A, Ying J, Peng J, et al. Inorg. Chem., 2008,47:3274-3283
[30]Janiak C. J. Chem. Soc., Dalton Trans., 2000:3885-3896
[31]Deakin L, Arif A M, Miller J S. Inorg. Chem., 1999,38:5072-5077
[32]Massoud S S, Mautner F A, Vicente R, et al. Inorg. Chim.Acta, 2006,359:1489-1500
[33]Sadakane M, Steckhan E. Chem. Rev., 1998,98:219-237
[34]McCormac T, Fabre B, Bidan G J. Electroanal. Chem.,1997,425:49-54
