无功能性恶性嗜铬细胞瘤1例并文献复习
2013-06-15周思静洪艳艳周俊生刘胜萍
周思静,洪艳艳,周俊生,刘胜萍
(1合肥市第三人民医院,合肥230001;2安徽医科大学第二附属医院)
嗜铬细胞瘤是起源于肾上腺分泌儿茶酚胺的嗜铬细胞的肿瘤,是继发性高血压的重要原因之一。随着近年来对继发性高血压认识的提高,临床上对典型嗜铬细胞瘤的诊断及治疗均有很大进步。但对于一些特殊类型的嗜铬细胞瘤,如恶性嗜铬细胞瘤及无功能性静止型嗜铬细胞瘤,由于发病率低且表现不典型,临床认识不足,诊断仍存在困难,治疗上也缺乏大规模临床研究结果作为参照标准。本研究对1例无功能性恶性嗜铬细胞瘤患者临床资料进行分析,并复习国内外相关文献,以期提高对恶性嗜铬细胞瘤的认识。
1 病例报告
患者男,56岁,汉族,因反复左上腹疼痛半年,再发加重半个月入院。患者于2011年8月起无明显诱因间断出现左上腹隐痛,程度不重,未重视。2012年1月中旬腹痛再发并加重,于2012年2月1日就诊某市人民医院,腹部CT(图1)提示左肾上腺巨大占位,106 mm×80 mm×58 mm。2012年2月7日在该院行经腹肾上腺占位切除术,术中因占位组织与大血管粘连明显无法切除,2012年2月8日转至合肥市第三人民医院泌尿外科治疗。入院查体:T:36.5 ℃,P:98 次/min,R:20 次/min,BP:150/80 mmHg,神清,精神欠佳,皮肤黏膜无黄染及出血点,浅表淋巴结未扪及,颈软,气管居中,双肺呼吸音清,未闻及罗音,心律齐,未闻及病理性杂音,腹软,腹带加压包扎,左腹部可见一长约30 cm手术切口,左下腹引流管连接引流袋,引流出少许淡血性液体,全腹压痛、反跳痛阴性,膀胱区无隆起及压痛,双下肢无水肿,病理征未引出。辅助检查:血、尿、便常规及肝肾功能、电解质、血糖、血脂、PT系列正常;心电图未见明显异常;肾上腺内分泌功能检查:醛固酮、促肾上腺皮质、皮质醇水平均在正常范围。入院诊断:左肾上腺占位,性质待定:皮质腺癌?2012年2月16日再次手术,术中见大网膜与腹膜轻度粘连,肿瘤与左肾、膈肌角及脾脏粘连明显,左肾蒂血管被肿瘤包被,予以左肾上腺占位切除+左肾切除+脾脏切除术。术后病理:①恶性肾上腺嗜铬细胞瘤,大小约11 cm×7 cm×6 cm,与肾组织粘连,但未侵犯肾实质,肾盂及输尿管未见癌残留;②脾动脉广泛硬化合并破裂出血,破裂口长3 cm;③送检部分胰尾组织为坏死组织,未见癌组织;免疫组化RCC阴性,CD阴性,VIM 阳性,CD34阴性,α-inhibin阳性,MclanA阴性,CgA阳性,syn阳性,ki67(80%阳性),EMA阴性,CK(少许阳性),CEA阴性。术后恢复好,KPS 90分,转至肿瘤科治疗,期间监测血压、心率,均在正常范围。2012年3月19日开始行吉西他滨联合吡喃阿霉素化疗,21 d为1周期,过程顺利,患者无特殊不适。出院诊断:左侧肾上腺恶性嗜铬细胞瘤。
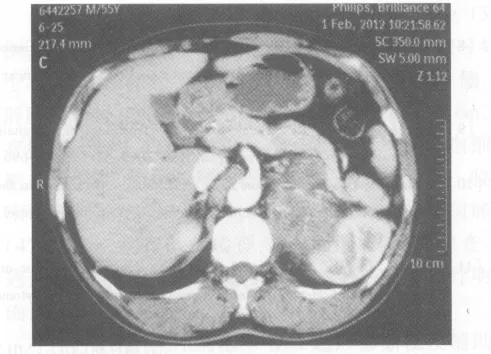
图1 腹部增强CT
2 讨论
嗜铬细胞瘤发病率为1~2/100万,其中特殊类型少见,占恶性嗜铬细胞瘤的5% ~26%;静止型嗜铬细胞瘤更为少见,占特殊类型的 1.5% ~23.0%[1],常表现为血压正常。静止型嗜铬细胞瘤分为两种[2]:一种为隐匿功能性嗜铬细胞瘤,平时无血压增高,但是在应激条件下血压可急骤上升;另一种为无功能性嗜铬细胞瘤,因无儿茶酚胺类物质释放,在任何时期均无血压波动。本例就属于无功能性恶性嗜铬细胞瘤,这类病例国内外报道较少。
具有典型心血管症状的嗜铬细胞瘤,依据临床表现及儿茶酚胺及其代谢产物等生化检查确诊并不困难,诊断确立后各种影像学检查能进一步对肿瘤进行定位,从而为继续治疗提供帮助。但无功能性恶性嗜铬细胞瘤患者,临床症状不典型,生化指标检测无异常,给临床诊断带来困难。良、恶性嗜铬细胞瘤组织病理学形态相似,而且,目前恶性嗜铬细胞瘤的诊断标准对于早期患者临床区分良恶性也存在困难。回顾文献,分析恶性嗜铬细胞瘤诊断具有以下特点:①临床特点:多见于男性,与良性病变相比患者发病年龄小,病程短,虽然和良性病变一样具有儿茶酚胺增多的相关症状,但其多伴有疼痛及消瘦[4]。②生化检查:恶性嗜铬细胞瘤患者24 h尿去甲肾上腺素比良性者增高更明显,良性病变者少有>1 000μg/24 h;此外,恶性嗜铬细胞瘤患者尿多巴胺可增高,但良性病变者多在正常范围。③影像学检查:通常用于协助确诊患者进行定位诊断。有研究分析良、恶性嗜铬细胞瘤影像学的异同,发现恶性嗜铬细胞瘤体积较大,直径常>7 cm,且内部结构不均一[4],但并非绝对,因此,无论是超声、CT 还是MRI均不能作为确定肿瘤良恶性的标准。④核素显像:碘苄胍(MIBG)对肾上腺组织具有亲和力,奥曲肽为内源性生长抑素类似物,两者均能与神经内分泌细胞结合,因此,两者的放射性标记物131I-间-MIBG及99Tcm-HTOC常用于诊断及治疗神经内分泌肿瘤。有研究认为,99Tcm-HTOC显像对异位(心脏部位)嗜铬细胞瘤和恶性多发病灶的探测优于131I-间-MIBG,而对肾上腺嗜铬细胞瘤,131I-间-MIBG则更敏感,两种显像存在互补关系。由于核素显像能发现肾上腺外及全身转移病灶,而是否存在转移病灶是诊断恶性嗜铬细胞瘤的标准,因此,131I-间-MIBG或奥曲肽显像对诊断恶性嗜铬细胞瘤是有意义的。此外,有研究显示,恶性嗜铬细胞瘤患者行18F-脱氧葡萄糖标记的PET检查,病灶通常呈高代谢,而良性病变常无异常[5],因此,PET-CT为诊断恶性嗜铬细胞瘤提供帮助。⑤病理学检查:由于良、恶性嗜铬细胞瘤组织病理学形态相似,因此,鉴别良、恶性病变可借助免疫组化帮助,通常CgA在良、恶性嗜铬细胞瘤中均呈强阳性表达,但是良性病变通常S-100呈阳性,而恶性病变常有Ki-67表达增高。
恶性嗜铬细胞瘤的治疗除针对儿茶酚胺增多相关症状的内科对症治疗外,其他均与恶性肿瘤治疗相同,治疗主要依靠手术、放疗及化疗。手术治疗是治疗恶性嗜铬细胞瘤的有效方法,也是首选方法,即使已发生远处转移,原则上也应行原发灶及转移灶切除。但是,临床上常遇到因恶性嗜铬细胞瘤瘤体巨大或与重要组织粘连而无法切除,此外,即使一部分恶性嗜铬细胞瘤行根治性手术治疗,但因复发率高,且发生转移时常为多发病灶,对转移病灶行根治性手术很困难。因此,术后辅助治疗具有重要意义。利用儿茶酚胺结节的再摄取机制,使用131I-间-MIBG,除了可使嗜铬细胞瘤显像,同时可利用其释放的β射线杀灭肿瘤细胞。但是,131I-间-MIBG的治疗效应与肿瘤体积密切相关,瘤体巨大者应先行手术切除,残留病灶直径最好控制在1~2 cm。遗憾的是,131I-间-MIBG治疗过程中能达到完全缓解的比例很小,常在几年内复发、转移。虽然部分研究表明,少数患者通过大剂量的核素放疗可使病情得到长时间完全缓解,但是大剂量放疗可引起严重骨髓抑制,而且总体生存率并未得到提高[6]。此外,该治疗措施对于不摄取131I-间-MIBG的肿瘤无效,因此,这部分患者选择手术后化疗。目前,公认的恶性嗜铬细胞瘤最有效的化疗方案为CVD(环磷酰胺750 mg/m2第1天,长春新碱1.4 mg/m2第1天,达卡巴嗪600 mg/m2第1、2天,21 d为1周期)。该方案在治疗神经母细胞瘤上取得较大成功,而恶性嗜铬细胞瘤与神经母细胞瘤同属内分泌肿瘤。1988年Averbuch等[7]报道用此方案治疗恶性嗜铬细胞瘤,结果显示55%的患者肿瘤缩小,但中位有效时间仅为20个月。此后陆续有新的化疗方案提出,如环磷酰胺、阿霉素联合达卡巴嗪,其治疗有效率达46%[8],比CVD方案稍低。另有一些方案,如顺铂联合5-氟尿嘧啶,依托泊苷、卡铂、长春新碱、环磷酰胺及阿霉素,环磷酰胺联合甲氨蝶呤等[9],但是,关于这些方案的研究入组病例数均较少,大部分结果不理想,因此,尚不能证明这些治疗方案适用于恶性嗜铬细胞瘤。随着分子靶向药物的兴起,寻找治疗恶性嗜铬细胞瘤合适的分子靶向药物也成为重点。一些研究表明,在恶性嗜铬细胞瘤的肿瘤细胞中,HSP90、mTOR、VEGF、HIF-1α、bFGF 等表达增多[10],通过抑制这些因子生成的相关通路以抑制肿瘤细胞增殖及分化,成为目前热议的问题。2009年Park等[11]报道了1例使用传统化疗方案治疗失败的恶性嗜铬细胞瘤,在使用舒尼替尼治疗后,临床儿茶酚胺分泌过多症状明显改善,为恶性嗜铬细胞瘤治疗提供了新的治疗策略。
[1]Barzon L,Boscaro M.Diagnosis and management of adrenal incidentalomas[J].J Urol,2000,163(2):398-407.
[2]鲁功成.静止嗜铬细胞瘤新概念的探讨[J].临床泌尿外科,1995,10(1):15-16.
[3]Mundschenk J,Kopf D,Lehnert H.Therapy of malignant pheochromocytoma.Invitation to participate in a randomized multicenter study[J].Dtsch Med Wochenschr,1998,123(1-2):32-33.
[4]杨德安,李慎勤,李香铁,等.恶性嗜铬细胞瘤的诊断与治疗[J].中华外科杂志,1999,37(2):104-105.
[5]Pacak K,Eisenhofer G,Carrasquillo JA,et al.6-[18F]fluorodopamine positron emission tomographic(PET)scanning for diagnostic localization of pheochromocytoma[J].Hypertension,2001,38(1):6-8.
[6] Sisson JC.Radiopharmaceutical treatment of pheochromocytomas[J].Ann N Y Acad Sci,2002,970(1):54-60.
[7]Averbuch SD,Steakley CS,Young RC,et al.Malignant pheochromocytoma:effective treatment with a combination of cyclophosphamide,vincristine,and dacarbazine[J].Ann Intern Med,1988,109(4):267-273.
[8]Patel SR,Winchester DJ,and Benjamin RS.A 15-year experience with chemotherapy of patients with paraganglioma[J].Cancer,1995,76(8):1476-1480.
[9] Adjalle R,Plouin PF,Pacak K,et al.Treatment of malignant pheochromocytoma[J].Horm Metab Res,2009,41(9):687-696.
[10]Raymon H,Grogan M,Elliot J,et al.Changing paradigms in the treatment of malignant pheochromocytoma[J].Cancer Control,2010,18(2):104-112.
[11]Park KS,Lee JL,Ahn H,et al.Sunitinib,a novel therapy for anthracycline-and cisplatin-refractory malignant pheochromocytoma[J].Jpn JClin Oncol,2009,39(5):327-331.
