高聚物萃取分光光度法测定茶多酚含量的研究
2013-05-18杜建中文超燕
杜建中,姚 媛,文超燕
(湛江师范学院化学科学与技术学院,广东湛江524048)
茶多酚属于多酚类物质,是茶叶中含有2-苯基苯并吡喃的衍生物的多酚类物质的总称,因其分子结构中含有较多的还原性酚羟基而具有很强的清除体内自由基的功能,是一种纯天然的抗氧化剂,具有优越的抗氧化能力,并具有抗癌、抗衰老、抗辐射、清除人体自由基、降血糖、降血压、降血脂及杀菌等一系列药理功能,在油脂、食品、医药、日化、化妆品、保健品及饮料等领域具有广泛的应用前景[1-3]。我国卫生部已批准了茶多酚天然抗氧化剂为我国的食品添加剂之一。茶饮料因风味独特,兼有营养、保健功效,是清凉解渴、深受消费者欢迎的多功能饮料。因此,茶多酚含量的高低是评价茶饮料质量的一个主要指标。茶多酚含量的测定方法主要有氧化还原滴定法[4]、可见分光光度法[5-7]、差示分光光度法[8]、三波长分光光度法[9]、重氮化-偶合分光光度法[10]紫外分光光度法[11]、流动注射法[12-14]、离子电极法[15]、电化学法[16]、原子吸收法[17]、高效液相色谱法[18]等。根据茶饮料的组成特点,本实验采用高聚物水溶液对茶饮料中的茶多酚进行了定量萃取,并利用分光光度法对茶多酚含量进行了定量测定,取得了较满意的结果。
1 材料与方法
1.1 材料与仪器
没食子酸丙酯 国药集团化学试剂有限公司;三羟甲基氨基甲烷 珠海市华成达化工有限公司;酒石酸钾钠 天津市大茂化学试剂厂;硫酸亚铁 天津市致远化学试剂有限公司;聚乙二醇-4000 国药集团化学试剂有限公司;硫酸铵 天津市大茂化学试剂厂;所有实验用水 均为去离子水;试剂 均为分析纯;劲凉冰红茶、柠檬茶、绿茶、冰醇茉莉、冰红茶 市售。
UV-2550紫外可见分光光度计 日本岛津制作所;精密pH计 广州广一科学仪器有限公司;分析天平 上海济成分析仪器有限公司;DT100电子天平常熟市双杰测试仪器厂。
1.2 实验方法
1.2.1 溶液的配制 没食子酸丙酯标准储备液:准确称取0.250g没食子酸丙酯,用水溶解后定容至250mL,其浓度为4.71mmol·L-1,实验时稀释至0.471mmol·L-1;酒石酸亚铁溶液:称取七水合硫酸亚铁0.1g,四水合酒石酸钾钠0.5g,溶于水并稀释至100mL(避光,现配现用);300g·L-1的聚乙二醇-4000溶液:称取150g聚乙二醇-4000,溶解、稀释至500mL,移至棕色瓶避光保存;0.2mol·L-1三羟甲基氨基甲烷溶液:称取4.8g三羟甲基氨基甲烷,加水溶解至200mL,实验时,调至所需pH。
1.2.2 吸收曲线的绘制 准确移取10.00mL 0.471mmol·L-1的没食子酸丙酯标准溶液置于60mL的分液漏斗中,加入5.0mL 300g·L-1聚乙二醇-4000,摇匀后加入4.0g(NH4)2SO4固体,振荡2min,静置。待两相分层清楚后,弃去下层水相,将上层高聚物相转移至25mL容量瓶中,润洗分液漏斗3次,洗液并入容量瓶中。加入5.0mL pH8.0三羟甲基氨基甲烷缓冲溶液,5.0mL酒石酸亚铁溶液,定容,摇匀。10min后,以未加没食子酸丙酯的高聚物萃取相的试剂空白为参比溶液,400~800nm范围进行波长扫描,绘制吸收曲线。
1.2.3 缓冲溶液的选择 准确移取10.00mL 0.471mmol·L-1没食子酸丙酯标准溶液于4个分液漏斗中,按照“1.2.2”操作萃取分离。分别加入pH8.0的磷酸盐缓冲溶液、硼砂缓冲溶液、三乙醇胺缓冲溶液、三羟甲基氨基甲烷缓冲溶液,5.0mL酒石酸亚铁溶液,定容,摇匀。
1.2.4 缓冲溶液的pH的影响 准确移取10.00mL 0.471mmol·L-1没食子酸丙酯标准溶液于8个分液漏斗中,按照“1.2.2”操作萃取分离。分别加入5.0mL pH为7.0、7.5、8.0、8.5、9.0的三羟甲基氨基甲烷缓冲溶液,5.0mL酒石酸亚铁溶液,定容,摇匀。分别以pH为7.0、8.0、8.5、9.0的未加没食子酸丙酯的高聚物萃取相的试剂空白为参比溶液,在518nm测定其吸光度值。
1.2.5 缓冲溶液用量的影响 准确移取10.00mL 0.471mmol·L-1没食子酸丙酯标准溶液于分液漏斗中,按照“1.2.2”操作萃取分离后,分别加入pH8.0的三羟甲基氨基甲烷缓冲溶液0.5、1.0、2.0、3.0、5.0、7.0、9.0mL,酒石酸亚铁溶液5.0mL,定容,摇匀。在518nm分别测定其吸光度。
1.2.6 显色液用量的影响 准确移取0.471mmol·L-1没食子酸丙酯标准溶液10.00mL,按照“1.2.2”操作萃取分离。加入pH8.0的三羟甲基氨基甲烷缓冲溶液2.0mL,分别加入酒石酸亚铁溶液1.0、2.0、3.0、4.0、5.0、7.0、9.0mL,定容,摇匀。以未加没食子酸丙酯的高聚物萃取相的试剂空白为参比溶液,在518nm分别测定其吸光度。
1.2.7 显色时间的确定 准确移取0.471mmol·L-1的没食子酸丙酯标准溶液10.00mL,按照“1.2.2”操作萃取分离。加入酒石酸亚铁溶液3.0mL,pH8.0的三羟甲基氨基甲烷缓冲溶液2.0mL,定容,摇匀。以未加没食子酸丙酯的高聚物萃取相的试剂空白为参比溶液,在518nm测定显色时间为2、5、7.5、10、15、20、25min时溶液的吸光度。
1.2.8 萃取率的测定 为了解聚乙二醇-4000对茶饮料中茶多酚的萃取效率,移取茶饮料5.00mL于60mL分液漏斗中,加入300g·L-1聚乙二醇-4000溶液5.0mL,摇匀后加入4.0g(NH4)2SO4固体,振荡2min,静置。待两相分层后,将萃余水相转移至25mL容量瓶中,加入pH8.0的三羟甲基氨基甲烷缓冲溶液2.0mL,酒石酸亚铁溶液3.0mL,定容,摇匀。10min后,以未加茶饮料的萃余水相的试剂空白为参比溶液,在400~800nm范围扫描其吸收曲线。
1.2.9 标准曲线的绘制 分别准确移取不同体积的0.471mmol·L-1没食子酸丙酯标准溶液于60mL的分液漏斗中,加水至约10mL,加入5.0mL 300g·L-1聚乙二醇-4000,摇匀后加入4.0g(NH4)2SO4固体,振荡2min,静置。待两相分层清楚后,弃去下层水相,将上层高聚物相转移至25mL容量瓶中,润洗分液漏斗3次,洗液并入容量瓶中,加入pH8.0的三羟甲基氨基甲烷缓冲液2.0mL,酒石酸亚铁溶液3.0mL,定容,摇匀,配制成没食子酸丙酯系列标准显色溶液。10min后,用1cm比色皿,以未加没食子酸丙酯的高聚物萃取相的试剂空白作为参比,在518nm处测定吸光度,绘制吸收曲线。
1.2.10 样品的测定 准确移取4.00mL待测样品液于60mL分液漏斗中,按“1.2.2”步骤操作萃取分离。加入pH8.0的三羟甲基氨基甲烷缓冲液2.0mL,酒石酸亚铁溶液3.0mL,定容,摇匀,在518nm处测定吸光度。代入线性方程,计算溶液中茶多酚的浓度,并求出样品中茶多酚的含量。
1.2.11 茶多酚质量浓度的计算 换算公式如下:

式中,C为根据溶液吸光度测得样品中茶多酚的物质的量浓度;V为样品体积(1升),M没食子酸丙酯为没食子酸丙酯的摩尔质量;1.5为换算因子。
2 结果与讨论
2.1 测定条件的确定
2.1.1 测定波长的确定 由吸收曲线可知,在pH8.0的三羟甲基氨基甲烷溶液中,没食子酸丙酯与酒石酸亚铁形成的络合物在518nm处有最大吸收,故选择518nm为实验的测定波长。

图1 吸收曲线Fig.1 Absorption curve
2.1.2 缓冲溶液的确定 磷酸盐、硼砂会使有机相产生浑浊,对检测不利;三乙醇胺能与没食子酸丙酯产生颜色反应,生成桃红色物质,对实验的检测产生影响;三羟甲基氨基甲烷无任何肉眼可见的不良现象,故选择其为缓冲溶液。

图2 缓冲溶液pH影响Fig.2 Effect of pH of the buffer solutions
2.1.3 缓冲溶液的pH及其用量确定 酸度对显色反应的影响很大,溶液酸度直接影响着金属离子、显色剂的存在形式和有色络合物的组成、稳定性等。很多显色剂本身就是酸碱指示剂,酸度不同时,它们的颜色不同,可能造成显示剂颜色与络合物的颜色相近而影响测定。由图2可知,在其他条件相同的情况下,没食子酸丙酯与酒石酸亚铁形成的络合物在pH7.5~8.5时吸光度最大,故实验选择三羟甲基氨基甲烷溶液pH为8.0。由图3可知,在实验条件下,三甲羟基甲氨基烷溶液用量在1mL以上时,溶液的吸光度基本不变,为保证溶液有足够的缓冲能力,实验选择三羟甲基氨基甲烷缓冲溶液用量为2.0mL。

图3 缓冲溶液用量的影响Fig.3 Effect of the buffer solutions
2.1.4 显色剂用量及显色时间的确定 为保证显色反应进行完全,加入过量的显色剂是必要的,但过多的显色剂不仅会造成试剂的浪费,还可能影响显色效果。由图4可知,加入酒石酸亚铁溶液在2.0~3.5mL时,溶液的吸光度最大,实验选择酒石酸亚铁溶液用量为3.0mL。在显色反应中,时间包括两个含义,显色时间和稳定时间,显示时间太短显色反应可能不完全,显示时间太长造成实验用时延长。由图5可知,本实验显色时间8min以后,溶液的吸光度基本稳定不变,实验选择显示反应时间10min。

图4 显色剂用量的影响Fig.4 Effect of color reagent

图5 显色时间的影响Fig.5 Effect of color reaction times
2.2 萃取率的测定
实验重要环节之一是将茶饮料中的茶多酚萃取至高聚物相,萃取效率的高低对测定结果有很大的影响,通过在萃余水相加入pH8.0三羟甲基氨基甲烷缓冲溶液和酒石酸亚铁溶液后,观察其显色情况,若萃余水相中含有茶多酚,酒石酸亚铁将与茶多酚发生显色反应,在测定波长下产生吸收,萃余水相中茶多酚含量越高吸收越大,利用萃余水相的吸收曲线可判断萃取效率的高低。由图6可知,茶饮料的萃余水相中加入酒石酸亚铁,在400~700nm波长范围没有吸收,说明茶饮料中的茶多酚已全部转移至聚乙二醇-4000相。
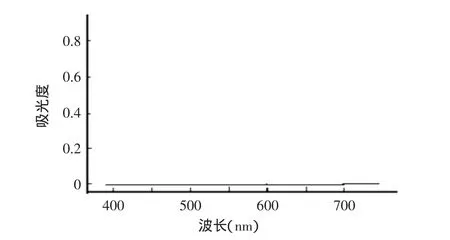
图6 萃余水相的吸收曲线Fig.6 Absorption curve of aqueous phase
2.3 标准曲线的绘制
测定出系列标准溶液的吸光度,以吸光度A为纵坐标,没食子酸丙酯的浓度C(mmol·L-1)为横坐标绘制标准曲线,见图7,其线性方程为:A=3.1106C-0.0056,R2=0.9999。进一步实验,没食子酸丙酯在0.004~0.4mmol·L-1浓度范围内,具有良好的线性关系。
2.4 样品测定及精密度实验
对市场上销售的5种茶饮料,按“1.2.10”方法平行测定5次,测定结果见表1。
相对标准偏差数据显示,该方法测定的数据具有较高的精密度,RSD范围为1.0%~3.2%。

表1 样品测定及精密度实验(n=5)Table 1 Determination of the samples and test of precision(n=5)

表2 样品回收率实验(n=5)Table 2 Rate of recovery results(n=5)
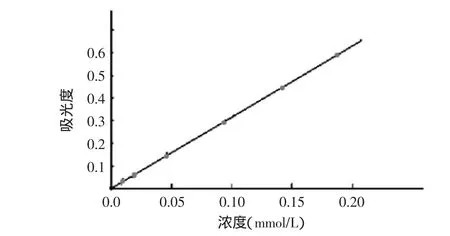
图7 标准曲线Fig.7 Standard curve
2.5 回收实验
分别准确移取劲凉冰红茶和冰醇茉莉4.00mL各5份于60mL的分液漏斗中,加入一定量没食子酸丙酯标准溶液,加水至10mL,按“1.2.10”操作,测定吸光度,作加标回收实验,其回收率在92.4%~103.5%,说明方法具有较高的准确度。结果见表2。
3 结论
实验证明,利用水溶性高聚物可将茶饮料中的茶多酚全部转移至聚乙二醇-4000相中,达到了从茶饮料中定量提取茶多酚,减少茶饮料中其他成分对茶多酚测定干扰的目的。在pH8.0的三羟甲基氨基甲烷缓冲液中,以酒石酸亚铁为显色剂,利用分光光度法实现了对茶饮料中茶多酚含量的定量测定。该方法操作简单方便,方法可靠,准确度较高,且使用的萃取剂无毒、不挥发,避免了使用有机溶剂为萃取剂进行操作时对实验者身心健康的伤害,为茶饮料中茶多酚的定量测定提供了较理想的分析方法。
[1]李淑娟.茶多酚的保健和药理作用研究进展[J].西北药学杂志,2010,25:78-79.
[2]陈铃容.茶多酚的结构特性及开发前景[J].茶叶科学技术,2005(2):21.
[3]孙秋香,肖婷.茶叶中茶多酚的提取测定及应用[J].湖北第二师范学院学报,2009,26(8):47-49.
[4]袁勇,张素芳,双少敏,等.邻二氮菲亚铁指示剂法测定叶中茶多酚的含量[J].食品科学,2008,29(3):403-405.
[5]王红菊,张欣,姜立芬,等.市场茶饮料中茶多酚含量的测定与分析[J].呼伦贝尔学院学报,2010,22(5):80-82.
[6]廖晓玲,朗惠云,徐文峰,等.钼酸铵分光光度法测定茶多酚含量[J].分析实验室,2003,25(2):70-72.
[7]张素芳,袁勇,双少敏,等.重铬酸钾可见分光光度法测定绿茶中茶多酚总量的研究[J].食品科学,2009,30(2):208-220.
[8]郎惠云,廖晓玲,杜月琴.示差分光光度法测定茶多酚的含量[J].分析科学学报,2003,19(2):151-153.
[9]回瑞华,侯冬岩,关崇新,等.三波长分光光度法测定沱茶中茶多酚的含量[J].分析测试学报,2003,22(6):60-63.
[10]李楠,秦学孔,彭辉.茶多酚含量重氮化-偶合分光光度法测定[J].大连理工大学学报,2007,40(4):425-427.
[11]黄海燕,彭飞.紫外分光光度法测定减肥茶中茶多酚的含量[J].西北医学杂志,2010,25(6):410-411.
[12]衷明华.茶多酚的流动注射-共振光散射法测定 [J].食品科学,2009,30(10):219-221.
[13]米娟,王九春,马永钧,等.流动注射化学发光法测定茶叶中的茶多酚[J].宁夏大学学报,2011,32(2):168-171.
[14]谷素英,黎源倩,邹晓莉.流动注射-二极管阵列检测分光光度法测定茶多酚[J].现代预防医学,2006,33(2):195-197.
[15]王晓岗,李静,樊雅娟.聚天冬氨酸膜修饰电极测定茶饮料中茶多酚[J].化学世界,2010,52(2):80-83.
[16]朱丹,须海荣.电化学法快速测定茶多酚含量的研究[J].茶叶科学,2011,31(3):179-186.
[17]王吉德,田笠卿,王连生.原子吸收法在有机分析中的应用(Ⅲ)-茶叶中茶多酚的测定[J].高等学校化学学报,1995,16(4):536-539.
[18]侯冬岩,回瑞华,李铁纯.高效液相色谱法对绿茶中茶多酚含量的测定[J].食品科学,2010,31(24):305-307.
