光学相干断层成像方法评价冠状动脉介入治疗术后即刻药物洗脱支架贴壁情况
2013-04-20刘小宁杨跃进吴永健颜红兵陈珏袁晋青钱杰邱洪杨伟宪俞梦越慕朝伟高展唐熠达王天杰徐波许亮孙中伟谢丽华宁宇
刘小宁,杨跃进,吴永健,颜红兵,陈珏,袁晋青,钱杰,邱洪,杨伟宪,俞梦越,慕朝伟,高展,唐熠达,王天杰,徐波,许亮,孙中伟,谢丽华,宁宇
光学相干断层成像方法评价冠状动脉介入治疗术后即刻药物洗脱支架贴壁情况
刘小宁,杨跃进,吴永健,颜红兵,陈珏,袁晋青,钱杰,邱洪,杨伟宪,俞梦越,慕朝伟,高展,唐熠达,王天杰,徐波,许亮,孙中伟,谢丽华,宁宇
目的:评价急性 ST 段抬高型心肌梗死(STEMI)直接经皮冠状动脉介入(PCI)治疗与不稳定性心绞痛(UAP)和稳定性心绞痛(SAP)择期 PCI治疗术后即刻药物洗脱支架(DES)贴壁情况。
心肌梗死;光学相干断层成像;支架贴壁不良
(Chinese Circulation Journal, 2013,28: 356.)
经皮冠状动脉(冠脉)介入治疗(PCI)已成为冠心病血管重建的主要方法之一。临床研究显示药物洗脱支架(DES)与裸金属支架(BMS)相比,可以明显降低内膜增生、支架内再狭窄发生率[1]。然而无论是 BMS还是DES都存在发生支架内血栓的可能。有研究显示急性 ST 段抬高型心肌梗死(STEMI)患者直接PCI后 6个月时支架贴壁不良及内膜覆盖延迟发生率高于稳定性心绞痛(SAP)及不稳定性心绞痛(UAP)患者[2],而支架贴壁不良及内膜覆盖延迟有可能会增加支架内血栓风险[3,4]。另有研究显示随访至术后 10 个月时光学相干断层成像(OCT)评价 DES晚期支架贴壁不良的主要来源为术后即刻贴壁不良持续存在[5]。因此如何减少术后即刻支架贴壁不良的发生仍需重视。本研究应用OCT对冠脉造影显示成功的 STEMI直接 PCI及 UAP、SAP 择期 PCI术后即刻支架贴壁情况进行评价,以指导临床。
1 资料和方法
研究对象: 2009-06 至 2010-06 在我院接受 PCI治疗并行术前、术后 OCT 检查的 50例患者。术前患者均已签署知情同意书。置入 DES包括:西罗莫司洗脱支架(Cordis,USA,Cypher Select,sirolimuseluting stent,SES),佐他莫司洗脱支架(Medtronic,USA,Endeavor,zotarolimus-eluting stent,ZES)。50例患者中 STEMI 18 例(STEMI 组 ),UAP 16 例(UAP组),SAP 16 例(SAP 组)。排除标准:肾功能不全(血肌酐≥ 2.5 mg/dl),严重心功能不全(左心室射血分数 <30%),无保护左主干病变,严重钙化病变,严重迂曲病变及累及大分支开口病变,存在抗血小板治疗禁忌症等。
冠脉造影及 PCI:所有患者介入治疗前均至少服用阿司匹林(300 mg)及氯吡格雷(300 mg 负荷量)。经桡动脉或股动脉途径完成冠脉造影,以标准技术进行冠脉内支架置入术。支架术成功包括术后无明显残余狭窄(<30%),心肌梗死溶栓治疗临床试验(TIMI)血流 3 级,住院期间无严重心脏不良事件(MACE,包括:心原性死亡、心肌梗死及靶血管再次血运重建 )。定量冠脉造影分析通过 QAngio XA Version 7.2(Medis Medical Imaging System Inc.,Leiden,Netherlands)软件测量。
OCT 检查过程:本研究所使用的为时域 OCT,M2系统(美国乐普公司)。成像导丝回撤速度设定为 2.0mm/s,扫描频率 20 帧 /s。支架术前、术后常规送入OCT导管至冠脉内。阻塞导管位于支架近端,成像导管位于支架远端。成像过程中阻断球囊膨胀到 0.4 ~ 0.6atm,乳酸林格氏液以 1.5 ml/s 的速度注入,成像导丝由远及近自动回撤连续记录图像以便进行分析。
OCT 图像分析:首先对所有 OCT 图像进行校正[6]。每隔约 0.5 mm(5 帧)选取一幅 OCT 图像横断面进行分析,通过软件 QIVUS 2.1 Bate Version with OCT Module(Medis Medical Imaging System Inc.,Leiden,Netherlands)处理。本研究排除分支节段和重叠支架节段,共选取 3 537帧图像,其中 283 帧(8.00%)由于图像质量差未能处理。图像测量内容包括:血管管腔面积、支架内面积、支架丝数目及贴壁距离等。支架贴壁不良定义为支架丝与血管内壁分离,即测量支架丝表面中点至血管壁的垂直距离大于支架丝厚度加 OCT分辨率(SES>160 μm,ZES>110 μm)[7]。
统计学分析:计量资料用均数±标准差表示,组间比较采用单因素方差分析;计数资料用百分比表示,组间比较采用卡方检验,小概率事件组间比较采用确切概率计算法。P<0.05 认为差异有统计学意义。所有分析均以 SPSS16.0 软件包进行。
2 结果
基线特点:三组患者年龄、性别、体重指数、吸烟史、左心室射血分数及合并高血压病、高脂血症、2型糖尿病、既往心肌梗死病史等基线资料间差异均无统计学意义(P均 >0.05)。
冠脉造影及介入结果分析:STEMI组 C 型病变比例多于 UAP 和 SAP 组,且均为闭塞病变,差异有统计学意义(P均 <0.01)。STEMI组预扩张比例多于 SAP 组,总后扩张比例少于 UAP 和 SAP 组,差异有统计学意义(P均 <0.05)。余指标三组间差异无统计学意义(P均 >0.05)。表1

表1 冠状动脉造影及介入结果资料(±s)
三组患者支架置入前、后OCT测量管腔定量资料见表2。UAP 组与 SAP 组支架前最小管腔面积大于 STEMI组,管腔狭窄程度小于 STEMI组 (P<0.001),UAP 组支架前管腔狭窄程度大于 SAP 组,差异均有统计学意义(P<0.01)。
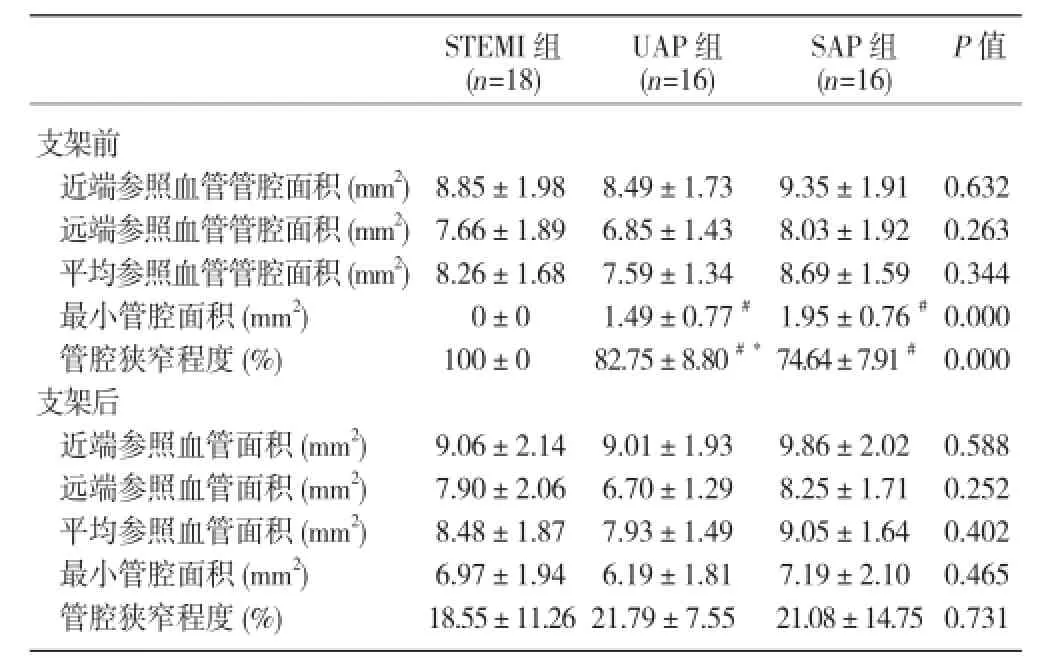
表2 三组患者光学相干断层成像测量冠状动脉定量资料(±s)
OCT评价支架丝贴壁情况:本研究分析支架丝总 数 为 30 093 个,其中 STEMI 组 12 005 个,UAP组 10 150 个,SAP 组 7 938 个。 术 后 即 刻 支 架 丝总贴 壁不良发 生率为(7.78±4.11)%,三组间差异有统计学意义 [STEMI组(9.13±3.34)%,UAP 组(8.52±4.79)%,SAP 组(5.52±3.78)%,P<0.05],STEMI组高于 SAP 组,差异有统计学意义(P<0.05),UAP 组与 STEMI组和 UAP 组与 SAP 组间差异均无 统 计学 意 义(P 均 >0.05)。SES 术后 即 刻支 架丝 贴 壁 不 良 发 生 率 高 于 ZES [(9.91±4.01)% vs(4.81±3.33)%,P<0.05)]。
回归分析:将上述单因素分析中对术后即刻贴壁不良有影响的支架种类、临床诊断两个因素带入行多元线性回归分析,结果显示 SES(β 系数 7.4%,95%CI:5.2%~9.6%,P<0.001)、STEMI(β 系数 6.7%,95%CI:4.2%~9.2%,P<0.001)、UAP(β 系数 3.4%,95%CI:0.8%~6.1%,P<0.05),差异均有统计学意义,为贴壁不良发生的危险因素。
3 讨论
据我们所知,目前尚未有研究应用 OCT 比较STEMI行直接 PCI与 UAP、SAP 择期 PCI术后即刻支架丝贴壁情况。本研究初步表明 STEMI直接 PCI术后即刻 DES 贴壁不良率高于 SAP,SES 术后即刻贴壁不良率高于 ZES。
本研究术后即刻支架丝总贴壁不良率为(7.78±4.11)%,其中 STEMI占 36%,UAP 占 32%,SAP 占 32%。Tanigawa 等[7]报 道 OCT 测 量术后 即刻DES 贴壁不良率为(9.1±7.4)%,其中急性冠脉综合征 占 44%,SAP 占 56%。Ozaki等[5]报 道 OCT 测 量术后即刻 SES 贴壁不良率为 7.15%,其中 NSTEMI占28.1%,UAP 占 15.6%,SAP 占 56.3%。 因 入 选 样 本间差异,无法对上述测量结果详细比较,但本研究与文献中术后即刻贴壁不良率无明显偏差。
本研究显示 STEMI术后即刻贴壁不良率高于SAP,而 UAP 与 SAP 比较有升高趋势但组间差异无统计学意义。这可能与病变部位的管腔重构有一定关系,有研究[8,9]显示急性冠脉综合征病变部位冠脉多为正性重构,SAP多为负性重构,且急性心肌梗死正性重构程度大于 UAP。此外,Kim 等[10]应用IVUS 的相关研究发现,冠脉内血栓为 DES 术后即刻支架贴壁不良的危险因素,这与大量的冠脉内血栓影响支架丝贴壁有关。本研究显示 SES 较 ZES 术后即刻贴壁不良发生率高。既往应用 OCT 和 IVUS的研究均有报道 SES 是 DES 术后即刻贴壁不良的危险因素[7,10,11]。与本研究结果相符。原因可能与支架设计有关,SES 支架丝厚度厚且为闭环结构,致使其顺应性差,术后即刻贴壁不良发生率较高。
既往应用 IVUS 的研究有结果表明晚期贴壁不良(术后 6~8 个月)主要来源于术后即刻贴壁不良持续存在[12,13],但亦有研究结果与此相反,显示晚期贴 壁不 良主要 来源 于晚期 获得 性贴壁 不良[14,15]。Ozaki等[5]对 32 例 置 入 SES 患 者 应 用 OCT 测 量 术后即刻支架丝贴壁不良发生率为 7.15%,随访 10 个月后复查 OCT,其中持续型贴壁不良为 4.67%,而晚期获得性贴壁不良为 0.37%,表明持续型贴壁不良为晚期贴壁不良的主要来源,且伴有贴壁不良和新生内膜覆盖不全的支架丝血栓发现率明显升高。这可能与 OCT 分辨率较 IVUS 提高有关[16],并提示术后即刻贴壁不良需引起重视,其转归仍需大样本量研究的进一步观察。
张 燕 等[17]通 过 回 顾 性 分 析 证 实 急 性 心 肌 梗死是急性、亚急性支架内血栓形成的危险因素。Nakazawa 等[18]通 过尸 检证 实,急 性心 肌梗 死患 者置入 DES后较 SAP 患者晚期支架内血栓形成发生率高(41% 比 11%,P=0.04)。因此急性心肌梗死本身即为预后不良的危险因素,除却急性心肌梗死患者较非心梗患者心功能差及病变血管局部炎症反应重等因素外,其中是否存在术后即刻支架丝贴壁不良发生率高对预后的影响目前未有定论。支架贴壁不良与支架内血栓可能相关的主要机制包括:①支架贴壁不良导致局部管腔延迟内皮化,支架外血管的慢性炎症,损伤血管的舒缩活性,引起血小板粘附,引发血栓形成;②支架与邻近管壁间形成腔隙,其间血流缓慢,局部血流动力学异常,有利于纤维蛋白与血小板沉积;③由于局部血流动力学异常所致管壁所受切应力差异或(和)局部炎症,导致局部斑块破裂受损,形成血栓。因此DES术后即刻贴壁不良是否增加支架内血栓的潜在风险仍需大量的临床病例的长期随访观察。
[1]Lemos PA, Lee CH, Degertekin M, et al. Early outcome after sirolimus-eluting stent implantation in patients with acute coronary syndromes: insights from the Rapamycin-Eluting Stent Evaluated At Rotterdam Cardiology Hospital(RESEARCH) registry. J Am Coll Cardiol, 2003, 41: 2093-2099.
[2]Gonzalo N, Barlis P, Serruys PW, et al. Incomplete stent apposition and delayed tissue coverage are more frequent in drug-eluting stents implanted during primary percutaneous coronary intervention for STSegment Elevation myocardial infarction than in drug-eluting stents implanted for stable/unstable angina. J Am Coll Cardiol Intv, 2009, 2: 445-452.
[3]Cook S, Wenaweser P, Togni M, et al. Incomplete stent apposition and very late stent thrombosis after drug-eluting stent implantation. Circulation, 2007, 115: 2426-2434.
[4]Finn AV, Joner M, Nakazawa G, et al. Pathological correlates of late drug-eluting stent thrombosis: strut coverage as a marker of endothelialization. Circulation, 2007, 115: 2435-2441.
[5]Ozaki Y, Okumura M, Ismail TF, et al. The fate of incomplete stent apposition with drug-eluting stents: an optical coherence tomographybased natural history study. European Heart Journal, 2010, 31: 1470-1476.
[6]Tanigawa J, Barlis P, Di Mario C, et al. Intravascular optical coherence tomography: optimization of image acquisition and quantitative assessment of stent strut apposition. EuroIntervention, 2007, 3: 128-136.
[7]Tanigawa J, Barlis P, Dimopoulos K, et al. The influence of strut thickness and cell design on immediate apposition of drug-eluting stents assessed by optical coherence tomography. Int J Cardiol, 2009, 134: 180-188.
[8]Nakamura M, Nishikawa H, Mukai S, et al. Impact of coronary artery remodeling on clinical presentation of coronary artery disease: An intravascular ultrasound study. J Am Coll Cardiol, 2001, 37: 63-69.
[9]Schoenhagen P, Ziada KM, Kapadia SR. Extent and direction of arterial remodeling in stable versus unstable coronary syndromes: An intravascular ultrasound study. Circulation, 2000, 101: 598-603.
[10]Kim YS , Koo BK, Seo JB, et al. The Incidence and predictors of postprocedural incomplete stent apposition after angiographically successful drug-eluting stent implantation. Catheterization and Cardiovascular Interventions, 2009, 74: 58-63.
[11]Tanigawa J, Barlis P, Kaplan S, et al. Stent strut apposition in complex lesion using optical coherence tomography. Am J Cardiol, 2006, 98(Suppl 1): 97M.
[12]Kimura M, Mintz GS, Carlier S, et al. Outcome after acute incomplete sirolimus-eluting stent apposition as assessed by serial intravascular ultrasound . Am J Cardiol, 2006, 98: 436-442.
[13]Ako J, Morino Y, Honda Y, et al. Late incomplete stent apposition after sirolimus-eluting stent implantation a serial intravascular ultrasound analysis. J Am Coll Cardiol, 2005, 46: 1002-1005.
[14]Siqueira DA, Abizaid AA, Costa JR, et al. Late incomplete apposition after drug-eluting stent implantation: incidence and potential for adverse clinical outcomes. European Heart Journal, 2007, 28: 1304-1309.
[15]Tanabe K, Serruys PW, Degertekin M, et al. Incomplete stent apposition after implantation of paclitaxel-eluting stents or bare metal stents insights from the randomized TAXUS II trial. Circulation, 2005, 111: 900-905.
[16]王天杰 , 赵杰 , 杨跃进 . 冠状动脉内光学相干断层成像技术的临床应用 . 中国循环杂志 , 2011, 26: 72-73.
[17]张燕 , 任艺虹 , 周超飞 , 等 . 经皮冠状动脉介入治疗术后急性、亚急性支架内血栓形成的危险因素分析 . 中国循环杂志 , 2013, 28: 17-20.
[18]Nakazawa G, Finn AV, Joner M, et al. Delayed arterial healing and increased late stent thrombosis at culprit sites after drug-eluting stent placement for acute myocardial infarction patients an autopsy study . Circulation, 2008, 118: 1138-1145.
Assessment for Immediate Stent Apposition of Drug-Eluting Stents After Percutaneous Coronary Intervention by Optical Coherence Tomography
LIU Xiao-ning, YANG Yue-jin, WU Yong-jian, YAN Hong-bing, CHEN Jue, YUAN Jin-qing, QIAN Jie, QIU Hong, YANG Wei-xian, YU Meng-yue, MU Chao-wei, GAO Zhan, TANG Yi-da, WANG Tian-jie, XU Bo, XU Liang, SUN Zhong-wei, XIE Li-hua, NING Yu.
Department of Cardiology, Cardiovascular Institute and Fu Wai Hospital, CAMS and PUMC, Beijing (100037), China
YANG Yue-jin, Email: yangyjfw@yahoo.com.cn
Objective: To assess the immediate incomplete stent apposition (ISA) of drug-eluting stents in patients with ST-segment elevation myocardial infarction (STEMI), unstable angina pectoris (UAP) and stable angina pectoris (SAP) after percutaneous coronary intervention (PCI) by optical coherence tomography (OCT).Methods: We retrospectively analyzed 50 patients with PCI treatment in our hospital from June 2009 to June 2010. The patients were divided into 3 groups, STEMI group, n=18, the patients received primary PCI, UAP group, n=16, the patients received elective PCI and SAP group, n=16. Pre- and post-PCI OCT were respectively conducted in all patients and ISA was compared among different groups; the effects of sirolimus-eluting stent (SES) and zotarolimus-eluting stent (ZES) on ISA were also compared.Results: The overall ISA occurrence rate was (7.78±4.11)%, and the ISA in STEMI group, UAP group and SAP groupwere (9.13 ± 3.34)%, (8.52±4.79)% and (5.52±3.78)% respectively. The ISA rate in STEMI group > SAP group, P<0.05 and the ISA between STEMI group and UAP group was similar, P>0.05. The ISA occurrence rate in SES (9.91±4.01)% > ZES (4.81±3.33)%, P<0.05. Multi regression analysis indicated that SES (β:7.4%,95%CI: 5.2%-9.6%, P<0.001), STEMI (β: 6.7%,95%CI:4.2%-9.2%,P<0.001) and UAP (β: 3.4%, 95%CI:0.8%-6.1%,P<0.05) were the predictors of ISA.Conclusion: The ISA occurrence rate in patients with STEMI was higher than that in SAP; and ISA rate in SES was more than that in ZES.
Myocardial infarction; Optical coherence tomography; Incomplete stent apposition
2013-07-04)
(编辑:汪碧蓉)
100037 北京市,中国医学科学院 北京协和医学院 心血管病研究所 阜外心血管病医院 冠心病诊治中心(刘小宁、杨跃进、吴永健、颜红兵、陈珏、袁晋青、钱杰、邱洪、杨伟宪、俞梦越、慕朝伟、高展、唐熠达、王天杰),介入治疗中心(徐波、许亮、孙中伟、谢丽华、宁宇)
刘小宁 主治医师 博士研究生 主要从事冠心病诊治研究 Email:ning_christina@126.com 通讯作者:杨跃进 Email:yangyjfw@yahoo.com.cn
R54
A
1000-3614(2013)05-0356-04
10.3969/j.issn.1000-3614.2013.05.011
方法:回顾性分析 2009-06 至 2010-06 介入治疗前、后均行光学相干断层成像(OCT)检查的 50 例患者资料,其中 STEMI 行直接 PCI治疗者 18 例(STEMI组 ),择期 PCI 治疗的 UAP16 例(UAP 组)、SAP 16 例(SAP 组 ),评价术后即刻支架贴壁情况。比较西罗莫司洗脱支架(SES)和佐他莫司洗脱支架(ZES)对术后即刻贴壁不良的影响。
结 果:术 后 即 刻 支 架 丝 总 贴 壁 不 良 发 生 率 为(7.78±4.11)%, 其 中 STEMI 组(9.13±3.34)%,UAP 组(8.52±4.79)%,SAP 组(5.52±3.78)%,STEMI 组高于 SAP 组,差异有统计学意义(P<0.05),UAP 组与 STEMI 组和 SAP 组间差异均无统计学意义(P 均 >0.05)。SES 组术后即刻支架丝贴壁不良发生率高于 ZES 组 [(9.91±4.01)% vs( 4.81±3.33)%,P<0.05]。多元线性回归分析显示,SES(β 系数 7.4%,95%CI:5.2%~9.6%,P<0.001)、STEMI(β系数 6.7%,95%CI:4.2%~9.2%,P<0.001)、UAP(β 系数 3.4%,95%CI:0.8%~6.1%,P<0.05)为术后即刻支架丝贴壁不良的预测因素。
结论:本研究初步表明 , STEMI 术后即刻贴壁不良发生率高于 SAP,SES 术后即刻贴壁不良发生率高于 ZES。其相关因素有待于进一步探讨。
