药物洗脱支架置入术后支架内再狭窄的血管内超声观察
2013-04-20王天松冯旭霞姚震
王天松,冯旭霞,姚震
药物洗脱支架置入术后支架内再狭窄的血管内超声观察
王天松,冯旭霞,姚震
目的:通过药物洗脱支架(DES)置入术后支架内再狭窄的血管内超声观察,探讨斑块成分及其形成原因。
冠状动脉疾病;药物洗脱支架;冠状动脉再狭窄;血管内超声
(Chinese Circulation Journal, 2013,28: 348.)
药物洗脱支架 (DES)的应用使支架内再狭窄有所减少,但仍然有相当比例的存在。因此,再狭窄是一个持续存在尚未完全解决的问题,其发生机制和进展过程仍未完全阐明。本研究采用血管内超声虚拟组织学检查评价再狭窄病变,探讨支架内再狭窄的发生机制。
1 资料与方法
研究对象:对 2006-10 至 2012-12 我院 64 例 DES置入术后随访定量冠状动脉(冠脉)造影估测狭窄>50% 的患者进行血管内超声虚拟组织学检查。排除标准:血流动力学不稳定;狭窄过重或血管扭曲,血管内超声导管不能通过狭窄病变;左主干或静脉桥血管病变;急性心肌梗死。64例中4例因支架扩张不完全而非内膜增生导致的再狭窄被排除,最终纳入60例患者,其中稳定型冠心病 25 例(SCAD 组),非 ST 段抬高的急性冠脉综合征 35 例(NSTEACS 组)。2 组除术前肌钙蛋白 I峰值差异有统计学意义外(P< 0.05),其余一般临床特征均差异无统计学意义(P>0.05),见表1。本研究方案获得我院医学伦理委员会的批准并且符合世界医学协会联合国大会修订的赫尔辛基宣言的精神。

表1 2 组一般临床特征
手术方法与数据采集:冠状动脉造影后,选择狭窄程度最大的一帧图像应用定量冠状动脉造影技术测量狭窄程度。再狭窄定义为:血管直径狭窄>50%。分类[1]:I 型:病变长度≤ 10 mm,位于支架交界处未被支架覆盖、支架内、支架近远端边缘处、或上述各种情况的组合;II型:病变长度> 10 mm,不超出支架两端;III型:病变长度> 10 mm,并超出支架两端;IV 型:再狭窄造成完全闭塞,心肌梗死溶栓治疗临床试验(TIMI)血流 0 级。血管内超声检查前,先经指引导管向冠脉内注射 0.2 mg 硝酸甘油,再将带有 20-MHz 电子传感器的 2.9F Eagle Eye 血管内超声导管 (Volcano Corp, Rancho Cordova, CA)沿导丝送至狭窄远端参考血管,使用自动回撤装置以 0.5 mm/s的速度边回撤边扫描至支架近端参考血管。
血管内超声虚拟组织学分析:应用 Volcano 血管内超声仪检查支架近远端 5 mm 范围内的血管,每间隔 1 mm 测量 1 次。使用虚拟组织学软件分析支架内缘与管腔外缘之间各斑块成分的体积、比例:纤维组织显示为绿色,纤维脂肪组织为黄绿色,钙化成分为白色,坏死组织为红色。支架扩张不完全定义为:最小支架内面积 <5 mm2。薄层纤维帽硬化斑块(TCFA)定义为[2,3]:在管腔横截面斑块负荷大于 40%的血管段,连续3帧血管内超声虚拟组织学图像上融合的坏死核大于斑块面积的 10%,坏死核与管腔直接接触,表面没有纤维帽,钙化少于 10%。
统计分析:采用 SPSS 11.0 版统计软件。计量资料表示为中位数及四分位数间距;计数资料用频数(或百分位数)表示。计量资料的比较采用秩和检验,计数资料的比较采用 χ2检验。P<0.05(双侧)为差异有统计学意义。
2 结果
2 组随访时病变基本特征比较:与 NSTEACS 组比,SCAD 组除随访时间较短、TCFA 发生率较低、斑块体积较小、纤维脂肪组织比例较低、坏死组织比例较低、肌酸激酶MB同工酶水平较低,差异均有统计学意义外(均 P< 0.05),其它病变基本特征差异均无统计学意义(P>0.05)。表2
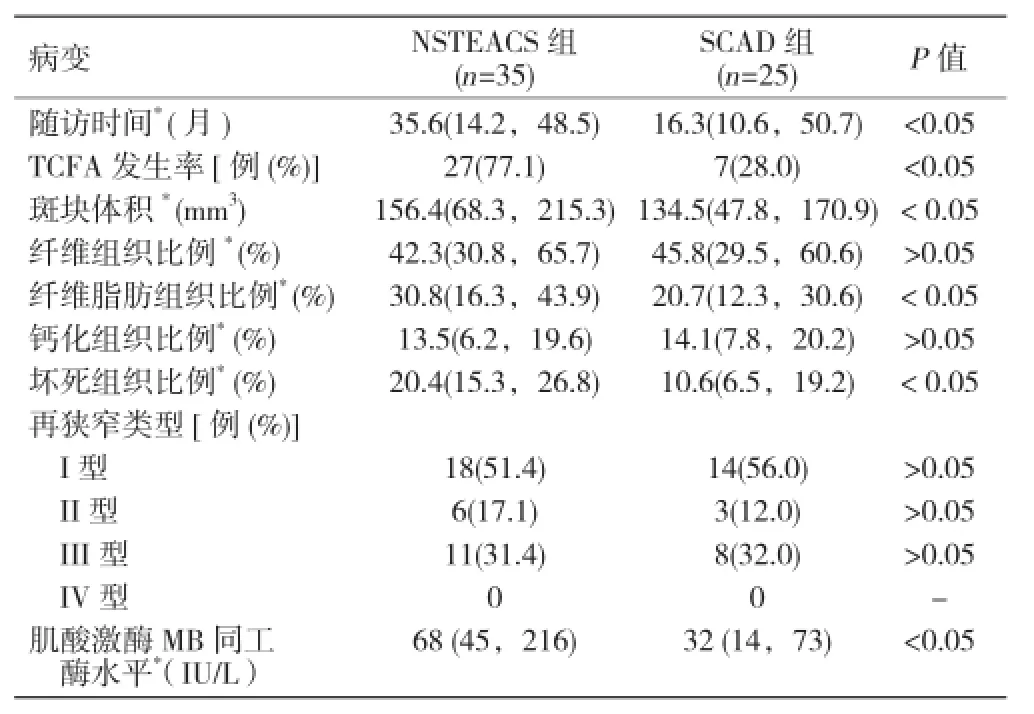
表2 2 组随访时病变基本特征比较
60例患者不同随访时间的病变基本特征比较:与随访时间 >20 个月比,随访时间 < 20 个月除TCFA 发生率较低、斑块体积较小、纤维脂肪组织比例较低、坏死组织比例较低,差异均有统计学意义外(均 P< 0.05),其它病变基本特征差异均无统计学意义(P>0.05)。表3
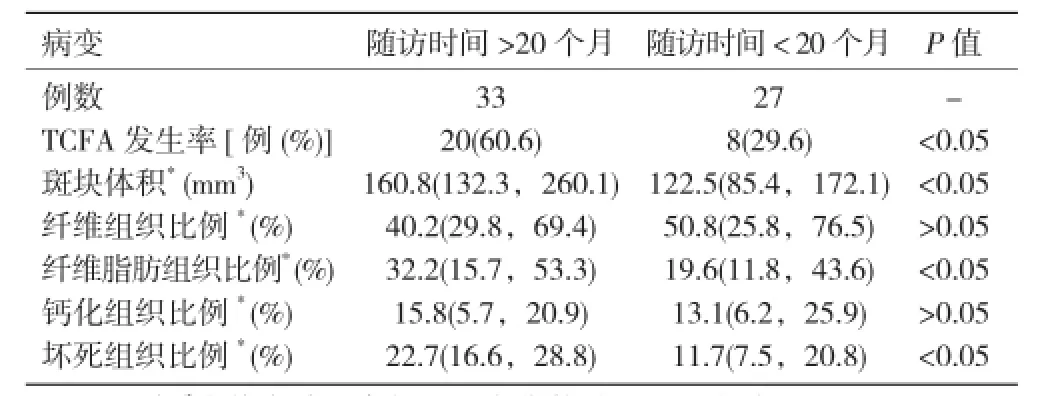
表3 60 例患者不同随访时间的病变基本特征比较
3 讨论
DES时代,支架内再狭窄仍然是一个重要的问题,尤其是在有糖尿病等高危因素存在时更加显著[4]。Kang 等[5]的研究认为,再狭窄的主要机制是血管内膜过度增生。但该研究应用的是灰阶血管内超声检查,因此并不能准确地从影像上区分内膜增生和新生粥样硬化斑块。本研究应用了血管内超声虚拟组织学技术,弥补了灰阶血管内超声的缺陷,结果发现再狭窄患者广泛存在支架内新生粥样硬化斑块现象,而且随访时间越长,新生粥样硬化斑块体积越大。这些发现对揭示 DES置入术后支架内再狭窄的机制有重要意义。DES术后支架内可形成新生粥样硬化斑块,这一现象表明,动脉粥样硬化的进程从未停止,从支架置入的那一刻开始,高血糖[6]、血脂异常、高血压、内皮功能障碍等因素促进动脉粥样硬化的作用与支架所携带药物的抑制增生作用就交织在一起,金属支架和聚合物涂层引起的炎症反应也参与其中。当药物不能有效抑制促动脉粥样硬化因素的效应时,新生粥样硬化斑块将逐渐形成,而且随时间不断进展,成为导致支架内再狭窄的重要机制之一。根据上述推论,解决再狭窄问题首先要更多了解促进动脉粥样硬化危险因素的种类及作用机制,寻找更加有效的治疗手段,对已知的危险因素应进行更加严格地控制;其次,应开发新型支架和涂层材料,以减少炎症反应;最后,应不断寻找更加有效的药物来提高 DES 的疗效,因为 Le 等[7]的研究已经提示部分患者存在针对紫杉醇等药物的抵抗现象。
DES术后晚期发生的急性冠脉综合征引起了越来越多地关注。对于其发生机制多数研究将焦点放在支架内皮化不全诱发晚期血栓形成方 面[8,9]。 然 而 本 研 究 发 现,DES 术 后 晚 期 大 部分 NSTEACS 患者可见支架内新生 TCFA。TCFA容易发生纤维帽破裂诱发血栓形成从而导致NSTEACS[10]。 因 此, 这 一 发 现 表 明 TCFA 的 形 成和破裂是 DES 术后发生 NSTEACS 的重要机制之一。此外,随访时间越长,TCFA 越多这一现象提示新生粥样硬化斑块在形成初期很可能只是慢性稳定性斑块,在某些因素作用下逐渐演变成了TCFA。上述发现对 DES 术后 NSTEACS 的防治具有指导意义。首先,术后晚期发生 NSTEACS 的患者,在病因方面除支架贴壁不良、支架内皮化不全、血管正性重构之外,还要考虑不稳定新生粥样硬化斑块的因素,因此,必须经影像学检查确定病因后给予对应处理才能取得满意疗效;其次,为预防 TCFA 的形成,应更多地研究哪些因素促使稳定斑块向 TCFA 转化,并寻找相应的控制手段;最后,本研究还发现,28.0% 的 SCAD 患者再狭窄病变内存在 TCFA 但并未发生 NSTEACS,这一现象表明 DES 术后 NSTEACS 的形成除 TCFA 外还需要其他因素的参与,进一步寻找这些影响因素并给予有效控制是未来研究的方向。
本研究发现,DES 术后 NSTEACS 组比 SCAD组斑块体积更大、坏死及纤维脂肪成分比例更高,随访时间越长,坏死、纤维脂肪成分比例越高,这与以往的研究结果相似[11,12];这些 患者经皮冠状动脉介入治疗术后肌酸激酶MB同工酶峰值增高,这与 原 位 血 管 的 研 究 结 果 相 似[13]。 肌 酸 激 酶 MB 同工酶峰值的增高表明可能存在围术期心肌梗死,是预 后不 良的 预测因子[14]。 上述发 现提 示 DES 术后NSTEACS 患者进行经皮冠脉介入治疗时应注意预防围术期心肌梗死。目前认为这种心肌梗死的可能机制包括支架置入后部分小动脉开口被移行的斑块成份堵塞;斑块被挤压破裂,其中的坏死组织、脂肪成份和血栓脱落形成微栓子,随血流到达远端微血管引起栓塞导致心肌细胞缺血坏死[15];破裂斑块内包含的自由基等活性物质释放入血也可能造成心肌损伤[16]。为了更好地防治围术期心肌梗死,首先应更多地探索其发生机制并寻找有效的控制手段;其次,应探讨针对微栓塞采取远端保护装置等必要的措施进行预防的可行性;最后,针对自由基等活性物质的损伤作用寻找有效的预防方法,是未来研究的方向。
总之,DES置入术后新生粥样硬化斑块广泛存在,可能是导致支架内再狭窄的重要机制之一;而TCFA 的形成和破裂可能是 DES 术后发生 NSTEACS的重要机制之一。由于本研究是一个回顾性研究,因此不能精确反应 DES置入后内膜增生及斑块形成的全过程。研究纳入的样本量较小,可能使结果存在偏差。因此,上述结论需要更多前瞻性、大规模临床试验进一步证实。
[1]Mehran R, Dangas G, Abizaid AS, et al. Angiographic patterns of instent restenosis: classification and implications for long-term outcome. Circulation, 1999, 100: 1872-1878.
[2]Rodriguez-Granillo GA, Garcia-Garcia HM, Mc Fadden EP, et al. In vivo intravascular ultrasound-derived thin-cap fibroatheroma detection using ultrasound radiofrequency data analysis. J Am Coll Cardiol, 2005, 46: 2038-2042.
[3]Hong MK, Mintz GS, Lee CW, et al. A three-vessel virtual histology intravascular ultrasound analysis of frequency and distribution of thincap fibroatheromas in patients with acute coronary syndrome or stable angina pectoris. Am J Cardiol, 2008, 101: 568.
[4]Zahn R, Hamm CW, Schneider S, et a1. Coronary stenting with the sirolimus-eluting stent in clinical practice: final results from the prospective multicenter German cypher stent registry. J Interv Cardiol, 2010, 23: 18-25.
[5]Kang SJ, Mintz GS, Park DW, et a1. Mechanisms of in-stent restenosis after drug-eluting stent implantation intravascular ultrasound analysis. Circ Cardiovasc Interv, 2011, 4: 9-14.
[6]金琴花 , 王禹 , 盖鲁粤 , 等 . 冠状动脉介入治疗后造影复查支架再狭窄结果分析 . 中国循环杂志 , 2008, 23: 411-414.
[7]Le XF, Bast RC. Scr family kinases and paclitaxel sensitivity. Cancer Biol Ther, 2011, 12: 260-269.
[8]Camenzind E, Wijns W, Mauri L, et a1. Stent thrombosis and major clinical events at 3 years after zotarolimus-eluting or sirolimus-eluting coronary stent implantation: a randomised, multicentre, open-label, controlled trial. Lancet, 2012, 380: 1396-1405.
[9]窦克非 , 尹栋 , 吴元 , 等 . 冠心病合并糖尿病患者置入雷帕霉素洗脱支架和紫杉醇洗脱支架长期有效性及安全性观察 . 中国循环杂志 , 2012, 27: 174-177.
[10]Calvert PA, Obaid DR, O'Sullivan M, et a1. Association between IVUS findings and adverse outcomes in patients with coronary artery disease: the VIVA (VH-IVUS in Vulnerable Atherosclerosis) Study. JACC Cardiovasc Imaging. 2011, 4: 894-901.
[11]Kang SJ, Mintz GS, Akasaka T, et al. Optical coherence tomographic analysis of in-stent neoatherosclerosis after drug-eluting stent implantation. Circulation, 2011, 123: 2954-2963.
[12]金至赓 , 刘惠亮 , 张卓奇 , 等 . 血管内超声虚拟组织学成像评价可降解涂层雷帕霉素洗脱支架对冠状动脉壁的影响 . 中国循环杂志 , 2012, 27: 13-16.
[13]Rodriguez-Granillo GA, McFadden EP, Valgimigli M, et al. Coronary plaque composition of nonculprit lesions, assessed by in vivo intracoronary ultrasound radio frequency data analysis, is related to clinical presentation. Am Heart J, 2006, 151: 1020-1024.
[14]Lindsey JB, Kennedy KF, Stolker JM, et a1. Prognostic implications of creatine kinase-MB elevation after percutaneous coronary intervention: results from the Evaluation of Drug-Eluting Stents and Ischemic Events (EVENT) registry. Circ Cardiovasc Interv, 2011, 4: 474-480.
[15] Patti G, Pasceri V, Nusca A, et a1. Prevention of periprocedural myocardial damage in patients undergoing percutaneous coronary intervention. Ital Heart J Suppl, 2005, 6: 553-560.
[16]Ang L, Thani KB, Ilapakurti M, et a1. Elevated plasma fibrinogen rather than residual platelet reactivity after clopidogrel pre-treatment is associated with an increased ischemic risk during elective percutaneous coronary intervention. J Am Coll Cardiol, 2013, 61: 23-34.
Intravascular Ultrasound Observation for In-Stent Re-Stenosis in Patients After Drug Eluting Stent Implantation
WANG Tian-song, FENG Xu-xia, YAO Zhen.
Department of Cardiology, People’s Hospital of Sanya, Sanya (572000), Hainan, China
WANG Tian-song, Email: wts0425@163.com
Objective: To explore the coronary plaque composition by intravascular ultrasound (IVUS) observation for in-stent re-stenosis (ISR) in patients after drug eluting stent (DES) implantation.Methods: A total of 60 patients with quantitative coronary angiography confirmed ISR were divided into 2 groups as non-ST elevated acute coronary syndrome (NSTEACS) group, n=35 and stable coronary artery disease (SCAD) group, n=25. The ISR lesions were evaluated by IVUS virtual histology in both groups.Results: For basic characteristics of the lesion: compared with NSTEACS group, the patients in SCAD group had the shorter follow-up time, lower incidence of IVUS-defined thin-cap fibroatheroma (TCFA), smaller plaque volume, lower ratio of fibro-lipid tissue, lower ratio of necrotic core, lower level of CK-MB, all P<0.05; and the other characteristics were similar, P>0.05. For basic characteristics at different followed-up time: compared with DES implantation>20 months, the patients with DES implantation<20 months presented the lower incidence of TCFA, smaller plaque volume, lower ratio of fibro-lipid tissue, lower ratio of necrotic core, all P<0.05; and the other characteristics were similar, all P>0.05.Conclusion: The neoatherosclerotic plaque may be one of the important reasons for ISR in patients after DES implantation. TCFA formation and rupture could cause NSTEACS after DES implantation.
Coronary artery disease; Drug eluting stent; Coronary re-stenosis; Intravascular ultrasound
2013-04-24)
(编辑:王宝茹)
572000 海南省,三亚市人民医院 心内科
王天松 副主任医师 硕士 主要从事冠心病介入诊疗和易损斑块的识别与治疗研究 Email: wts0425@163.com 通讯作者:王天松
R54
A
1000-3614(2013)05-0348-04
10.3969/j.issn.1000-3614.2013.05.009
方法:入选 60 例定量冠状动脉造影确认为支架内再狭窄的患者,根据临床表现分为非 ST 段抬高的急性冠脉综合征 35 例 (NSTEACS 组)和稳定性冠心病 25 例(SCAD 组)。用血管内超声虚拟组织学检查评价再狭窄处病变。
结果:2 组随访时病变基本特征比较:与 NSTEACS 组比,SCAD 组除随访时间较短、薄层纤维帽硬化斑块(TCFA)发生率较低、斑块体积较小、纤维脂肪组织比例较低、坏死组织比例较低、肌酸激酶MB同工酶水平较低,差异均有统计学意义外(均 P< 0.05),其它病变基本特征差异均无统计学意义(P>0.05)。60 例患者不同随访时间的病变基本特征比较:与随访时间 >20 个月比,随访时间 < 20 个月除 TCFA 发生率较低、斑块体积较小、纤维脂肪组织比例较低、坏死组织比例较低,差异均有统计学意义外(均 P< 0.05),其它病变基本特征差异均无统计学意义(P>0.05)。
结论:新生粥样硬化斑块可能是 DES置入术后支架内再狭窄的重要机制之一,TCFA 的形成和破裂可能是 DES术后发生 NSTEACS 的重要机制之一。
