HPLC-MS/MS测定饲料中16种氟喹诺酮类药物残留量
2013-01-30梁君妮刘宁曹鹏孙磊丽牟妍关丽丽李彦沙美兰徐娟
梁君妮,刘宁,曹鹏,孙磊丽,牟妍,关丽丽,李彦,沙美兰,徐娟
(1.烟台出入境检验检疫局,山东烟台264000;2.青岛科技大学,山东青岛264200)
氟喹诺酮类(Fluoroquinolones),又称吡啶酮酸类药物,属于化学合成抗菌药。具有抗菌谱广、杀菌力强、使用方便、不良反应少等特点[1]。因此被广泛用于治疗小动物、禽类、家畜及水生动物由细菌、支原体引起的消化、呼吸、泌尿、生殖等系统疾病以及皮肤软组织的感染性疾病[2-4]。但是该类药物本身具有一定毒性,超剂量或长期反复使用该药可引起中枢神经系统等不良反应[5]。随着社会的发展和生活水平的不断提高,食品安全问题愈来愈受到关注。饲料是动物的直接食品,它的安全与否直接关系到动物性食品的安全,饲料的不安全因素会通过食物链对人类的健康造成危害。人若长期食用含抗生素的畜禽产品,可产生耐药性及其他不良反应[6]。为了保障畜禽产品的质量安全和人类健康,已禁止喹诺酮类药物作为药物添加剂在商品饲料中添加[7],但是滥用该类药物的情况依然存在,必须从整个食物链的源头--饲料抓起。因此建立一种同时检测饲料中多种喹诺酮类药物的方法具有重要意义。
目前饲料中氟喹诺酮类药物检测主要采用高效液相色谱法[8-10]、毛细管电泳法[11]和液质联用法[12-18]。高效液相色谱法分析时间长,定性能力差,假阳性率高。液质联用法是近几年兴起的新技术,与液相色谱法比较具有更高的灵敏度、选择性。本研究用液相色谱串联质谱法同时检测饲料中16 种氟喹诺酮类药物,通过对前处理方法和质谱方法等的研究,建立一种快速、准确的检测方法。
1 材料与方法
1.1 主要仪器与试剂
1200 型高效液相色谱、6410B 三重四级杆质谱仪:美国Agilent 公司;CF16RXⅡ型高速冷冻离心机:日本Hitachi 公司;Milli-Q 超纯水:美国Millipore 公司;氮吹浓缩仪:美国Organomation Associates 公司;RE-2000 旋转蒸发仪:瑞士BUCHI 公司;SB5200 型超声波清洗机:SHANGHAI BRANSON;Oasis MCX 固相萃取小柱:美国Waters 公司。
标准品:恩诺沙星、环丙沙星、氧氟沙星、诺氟沙星、培氟沙星、二氟沙星、丹诺沙星、沙拉沙星、麻保沙星、萘啶酸、氟甲喹、恶喹酸、依诺沙星、洛美沙星、司帕沙星、奥比沙星,均购于Dr.Ehrenstorfer 公司,纯度>95%,
乙腈、甲醇(色谱纯,德国Merk 公司),乙酸、甲酸(色谱纯,TEDIA),水为超纯水。饲料均购于市场。
1.2 标准溶液的配置
1.2.1 16种喹诺酮类标准储备液
精密称取16 种氟喹诺酮类药物,用30 mmol/L 氢氧化钠溶解后移入100 mL 容量瓶中,并稀释至刻度,配制成含量为100.0 mg/kg 的溶液。
1.2.2 标准中间液
将标准储备液用30 mmol/L 氢氧化钠稀释成1.0 mg/kg。
1.2.3 标准使用液
将标准中间液用30 mmol/L 氢氧化钠依次稀释至100.0、50.0、20.0、10.0、5.0 μg/kg 的标准系列溶液,待用。
以上标准溶液均于4 ℃冰箱中避光保存。
1.3 样品前处理
准确称取5.0 g 样品,置于50 mL 离心管中,加入适量水浸泡1 h(保证饲料样品完全润湿),加入1%乙酸的乙腈溶液15 mL,超声提取20 min,振荡提取5 min,5 000 r/min 离心10 min,收集上清液于鸡心瓶中,重复上述提取步骤一次,合并上清液,40 ℃快速浓缩至干。向鸡心瓶中加入1.0 mL 甲醇,涡混溶解残渣,加入9 mL超纯水,混合均匀,分取10 mL 作为上样液,使用Oasis MCX 固相萃取柱进行净化处理。依次用3 mL 甲醇及3 mL 超纯水活化MCX 固相萃取柱,将提取液以不超过1.0 mL/min 的速度通过固相萃取柱,加入3 mL 水及3 mL 甲醇淋洗,抽干。5.0 mL 氨化甲醇(5%氨水)洗脱,洗脱液于40 ℃氮吹仪吹干,加入1.0 mL 乙腈-0.1%甲酸水溶液(20 ∶80/体积比)溶解残渣,过0.2 μm的滤膜,待测。
1.4 检测方法
1.4.1 高效液相色谱条件
色谱柱:Agilent Eclipse Plus C18柱(2.1×150 mm,3.5 μm);柱温:35 ℃;进样体积:10 μL;流动相A 为0.1%甲酸水,流动相B 为乙腈;流速:0.3 mL/min;梯度洗脱程序:0~5.00 min,10%B;5.00 min~8.00 min,20%B~90%B;8.00 min~9.00 min,90%B;9.01 min~12.00 min,90%B~10%B。
1.4.2 质谱条件
离子源:电喷雾离子源(ESI+),扫描方式:多反应监测(MRM),Delta EMV:500 V,雾化气压力:35 psi,干燥气温度:350 ℃,干燥气流速:600 L/min,毛细管电压:4 000 V。质谱采集参数见表1。
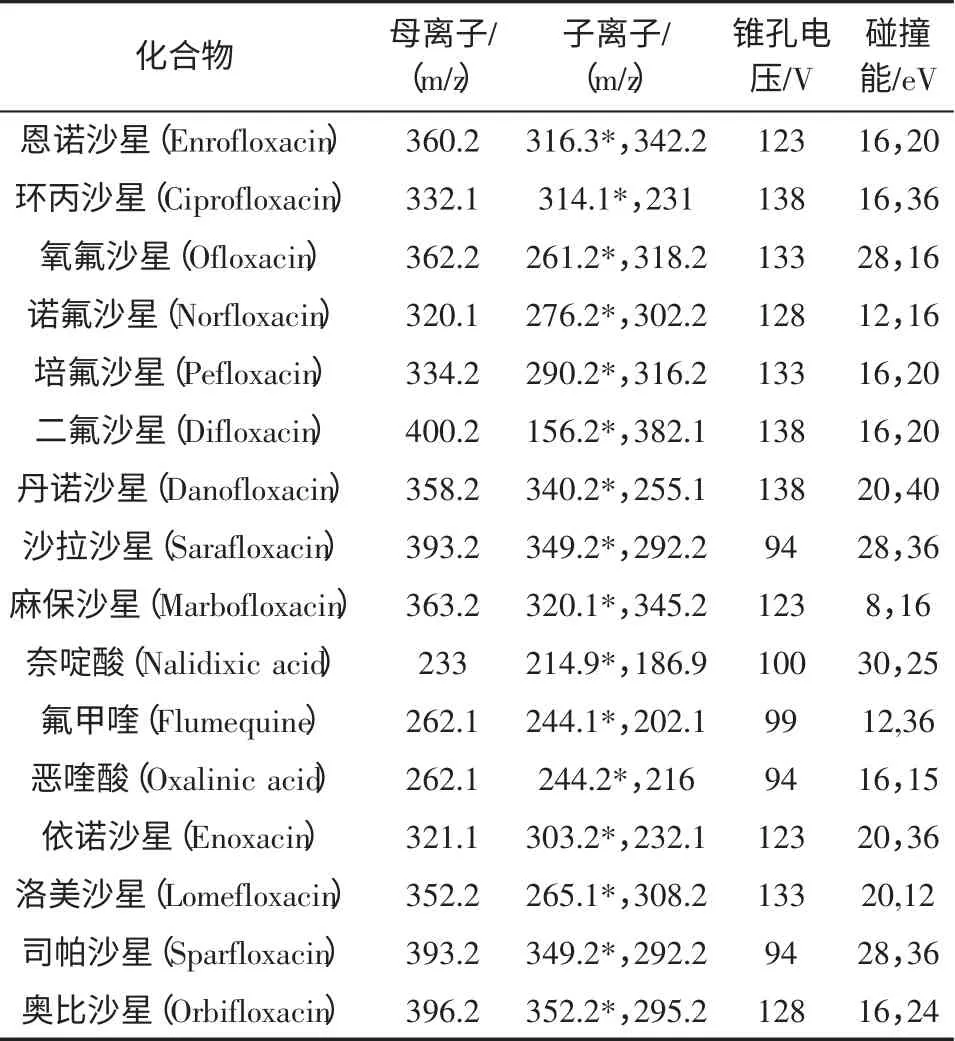
表1 16 种喹诺酮类的质谱条件Table 1 MS/MS conditions of 16 Quinolones
2 结果与讨论
2.1 样品前处理方法的选择
2.1.1 提取方法的优化
本方法的基质饲料吸湿性很强,如果直接用提取溶剂提取,会造成大量损失,回收率大大下降。乙酸的加入是沉淀蛋白。本方法通过对提取溶剂种类、乙酸添加的比例、提取方法、提取液用量、提取时间等因素对提取效果影响的考察,发现在样品中加入适量水浸泡,加入1%乙酸的乙腈溶液15 mL,超声提取20 min,振荡提取5 min,重复提取两次,提取效果较好。
2.1.2 净化方法的优化
由于饲料样品基质复杂,如果采用正己烷净化效果较差,所以选择SPE 固相萃取柱对样品进行净化处理[19]。考察了Oasis HLB、碱性氧化铝、Oasis MCX 柱3 种固相萃取柱及淋洗液、洗脱液种类、洗脱液体积等对回收率和净化效果的影响。实验结果表明,Oasis MCX效果最好,每种药物均能获得较高的回收率,且能很好的去除杂质干扰,见图1。因此最终选择Oasis MCX柱进行净化。
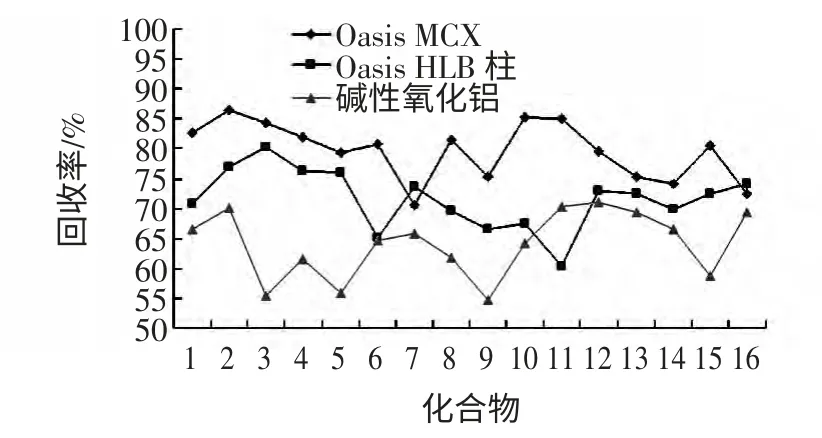
图1 不同净化柱对回收率的影响Fig.1 Effects on the recoveries of 16 quinolones with different columns
2.2 方法学验证
2.2.1 线性关系
用16 种氟喹诺酮类混合标准工作液,分别为100.0、50.0、20.0、10.0、5.0 μg/kg,按上述色谱和质谱条件测定其峰面积,以质量浓度X(μg/kg)为横坐标,峰面积的比值Y 为纵坐标,绘制16 种氟喹诺酮类混合标准溶液工作曲线,计算回归方程和相关系数,见表2。
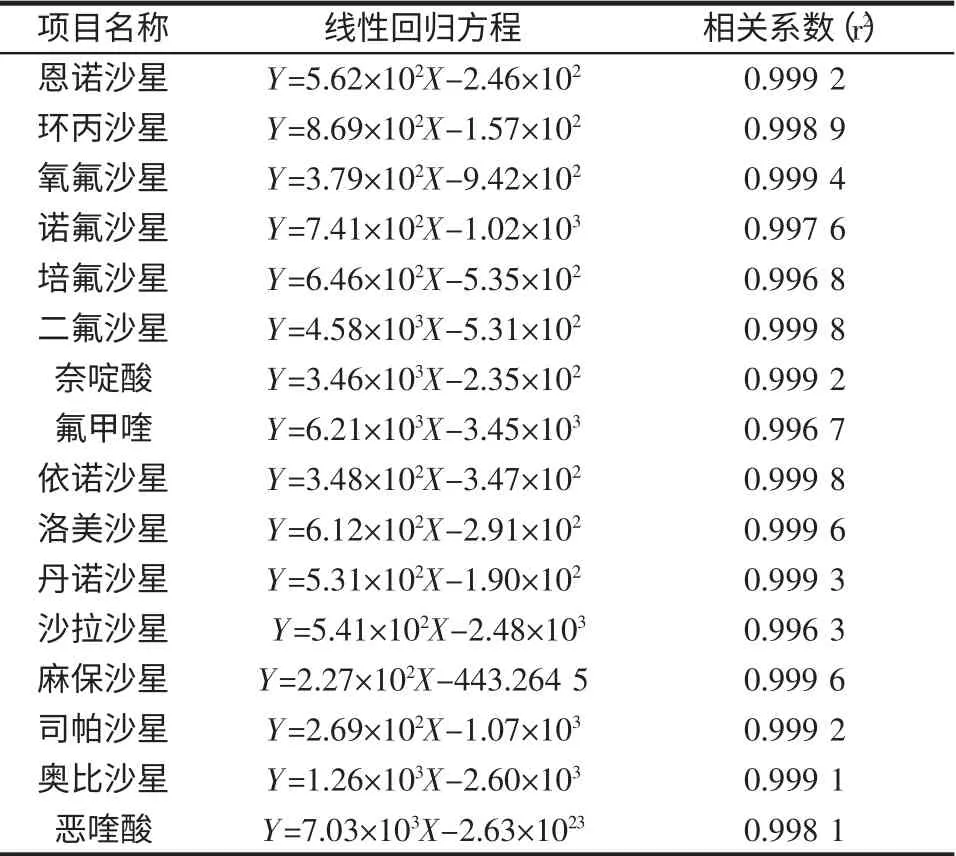
表2 16 种氟喹诺酮类药物的线性回归方程和相关系数Table 2 Equations of linear regression and correlation coefficients of 16 veterinary quinolones
结果表明,16 种氟喹诺酮类药物浓度与对应的峰面积呈现良好的线性关系,线性范围:5.0 μg/kg~100.0 μg/kg。
2.2.2 检测低限
按所建立的色谱条件,以3 倍噪音比作为检测低限,测得本方法16 种氟喹诺酮类药物的测定低限均可以达到10.0 μg/kg,满足国内和国际对喹诺酮类药物残留监控的要求。
2.2.3 基质效应的消除
由于空白样品基质溶液对16 种氟喹诺酮类标准物质有不同程度的影响,本文采用配制基质匹配标准溶液用于定量的方法,很好的消除了基质影响,完全能满足残留检测的要求。
2.2.4 方法的灵敏度和精确度
以空白饲料为样品,制备添加10.0、20.0、100.0 μg/kg 3 个水平的16 种氟喹诺酮类药物混标,制成模拟加标样品,按上述实验方法进行测定,每个添加水平重复测定6 个样品,同时做空白对照。所得到的样品中各待测组分的添加回收率均70.7%~86.4%之间,相对标准偏差3.8%~9.2%,方法准确度及精密度满足要求。
保留时间(min):恩诺沙星(7.125)、环丙沙星(6.307)、氧氟沙星(6.038)、诺氟沙星(6.039)、培氟沙星(6.220)、二氟沙星(7.757)、丹诺沙星(10.612)、沙拉沙星(7.718)、麻保沙星(8.961)、萘啶酸(8.896)、氟甲喹(8.481)、恶喹酸(8.481)、依诺沙星(5.662)、洛美沙星(5.535)、司帕沙星(4.090)、奥比沙星(7.261)。
饲料添加浓度为10.0 μg/kg 的样品的LC-MS/MS TIC 图和部分选择离子流图谱图见图2 和图3。
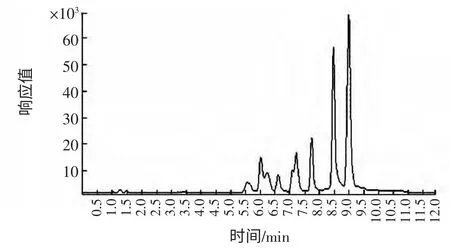
图2 TIC 图Fig.2 Total iron chromatograms
3 结论
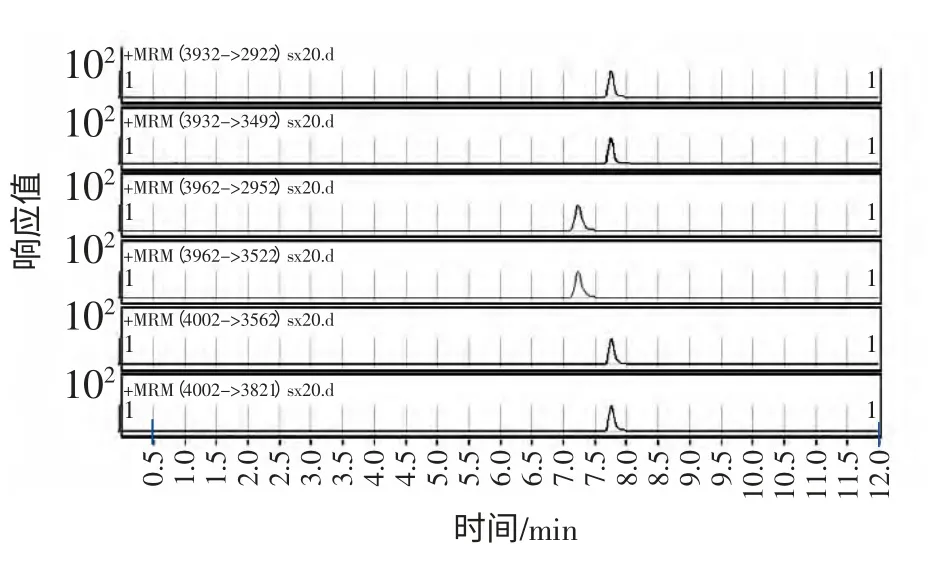
图3 添加10.0 μg/kg 16 种氟喹诺酮类饲料样品的部分选择离子流图Fig.3 Some selected ion chromatograms of 16 quinolones in the feed adding 10.0 μg/kg
建立了饲料中恩诺沙星、环丙沙星、氧氟沙星、诺氟沙星、培氟沙星、二氟沙星、丹诺沙星、沙拉沙星、麻保沙星、萘啶酸、氟甲喹、恶喹酸、依诺沙星、洛美沙星、司帕沙星、奥比沙星16 种氟喹诺酮类残留量的液相色谱-串联质谱测定方法。试样用水浸泡1 h,1%乙酸的乙腈溶液提取,Oasis MCX 固相萃取柱净化,以乙腈-0.1%甲酸水溶液为流动相,HPLC-MS/MS 法检测,同时定性、定量测定16 种氟喹诺酮类抗生素残留。16 种氟喹诺酮类抗生素在色谱柱上分离效果较好,回收率在70.7%~86.4%之间,相对标准偏差在3.8%~9.2%之间,均能满足兽药残留分析的要求,方法准确、简便、快速,为饲料中多种兽药残留测定提供了可靠的前处理方法和检测手段。
[1] 陈杖榴.兽医药理学[M].2 版.北京:中国农业出版社,2002:234
[2] 郑国安,宋庆华.动物性食品兽药残留的危害与对策初探[J].河南农业科学,2005(11):98-99
[3] 贡玉清.喹诺酮类药物的残留分析[J].畜牧与兽医,2002(8):31-32
[4] 杜黎明,卫洪清,张俊燕,等.高效液相色谱法测定氟喹诺酮类药物[J].分析化学,2003(5):637
[5] 张俊丰,陈琳.氟喹诺酮类药物在兽医临床的应用[J].兽药与饲料添加剂,2002,7(5):13-15
[6] 李登赴.饲料与畜禽产品质量安全问题浅析[J].贵州畜牧兽医,2008,32(6):19-21
[7] 晓同.农业部发布《饲料药物添加剂使用规范》[J].中国饲料,2001(15):2
[8] 贾涛.液相色谱-荧光法测定饲料中氟喹诺酮类药物[J].检测分析,2012(12):43-46
[9] 施杏芬,任玉琴,陈勇,等.高效液相色谱法测定复合预混合饲料中9 种喹诺酮类药物[J].中国农业科技导报,2008,10(S2):27-31
[10] 左文霞,王莹,于小雷,等.饲料中氟喹诺酮类药物检测方法研究[J].饲料研究,2012(2):72-74
[11] 李慧,祁克宗,邵黎,等.高效毛细管电泳用于饲料中5 种氟喹诺酮类药物的同时测定[J].中国饲料,2009(20):33-37
[12] 李岩,李彦伸,张素霞,等.LC-MS-MS 法检测猪全价饲料中喹恶林类药物[C].中国畜牧兽医学会兽医药理毒理学分会第十次研讨会论文摘要集,2009:132
[13] 严丽娟,张峰,方恩华,等.超高效液相色谱-电喷雾串联质谱法测定动物饲料中的大环内酯类和林可胺类抗生素[J].色谱,2010,28(11):1038-1042
[14] 张毅,蓝芳,张峰,等.液相色谱-串联质谱法测定谷物类饲料中的41 种激素[J].色谱,2011,29(6):523-534
[15] 秦燕,张美金,林海丹.高效液相色谱-电喷雾串联质谱法测定动物饲料中的10 种磺胺[J].色谱,2005,23(4):397-400
[16] L Kantiani,M Farré, I Grases, et al.Development and validation of a pressurised liquid extraction liquid chromatography-electrospraytandem mass spectrometry method for beta-lactams and sulfonamides in animal feed Anal[J]. Bioanal Chem, 2010,398(3):1195-1205
[17] M Dousa, Z Sikac, M Halama, et al. HPLC determination of lincomycin in premixes and feedstuffs with solid-phase extraction on HLB OASIS and LC-MS/MS confirmation[J].J Pharma Biomed Anal,2006,40(4):981-986
[18] J Barbosa,S Moura,R Barbosa,et al.Determination of nitrofurans in animal feeds by liquid chromatography-UV photodiode array detection and liquid chromatography-ionspray tandem mass spectrometry[J].Anal Chim Acta,2007,586(1/2):359-365
[19] 刘瑜,赵颖,李晓东,等.用超高效液相色谱-串联质谱法同时检测浓缩饲料中的多种兽药残留[J].化学通报,2013,76(2):157-162
