油炸型膨化食品中丙烯酰胺含量的结果分析
2013-01-28陈旭明李婷王侠文
陈旭明,李婷,王侠文
(广东省潮州市质量计量监督检测所,广东潮州521011)
丙烯酰胺(CAS 76-06-01)是结构简单的小分子化合物,主要在高碳水化合物、低蛋白质的植物性食物加热(120 ℃以上)烹调过程中形成,140 ℃~180 ℃为生成的最佳温度。是国际癌症研究中心(IARC)认定的2A 类致癌物质[1]。动物实验和体外细胞实验都证明,丙烯酰胺具有潜在的神经毒性、遗传毒性和致癌性[2]。在发现高温加热的食品中含有高剂量的丙烯酰胺之前,国内外学者认为人群暴露于丙烯酰胺除职业接触外,主要是饮水和吸烟两种途径。2000年,瑞典学者首次提出食品高温加热过程可能产生丙烯酰胺,当时没有引起足够的重视。2002年4月,来自斯德哥尔摩大学和瑞典国家食品管理局的科学家发表了学术论文,指出高温加热的多种食品中含有高剂量的丙烯酰胺,引起了国际上的强烈反响。随后,其他各国食品管理机构如挪威、瑞士、德国和美国等相继确认食品中含有丙烯酰胺[3]。这一研究结果引起了世界各国的政府部门和学术界的广泛关注。潮州的膨化食品生产企业有110 多家,对油炸型膨化食品中丙烯酰胺进行测定分析,了解本地区该类食品中丙烯酰胺的含量水平也就显得尤为迫切。
目前在国际上对于食品中丙烯酰胺含量的分析方法有气相色谱-质谱联用法[4-5]以及液相色谱-质谱联用方法[6-7]。GC-MS 需要衍生化处理,但是灵敏度高,方法稳定;LC-MS/MS 不用衍生化,但是通常要求建立一整套严格而又繁琐的固相萃取净化步骤。本文用水热提取油炸型膨化食品中的丙烯酰胺,正己烷提取油脂类物质,经蛋白变性净化后用溴水进行衍生化,由GC-MS 联用仪检测,方法只需除去油脂和蛋白变性净化步骤就能有效地消除干扰,避免了固相萃取净化步骤,不仅提高了效率,而且降低了分析成本。
1 材料与方法
样品来源:2012年6月~8月在潮州市的部分膨化食品生产企业的成品仓库随机抽取了30 件油炸型膨化食品样品。
1.1 材料与仪器
Clarus 600 型气质联用仪(配备电子轰击离子源(EI)):美国PE 公司;RE600 型旋转蒸发仪:日本Yamato 公司;XW-80A 型旋涡混合器:上海医科大学仪器厂;HH.S21.Cr4Ⅱ型电子恒温水浴锅:汕头市电子设备厂有限公司;丙烯酰胺标准品:德国Dr.Ehrenstorfer GmbH 公司,纯度≥99%;乙酸乙酯(色谱纯);正己烷(分析纯);饱和溴水(含量≥3%);氢溴酸(分析纯);溴化钾(优级纯);CarrezI 溶液(57.6%硫酸锌水溶液),CarrezII 溶液(28.8 %亚铁氰化钾水溶液)。
标准储备液及工作液:称取丙烯酰胺标准品100mg,用水溶解并定容至100 mL,此溶液浓度为l mg/mL(储存条件:0 ℃~4 ℃避光放置),根据需要配成适当浓度的标准工作溶液(储存条件:0 ℃~4 ℃避光放置,不得超过3 d,建议现配现用)。实验用水为蒸馏水。
1.2 实验方法
1.2.1 样品处理方法
准确称取已粉碎的样品10.00 g 于100 mL 比色管中,加入10 mL 正己烷,振荡10 min 后弃去正己烷层,加入适量水,70 ℃水浴2 h,再加入CarrezI 和CarrezII溶液各5mL,定容至100mL。静置分层后过滤,取25mL滤液于锥形瓶中,准备衍生化。在滤液中加入溴化钾7.5 g、用氢溴酸调节滤液至pH1~3,再加入8 mL 溴水,在4 ℃条件下衍生过夜。滴加硫代硫酸钠溶液至黄色消失。将溶液转移至分液漏斗中,加20 mL 乙酸乙酯,振荡10 min,静置分层,再分别用10 mL 乙酸乙酯提取2 次,合并提取液。过无水硫酸钠后,旋转蒸发(40 ℃)至近干,并定容至2.0 mL,待测。
1.2.2 仪器测定条件
色谱柱:Elite-5MS 30 m×0.25 mm×0.25 μm;色谱柱温度(程序升温):初始温度65 ℃(保持1 min),以15 ℃/min 升温至280 ℃(保持5 min);进样口温度:280 ℃;离子源温度:230 ℃;传输线温度:280 ℃;电离方式:EI 源;电离能量:70 eV;测定方式:选择离子监测(SIM),选择监测离子(m/z):106、108、150、152,以m/z150 定量;载气:高纯氦气(纯度99.999 %);流速1.0 mL/min;溶剂延迟时间:3 min;质量扫描范围:40 u~450 u;进样方式:不分流进样;进样量:1 μL。
2 结果与分析
2.1 工作曲线与检出限
吸取适量丙烯酰胺标准工作液于容量瓶中,逐级稀释,得到其质量浓度分别为2.0、1.0、0.5、0.25、0.1 μg/mL系列标准工作液,分别吸取25 mL 标准液于三角瓶中,依“1.2”节方法衍生化步骤直接衍生化。按照前面的仪器条件进样分析后,以质量浓度(μg/mL)为横坐标(X),丙烯酰胺定量离子的峰面积为纵坐标(Y)作标准曲线,得到的线性方程为Y=147 509X-3 129.46,相关系数为0.998 6,这表明在0.1 μg/mL~2 μg/mL 范围内呈现出良好的线性关系。根据检出限浓度处的信噪比S/N=3 这一原则,对方法检测限进行推算,选定3 种低浓度0.01、0.02、0.04 μg/mL 的标准溶液进行测试,结果表明此方法的检出限0.02 μg/mL。校准曲线见图1。

图1 丙烯酰胺标准曲线Fig.1 The standard curve of acrylamide
2.2 分析方法的准确度及精密度
为了验证方法的准确性和可靠性,对测定方法进行加标回收实验。按上述实验条件对添加0.1、0.5、1 μg/mL 等3 个水平标准溶液的不同样品进行实验,实验数据见表1。丙烯酰胺衍生物2,3-二溴丙烯酰胺(2,3-DBPA)选择离子色谱图、选择离子质谱图及样品加标回收谱图分别见图2、图3 和图4。
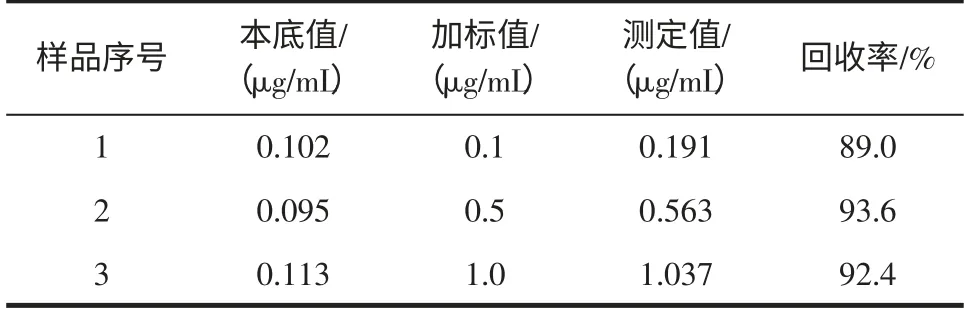
表1 丙烯酰胺的加标回收率测定Table 1 The recovery of acrylamide added to urine
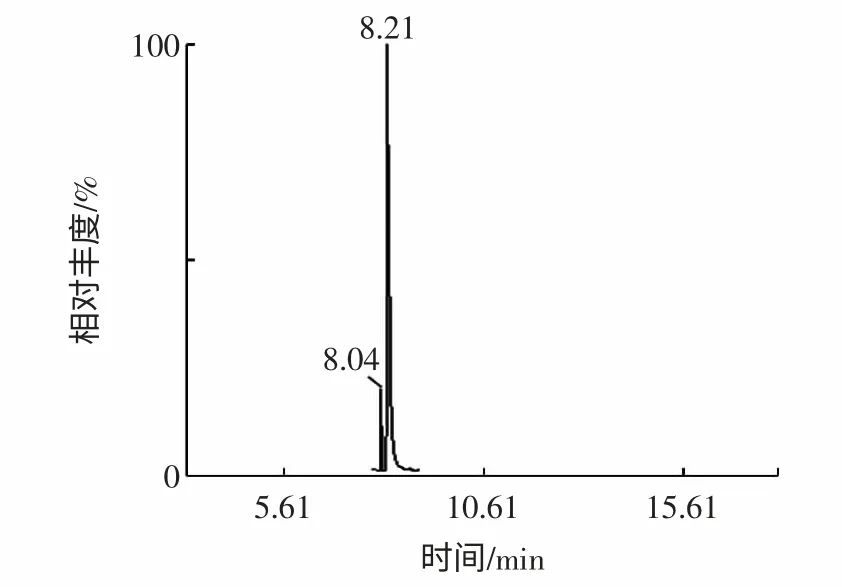
图2 2,3-DBPA 选择离子色谱图Fig.2 Chromatogram of 2,3-DBPA with selected ion
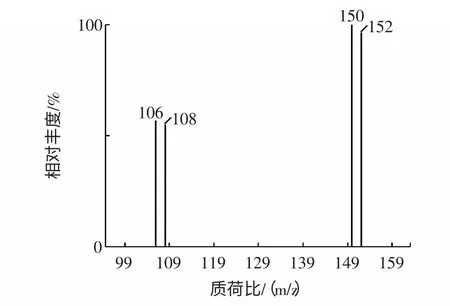
图3 2,3-DBPA 选择离子质谱图Fig.3 Mass spectrum of 2,3-DBPA with selected ion
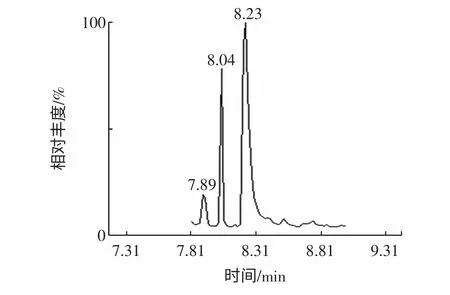
图4 样品中添加丙烯酰胺色谱图Fig.4 Chromatogram of acrylamide in sample
从以上结果可以发现,样品回收率在不同添加量,不同样品中其回收率不同,但回收率都在89.0 %~93.6 %之间。
配制进样浓度为0.1、0.5、1.0 μg/mL 的丙烯酰胺标准溶液,分别进行6 次平行测定实验,结果如下表2。
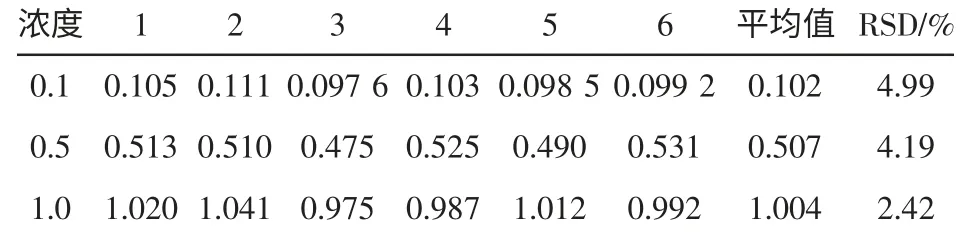
表2 精密度实验结果Table 2 The results of precision tests(n=6,μg/mL)
2.3 样品测定
利用该方法对从2012年6月~8月在潮州市的部分膨化食品生产企业的成品仓库中随机抽取的30 件油炸型膨化食品样品进行测试,30 个样品中均含有一定数量的丙烯酰胺,其含量在192 μg/kg~1 037 μg/kg范围内(见表3),含量最高的样品是含量最低样品的5倍多,反映出即使同是油炸型膨化食品,丙烯酰胺含量存在较大的波动,这主要是由加工过程中的油炸温度不同、油炸时间长短以及原料类别差异所引起的。平均含量为451 μg/kg,与相关文献报道中蒸馒头的平均含量为0 μg/kg[8]、煮马铃薯的平均含量为<5 μg/kg[9]比较,明显高于通过蒸、煮等非油炸方式加工的食物中丙烯酰胺的含量。这是因为油炸过程中温度一般都在100 ℃以上,达到其生成的温度条件,而且油炸过程中食品失水较快,因此在比较干硬部分容易产生丙烯酰胺。而蒸、煮过程温度最高也仅为100 ℃,因此产生的丙烯酰胺很少甚至没有。由此可见,油炸型膨化食品生产过程中的油炸温度是影响其丙烯酰胺含量最重要的因素,Mottram 等将天门冬酰胺与葡萄糖一起加热,发现在120 ℃时开始生成丙烯酰胺,随着温度的升高而升高[10]。Franco Pedreschi 实验表明,在炸土豆片过程中,当温度从190 ℃减低至150 ℃时,丙烯酰胺的含量急剧下降[11]。因此,控制油炸型膨化食品生产过程中的油炸温度成了控制丙烯酰胺含量的关键。

表3 30 个油炸型膨化食品样品中丙烯酰胺的测定结果Table 3 The determination results of acrylamide in 30 fried puffed food samples
2.4 预防措施
到目前为止,尽管无食品中丙烯酰胺的限量标准,但油炸型膨化食品中丙烯酰胺的含量却远远超过饮用水中的最大允许量0.5 μg/L[12]。WHO 推荐的丙烯酰胺日安全摄入量为1 μg/kg·bw/d,如按这些评估标准,成年男子日摄入100 g 油炸型膨化食品,就可能有很高的健康风险。鉴于丙烯酰胺的危害性,就降低丙烯酰胺摄入量而言,建议人们少吃油炸食品,多食新鲜蔬菜和水果。家庭生活中多采用蒸、煮,少用煎、炸的方式来烹饪食品,通过降低烹调的温度和缩短烹调的时间,来减少有关食品中的丙烯酰胺的含量,从而可以达到预防的目的。
3 结论
用气相色谱-质谱联用法对油炸型膨化食品中的丙烯酰胺含量进行分析。所用的方法灵敏度高,精密度及回收率均可满足实际工作的要求,准确可靠。调查结果较为客观地反映了潮州市油炸型膨化食品中丙烯酰胺含量的情况。
[1] 仲维科,陈冬东,雍炜,等.气相色谱-质谱法测定油炸淀粉类食品中的丙烯酰胺[J].色谱,2005,23(3):312-314
[2] RG Tardiff,ML Gargas,CR Kirman,et al. Estim ation of safe dietary intake levels of acrylamide for hu-mans[J].Food Chem Toxicol,2010,48(2):658-667
[3] K Svensson, L Abramsson, WBecker, et al. Dietary intake of acrylamide in Sweden[J]. Food and Chemical Toxicology, 2003,41(11):1581-1586
[4] 杨斯超,张慧,汪俊涵,等.柱前衍生化-气相色谱-质谱法定量测定食品中丙烯酰胺的含量[J].色谱,2011,29(5):404-408
[5] Lagalante AF,Felter MA.Silyation of acrylamide for analysis by solid-phase microextraction/gas chromatography ion-trap mass spectrometry[J].J Agri Food Chem,2004,52(12):3744-3748
[6] 王浩,刘艳琴,杨红梅,等.高效液相色谱-串联四极杆质谱联用测定饼干中丙烯酰胺残留量[J].食品研究与开发,2009,30(2):108-110
[7] Hoenicke K,Gatermann R,Harder W,et al.Analysis of acrylamide in different foodstuffs using-tademmass spectrometry[J]. Analytica Chimica Acta,2004,520(1/2):207-215
[8] 张辉珍,梁惠,刘颖,等.食品中丙烯酰胺含量及其产生因素分析[J].青岛大学医学院学报,2011,47(4):301-304
[9] 葛宇,赵旭丽,巢强国.食品中的丙烯酰胺分布及其检测方法研究进展[J].粮油加工,2008,5(6):108-112
[10] Mottram DS,Wedzicha BL,Donson AT.Acrylamide is formed in the mailard reaction[J].Nature,2002,419(6906):448-449
[11] Franco Pedreschi.Reduction of acrylamide formation in potato sclices during frying[J].Lebensm wiss u Technol,2004,37(6):679-685
[12] 张凌云,刘波,徐荣,等.液相色谱-串联质谱法测定饮用水中的丙烯酰胺[J].环境化学,2010,29(1):152-153
