间接竞争酶联免疫法检测水样中的重金属镉
2012-12-27王俊平方淑兵
王 津 生 威 王俊平 方淑兵
杨依锦 张曙光 王 硕
(天津科技大学食品营养与安全教育部重点实验室,天津 300457)
间接竞争酶联免疫法检测水样中的重金属镉
王 津 生 威 王俊平 方淑兵
杨依锦 张曙光 王 硕
(天津科技大学食品营养与安全教育部重点实验室,天津 300457)
利用重金属镉多克隆抗体,建立一种低仪器成本的检测水样中重金属镉的间接竞争酶联免疫法,其检测限(IC15)为0.76μg/L,灵敏度(IC50)为11.33μg/L。交叉反应结果表明,该抗体除与汞螯合物的交叉反应率为10.9%,与其他金属(锰,铬,镁,铁,铅,镍,银和铜)螯合物的交叉反应率均低于1.32%。自来水和河水样品中镉的添加回收率为93.95%~107.40%,变异系数为3.97%~14.69%。
镉;重金属免疫学检测法;多克隆抗体;酶联免疫法;自来水;河水
镉是一种毒性很强的重金属,是人体非必需元素,它的半衰期超过10年[1,2]。镉通过食物链被人体吸收后蓄积在肝、肾中,造成对人体的危害。日本发生的“骨痛病”就是由于镉废水污染土壤后转移至农产品中,通过食物链转移到人体内而造成的。
目前用于检测重金属镉离子的方法有原子吸收光谱法(AAS)、原子荧光法(AFS)、电感耦合等离子体原子发射光谱法(ICP-AES)、电感耦合等离子体质谱法(ICPMS)[3-6],这些方法需要昂贵的仪器、专业的技术人员和复杂耗时的样品处理过程,不适于快速现场检测。重金属免疫学检测方法[7]与上述方法相比有着仪器成本低和适合现场检测的优点。
本试验建立了重金属镉离子的间接竞争酶联免疫检测方法。为了验证方法的准确性,同时将其应用于自来水和河水样品的添加回收试验。
1 材料与方法
1.1 试剂与仪器
标准镉、汞、锰、铬、镁、铁、铅、镍、银溶液:中国科学计量研究院;
牛血清白蛋白(BSA)、弗氏完全佐剂、弗氏不完全佐剂、过氧化氢脲、3,3’,5,5’-四甲基联苯胺(TMB)、吐温-20、二甲基亚砜(DMSO)、4-羟乙基哌嗪乙磺酸(Hepes):美国Sigma公司;
脱脂乳粉:美国BD公司;
HRP-标记羊抗兔二抗:美国Promega公司;
β-环糊精:德国Merck公司;
乙二胺四乙酸(EDTA):上海生工生物工程技术服务有限公司;
针对重金属镉的多克隆抗体、Cd-ITCBE-BSA包被原:本实验室自制
超纯水仪:Milli-Q Avantage A10,美国 Milipore公司;
酶标仪:Multiskan Ascent,美国Thermo公司;
紫外分光光度计:UV-2450,日本岛津公司;
96孔酶标板:丹麦Nunc公司。
1.2 标准品的制备
本试验采用乙二胺四乙酸(EDTA)作为镉的螯合剂,螯合方法如下:准确量取1mL的1 000μg/mL的镉标准品,与2.6mg等体积的EDTA(EDTA溶解在Hepes缓冲溶液中)进行螯合,摩尔比为1∶1,然后使用三乙胺调节反应物的pH至中性,室温搅拌反应16h,即形成500μg/mL的Cd-EDTA螯合物。
1.3 间接竞争酶联免疫法的建立
包被原Cd-ITCBE-BSA用pH 9.6的碳酸盐缓冲液稀释成0.004μg/孔,包被在96孔酶标板上,100μL/孔,4℃孵育过夜。PBST洗板3次,每孔加入200μL封闭液(1%脱脂乳粉),室温放置1h。PBST洗板3次,每孔加入50μL梯度稀释的Cd-EDTA螯合物和50μL的抗体,室温震荡孵育1h。PBST洗板3次,加入HRP标记的羊抗兔,每孔100μL,室温震荡孵育30min。PBST洗板3次,加入底物液,每孔100μL,37℃显色10min。加入终止液,每孔50μL。酶标仪读数。根据OD值按照式(1)计算抑制率:

式中:
IR—— 抑制率,%;
OD——加入标准品和抗体的吸光度值;
OD对照——不加标准品的吸光度值;
OD空白——不加标准品和抗体的吸光度值。
此绘制的抑制率曲线的X轴为Cd-EDTA浓度的对数值,Y轴为相应的抑制率,并且标准曲线的形状是典型的S型曲线。
1.4 交叉反应
抗体与结构类似化合物的交叉反应程度,用交叉反应率(CR%)表示。它是以抑制抗体最大结合率的50%所需目标分析物的浓度IC50(Cd-EDTA)与所测各种结构类似化合物的浓度IC50(其他金属离子EDTA螯合物)之比的百分数表示,按照式(2)计算交叉反应率:

式中:
CR——交叉反应率,%;
IC50(Cd-EDTA)—— 抑制率为50% 时 Cd-EDTA的浓度,μg/L;
IC50(Metal-EDTA)—— 抑 制 率 为 50% 时 其 他 金 属EDTA螯合物的浓度,μg/L。
交叉反应率越小,则抗体特异性越高。本试验选择汞、锰、铬、镁、铁、铅、镍、银和铜等重金属的螯合物,同时进行标准曲线的绘制,计算各竞争物的IC50值,比较重金属镉多克隆抗体对它们的亲和性。
1.5 样品添加回收试验
1.5.1 基质影响消除 将河水样品先使用0.22μm的滤膜进行过滤,而自来水无需进行过滤,然后用0.01mol/L的PBS将自来水、河水样品分别稀释2倍,5倍,10倍,分别和标准曲线对比,若基质曲线能与标准曲线重合,即基质影响消除。
1.5.2 添加回收试验 向自来水、河水样品中添加一定浓度的重金属镉,将海河水样品先使用0.22μm的滤膜进行过滤,而自来水无需过滤。然后用0.01mol/L的PBS稀释一定倍数后,用间接竞争酶联免疫法检测样品中重金属镉的含量并计算相应的回收率。
2 结果与讨论
2.1 间接竞争酶联免疫法的建立
将制备 好 的500μg/mL的 Cd-EDTA 螯 合 物 使 用0.01mol/L的 PBS稀释到1 000μg/L,然后从1 000μg/L开始5倍梯度稀释成6个浓度,分别为0.32,1.6,8,40,200,1 000μg/L。根据式(1)计算Cd-EDTA各个浓度下的抑制率,然后绘制出重金属镉的标准曲线,见图1。
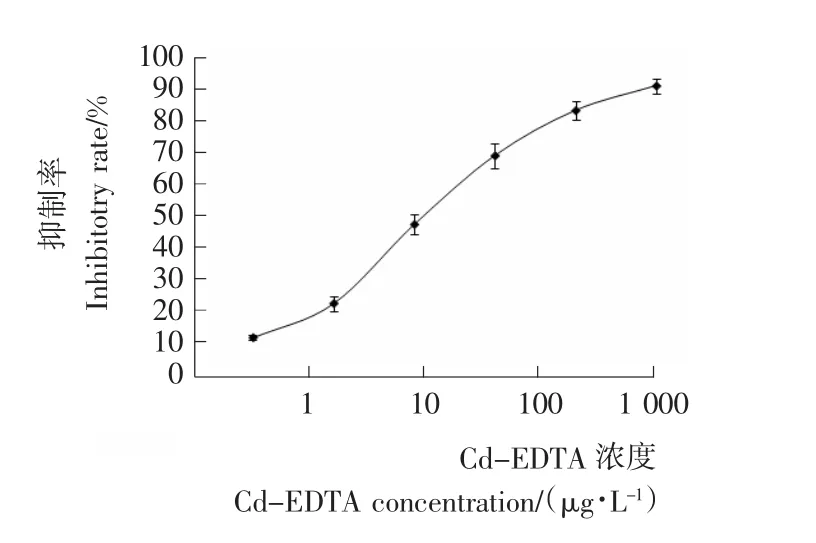
图1 重金属镉间接竞争酶联免疫法的标准曲线Figure 1 Standard curve of heavy metal cadmium using indirect competitive enzyme-linked immunosorbent assay
由图1可知,建立的重金属镉间接竞争酶联免疫法的检测限(IC15,抑制率为15%时对应的Cd-EDTA的浓度值)为0.76μg/L,灵敏度(IC50,抑制率为50%时对应的 Cd-EDTA的浓度值)为11.33μg/L。
2.2 交叉反应
为了判断重金属镉多克隆抗体的特异性,本试验选取了9种金属,分别是汞(Hg)、锰(Mn)、铬(Cr)、镁(Mg)、铁(Fe)、铅(Pb)、镍(Ni)、银(Ag)、铜(Cu)。它们与EDTA螯合后进行交叉反应,计算该抗体与金属EDTA螯合物的交叉反应率(CR%),见表1。
由表1可知,重金属镉多克隆抗体除了与重金属汞的交叉反应率为10.9%,与其他金属锰(Mn)、铬(Cr)、镁(Mg)、铁(Fe)、铅(Pb)、镍(Ni)、银(Ag)、铜(Cu)的交叉反应率均低于1.32%。本试验发现重金属镉多克隆抗体与金属汞之间有一定的交叉反应,其原因可能是由汞和镉与螯合剂螯合后形成的空间构型极为相似造成[8]。本试验得到的重金属镉抗体与其他金属螯合物的交叉反应率很低,这表明此抗体对于重金属镉螯合物有很强的特异性。

表1 抗体与金属EDTA螯合物的交叉反应Table 1 Cross-activities of the antibody with metal-chelates
2.3 水样品的处理
将自来水样品使用PBS分别稀释2倍,5倍,10倍,而河水样品使用滤膜过滤后也使用PBS进行稀释,与建立的标准曲线进行对比,由图2和图3可知,自来水和河水样品使用0.01mol/L的PBS稀释5倍后,样品的基质曲线和重金属镉标准曲线重合,即可消除基质影响。本试验两种水样都是使用PBS稀释5倍后基质影响消除而非其他倍数,可能是水样中离子强度也会影响基质曲线与标准曲线的重合。

图2 自来水样品的基质影响消除Figure 2 Elimination of matrix effect in tap water samples

图3 河水样品的基质影响曲线Figure 3 Elimination of matrix effect in river water samples
2.4 回收率
分别向自来水和河水样品中添加一定浓度的重金属镉进行回收率的测定,见表2。

表2 间接竞争酶联免疫法重金属镉的回收率Table 2 Recovery of heavy metal cadmium using indirect competitive enzyme-linked immunosorbent assay
由表2可知,自来水和河水中镉的平均回收率在93.95%~107.40%,变异系数在3.97%~14.69%。以上结果表明本试验建立的间接竞争酶联免疫检测法有较高的准确度和精确度,适用于水样品中重金属镉的分析。
3 结论
本试验成功制得了针对重金属镉的高特异性多克隆抗体,以此建立了水样中重金属镉的间接竞争酶联免疫分析方法。水样直接进行稀释即可用于检测,有效提高了检测效率。本方法可以用于水样品中重金属镉的现场筛选和检测。
1 Diane A Blake,R Mark Jones,Robert C Blake II.Antibodybased sensors for heavy metal ions[J].Biosensors and Bioeletronics,2001,16(9):799~809.
2 Mehraban Khosraviani,Andrey R Pavlov,George C.Flowers:detection of heavy metals by immunoassay:optimization and validation of a rapid,portable assay for ionic cadmium[J].Environmental Science Technology,1998,32(1):137~142.
3 唐勇,向军俭,罗辉武,等.重金属镉离子单克隆抗体的制备[J].食品科学,2005,26(9):350~353.
4 王志坤,徐建伟,郭明.重金属镉离子检测技术研究进展[J].食品工程,2008,2(6):62~65.
5 Ibrahim A Darwish,Diane A Blake.One-step competitive immunoassay for cadmium ions:development and validation for environmental water samples[J].Analytical Chemistry,2001,73(8):1 889~1 895.
6 吕彩云.重金属检测方法研究综述[J].资阳开发与市场,2008,24(10):887~898.
7 吴晓萍,廖爱琳,章超华,等.企鹅珍珠贝Cd-MT的酶联免疫检测试剂盒的研制[J].食品与机械,2011,27(5):107~110.
8 唐勇,王建华,向军俭,等.镉离子单克隆抗体的鉴定与竞争ELISA的建立[J].免疫学杂志,2009,25(2):214~217.
Development of heavy metal cadmium in water samples by indirect competitive enzyme-linked immunosorbent assay
WANG Jin SHENG Wei WANG Jun-ping FANG Shu-bing
YANG Yi-jin ZHANG Shu-guang WANG Shuo
(Key Laboratory of Food Nutrition and Safety,Tianjin University of Science and technology,Tianjin300457,China)
An indirect competitive enzyme-linked immunosorbent assay was developed to low instrument cost detect cadmium in water samples using the polyclonal antibody.The limit of detection(IC15)was 0.76μg/L,and the sensitivity(IC50)was 11.33μg/L.The cross-reactivity rates of the antibody with other metals(Mn,Cr,Mg,Fe,Pb,Ni,Ag and Cu)chelates were below 1.32%,except for Hg-chelate with a cross-reactivity rate 10.9%.The recoveries of cadmium in spiked tap water and river water were 93.95%~107.40%,and the coefficients of variation were 3.97%~14.69%.
cadmium;heavy metals immunological detection method;polyclonal antibody;ELISA;tap water;river water
10.3969/j.issn.1003-5788.2012.03.023
王津(1987-),女,天津科技大学在读硕士研究生。E-mail:choupiyuanyuan@163.com
王硕
2011-12-01
