复合垂直流湿地去除模拟河水中氮磷的研究
2012-12-25刘婧邢奕金相灿卢少勇郭家盛
刘婧,邢奕,金相灿 ,卢少勇,郭家盛
1.北京科技大学土木与环境工程学院,北京 100083
2.中国环境科学研究院湖泊工程技术中心湖泊环境创新基地,北京 100012
随着湖泊富营养化程度的加剧,对氮磷入湖负荷的削减日益紧迫,针对水体富营养化问题我国开展了大量工作。相对于其他污水处理工艺而言,人工湿地系统具有建设和运行费用低,氮磷去除能力强,维护管理简便,耐冲击负荷能力强等优点[1-3],是适合污染河水处理的一项重要技术。复合垂直流湿地是近年来兴起的新型湿地技术,由下行流池和上行流池组成,通过系统中物理、化学和生物过程的协同,去除水中的污染物[4]。
1 材料与方法
1.1 湿地装置
人工湿地模拟装置由4个等体积池组成,为两组下行-上行流湿地单元,1#池和2#池构成前部单元,3#池和4#池构成后部单元,单池尺寸为0.4 m×0.4 m×1.0 m。池内填充沸石填料,1#池和4#池填料粒径为5~6 cm,填充高度均为0.35 m,2#池和3#池填料粒径为1~2 cm,填充高度分别为0.70和0.35 m;4个池的水面高度均为0.70 m。湿地装置表面未种植植物,1#池设进水管(供给原水),4#池设出水管。在湿地装置沿程设5个取样点,原水桶中设1个取样点,研究湿地各出水指标随时间及沿程的变化(图1)。
1.2 运行参数
湿地系统置于温室内(平均室温25℃),原水自原水桶经蠕动泵泵入1#池内,水力负荷为0.375 m3/(m2·d)。系统采用间歇进水方式运行,其中进水运行期为10 d(前3.5 d为进水期,之后为运行期,第10天排水),排空闲置期为2 d(系统自然复氧),周期性干湿交替以促进湿地的硝化和反硝化[6-8]。装置于2008年开始投入运行,笔者的试验周期为2010年9月17日—2011年1月20日。
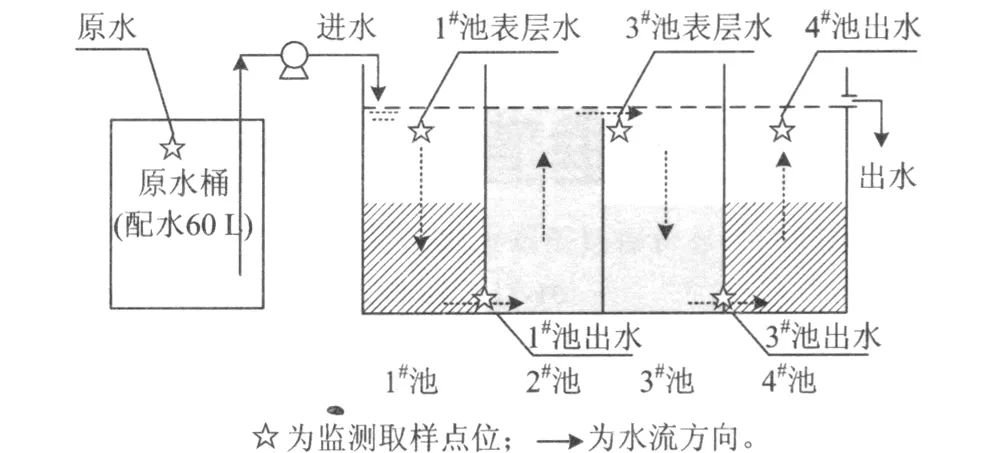
图1 复合垂直流湿地试验装置[5]Fig.1 Experimental equipment of integrated vertical flow constructed wetland
1.3 试验水质
模拟太湖梅梁湾入湖河水的CODMn和氮、磷浓度,人工配制原水(进水)置于原水桶内。进水中的有机物(以 CODMn计),氨氮(NH3-N),硝态氮(NO3--N)和总磷〔TP,以磷酸盐(PO43-)计〕分别用分析纯的葡萄糖(国药集团化学试剂有限公司)、氯化铵(西陇化工股份有限公司)、硝酸钾(天津市津科精细化工研究所)和磷酸二氢钾(天津市赢达稀贵化学试剂厂)固态药剂配制,进水水质监测值如表1所示。
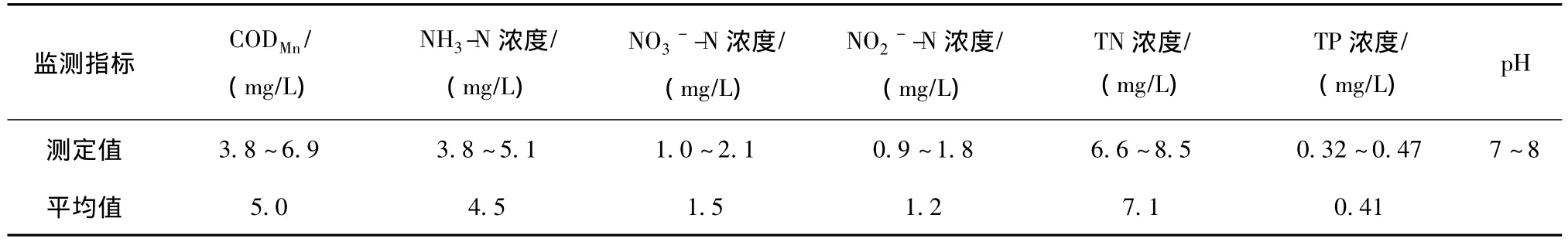
表1 复合湿地进水水质Table 1 Characteristics of influent water in integrated wetland system
1.4 监测方法
测定指标包括进出水的理化参数,氮磷浓度等,各指标的测试方法如表2所示[9]。
2 结果与讨论
2.1 湿地系统水质理化参数
每次采集水样时,现场测定系统进出水理化参数,包括DO浓度,pH及水温等。
2.1.1 DO浓度
系统进出水与各池表层水DO浓度变化如图2所示,由图2可知,湿地中水体的DO浓度随时间变化明显,08:00最低,之后渐升,16:00出现最高值,随后缓降。DO浓度的变化趋势与光照规律一致,表明湿地系统表层水的DO浓度受光照的影响。

表2 水质监测方法Table 2 Methods of monitoring water quality
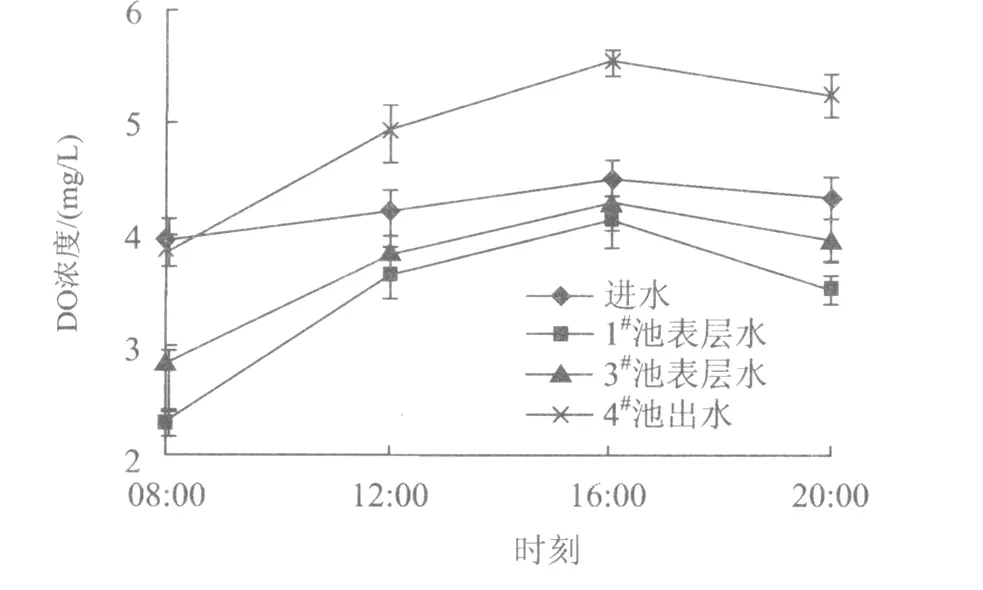
图2 系统进出水与各池表层水DO浓度随时间的变化Fig.2 Variation of DO along the time
图2显示1#~4#池表层水的DO浓度依次升高,这与湿地系统CODMn的去除主要发生在前段有关。因系统正常运行时,其总耗氧量主要来自有机物的降解,而NH3-N被氧化为亚硝态氮和硝态氮所需氧量比例很低[10]。
2.1.2 pH
pH是湿地的重要理化指标之一,其过低、过高或波动太大对湿地微生物的活性影响较大。研究表明,人工湿地的pH为7.2~8.0时,利于硝化过程进行,反之,硝化过程会受抑制[11]。有学者[12]发现,在厌氧环境下湿地下部有机质降解后形成一些有机酸性物质,同时,植物生产、死亡和分解也产生一定的天然酸度,导致pH下降,当pH小于7.2时利于反硝化,系统pH变化如图3所示。由图3可知,该系统pH为7.5~7.8,出水pH约为7.6。试验进水有机物浓度较低,且未种植植物,pH在系统内变化不大,因此该湿地适于硝化反应进行。
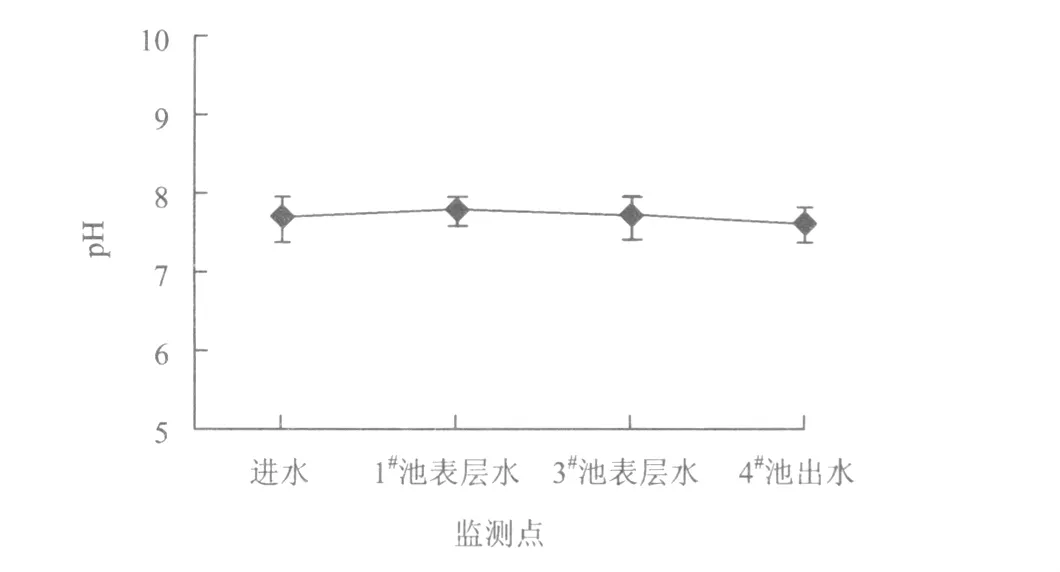
图3 系统pH沿程变化Fig.3 pH variation in flow pathway
2.1.3 温度
气温及系统水温随时间的变化,以及水温的沿程变化如图4所示。该装置位于温室中,温度较稳定,平均室温约25℃。由图4(a)可知,系统内部温度变幅低于外界温度变幅,湿地系统对水流有一定保温作用。这与文献[13-14]的观点一致;由图4(b)可知,水温在系统内沿程呈上升趋势,但变幅不大。
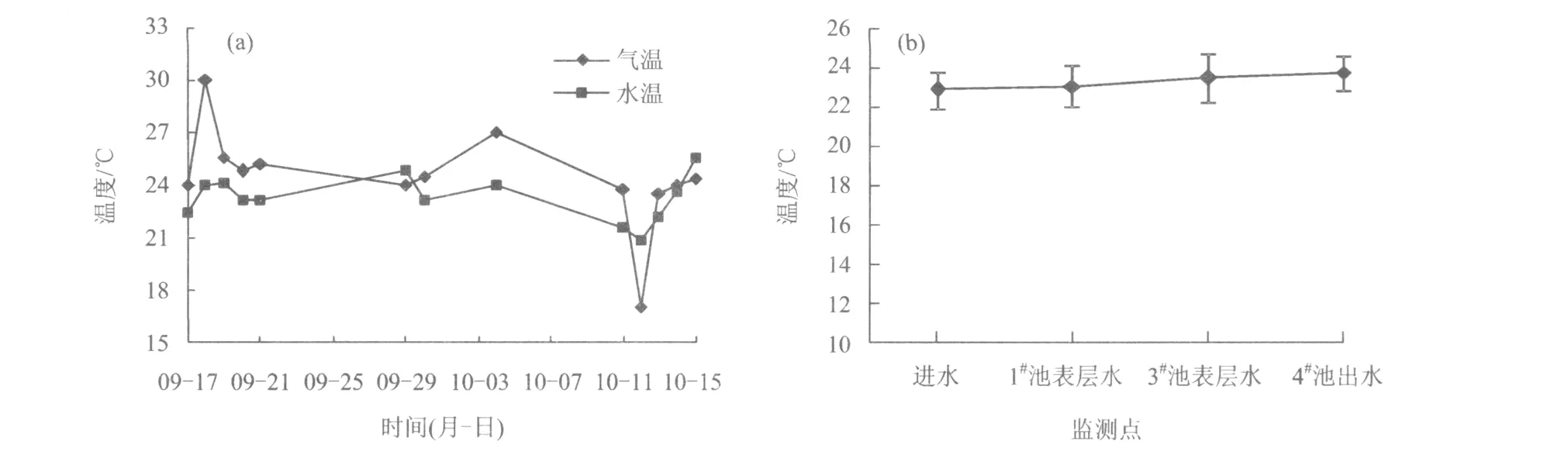
图4 气温及系统水温随时间的变化及水温的沿程变化Fig.4 Varying relationship between internal and external temperature and water temperature variation in flow pathway
2.2 CODMn、氮、磷的去除效果
2.2.1 CODMn的去除
系统进出水CODMn和去除率,及CODMn沿程变化如图5所示。由图5(a)可知,系统进水CODMn较低,平均约为5 mg/L,出水CODMn基本稳定,平均去除率大于75%;由图5(b)可知,进水中CODMn在1#池即被降解65%以上,此后CODMn在系统内部总体呈下降趋势,4#池出水约为1 mg/L,其主要是因为有机物浓度较低,且系统中的微生物群落死亡后会随出水流出,这些有机生物体,对出水CODMn有一定贡献。
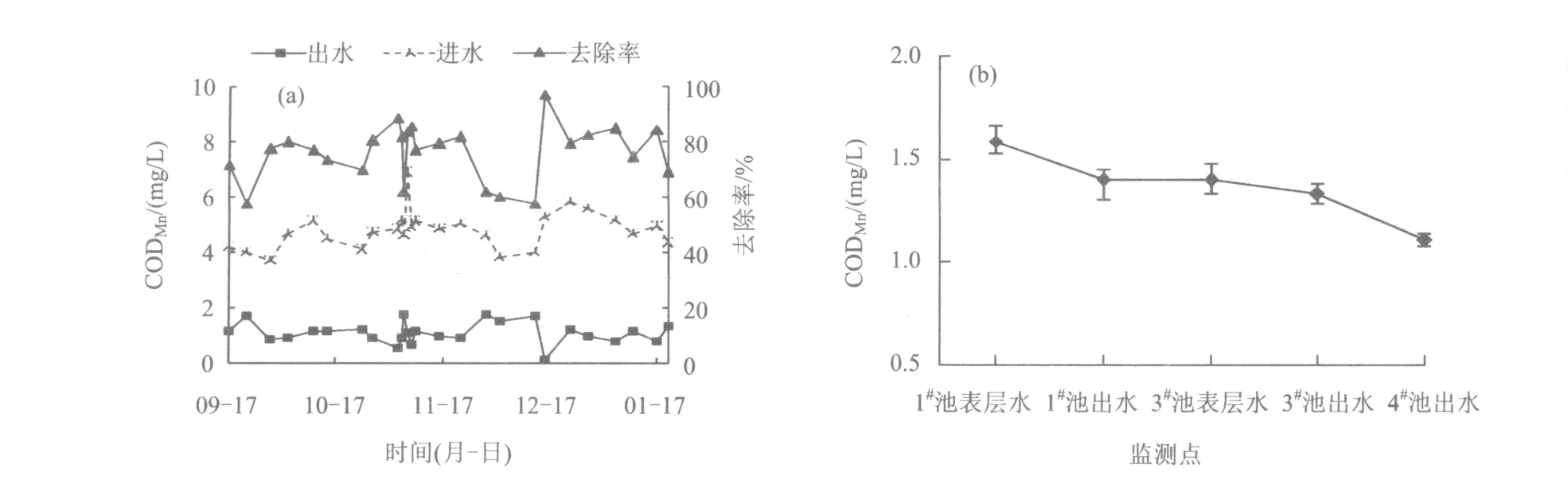
图5 系统进出水CODMn和去除率及CODMn沿程变化Fig.5 Variation of CODMn and CODMn removal efficiency and CODMn variation in flow pathway
2.2.2 氮的去除
2.2.2.1 NH3-N
系统进出水NH3-N浓度和去除率,及NH3-N浓度沿程变化如图6所示。连续监测数据〔图6(a)〕表明,系统对NH3-N的去除效果较好,进水平均浓度为4.50 mg/L,出水平均浓度为0.11 mg/L,达到GB 3838—2002《地表水环境质量标准》Ⅱ类标准,平均去除率为97.5%。从日均变化曲线〔图6(b)〕可见,对NH3-N的去除率前部单元为56.6%,后部单元为94.1%,系统NH3-N浓度呈连续下降趋势。主要是由于系统处于敞口状态,且间歇运行,周期性复氧,利于硝化作用进行。
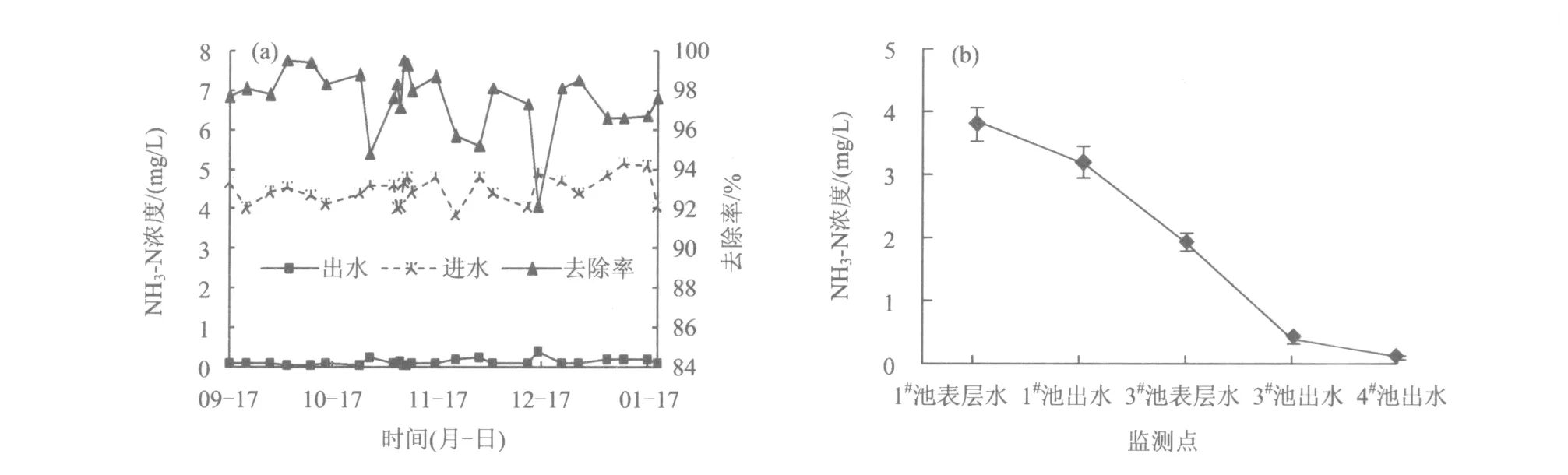
图6 系统进出水NH3-N浓度和去除率及NH3-N浓度沿程变化Fig.6 Variation of NH3-N concentration and NH3-N removal efficiency and NH3-N concentration variation in flow pathway
2.2.2.2 NO3--N
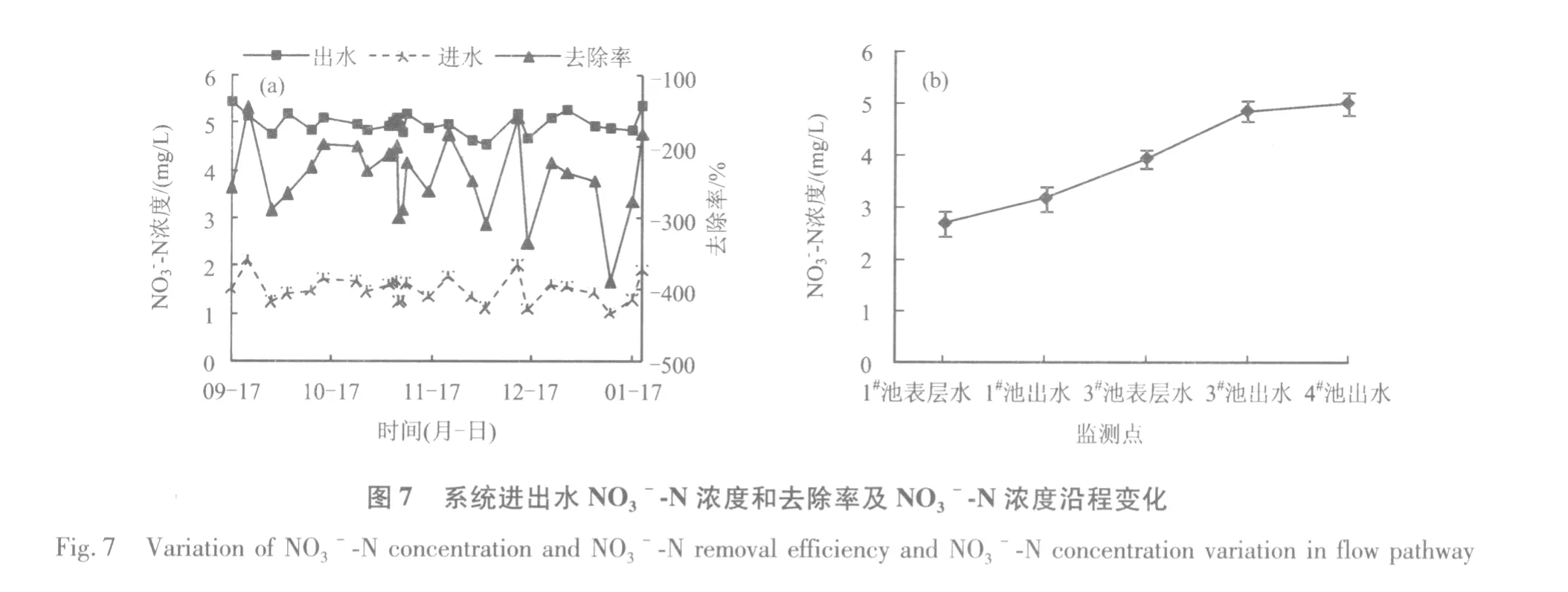
系统NO3--N进出水浓度和去除率,及NO3--N浓度沿程变化如图7所示。NO3--N浓度随水流方向渐升,系统进水、3#池表层水、4#池出水平均浓度分别为1.51,3.93和5.00 mg/L,可见 NO3--N在系统内逐步积累,出水中 NO3--N浓度约占TN的96.7%,因系统NO3--N的去除主要靠反硝化作用,反硝化耗能,需充足碳源[15]。通常,用于反硝化的最佳 C/N(碳以 CODMn计)为4 ~5[16]。由表1 可知,试验用水中的CODMn/TN小于1,水中有机物浓度低是限制反硝化作用,影响NO3--N去除率的一个重要因素。此外,反硝化菌常需厌缺氧条件,而该系统处于敞口开放状态,进水水质耗氧类物质负荷不高,供氧相对较好,因此,系统NO3--N去除效果不佳。
2.2.2.3 NO2--N
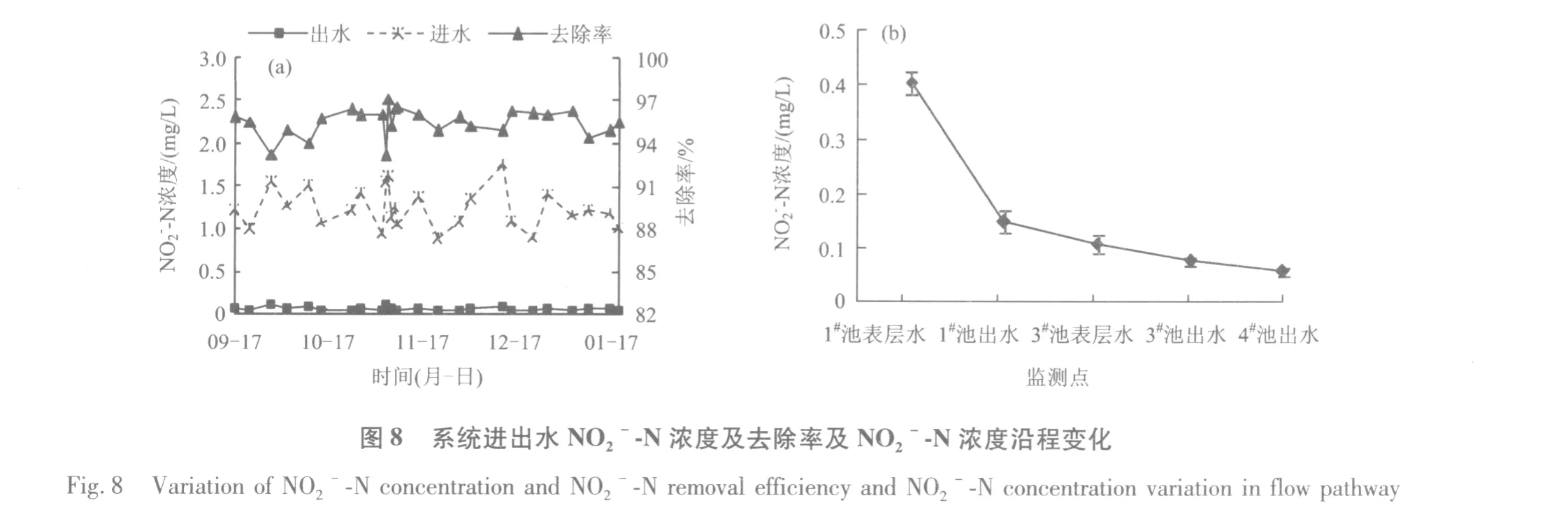
系统NO2--N进出水浓度和去除率,及NO2--N浓度沿程变化如图8所示。由图8(b)可知,NO2--N在湿地内部的浓度较低,为0~0.4 mg/L,前部单元NO2--N浓度较高,且沿程降低。在稳态条件下,通常,NO2--N是氨氧化菌在氧化NH3-N过程中产生的中间体,量很少[4],不会在湿地积累。就该湿地系统而言,相对于1#池表层对进水中N的去除率,前部单元下部NO2--N去除弱;而后部单元出水中,NO2--N浓度略低,这可能是由于前部单元溶解氧相对较低使硝化反应不充分。总体上,该系统 NO2--N积累不多,NH3-N降解产生的NO2--N很快被硝化细菌转化为NO3--N。
2.2.2.4 TN
系统TN进出水浓度和去除率,及TN浓度沿程变化如图9所示。由图9(a)可知,系统进出水TN平均浓度分别为7.13和5.23 mg/L,系统TN最高去除率为39.4%,平均去除率为26.6%。垂直流湿地的硝化作用虽强,但其只改变了氮形态[17],而反硝化作用受抑制,影响TN的去除;且系统进水氮形态影响TN去除率[18],进水氮形态以NH3-N为主的TN去除率较以NO3--N为主的低。
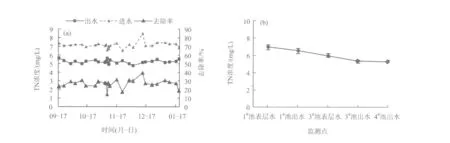
图9 系统进出水TN浓度和去除率及TN浓度沿程变化Fig.9 Variation of TN concentration and TN removal efficiency and TN concentration variation in flow pathway
由图9(b)可知,受进水中NH3-N和NO3--N浓度总和的影响,通常湿地前部单元的TN浓度较高。在湿地后部单元,NH3-N大部分被降解,NO3--N为主要形态,此时TN浓度有一定程度下降。但出水中TN降解不多,这与水中低CODMn有关,反硝化作用因缺少碳源而受抑制[19]。湿地系统对氮有吸收作用,且NH3挥发与pH有关,当pH小于8.0时,NH3从湿地中通过挥发损失并不严重;pH为9.3时,NH3与 NH4+的比例为1∶1,通过挥发造成的NH3-N损失显著[20]。由于该系统未种植植物且pH为7.5~7.8,故可忽略植物吸收及NH3挥发对氮的去除。该系统已连续运行两年以上,内部沸石的吸附位有一定程度的减少。该系统中硝化反硝化作用为重要的除氮途径,且硝化作用强于反硝化作用。
2.2.2.5 强化建议
有研究[21-22]表明,通过投加外加碳源(甲醇)能显著提高反硝化效果,但存在运行管理复杂和成本高等弊端。枯叶层是湿地反硝化进行的重要场所[23],因此,针对湿地系统反硝化作用受抑制导致NO3--N去除率较低的状况,通过投加一定量收割的或经预处理的枯叶,使其发酵释放易被生物利用的小分子有机物,提供反硝化所需碳源,提高反硝化能力;此外,可考虑在该系统中增加植物;还可通过出水回流的方式强化系统的出水效果。对NH3-N吸附饱和的湿地系统可将出水引入单独的吸附单元中,待吸附饱和后对其填料生物再生,并将再生水回流至系统处理。实际应用时可设若干组湿地单元交替运行,从而提高长期运行系统的除氮性能[24]。
2.2.3 TP的去除
系统进出水TP浓度和去除率,及TP浓度沿程变化如图10所示。由图10可知,出水TP浓度最大值为0.37 mg/L,最小值为 0.27 mg/L,平均值为0.33 mg/L。根据GB 3838—2002中的水质标准分类,进水属劣Ⅴ类水质,出水属Ⅴ类水质,提高了一个等级。
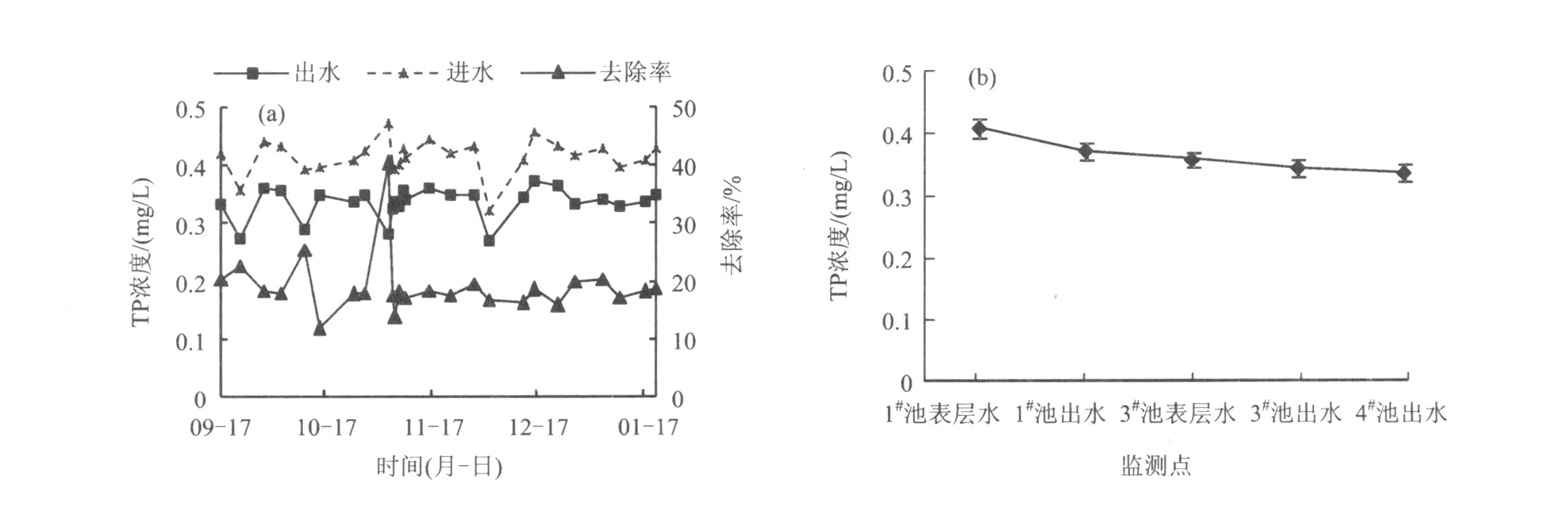
图10 系统进出水TP浓度和去除率及TP浓度沿程变化Fig.10 Variation of TP concentration and TP removal efficiency and TP concentration variation in flow pathway
Drizo等[25]研究表明,湿地中磷可通过基质吸附和化学沉淀、微生物吸收和积累、植物和藻的吸收去除。其中,最主要的是基质吸附和化学沉淀作用[26-27],该系统流程长,利于基质对磷的吸附和化学沉淀。由图10(a)可见,在整个系统中,除个别点外,磷去除率曲线较平直,未出现类似含氮化合物那样的变化,但沸石并非为磷的强吸附填料,因此,微生物作用是该系统中磷去除的重要贡献者之一。
该系统对TP的去除率不高,最高值为40.2%,平均值为18.9%,这是因为试验所用填料为沸石[28-29],在选沸石做湿地基质时,若要提高磷的去除率,可考虑强化除磷手段:1)增加湿地植物的生物量,增强植物除磷量;2)在不影响植物生长和不造成二次污染的前提下添加人工或天然的化学絮凝剂或沉淀剂[23]。由于系统已运行两年,并非新填料,虽干湿交替运行有助于磷吸附能力恢复,但总体上,沸石吸附位有一定程度的减少,此外沸石能促进难溶性磷的释放。
3 结论
(1)复合垂直流湿地对模拟河水中的NH3-N有较好的去除效果,平均去除率为97.5%。出水中TN和TP浓度也有所降低,平均去除率分别为26.6%和18.9%。出水CODMn基本稳定,平均去除率在75%以上。
(2)湿地下部因碳源缺乏抑制了反硝化,出水NO3--N浓度升高。
(3)湿地系统中未种植植物,且pH为7.5~7.8,可忽略植物吸收及NH3挥发对氮的去除。由于系统已连续运行两年以上,内部沸石的吸附位有一定程度减少,故系统填料对氮的吸附作用较低。硝化反硝化作用是该系统重要除氮途径,且硝化作用强于反硝化作用。
[1]LAI D Y F,LAM K C.Phosphorus sorption by sediments in a subtropical constructed wetland receiving storm water runoff[J].Ecological Eng,2009,35(5):735-743.
[2]CHUNG A K C,WU Y,TAM N F Y,et al.Nitrogen and phosphate mass balance in a sub-surface flow constructed wetland for treating municipal wastewater[J].Ecological Eng,2008,32(1):81-89.
[3]TEE H C,SENG C E,NOOR A M,etal.Performance comparison of constructed wetlands with gravel-and rice husk-based media for phenoland nitrogen removal[J].Sci Total Environ,2009,407(11):3563-3571.
[4]HE R,ZHOU Q,ZHANG J.Treating domestic sewage by the free water surface constructed wetlands[J].Ecology Environ,2004,13(2):180-181.
[5]CAI M M,ZHOU B H,LU S Y,et al.Characteristics of nitrogen and microorganism in integrated vertical-flow constructed wetland treating low pollution water[C]//2009 Beijing International Environmental Technology Conference.Beijing:[s.n.],2009.
[6]GUMBRICHT T.Nutrient removal process in freshwater submersed macrophyte systems[J].Ecological Eng,1993,2(1):29-30.
[7]卢少勇,桂萌,余刚,等.人工湿地中沸石和土壤的氮吸附与再生试验研究[J].农业工程学报,2006,22(11):64-68.
[8]卢少勇,金相灿,余刚.人工湿地的氮去除机理[J].生态学报,2006,26(8):2670-2676.
[9]国家环境保护总局.水和废水监测分析方法[M].北京:中国环境科学出版社,2002:200-284.
[10]吴树彪,张东晓,柳清青,等.潮汐流人工湿地床处理生活污水的优化研究[J].中国农业大学学报,2010,15(2):106-113.
[11]邓春光,蔡明凯.人工湿地脱氮性能优化分析及研究建议[J].节水灌溉,2007(4):10-12.
[12]王世和.人工湿地污水处理理论与技术[M].北京:科学出版社,2007:1-180.
[13]卢少勇,张彭义,余刚,等.农业排灌水稳定塘-植物床复合系统处理[J].中国环境科学,2004,24(5):605-609.
[14]付融冰,朱宜平,杨海真,等.连续流湿地中DO、ORP状况及与植物根系分布的关系[J].环境科学学报,2008,28(10):2036-2041.
[15]代嫣然,梁威,吴振斌.低碳高氮废水的人工湿地脱氮研究进展[J].农业环境科学学报,2010,29(增刊):305-309.
[16]HANAKI K,HONG Z,MATSUO T.Production of nitrous oxide gas during denitrification of wastewater[J].Water Sci Technol,1992,26(6):1027-1036.
[17]帖靖玺,郑正,钟云,等.潜流-上行垂直流复合人工湿地对氮磷去除效果[J].生态学杂志,2006,25(3):265-269.
[18]连小莹,金秋,李先宁,等.氮形态对人工湿地氮去除效果的影响[J].环境科技,2011,24(1):26-28.
[19]LIN Y F,JING S R,WANG T W.Effects of macrofhytes and external carbon sources on nitrate removal from groundwater in constructed wetlands[J].Environ Pollut,2002,119(3):413-420.
[20]高拯民,李宪法,王绍堂,等.城市污水土地处理利用设计手册[M].北京:中国标准出版社,1990.
[21]LABER J,PERFLER R,HABERL R.Two strategies for advanced nitrogen elimination in vertical flow constructed wetlands[J].Water Sci Technol,1997,35(5):71-77.
[22]刘刚,闻岳,周琪.人工湿地反硝化碳源补充研究进展[J].水处理技术,2010,36(4):1-5.
[23]ISENHART T M,CRUMPTON W G.The role of plantlitter in the transformation and fate of non-point source nitrate in freshwater wetlands[J].Bulletin Ecological Society America,1993,74(2):289.
[24]付融冰.强化人工湿地对富营养化水体的修复及作用机理研究[D].上海:同济大学,2007.
[25]TOUATY M,BONSANG B.Hydrocarbon emissions in a highway tunnel in the Paris area[J].Atmospheric Environ,2000,34(6):985-996.
[26]SAKADEVAN K, BAVOR H J.Phosphate adsorption characteristics of soils,lags and zeolite to be used as substrate in constructed wetland systems[J].Water Res,1998,32(2):393-399.
[27]卢少勇,金相灿,余刚.人工湿地的磷去除机理[J].生态环境,2006,15(2):391-396.
[28]袁东海,景丽洁,高士祥,等.几种人工湿地基质净化磷素污染性能的分析[J].环境科学,2005,26(1):51-55.
[29]贺凯,卢少勇,金相灿,等.五种填料对磷酸盐的等温吸附-解吸特性[J].农业工程学报,2008,24(8):232-235. ○
