羟基蛋氨酸钴螯合物稳定常数测定及其质量评价
2012-09-22丽盖利刚李宁李
马 丽盖利刚李 宁李 梅
(1.山东轻工业学院化学与制药工程学院,山东济南 250353;2.青岛宝博生物科技有限公司,山东青岛 266100)
在动物饲料和预混料产品中,羟基蛋氨酸可以等摩尔地转变成L-蛋氨酸;换言之,等摩尔的羟基蛋氨酸和D,L-蛋氨酸具有相同的生物学效价[1-2]。蛋氨酸是动物生长发育所必需的氨基酸,动物缺乏蛋氨酸会引起发育不良、体重减轻、肝肾机能减弱、肌肉萎缩、皮毛变质等[2-3]。钴是动物体内所必需的微量元素,是维生素B12极其重要的组成成分;钴可影响甲状腺代谢,能参与胆碱、蛋氨酸等的合成及脂肪与糖的代谢;钴还与其它微量元素(如锌、铜、锰等元素)有协同作用,能促进这些微量元素在动物体内的吸收[4-5]。钴作为中心离子能与羟基蛋氨酸螯合成羟基蛋氨酸钴,但这种新型的有机微量元素添加剂到目前为止鲜有报道[6-7]。
近来,我们实验室以价廉、低毒的醇水溶液为介质,以市售羟基蛋氨酸和氢氧化钴为原料,制得了羟基蛋氨酸钴,并对其进行了物相分析、形貌观测、表面元素分析及热稳定性考察[8]。有机微量元素螯合物的配位数和稳定常数是影响其生物学利用率的重要指标[9],能够为配合物结构的确定提供重要的信息;但是,由于羟基蛋氨酸微量元素螯合物的单晶很难培养,关于羟基蛋氨酸螯合物的化学结构到目前为止还没有可靠的数据,只能靠推测。本文采用分光光度法测定了羟基蛋氨酸钴样品的配位数和稳定常数,为合理推测其结构及评价其稳定性提供了依据。其次,采用自动电位滴定分析仪测定了样品中羟基蛋氨酸及羟基蛋氨酸钴的含量,对样品的质量进行了评价。本文的研究旨在为市场上同类产品的质量评价提供技术参考。
1 实验部分
1.1 试剂与仪器
化学试剂:氢氧化钠、邻苯二甲酸氢钾、六水合氯化钴(Ⅱ)、冰乙酸、浓盐酸(36%~38%)、五水合硫代硫酸钠、无水碳酸钠、重铬酸钾、碘化钾、浓硫酸、可溶性淀粉、溴酸钾、溴化钾、酚酞,以上试剂均为分析纯。市售88%的羟基蛋氨酸(MHA)由日本住友化学有限公司北方办事处提供。
实验仪器:KQ-700E型超声波清洗器(上海精密科学仪器有限公司生产),ZDJ-4A型自动电位滴定仪(上海永亨光学仪器制造有限公司生产),81-2型恒温磁力搅拌器(上海司乐仪器有限公司生产),DZF-6050型真空干燥箱(上海凯朗仪器设备厂生产),ESJ210-4A电子天平(上海先悦衡器设备有限公司生产),UV754A型紫外可见分光光度计(上海精密科学仪器有限公司生产)。
1.2 实验原理
1.2.1 羟基蛋氨酸钴稳定常数的测定
采用等摩尔数连续变化法(也叫浓比递变法或Job法)测定羟基蛋氨酸钴样品的稳定常数[10]。在保持溶液中金属离子浓度(cM)与配体浓度(cL)之和不变的前提下,改变cM和cL的相对量,配制一系列溶液。只有当溶液中金属离子与配体物质的量之比与配合物的组成一致时,配合物的浓度最大。用分光光度计测定上述一系列溶液的吸光值,以吸光值(A)为纵坐标,以摩尔分数(F)为横坐标作图,得吸光曲线。将曲线两边的直线部分延长相交,根据交点对应的横坐标值即可求出配合物MLn中配位体的数目n。
根据配合物离解平衡方程式(MLn=M+nL)和配合物的离解度(α)可确定表观稳定常数
1.2.2 羟基蛋氨酸及羟基蛋氨酸钴含量的测定
利用溴酸钾-溴化钾法[2,10-11]测定样品中羟基蛋氨酸的含量,并进而计算出样品中羟基蛋氨酸钴的含量。在酸性介质中,羟基蛋氨酸钴分解形成钴离子和羟基蛋氨酸阴离子。羟基蛋氨酸阴离子和溴酸钾-溴化钾标准溶液发生如下反应,见式(1)和(2):

进行电位滴定时,在待测液中插入一根铂和饱和甘汞电极组成的复合电极。随着KBrO3/KBr滴定液的加入,待测组分浓度不断变化,电极电位也发生相应的变化,在等电点附近发生电位突跃,以此确定滴定终点。
1.3 实验步骤
1.3.1 羟基蛋氨酸钴稳定常数的测定
1.3.1.1 羟基蛋氨酸水溶液的标定
称取约 8.6 g(精确至0.1 mg)市售羟基蛋氨酸,并将之全部转移至1 000 ml容量瓶中,用除去CO2的蒸馏水稀释、定容、摇匀;移取50 ml羟基蛋氨酸水溶液,加入2滴1%的酚酞指示剂,用按国标GB/T 601—2002规定的方法标定的NaOH标准溶液(0.091 8 mol/l)滴定至溶液由无色变为粉红色,并在30 s内不褪色。平行滴定三次并做空白实验。
1.3.1.2 吸光值的测定
配制与步骤1中羟基蛋氨酸水溶液浓度相同的氯化钴(Ⅱ)水溶液。按表1所示的体积比配制一系列混合溶液,分别用步骤1中的NaOH标准溶液调溶液的pH值约为6.5,然后稀释至60 ml;在85°C将混合溶液加热回流2 h,冷却至室温,测其290 nm处的吸光值。
1.3.2 羟基蛋氨酸及羟基蛋氨酸钴含量的测定
按国标GB/T 21034—2007规定的方法测定。称取约0.5 g(精确至0.1 mg)干燥的羟基蛋氨酸钴样品,置于100 ml烧杯中,加入50 ml混酸溶液(冰乙酸:水:浓盐酸=50:10:3,体积比),超声溶解后将烧杯置于磁力搅拌器上。将电极插入溶液中,调节搅拌速率至溶液平稳涡旋,用按国标GB/T 601—2002规定的方法标定的溴酸钾-溴化钾标准溶液(0.105 1 mol/l)滴定。当电位出现变化时,减慢滴定速率,当电位值发生突跃时,即为滴定终点,记录滴定溶液的体积。平行滴定三次。
3 结果与讨论
3.1 羟基蛋氨酸钴配位数及稳定常数的确定
经测定,羟基蛋氨酸水溶液的浓度为0.044 3 mol/l;因此,准确称取1.581 0 g六水合氯化钴(II),并将之溶解于150 ml除去CO2的蒸馏水中,以使配体溶液的浓度和金属离子溶液的浓度相等。对序号为5的溶液进行全波长扫描(200~800 nm),确定出最佳吸收峰出现在290 nm处,依次对所有溶液进行290 nm的单波长扫描,记录不同体积分数溶液的吸光值(见表1)。以吸光值为纵坐标,溶液中金属离子的摩尔分数{c(M)/[c(M)+c(L)]}为横坐标作图,得吸光曲线图(见图1)。
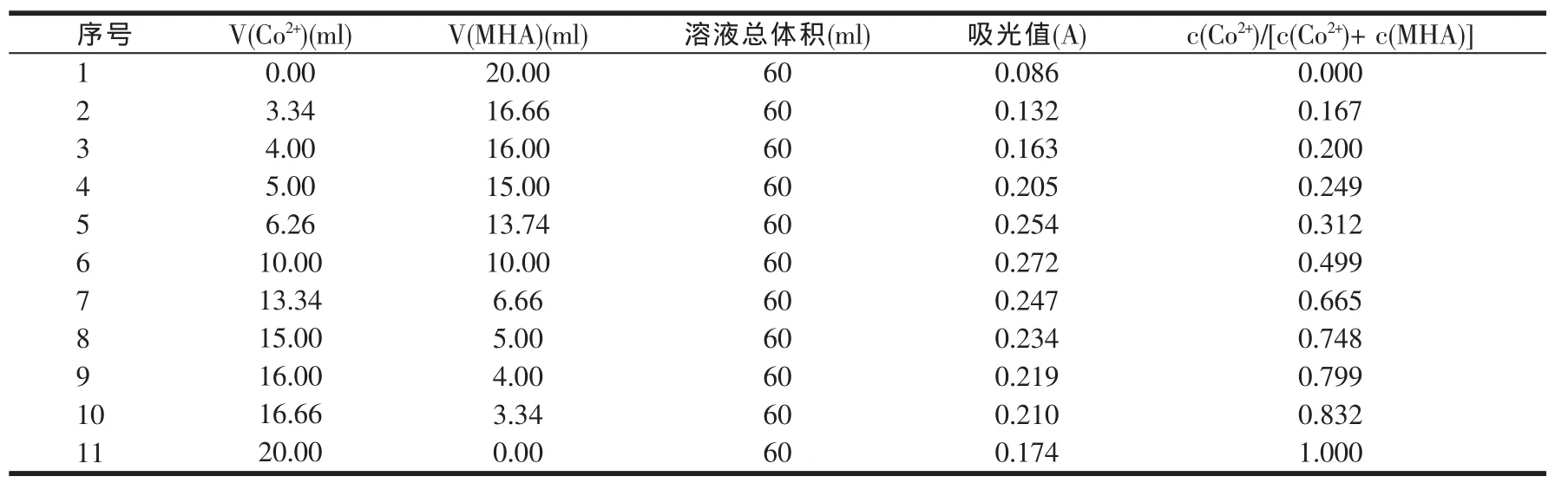
表1 配合物溶液配制及吸光值
由图1可以看出,吸光曲线两边直线部分延长相交于B点,B点对应金属离子的质量分数为0.355,即:c(M)/[c(M)+c(L)]=0.355,则:c(L)/c(M)=1.82≈ 2。考虑到羟基蛋氨酸根离子中α-羟基和羧酸根中的氧可与钴(II)离子形成稳定的五元环螯合物,则羟基蛋氨酸钴螯合物的配位数为4,这说明我们所推测的羟基蛋氨酸钴的结构式是合理的[8]。
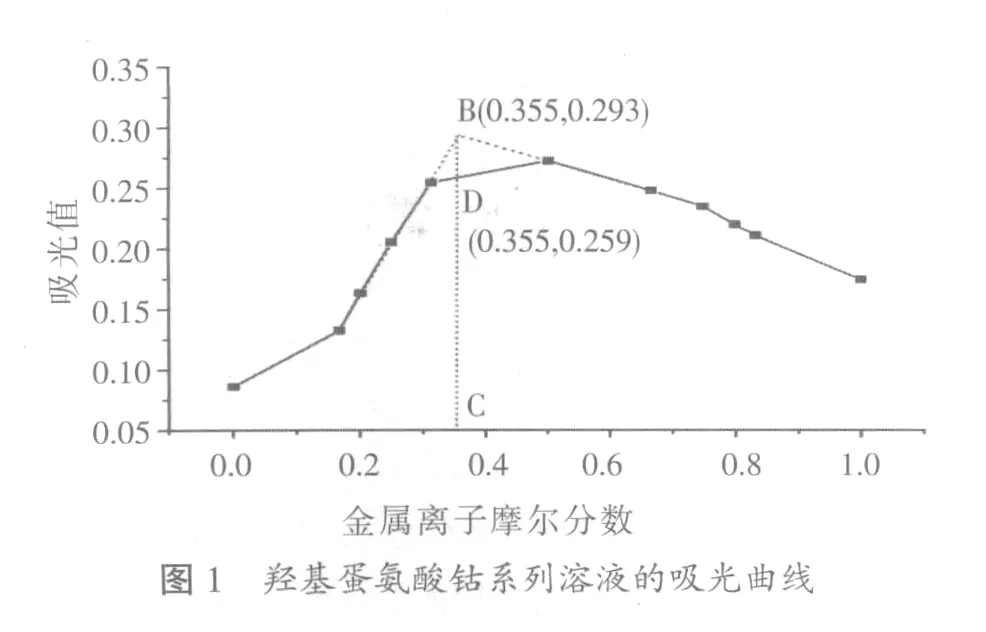
直线BC与吸光曲线相交于D点,由此可确定配合物的离解度α=(0.293-0.259)/0.293=0.116。B点对应的配合物浓度c=0.0443×0.355×20/60=5.24×10-3mol/l,则配合物的表观稳定常数为[(2×5.24×10-3)1.82×0.1162.82]=4.71×105.46。
配合物稳定常数测定的仪器分析方法主要有电化学法、分光光度法、色谱法和毛细管电泳法等,各种方法各有优缺点。其中,分光光度法和电位法相比,虽然准确性较差,但具有操作方便、检测迅速、溶液选择的范围广等优点[12]。虽然羟基蛋氨酸钴在蒸馏水中的溶解度较小,室温下约为0.8 g;实验结果表明,只要控制配合物溶液的浓度小于2.24×10-2mol/l,采用分光光度法测定羟基蛋氨钴螯合物的稳定常数是可行的。
3.2 羟基蛋氨酸和羟基蛋氨酸钴含量的测定
表2是采用自动电位滴定仪测定的羟基蛋氨酸钴样品中MHA含量实验数据表。根据反应式(1)和(2)可以确定样品中MHA的质量百分含量其中,c为KBrO3-KBr标准溶液的浓度(0.105 1 mol/l),M1为羟基蛋氨酸的摩尔质量(150.2)。由表2可见,样品中MHA的平均质量百分含量为83.20%,且偏差均小于0.5%,说明采用溶剂热法所制备的羟基蛋氨酸钴远比采用水热法所得的产物质量高[8,13]。

表2 样品中羟基蛋氨酸含量实验数据
表3是样品中羟基蛋氨酸钴含量实验测定数据表。根据反应式(1)和(2)及上述羟基蛋氨酸钴配位数的计算结果,可以确定样品中羟基蛋氨酸钴的质量百分含量,其中,M2为羟基蛋氨酸钴的摩尔质量(357.33)。由表3可见,样品中羟基蛋氨酸钴的平均含量高达98.97%,且各种偏差均小于0.5%。结合表2的实验数据,充分说明采用溶剂热法能够制得高质量的羟基蛋氨酸钴。
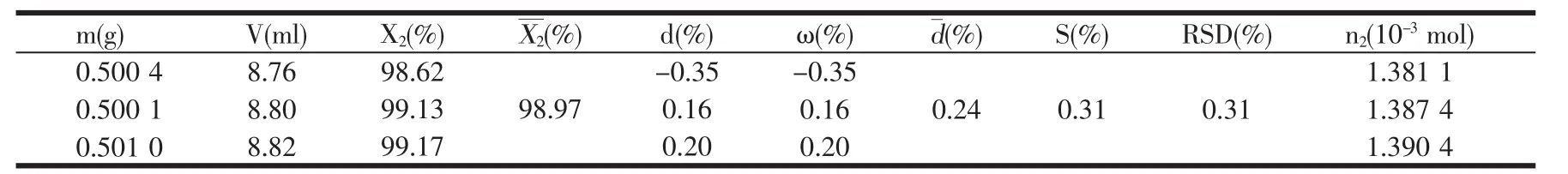
表3 样品中羟基蛋氨酸钴含量实验数据
4 结论
采用分光光度法测定了羟基蛋氨酸钴样品的表观稳定常数,采用自动电位滴定法测定了样品中羟基蛋氨酸及羟基蛋氨酸钴的含量。研究结果表明:羟基蛋氨酸钴样品的表观稳定常数为4.71×105.46,样品中羟基蛋氨酸的含量为83.20%,羟基蛋氨酸钴的含量为98.97%,结合分光光度法和自动电位滴定法对羟基蛋氨酸类似物进行质量评价,方法简单,操作方便,实验数据误差小、重现性好,可以作为同类产品生产企业日常质量检验的技术参考。
[1]H.Willemsen,Q.Swennen,N.Everaert,et al.Effects of dietary supplementation of methionine and its hydroxy analog D,L-2-hydroxy-4-methylthiobutanoic acid on growth performance,plasma hormone levels,and the redox status of broiler chickens exposed to high temperatures[J].Poult.Sci.,2011,90(10):2311-2320.
[2]徐丽丽,冯亚华,赵颖俊,等.自动电位滴定法测定羟基蛋氨酸钙[J].分析实验室,2009,28:57-60.
[3]B.G.Kim,M.D.Lindemann.Effect of methionine hydroxy analogfree acid on growth performance and chemical composition of liver of broiler chicks fed a corn-soybean based diet from 0 to 6 weeks of age[J].Anim.Sci.,2006,77(1):95-102.
[4]L.W.Cunningham,R.L.Fischer,C.S.Westling.The binding of zinc and cobat by insulin[J].J.Am.Chem.Sci.,1955,77:5703-5707.
[5]E.E.Roginski,W.A.Mertz.A biphasic response of rats to cobalt[J].J.Nutr.,1977,107:1537-1542.
[6]H.J.Hsu.Metal amino acid chelate[P].US Patent,5504055,1996.
[7]K.H.Lee,S.B.Lee,Method for preparation of organic chelate[P].US patent,7087775B2,2006.
[8]韩小云,陈鑫成,盖利刚,等.羟基蛋氨酸钴螯合物的制备及表征[J].饲料工业,2011,投稿.
[9]高占峰,吕林,李素芬,等.有机微量元素络(螯)合物的结构特征稳定性及其生物学意义[J].微量元素与健康研究,2008,25(3):50-54.
[10]陈虹锦,马荔,黄孟娇.实验化学[M].科学出版社,2003:8.
[11]张丽英,贺平丽,杨文军,等.羟基蛋氨酸钙含量测定方法比较研究[J].中国饲料,2005(19):26-28.
[12]袁佩,夏之宁,刘勇.络合物稳定常数测定的仪器分析方法[J].分析测试学报,2001,20(1):79-83.
