还原钛铁矿中金属铁锈蚀反应速率过程的强化
2012-07-31郭宇峰刘霞邱冠周姜涛
郭宇峰,刘霞,邱冠周,姜涛
(中南大学 资源加工与生物工程学院,湖南 长沙,410083)
现阶段具有利用价值的钛矿物主要是金红石和钛铁矿[1]。随着钛工业的发展,金红石资源逐渐枯竭,价格低廉的钛铁矿已成为钛工业的主要生产原料,但钛工业生产直接使用钛铁矿为原料,存在着设备产能低、流程长、“三废”量大和成本高等问题,一般需先将其制成高钛渣或人造金红石等富钛料产品,尤其是代表钛工业发展方向的氯化法钛白和海绵钛生产更是要求使用高品位的富钛料为原料[2-3]。已研究和提出的钛铁矿制取富钛料的方法主要有电炉熔炼法、选择氯化法、酸浸法、还原锈蚀法和还原磁选法等,目前在工业上获得应用的主要是电炉熔炼法、酸浸法和还原锈蚀法[4-5]。其中,还原锈蚀法因具有电耗少、化学试剂用量少、可利用廉价的褐煤、生产成本较低,并且在锈蚀过程中排出的废水接近于中性(pH=6.0~6.5)易于处理、污染小等优点[6],显示出了广阔的应用前景,但是,该方法存在锈蚀时间长和生产效率低的问题[7]。为了加快锈蚀反应速率,国内外学者做了大量研究,近期的研究表明,还原钛铁矿在锈蚀过程中添加一定数量的酸和提高氧势可以强化锈蚀过程,加快锈蚀速率。Jaya等[8-9]研究了印度砂矿锈蚀强化,结果表明锈蚀反应4 h后,添加甲醇+甲酸锈蚀率由51%提高到 86%,丙酮+甲酸锈蚀率达到 90%。Marinovich等[10]证明乙二醛、蔗糖和葡萄糖在锈蚀反应中由于氧化反应生成相应的羧酸,从而促进了锈蚀反应的速率。蒋云龙[11]提出在锈蚀反应时,添加1.5%盐酸后金属铁的锈蚀率比不添加盐酸的高30%以上。因此认为,酸有助于还原钛铁矿中金属铁锈蚀反应的进行。马晓文[12]提出采用纯氧替换空气,提高氧势,提高铁的阴极反应强度,锈蚀反应时间由8 h缩短为2 h。国内外学者对这2种方法强化锈蚀速率过程的内在反应机理并没有进行深入研究。在此,本文作者研究在NH4Cl溶液体系下盐酸和氧气对还原钛铁矿中金属铁锈蚀反应过程和钛铁分离效果的影响。通过锈蚀液成分分析,探讨盐酸和氧气在提高还原钛铁矿中金属铁的锈蚀反应速率和钛铁分离效果中的作用,同时对氧气强化锈蚀反应动力学过程进行研究,以揭示氧气强化还原钛铁矿中金属铁的锈蚀反应机理。
1 实验
1.1 原料
锈蚀试验所用还原钛铁矿是以攀枝花钛铁矿精矿为原料经压团烘干后在900 ℃下恒温预氧化15 min,以烟煤(灰分4.74%,挥发分37.22%,固定碳57.07%,质量分数)为还原剂,在还原温度为1 100 ℃,还原时间为2 h的条件下制备的,其主要化学成分见表1。锈蚀试验前将其破碎至粒径在0.147 mm以下。
试验所用的化学试剂为氯化铵和体积分数为30%的盐酸,气体为空气和氧气,氯化铵和盐酸为分析纯试剂,氧气体积分数为99.5%。
1.2 试验方法及装置
还原钛铁矿锈蚀试验采用的试验装置见图 1。以1 L三口烧瓶作为反应器,水浴锅用于恒温加热,冷凝管用于保持锈蚀体系液面。基准试验时,反应器中加入100 mL水,待水温升到60 ℃后恒温15 min,加入氯化铵,将溶液中氯化铵质量分数调整为1.6%,随后加入还原钛铁矿,其加入量按液固质量比10:1控制,通入空气搅拌并开始计时,搅拌速度控制在 400 r/min。盐酸强化试验时,在添加还原钛铁矿后加入盐酸,将溶液中盐酸体积分数调整为 2%。氧气强化试验时,采用氧气替换空气。锈蚀反应结束后,采用锈蚀率来衡量还原钛铁矿中金属铁的锈蚀程度。采用摇床重选将铁红和富钛料分离,用富钛料中TFe和TiO2的品位作为评价钛铁分离效果的判据。

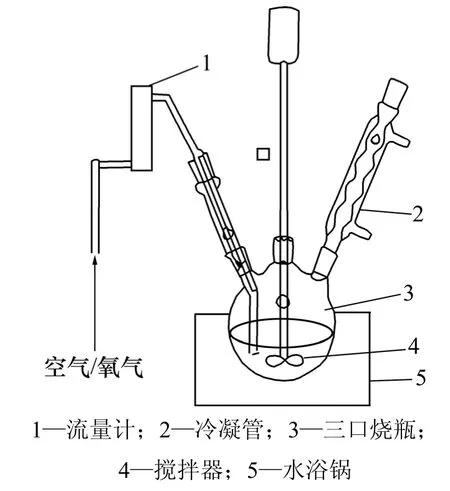
图1 锈蚀装置示意图Fig.1 Schematic of equipment of rusting process
2 结果与讨论
2.1 盐酸和氧气对锈蚀过程的影响
在NH4Cl溶液体系下,盐酸和氧气对还原钛铁矿锈蚀过程中金属铁的锈蚀率和钛铁分离效果的影响试验结果见表 2。在试验过程中,通气速率为 15×103L/(min·m3),锈蚀反应时间为 1 h。
由表2可知:加入盐酸和氧气后,还原钛铁矿中金属铁的锈蚀率可由 57.28%分别提高到 86.10%和85.36%。还原钛铁矿锈蚀产物经分离所得铁的质量分数由21.14%分别降为13.32%和15.79%,TiO2质量分数由65.89%分别提高到74.86%和71.46%。这表明:盐酸和氧气能有效提高还原钛铁矿中金属铁的锈蚀反应速率并且改善钛铁分离效果。

表2 盐酸和氧气对锈蚀率和钛铁分离效果的影响Table 2 Effect of Hydrochloric acid or oxygen on corrosion rate and ferrotitanium separation
钛铁矿还原锈蚀法制取富钛料的目的是使还原钛铁矿中的金属铁在NH4Cl溶液体系中借助于通入的空气发生锈蚀反应从而转化为铁红,然后,通过物理分选实现钛铁分离。在整个过程中,还原钛铁矿溶出,特别是铁溶出对锈蚀过程是不利的,因为这将影响锈蚀液的处理和铁的回收。为考查锈蚀过程中添加盐酸和通入氧气后还原钛铁矿是否发生溶出反应,对试验所得锈蚀产物进行分析,结果见表3。

表3 盐酸和氧气对还原钛铁矿主要组分溶出率的影响(质量分数)Table 3 Effect of hydrochloric acid or oxygen on main component dissolving rate about reduced ilmenite %
由表3可以看出:在基准试验中,进入到锈蚀液中的铁很少,SiO2,Al2O3和MgO溶出率均较低,只有CaO溶出率较高,达到了64.13%。这表明该过程主要是还原钛铁矿中的金属铁转变为铁红的锈蚀反应和CaO的溶出反应。添加盐酸后,进入到锈蚀液中的铁显著增加,SiO2,Al2O3和MgO溶出率略有提高,CaO的溶出率提高到91.14%,该过程有大量铁以离子形态进入锈蚀液。表2中添加盐酸后金属铁的锈蚀率提高,部分原因是把此部分进入锈蚀液中的铁计算在内。这表明:添加盐酸后还原钛铁矿中金属铁的锈蚀反应发生了改变,有转变为浸出反应的倾向,这不利于钛铁矿还原锈蚀法制取富钛料。NH4Cl溶液体系中通入氧气后,各组分的溶出情况和基准试验效果基本相当,由此可以确定还原钛铁矿中金属铁在NH4Cl溶液中发生的锈蚀反应历程。结果表明:在NH4Cl溶液体系下,通入氧气可加快还原钛铁矿中金属铁锈蚀反应速率过程。
2.2 通氧速率对锈蚀过程的影响
还原钛铁矿中的金属铁在还原钛铁矿颗粒内部被氧化为氢氧化亚铁,即发生所谓的“原位锈蚀”,形成的锈蚀产物将在矿物颗粒内部沉淀,很难再从还原钛铁矿颗粒内部分离出来,直接影响钛铁分离效果[13]。为查明通氧对还原钛铁矿中金属铁锈蚀过程影响,进行了通氧速率试验,结果见表4。

表4 通氧速率对锈蚀率和钛铁分离效果的影响Table 4 Effect of ventilation rate on corrosion rate and ferrotitanium separation
由表4可知:当通氧速率由5×103L/(min·m3)增大到10×103L/(min·m3)时,还原钛铁矿锈蚀率和富钛料品位明显提高;当通氧速率增大到 20×103L/(min·m3)时,金属铁的锈蚀率提高幅度很小,并且富钛料品位明显下降。这表明:采用通入氧气作为NH4Cl溶液体系加快还原钛铁矿中金属铁锈蚀速率过程的强化措施时,通氧速率有一个适当的范围;当通氧速率过低时,不利于发挥通氧的强化作用,通氧速率过高时,可能会使氧气扩散到还原钛铁矿微孔内部,发生所谓的“原位锈蚀”效应,不利于后续的钛铁分离。
2.3 氧气强化锈蚀反应动力学分析
还原钛铁矿中金属铁的锈蚀过程属于液-固相反应,通常可以用“未反应核收缩模型”来描述[14]。对于液-固相反应的锈蚀过程,其反应过程由以下 3个环节组成:液膜表面的外扩散、产物/反应表面的内扩散和反应粒子表面的化学反应[15]。为了解还原钛铁矿中金属铁的锈蚀反应控制环节及探讨氧气强化锈蚀速率过程的机理,对通入空气和氧气的还原钛铁矿中金属铁锈蚀动力学进行研究。
锈蚀动力学试验时,氯化铵质量分数为1.6%,搅拌速率 400 r/min,液固比为 10:1,通空气速率为15×103L/(min·m3),通氧气速率 10×103L/(min·m3),试验所得还原钛铁矿中金属铁等温锈蚀曲线分别见图2和图3。
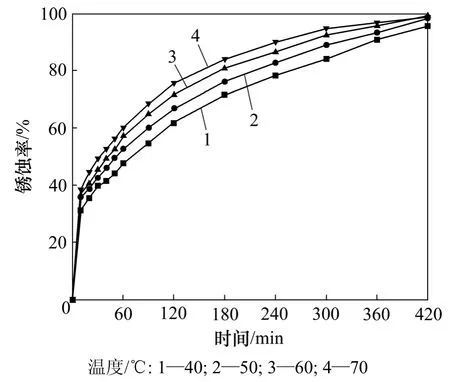
图2 空气中还原钛铁矿中金属铁等温锈蚀曲线Fig.2 Isothermal rusting curves of metallic iron in reduced ilmenite in air
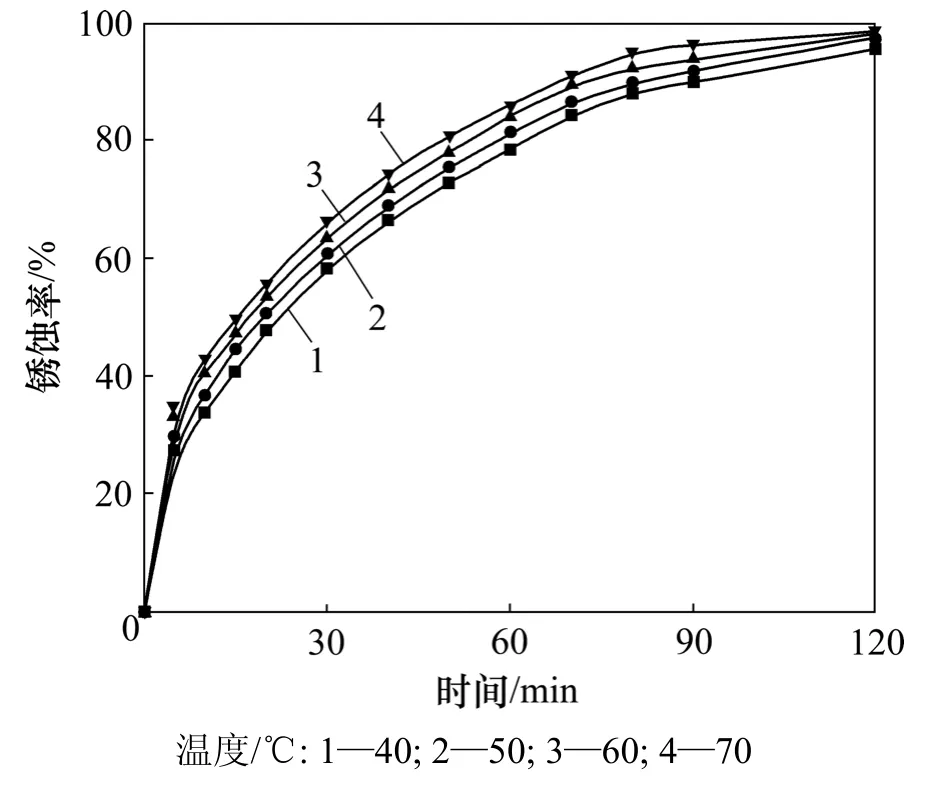
图3 氧气中还原钛铁矿中金属铁等温锈蚀曲线Fig.3 Isothermal rusting curves of metallic iron reduced ilmenite in oxygen
应用未反应核模型对还原钛铁矿锈蚀反应的等温试验结果进行分析,对图2和图3中锈蚀率r与时间t的关系分别以1-(1-r)1/3对时间t,1-2r/3-(1-r)2/3对时间t和以1+(1-r)1/3-2(1-r)2/3对t/1-(1-r)1/3作图。结果表明,在试验的温度范围内,1-2r/3-(1-r)2/3与时间t的线性关系最好,结果如图4和图5所示。这表明在试验温度范围内,该反应过程受内扩散控制。
由图4和图5中各直线的斜率可得出各温度下的速率常数k,见表5。
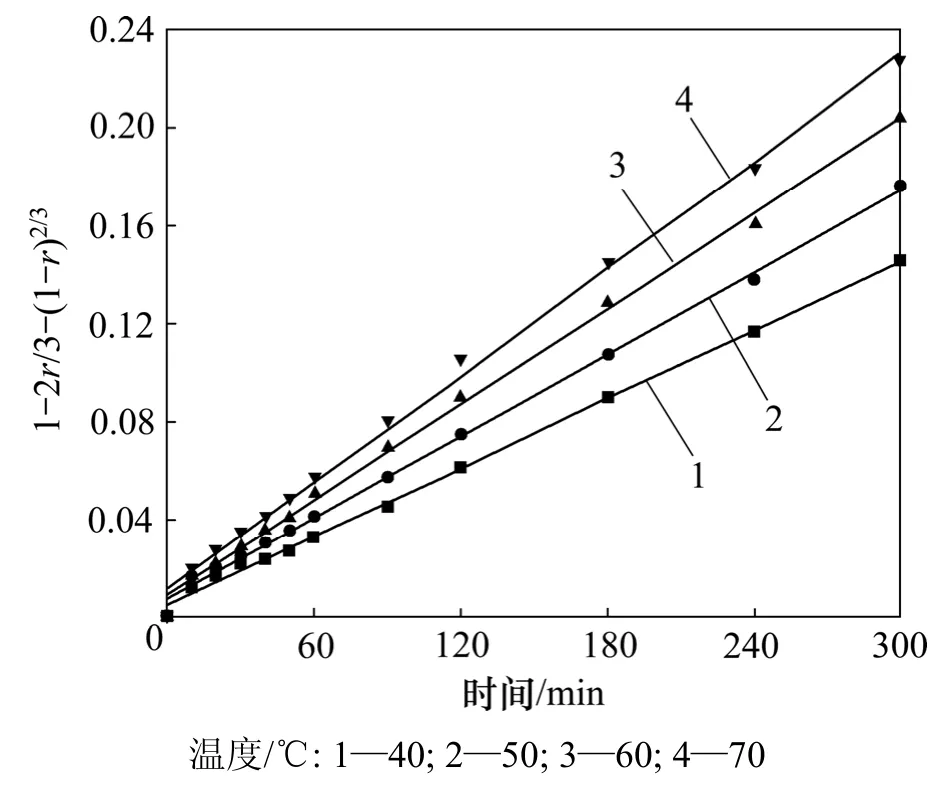
图4 空气中t与1-2r/3-(1-r)2/3的关系图Fig.4 Relationship between 1-2r/3-(1-r)2/3 and t in air
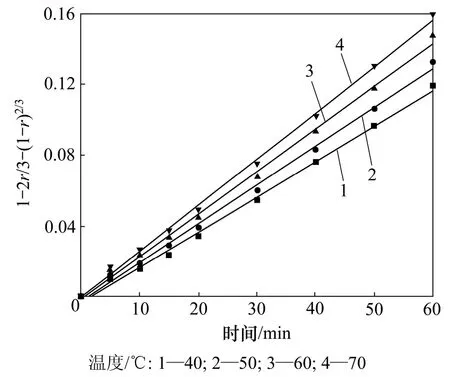
图5 氧气中t与1-2r/3-(1-r)2/3的关系图Fig.5 Relationship between 1-2r/3-(1-r)2/3 and t in oxygen
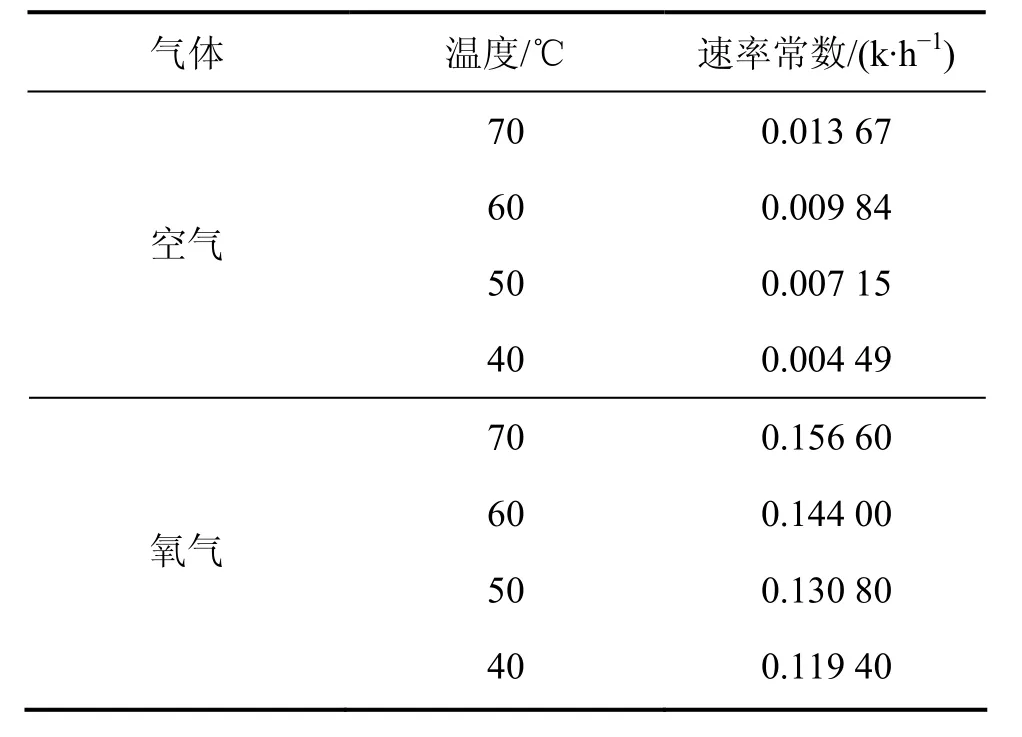
表5 还原钛铁矿中金属铁锈蚀速率常数Table 5 Oxidation reaction rate constant of iron in reduced ilmenite
根据表5中的反应速率常数,采用Arrhenius方程可求出还原钛铁矿中铁锈蚀反应的活化能,即:
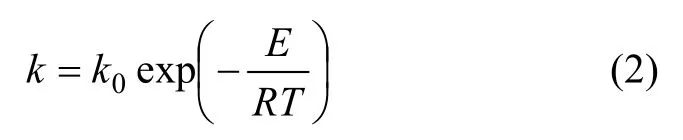
对上式两边取对数,可得:
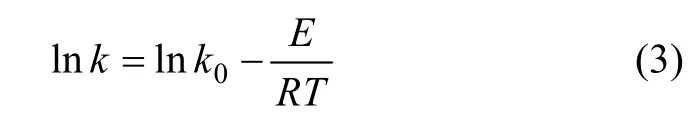
式中:E为活化能,kJ/mol;k0为系数,h/mol;k为速率常数,h/mol;R为气体常数,8.314×10-3kJ/(mol·K);T 为热力学温度,K。
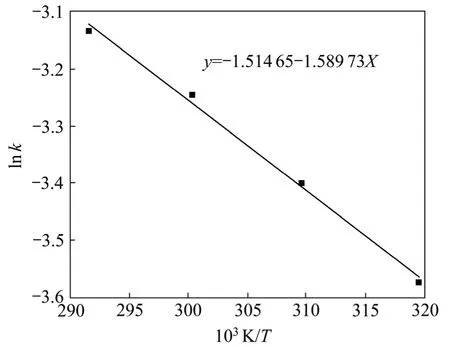
图6 空气中Arrhenius图Fig.6 Arrhenius plot in air
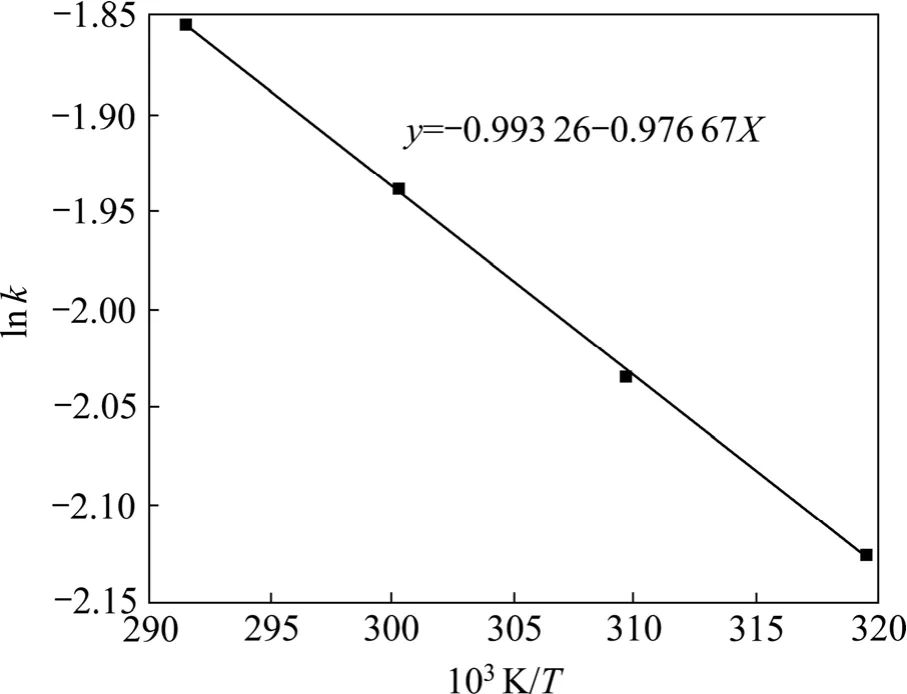
图7 氧气中Arrhenius图Fig.7 Arrhenius plot in oxygen
在40~70 ℃范围内,根据公式(3)将lnk对温度T的倒数作图,如图6和图7所示。从图6和图7可见:lnk与1/T呈线性关系,该直线的斜率为-E/R。图6和图 7中的关系式分别为 y=-1.514 65-1.589 73X,y=-0.993 26-0.976 67X,根据式(3)可求出还原钛铁矿中金属铁通入空气时锈蚀反应的表观反应活化能为13.28 kJ/mol,通入氧气时表观反应活化能为 8.12 kJ/mol。通入氧气后,还原钛铁矿中金属铁锈蚀表观反应活化能降低了5.16 kJ/mol。
Jayasekera等[16]通过研究发现:还原钛铁矿在锈蚀过程中,颗粒内的金属铁微晶相当于原电池的阳极,颗粒外表面相当于阴极。在阳极,Fe失去电子变为Fe2+离子进入溶液:
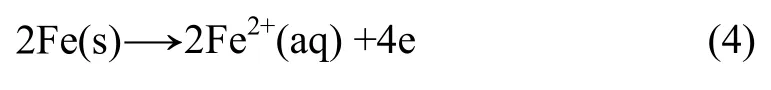
在阴极区,溶液中的氧接受电子生成OH-:

颗粒内溶解下来的Fe2+沿着还原钛铁矿颗粒中的微孔扩散到颗粒外表面的电解质溶液中,在溶液中进一步氧化生成水合氧化物铁细粒沉淀:

由上述锈蚀反应电化学机理来看,任何促进阳极和阴极反应过程的因素均有利于加快还原钛铁矿中的金属铁的锈蚀反应速率。
根据亨利定律[16],在一定的温度下,气体在液体中的溶解度和该气体的平衡分压成正比,即:

式中:X2为气体溶质在溶液中的原子数分数;P2为该气体的平衡分压;Kx为常数。
本试验中,采用纯氧代替空气,由于纯氧的氧分压为1 atm,空气的氧分压为21 kPa,通入纯氧提高了锈蚀溶液体系的氧分压,因而,锈蚀液中氧的溶解度会增大,将会增大锈蚀液本体与阴极反应区氧的浓度梯度,从而促进氧的内扩散过程,有利于反应(5)向正方向进行,其结果是加快了还原钛铁矿中金属铁的锈蚀反应速率过程。由此可见:锈蚀体系通入纯氧降低表观反应活化能的微观机理是纯氧加快了内扩散过程,促进了还原钛铁矿中金属铁锈蚀过程的阴极反应。
3 结论
(1) NH4Cl溶液体系中添加盐酸,还原钛铁矿中金属铁的锈蚀反应有转变为浸出反应的趋势。通入氧气,还原钛铁矿中金属铁在NH4Cl溶液中发生的仍是锈蚀反应历程。在锈蚀过程中,锈蚀速率显著加快,后续钛铁分离效果明显改善,通入氧气可加快锈蚀反应速率。
(2) 适宜的通氧量速率为 10×103L/(min·m3)~15×103L/(min·m3)。通氧速率过低,不利于发挥通氧的强化作用;通氧速率过高,锈蚀过程发生原位锈蚀,不利于后续的钛铁分离。
(3) 还原钛铁矿中金属铁在NH4Cl溶液体系下锈蚀过程受内扩散控制。通入氧气后还原钛铁矿中金属铁锈蚀过程的表观反应活化能由通入空气时的 13.28 kJ/mol降低至8.12 kJ/mol,其根本原因是通入氧气加快了内扩散过程,促进还原钛铁矿中金属铁锈蚀过程的阴极反应。
[1] 吴贤, 张健. 中国的钛资源分布及特点[J]. 钛工业进展, 2006,23(6): 8-12.WU Xian, ZHANG Jian. Geographical distribution and characteristics of titanium resources in China[J]. Titanium Industry Progress, 2006, 23(6): 8-12.
[2] 邓国珠, 黄北卫, 王雪飞. 制取人造金红石工艺技术的新进展[J]. 钢铁钒钛, 2004, 25(1): 44-49.DENG Guo-zhu, HUANG Bei-wei, WANG Xue-fei. Recent achievements in preparing technology of synthetic rutile[J]. Iron Steel Vanadium Titanium, 2004, 25(1): 44-49.
[3] 胡克俊, 锡淦, 姚娟, 等. 还原-锈蚀法生产人造金红石技术现状及攀钢采用该工艺可行性分析[J]. 钛工业进展, 2006,23(4): 17-22.HU Ke-jun, XI Gan, YAO Juan, et al. The feasibility analysis of becher process used in Panzhihua[J]. Titanium Industry Progress,2006, 23(4): 17-22.
[4] 杨保祥. 攀枝花矿产资源特征及循环经济发展策略探讨[J].四川有色金属, 2006(1): 1-5.YANG Bao-xiang. Study on characteristic of the Panzhihua mineral resources and strategy of circulation economy development[J]. Sichuan Nonferrous Metals, 2006(1): 1-5.
[5] 孙艳, 彭金辉, 黄孟阳, 等. 含钛料浸出除杂过程中的改性剂研究[J]. 钢铁钒钛, 2005, 26(3): 29-32.SUN Yan, PENG Jin-hui, HUANG Meng-yang, et al. Study on modifiers for impurities removal in microwave leaching of titanium material[J]. Iron Steel Vanadium Titanium, 2005, 26(3):29-32.
[6] 熊堃, 文书明, 郑海雷. 钛铁矿资源加工研究现状[J]. 金属矿山, 2010(4): 93-96.XIONG Kun, WEN Shu-ming, ZHENG Hai-lei. Research on mineral processing status of ilmenite resources[J]. Metal Mine,2010(4): 93-96.
[7] 莫畏, 邓国珠, 罗方承. 钛冶金[M]. 第二版. 北京: 冶金工业出版社, 2007: 188-189.MO Wei, DENG Guo-zhu, LUO Fang-cheng. Metallurgy of titanium[M]. 2nd ed. Beijing: Metallurgical Industry Press, 2007:188-189.
[8] Jaye K, Mohan P N. A structural model for the rusting of reduced ilmenite[J]. Hydrometallurgy, 2004,43(9): 13-20.
[9] Marinovich Y, Bailey S. A structural model for the rusting of reduced ilmenite[J]. Acta Metallurgica Slovaca, 2002, 35(14):13-18.
[10] Marinovich Y, Bailey S, Avraamides J, et al. An electrochemical study of reduced ilmenite carbon paste electrodes[J]. Appl Electrochem, 1995, 23(11): 34-35.
[11] 蒋云龙,李锦照. 还原-锈蚀法制取人造金红石[J]. 云南冶金,1989(4): 32-37.JIANG Yun-long, LI Jin-zhao. Artificial rutile produced by reduction-rusting process[J]. Yunnan Metallurgy, 1989(4):32-37.
[12] 马晓文. 强化还原钛铁矿锈蚀法钛铁分离的基础研究[D]. 长沙: 中南大学资源加工与生物工程学院, 2009: 50-58.MA Xiao-wen. Fundamental investigation on strengthening reduced ilmenite ferrotitanium separation[D]. Changsha: Central South University. School of Resources and Bioengineering, 2009:50-58.
[13] Jaye K, Berckman E. An electrochemical investigation of the rusting reaction of ilmenite using cyclic voltammetry[J].Hydrometallurgy, 1987(12): 217-221.
[14] 华一新. 冶金过程动力学导论[M]. 北京: 冶金工业出版社,2004: 188-198.HUA Yi-xin. The metallurgical process kinetics introduction[M].Beijing: Metallurgical Industry Press. 2004: 188-198.
[15] 黄希祜. 钢铁冶金原理[M]. 3版. 北京: 冶金工业出版社,2005: 82-87.HUANG Xi-hu. Principles of iron and steel metallurgy[M]. 3rd ed. Beijing: Metallurgical Industry Press, 2005: 82-87.
[16] Jayasekera S, Avraamides J. Rotating disc electrode apparatus for aqueous electrochemical studies at elevated temperatures and pressures application to the Becher process[C]//Proceedings of 6th AuslMM Extractive Metallurgy Conference. Brisbane: Aust Inst Min Metall Parkville, 1994: 123-126.
