威灵仙的化学成分研究*
2012-05-09梁丽珍李厚金文诗雅蓝文健
赵 阳,梁丽珍,李厚金,文诗雅,蓝文健,3
(1.中山大学药学院,广东 广州510006;2.中山大学化学与化学工程学院,广东 广州510275;3.广东省现代中药工程技术研究开发中心,广东 广州510006)
威灵仙(ClematischinensisOsbeck),属毛茛科植物。在临床治疗上,它用于治疗痛风顽痹、肢体麻木、筋脉拘挛,减弱风湿痹痛、诸骨鲠咽,减少水肿、降血压和治疗外伤等。
有关威灵仙的化学成分,近年来陆续有一些报道,但研究主要集中于威灵仙的大极性组分,如:1992年Song Chunqing等分离到由D-葡萄糖和4-羟基-3,5-二甲氧基苯甲酸组成的大环糖苷clemochinenoside[1]。此外,从威灵仙的根部提取物中分离得到一系列三萜甙[2-6]。威灵仙中所发现的大多数皂苷的苷元均为齐墩果酸,其总皂苷具有抗肿瘤及抗炎镇痛的作用。
我们对威灵仙根茎乙酸乙酯提取物的化学成分进行了系统的研究,分离鉴定了7个化合物:松脂素(Pinoresinol,1),Epipinoresinol(2),罗汉松脂素(Matairesinol,3),Salicifoliol(4),3,4,5-三羟基苯甲酸(5),4-羟基-3,5-二甲氧基-苯甲酸(6),异阿魏酸(7),化合物结构通过NMR和MS的分析得到确定。化合物1,2,3,4是木脂素类化合物,它们是首次从威灵仙中发现,具有多种重要的生理活性,其潜在药用前景明显。
1 实验部分
1.1 药材、试剂与仪器
威灵仙干燥根茎,由广东罗浮山国药股份有限公司提供。
石油醚、乙酸乙酯、甲醇、乙醇,市售分析纯;乙腈,HPLC级,购于Sigma公司。
美国Varian公司INOVA 500NB,Bruker公司AVANCE AV 400 MHz核磁共振仪。Thermo DSQ EI低分辨质谱仪,Thermo MAT95XP EI高分辨质谱仪。美国Finnigan公司TRACE DSQ气相色谱-质谱联用仪。岛津LC-20AT高效液相色谱仪,Shim-pack PRC-ODS (250 mm × 20 mm)制备型液相色谱柱,Inertsil®ODS-SP (5μm,4.6 mm × 250 mm) 分析型液相色谱柱。
1.2 化合物的提取与分离
取威灵仙干燥根茎500 g,碾碎。用1 Lw=50%的乙醇回流1 h,提取3次,合并提取液。低温旋转蒸发除去乙醇,残余水层用500 mL乙酸乙酯提取3次,合并乙酸乙酯提取液,低温旋转蒸发至干得32.2 g样品。乙酸乙酯提取物经硅胶柱层析分离,以石油醚-乙酸乙酯-甲醇梯度洗脱,收集石油醚-乙酸乙酯3∶1 (V/V)至石油醚-乙酸乙酯1∶2 (V/V)的组分,该收集组分经反相C18制备型高效液相色谱分离,以乙腈-水70∶30 (V/V)为流动相,分离、纯化得到化合物1、2、3、4、5、6、7,分别为416、271、46、39、42、55、121 mg。
1.3 高效液相色谱分析实验条件
样品溶于乙腈,进样量5 μL。以乙腈-水为溶剂,采用梯度洗脱方法。即:0~10 min,φ=30%的乙腈,然后线性梯度增加乙腈含量,至40 min乙腈的体积分数达100%,继续恒流至65 min。紫外检测波长为254 nm。
1.4 气相色谱-质谱分析实验条件
DB-5MS毛细管柱(30 m × 0.25 mm × 0.25 μm)。程序升温:初始温度80 ℃,保持3 min,以2 ℃/min升至180 ℃,保持4 min ,再以8 ℃/min升到200 ℃,保持4 min,以10 ℃/min升温至270 ℃,保持30 min。载气为氮气,流速为1 mL/min,分流比为30∶1,进样量1.0 μL。质谱条件:离子源为EI源,70 eV,离子源、连接口温度均为230 ℃。扫描质量范围为50~650 amu,全扫描方式。
1.5 化合物波谱数据
化合物1,2,3,4的1H和13C的数据见表 1。
化合物1和2, LR EI MSm/z358,343,327,312,259,234,221,205,189,180,163,151,137,131,124,117,103,91,81,65,55。
化合物3,LR EI MSm/z358,234,221,208,194,175,164,137,131,122,94。
化合物4,LR EI MSm/z250,235,233,219,207,198,191,175,165,151,137,123。
化合物5,13C NMR (CDCl3,100 MHz)δC: 170.1 (C),147.0 (2×C),138.5 (C),122.7 (C),109.6 (2×CH)。1H NMR (CDCl3,400 MHz)δH: 7.06 (s,2H),6.62 (brs,3H)。
化合物6,HREIMS:m/z198.0522 (C9H10O5,理论值198.052 3)。LREIMS:m/z198,183,168,149,137,109,97,93,81,65。13C NMR (CDCl3,100 MHz)δC: 171.1 (C),146.6 (2×C),139.9 (C),120.0 (C),107.2 (2×CH),56.5 (CH3)。1H NMR (CDCl3,400 MHz)δH: 7.40 (s,2H),6.05 (brs,1H),3.97 (s,6H)。
化合物7,13C NMR (DMSO-d6,100 MHz)δC: 167.6 (C),149.7 (C),146.4 (C),144.2 (CH),126.9 (C),121.1 (CH),116.0 (CH),113.8 (CH),111.9 (CH),55.7 (CH3)。1H NMR (DMSO-d6,400 MHz)δH: 9.27 (brs,1H),7.43 (d,J=15.9 Hz,1H),7.062 (dd,J=8.4,1.8 Hz,1H),7.060 (dd,J=1.8 Hz,1H),6.92 (d,J=8.4 Hz,1H),6.91 (brs,1H),6.23 (d,J=15.9 Hz,1H),3.79 (s,3H)。
2 结果与讨论
威灵仙根茎的乙酸乙酯提取物经HPLC分析,以254 nm为检测波长,分析结果见图2。由图可知该提取物中含有大量的分子中具有共轭体系结构的化合物。经硅胶柱层析和制备HPLC分离纯化得到化合物1,2,3,4,5,6,7,它们在HPLC分析中的保留时间分别为26.51,28.66,29.79,14.62,6.53,7.71,10.16 min。
化合物1,EI MS显示相对分子质量为358。13C NMR显示10个共振信号,其中3个季碳C,5个CH,1个CH2,1个CH3,提示分子结构对称,分子式为C20H22O6。3个季碳(δC132.5,145.0,146.5),3个CH [δC108.6 (δH6.90,d,1.5),114.2 (δH6.87,d,8.1),118.7 (δH6.81,dd,8.1,1.5)]构成一个1,3,4-三取代苯环。CH3O-[δC55.8 (δH3.85,s)]与苯环相连。连氧的CH [δC85.7 (δH4.76,d,4.5)]与苯环和另外1个CH [δC53.9 (δH3.12,m)]相连,而后者又与另一连氧的CH2[δC71.5 (δH4.26,dd,9.0,6.9;δH3.89,dd,9.0,3.6)]相连。δH6.06 (brs) 为苯环上的羟基信号。根据HMBC的相关关系,确定其结构为松脂素(Pinoresinol,又名4,4'-[(1S,3aR,4S,6aR)- tetrahydro -1H,3H- furo[3,4-c]furan-1,4-diyl] bis [2-methoxy- phenol])[7]。
化合物2,EI MS显示相对分子质量也为358。13C NMR显示20个共振信号,其中6个季碳C,10个CH,2个CH2,2个CH3,分子式为C20H22O6。对1H、13C、HMQC、以及HMBC的综合分析,确定化合物2和1具有完全一致的官能团和结构片段的连接顺序,它们仅仅是构型上存在差异。化合物2确定为Epipinoresinol,又名4,4'- [(1R,3aR,4S,6aR)-tetrahydro-1H,3H -furo [3,4-c] furan -1,4 -diyl] bis[2-methoxy- phenol][8]。
化合物3,EI MS显示相对分子质量也为358,分子式为C20H22O6。与化合物1和2一样,分子中含有2个3-甲氧基- 4-羟基取代苯结构单元。剩余6个碳包括1个羰基,2个CH,3个CH2,其中1个CH连氧。根据氢谱裂分、偶合常数、以及HMBC的相关关系分析,确定3个CH2均和CH相连,而-OCH2-和羰基共同构成一个五元内酯环,另外2个CH2则分别和苯环相连。由此,确定化合物3的结构为罗汉松脂素(Matairesinol)[7]。
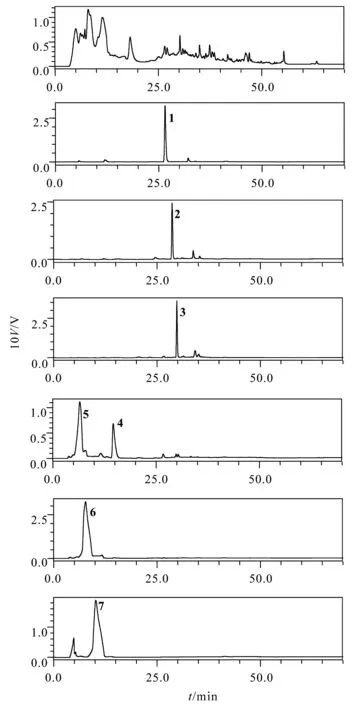
图2 威灵仙乙酸乙酯提取物和化合物1,2,3,4,5,6,7的高效液相分析图
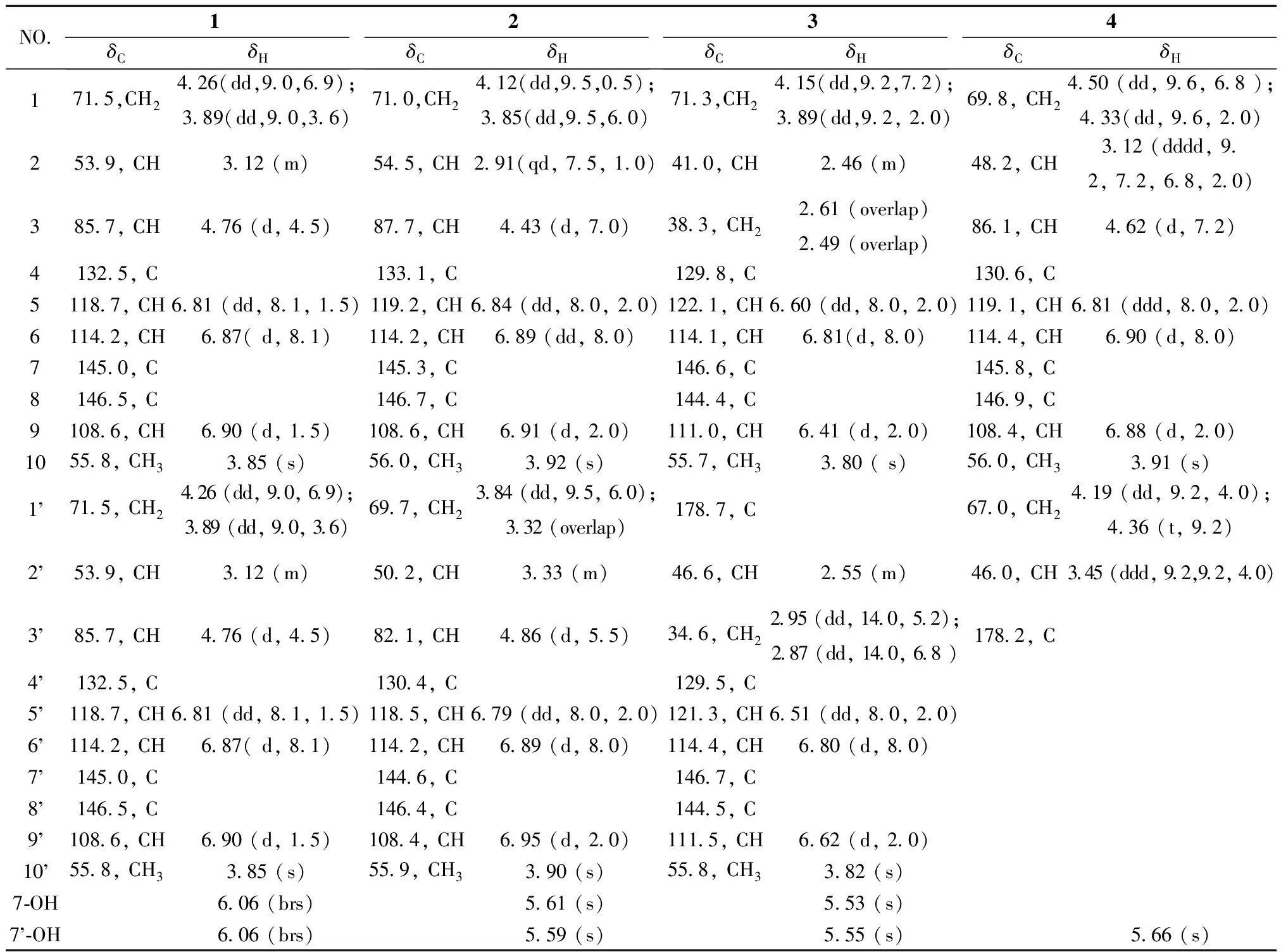
表1 化合物1,2,3,4的核磁共振数据
化合物4,EI MS显示相对分子质量为250,分子式为C13H14O5,其中4个季碳C,6个CH,2个CH2,1个CH3。分子中含有1个3-甲氧基- 4- 羟基取代苯结构单元,剩余6个碳包括1个羰基,3个CH,2个CH2。2个CH2(δC69.8和67.0)和1个CH(δC86.1)连氧,根据氢谱裂分、偶合常数可以确定CH2均与CH相连,而羰基(δC178.2)根据化学位移可以确定其为内酯。由HMQC、HMBC的相关关系分析,确定化合物4的结构为Salicifoliol[9]。
化合物5,6,7的结构根据其1H、13C NMR,以及MS数据分别确定为3,4,5-三羟基苯甲酸,4-羟基-3,5-二甲氧基-苯甲酸,异阿魏酸。
乙酸乙酯提取物样品用乙腈溶解,进行气相色谱-质谱实验。气相色谱-质谱总离子流图(图3)显示化合物1,2,3,4的保留时间分别为86.86,85.64,80.79,62.79 min,按峰面积归一化法计算各个化合物的百分含量分别为2.39,1.46,0.56,0.58。化合物1,2,3,4的气质联用质谱图(图4)与其纯化合物的LREIMS图基本一致。

图3 威灵仙乙酸乙酯提取物的气相色谱-质谱总离子流图
3 结 论
本研究发现威灵仙中富含结构多样性的木脂素类化合物,建立了木脂素的HPLC和GC-MS色谱分析方法,该方法具有快速、稳定和精确的特点。木脂素是由苯丙素单元聚合而成,它具有广泛的生物活性,如抗肿瘤、抗炎、抗菌、抗虫、抗氧化、保肝、抑制植物生长等[10-12]。因此,以威灵仙为药用原材料,研究与开发创新药物,前景广阔。而以木脂素类化合物的组成和含量分析也将可作为威灵仙药材质量检测和所制成的中成药质量控制的方法。
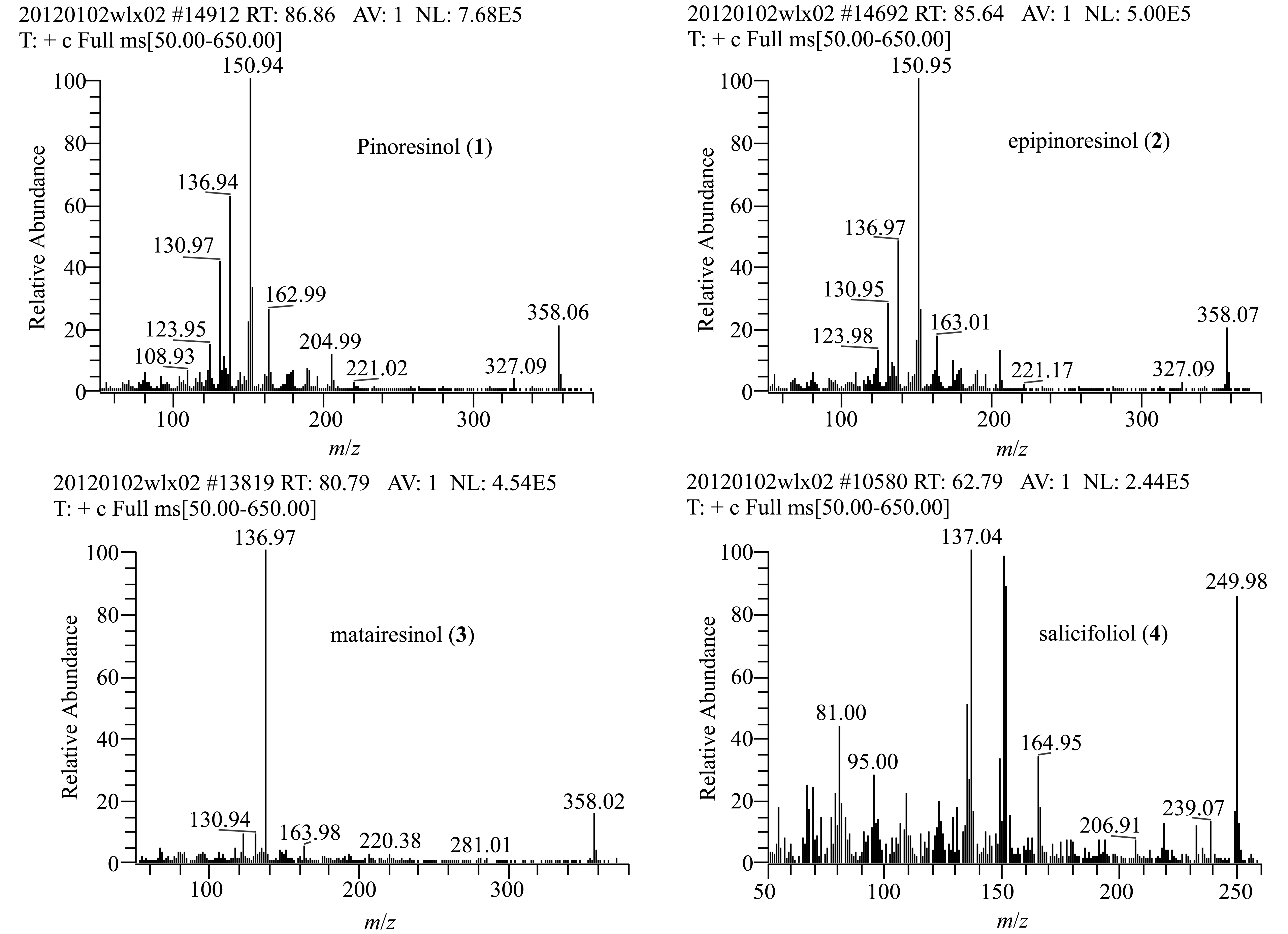
图4 化合物1,2,3,4的质谱图
参考文献:
[1]SONG C Q,XU R S.Clemochinenoside A,a macrocyclic compound fromClematischinensis[J].Chinese Chemical Letters,1992,3(2): 119-120.
[2]Fu Q,ZAN K,ZHAO M B,et al.Triterpene saponins fromClematischinensisand their potential anti-inflammatory activity [J].Journal of Natural Products,2010,73(7): 1234-1239.
[3]LIU L F,MA X L,WANG Y X,et al.Triterpenoid saponins from the roots ofClematischinensisOsbeck [J].Journal of Asian Natural Products Research,2009,11(5): 389-396.
[4]MIMAKI Y,YOKOSUKA A,HAMANAKA M,et al.Triterpene saponins from the roots ofClematischinensis[J].J Natural Products,2004,67(9):1511-1516.
[5]SHAO B P,QIN G W,XU R S,et al.Triterpenoid saponins fromClematischinensis[J].Phytochemistry,1995,38(6): 1473-1479.
[6]KIZU H,TOMIMORI T.Studies on the constituents ofClematisspecies.I.On the saponins of the root ofClematischinensisOsbeck [J].Chemical & Pharmaceutical Bulletin,1979,7(10): 2388-2293.
[7]NISHIBE S,TSUKAMOTO H,HISADA S.Effects of O-methylation and O-glucosylation on carbon-13 nuclear magnetic resonance chemical shifts of matairesinol,(+)-pinoresinol and (+)-epipinoresinol [J].Chem & Pharmaceutical Bulletin,1984,32(11):653-657.
[8]OKUYAMA E,SUZUMURA K,YAMAZAKI M.Pharmacologically active components ofTodoponPuok(Fagraearacemosa),a medicinal plant from Borneo [J].Chemical & Pharmaceutical Bulletin,1995,43(12): 2200-2204.
[9]GONZALEZ A G,ESTEVEZ-REYES R,MATO C.Salicifoliol,a new furolactone-type lignan fromBupleurumsalicifolium[J].Journal of Natural Products,1989,52(5):1139-1142.
[10]IONKOVA I.Anticancer lignans-from discovery to biotechnology [J].Mini-Reviews in Medicinal Chemistry,2011,11(10): 843-856.
[11]MITJANS M,VINARDELL M P.Biological activity and health benefits of lignans and lignins [J].Trends in Comparative Biochem & Physiology,2005,11:55-62.
[12]LEE K H,XIAO Z Y.Lignans in treatment of cancer and other diseases [J].Phytochemistry Reviews,2004,2003 (3): 341-362.
